
- •Общие методические указания
- •Контрольные задания
- •Teма 1. Основные понятия и законы химии.
- •Тема 2. Строение атома. Периодический закон и периодическая система элементов д.И.Менделеева.
- •Тема 3. Химическая связь и строение молекул.
- •Тема 4. Химическая кинетика и равновесие.
- •Тема 5. Энергетика химических процессов.
- •Тема 6. Концентрации растворов и способы их выражения.
- •Тема 7. Ионные реакции обмена
- •Тема 8. Гидролиз солей.
- •Тема 9. Гетерогенные равновесия. Произведение растворимости
- •Тема 10. Окислительно-восстановительные реакции
- •Тема 11. Электродные потенциалы и электродвижущие силы
- •Тема 12. Электролиз
- •Тема 13. Коррозия металлов
- •Тема 14. Полимеры
- •Рекомендуемая литература
- •Приложение Вопросы, предлагаемые студентам нф специальности «Разработка и эксплуатация нефтяных и газовых месторождений» для подготовки к экзамену по химии
Тема 9. Гетерогенные равновесия. Произведение растворимости
-
Растворимость ВаСО3 равна 8,9·10–5 моль/л. Вычислить произведение растворимости карбоната бария.
-
Произведение растворимости РbI2 равно 8,7·10–6. Вы числить концентрацию ионов Рb2+ и ионов I– в насыщенном растворе иодида свинца.
-
Растворимость АgI равна 1,2·10–8 моль/л. Вычислите произведение растворимости АgI.
-
Растворимость Fе(ОН)3 равна 1,9·10–10 моль/л. Вычислить произведение растворимости Fе(ОН)3.
-
В 2 л воды при температуре 25°С растворяется 2,2·10–4г бромида серебра. Вычислите произведение растворимости АgВr.
-
Растворимость сульфата бария в воде равна 2,45·10–3 г/л. Вычислите произведение растворимости ВаSО4.
-
Растворимость СаСО3 при 18°С равна 6,9·10–5 моль/л. Вычислите произведение растворимости СаСО3.
-
Растворимость РbВr2 при 18°С равна 2,7·10–2 моль/л. Вы числите произведение растворимости РbВr2.
-
Растворимость ВаСО3 равна 8,9·10–4 моль/л. Вычисли те концентрации ионов [Ва2+] и [СО32–] (моль/л), а также про изведение растворимости ВаСО3.
-
Произведение растворимости РbSО4 равно 2,3·10–8. Сколько литров воды потребуется для растворения 1г РbSО4?
-
Произведение растворимости СаSO4 равно 6,0·10–5. Вы падает ли осадок СаSО4, если смешать равные объемы 0,2 н/ растворов СаС12 и Н2SО4.
-
Произведение растворимости СаСО3 равно 4,8·10–9. Вы падает ли осадок, если смешать равные объемы 0,001М растворов СаС12 и Na2СО3?
-
Произведение растворимости АgС1 равно 1,8·10–10. Вы падает ли осадок, если смешать 20 мл 0,01 M раствора КС1 с 6 мл 0,01 M раствора АgNO3.
-
Произведение растворимости Аg2Сr2О7 равно 2,0·10–7. Выпадет ли осадок при смешении равных объемов 0,01 н. растворов АgNО3 и К2Сr2О7.
-
В 6 литрах насыщенного раствора РbSO4 содержится 0,186 г иона свинца(II). Вычислить произведение растворимости.
-
Произведение растворимости сульфата цинка ПP = 2,3·10–8. Образуется ли осадок, если к 0,1 М раствору Na2SО4 прибавить равный объем 0,1 н. раствора ацетата свинца Рb(СН3СОО)2?
-
Произведение растворимости МgF2 равно 7,0·10–9. Вычислите растворимость этой соли в молях на литр и в граммах на литр.
-
Вычислите произведение растворимости карбоната стронция, если в 5 л насыщенного раствора содержится 0,05 г этой соли.
-
Сколько воды потребуется для растворения 1 г ВаСО3, произведение растворимости которого равно 1,9·10–9?
-
Растворимость AgCl в воде при 25°С равна 1,3·10–5 моль/л. Вычислите произведение растворимости хлорида серебра при этой температуре и его растворимость в граммах на литр.
Тема 10. Окислительно-восстановительные реакции
-
Дайте определение понятию окислительно-восстановительные реакции. Какие из приведенных ниже реакций являются окислительно-восстановительными:
-
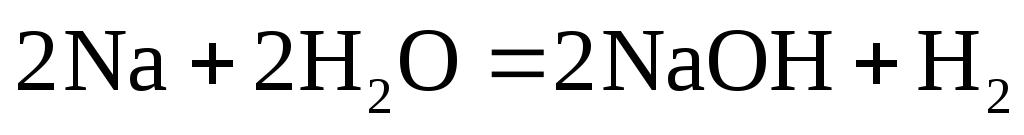 ;
; -
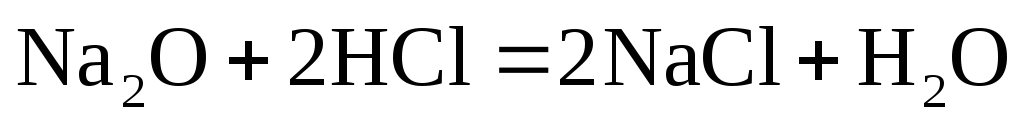 ;
; -
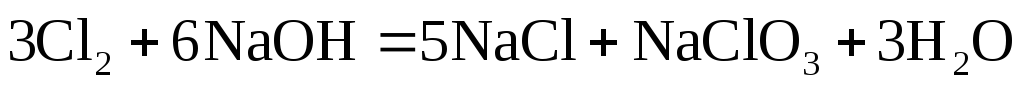 .
.
-
Какие частицы называют восстановителями. Руководствуясь строением атомов, решите, могут ли фигурировать в качестве восстановителей следующие ионы: Sn2+, Cl–, Zn2+.
-
Дайте определение понятию степень окисления. Определите степень окисления центрального атома в следующих ионах: SO42–, SO32–, S2O32–.
-
Какие частицы называют окислителями. Укажите, какие из перечисленных ионов могут быть окислителями: Fe3+, Br–, Cr3+
-
Какие из перечисленных частиц обладают двойственной окислительно-восстановительной природой, почему?
-
Fe2+, Fe3+, Fe+6;
-
H–1, H20, H+1;
-
N–3, N20, N+3;
-
C+2, Cu+1, F–1.
-
Укажите, какие из перечисленных частиц являются только окислителями:
-
N+5, S+6, Cl+3;
-
Cl+7, O20, F20;
-
H+, Br+7, C+4;
-
Cr+6, Mn+7, Mn+4.
-
Укажите, какие из перечисленных частиц являются только восстановителями:
-
H–, I–, Na+;
-
Ca0, N–3, O–1;
-
O–2, Cu+1, C+4.
-
Окислительно-восстановительные реакции выражаются приведенными схемами:
-
KMnO4 + N2H4 + H2SO4 N2 + MnSO4 + K2SO4 + H2O;
-
HgS + HCl + HNO3 S + HgCl2 + NO + H2O;
-
FeSO4 + HNO3 Fe(NO3)3 + NO + H2SO4 + H2O;
-
Mg + HNO3 NH4NO3 + Mg(NO3)2 + H2O;
-
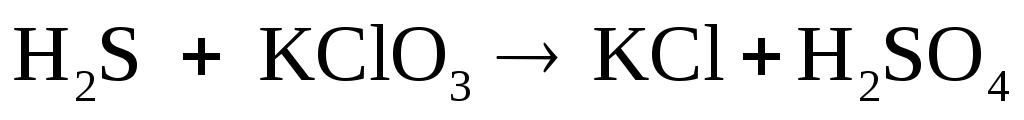 ;
; -
P + HIO3 + H2O H3PO4 + HI;
-
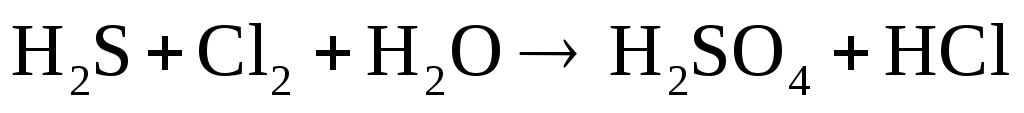 ;
; -
 ;
; -
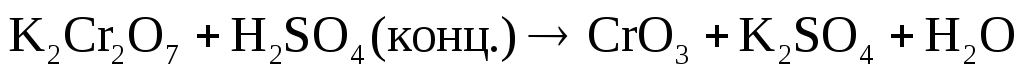 ;
; -
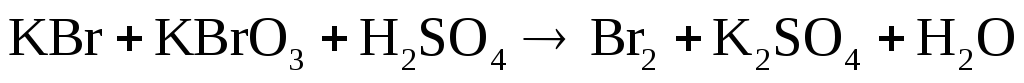 ;
; -
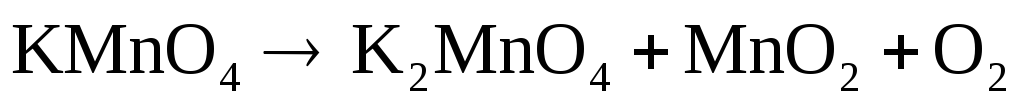 ;
; -
 ;
; -
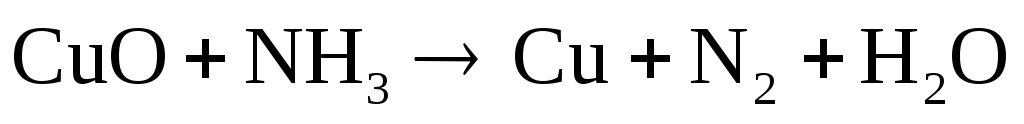 ;
; -
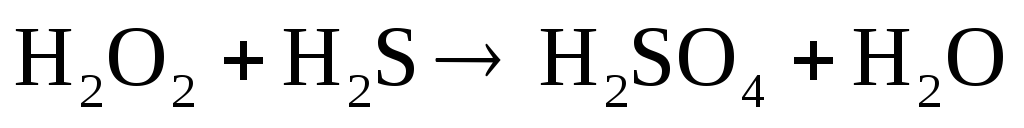 ;
; -

Подберите коэффициенты в предложенных реакциях методом электронного баланса. Укажите, какое вещество в каждом взаимодействии является окислителем, какое – восстановителем.
-
Окислительно-восстановительные реакции выражаются ионными уравнениями:
-
 ;
; -
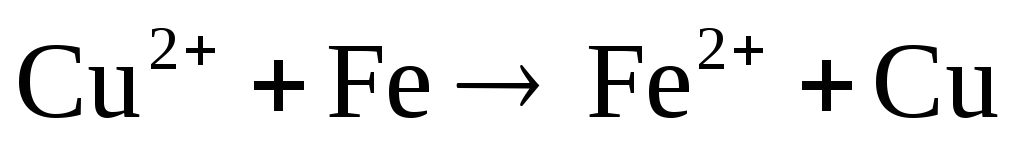
-
 ;
; -
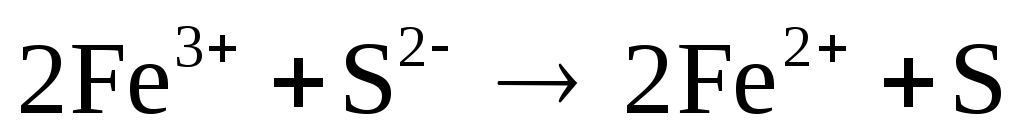 ;
; -
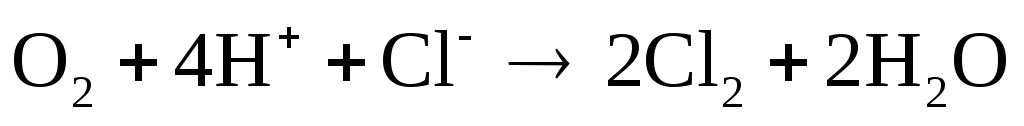 ;
; -
 ;
;
Составьте электронные и молекулярные уравнения. Для каждой реакции укажите, какой ион является восстановителем, какой – окислителем.
