
- •З біологічної хімії
- •Рецензент проф. В.Д. Бовт
- •Питання до іспиту……………………………………………………………… 79
- •Тематичне розподілення навчального матеріалу а. Тематичне розподілення лекційного матеріалу
- •В. Тематичний план лабораторних і семінарських занять
- •Техніка безпеки при роботі у біохімічній лабораторії
- •Забороняється з метою уникнення травм, опіків, нещасних випадків:
- •Перша домедична допомога
- •Вимоги до оформлення лабораторного журналу і робочого місця
- •Теоретична частина:
- •Практична частина:
- •Теоретична частина:
- •Практична частина:
- •Контрольні питання
- •Теоретична частина:
- •Практична частина:
- •Питання до семінарського заняття:
- •Теоретична частина:
- •Практична частина:
- •Контрольні питання
- •Теоретична частина:
- •Практична частина:
- •Контрольні питання
- •Теоретична частина:
- •Цитозін
- •Практична частина:
- •Контрольні питання
- •Теоретична частина:
- •Властивості ферментів:
- •Реакція
- •Практична частина:
- •Теоретична частина:
- •Практична частина:
- •Контрольні питання
- •Питання до семінарського заняття:
- •Теоретична частина:
- •Тканьовий подих
- •Практична частина:
- •Контрольні питання
- •Питання до семінарського заняття:
- •Теоретична частина:
- •Катаболізм амінокислот:
- •Біосинтез сечовини (орнітиновий цикл)
- •Практична частина:
- •Теоретична частина:
- •Практична частина:
- •Питання до семінарського заняття:
- •Теоретична частина:
- •Взаємний зв'язок різних форм обміну речовин в організмі
- •Практична частина
- •Контрольні питання
- •Питання до семінарського заняття:
- •Питання до іспиту
- •Список рекомендованої літератури
- •Практикум з біологічної хімії до лабораторних і семінарських занять для студентів біологічного факультету денної та заочної форм навчання
Питання до семінарського заняття:
-
Суть явища каталізу.
-
Швидкість хімічних реакцій.
-
Особливості ферментативного каталізу.
-
Механізм дії ферментів.
-
Властивості ферментів.
-
Вплив різних чинників середовища на ферментативні процеси.
-
Вплив інгібіторів на ферментативну активність.
-
Класифікація і номенклатура ферментів.
-
Коферменти, простетичні групи.
-
Роль вітамінів, металів і інших кофакторів у функціонуванні ферментів.
-
Основні уявлення про кінетику ферментативних процесів, залежність швидкості ферментативної реакції від концентрації субстрату. Рівняння Міхаеліса-Ментен.
-
Ізоферменти й інші різновиди ферментів.
-
Одиниці активності ферментів.
-
Локалізація ферментів у клітині.
-
Загальна характеристика вітамінів. Класифікація.
-
Вітаміни - попередники коферментів.
-
Характеристика жиророзчинних (А, Д, Є, К) і водорозчинних (В1, В2, В3, РР, В6, В12, В15, Н, С, Р) вітамінів по такій схемі:
-
Назва.
-
Формула. Характеристика фізичних і хімічних властивостей по формулі.
-
Джерела вітаміну.
-
Вплив на організм. Роль в обміні речовин.
-
Авітаміноз, гіповітаміноз, гіпервітаміноз.
-
-
Рішення задач.
Заняття № 11.
Тема: ВИЗНАЧЕННЯ КОНЦЕНТРАЦІЇ ГЛЮКОЗИ В КРОВІ за КОЛЬОРОВою РЕАКЦІєю З ортотолуІдином
Теоретична частина:
В основному вуглеводи виконують енергетичну функцію. Головними джерелами енергії є глюкоза та глікоген. До того ж, із вуглеводів можуть синтезуватися ліпіди, деякі амінокислоти, пентози.
Добова норма вуглеводів у їжі складає 400-500 г. Основними вуглеводами їжі є: крохмаль та дисахариди - сахароза, лактоза, мальтоза.
Гідроліз крохмалю починається в порожнині рота за участю ферменту амілази слини до декстринів. Потім його гідроліз продовжується у верхньому відділі кишечника під впливом панкреатичної амілази. У результаті з крохмалю утворюються дисахаридні залишки мальтози. Гідроліз всіх дисахаридів здійснюється на поверхні клітин кишечнику та каталізується специфічними ферментами: сахаразою, лактазою, мальтазою, які синтезуються в клітинах кишечника.
З кров’ю воротньої вени більша частина глюкози із кишечника надходить до печінки, решта глюкози через загальний кровообіг транспортується в інші тканини. Концентрація глюкози в крові у нормі піддержується на постійному рівні та складає 3,33-5,55 мкмоль/л, що відповідає 80-100 мг в 100 мл крові. Транспорт глюкози в клітини носить характер полегшеної дифузії, але регулюється в багатьох клітинах гормоном підшлункової залози – інсуліном.
В організмі вуглеводи можуть підлягати окисненню або використовуватися для синтезу глікогену – резервного вуглеводу тканин (печінки, м'язів, нервової тканини та ін.). Головним депо вуглеводів є печінка.
Вивчення енергетики м'язової діяльності показало, що при роботі м'язів відбувається розпад вуглеводів і утворення продуктів їх окиснення. Особливо велика роль вуглеводів як джерела енергії в умовах недостатнього постачання тканинам кисню (гіпоксія) і при м'язовій діяльності великої інтенсивності, коли різко зростає потреба організму в кисні, яка не може бути повністю задоволена.
Окиснення вуглеводів відбувається в 2 стадії. Перша стадія називається гліколізом. Вона полягає в неповному окисненні глюкози до двох молекул піровиноградної кислоти (аеробний гліколіз) або двох молекул молочної кислоти (анаеробний гліколіз). Всі десять реакцій гліколізу протікають у цитозолі та характерні для всіх органів та тканин. Друга стадія має назву окислювального циклу трикарбонових кислот (або циклу Кребса). Вона полягає в аеробному окисненні залишків піровиноградної кислоти (у виді ацетильних радикалів) до кінцевих продуктів окиснення – вуглекислоти і води.
Обидва процеси – і гліколіз, і цикл Кребса – складаються із багатьох проміжних реакцій. Унаслідок цього енергія, яка заключена у вуглеводах, звільняється поступово, перетворюючись у багаті енергією фосфорні сполуки - у кінцевому рахунку в аденозинтрифосфорну кислоту (АТФ).
Біохімічні перетворення глюкози починаються з утворення гексозофосфорних ефірів. Наступні перетворення цих ефірів під дією відповідних ферментів приводять до утворення з кожного глюкозного залишку двох молекул фосфогліцеринового альдегіду, який потім окиснюється. У результаті цієї реакції утворюється відновлений НАД(НАДН) і 1,3-дифосфогліцеринова кислота (або 3-фосфогліцероїлфосфат), змішаний ангідрид фосфорної і 3-фосфогліцеринової кислоти, в якому акумулюється енергія окиснювання гліцеральдегид-3-фосфату. Ангідрид такого типу називається ацилфосфатом і характеризується дуже високим значенням G°` гідролізу (-11,8 ккал/моль), тобто відноситься до категорії понадвисокоенергетичних фосфорильованих сполук (макроергічних сполук). Багатий енергією фосфорильний залишок (з 1 положення 1,3-дифосфогліцеринової кислоти) потім переноситься на АДФ із утворенням АТФ.
Другим етапом гліколізу, на якому відбувається синтез АТФ, є перетворення фосфоенолпіровиноградної кислоти у піровиноградну. Таким чином, у процесі гліколізу синтезуються десять молекул АТФ на одну молекулу глюкози. Із цих десяти молекул АТФ одна використається при утворенні глюкозо-6-фосфата, а інша - при утворенні фруктозо-1,6-дифосфата. У підсумку залишаються вісім молекул АТФ.
В умовах неповного задоволення потреби організму в кисні піровиноградна кислота приєднує водень від відновленої форми НАД, перетворюючись у молочну кислоту:
СН3 СН3
│ │
 2
С ═ О + 2 над∙
Н2
2 СН ─ ОН + 2 НАД+
2
С ═ О + 2 над∙
Н2
2 СН ─ ОН + 2 НАД+
│ │
СООН СООН
піровиноградна молочна
кислота кислота
У результаті утворюється тільки дві молекули АТФ.
Анаеробний розпад вуглеводів у деяких мікроорганізмів, наприклад, процес спиртового шумування в дріжджових клітинах подібний із процесом гліколізу у тваринних тканинах. Розходження має місце на кінцевих етапах розпаду вуглеводів. При спиртовому шумуванні відбувається декарбоксилування піровиноградної кислоти з утворенням оцтового альдегіду, який і служить акцептором водню з НАД Н+. Кінцевими продуктами спиртового шумування є етиловий спирт і вуглекислий газ.
Процес анаеробного розпаду вуглеводів може починатися не із глюкози (гліколіз), а із глікогену (глікогеноліз). Фермент глікогенфосфорилаза каталізує фосфоролітичне розщеплення α-I,4-глікозидного зв'язку в глікогені з боку термінального не редукованого залишку глюкози з утворенням глюкозо-1-фосфату. Дія глікогенфосфорилази на глікоген припиняється в крапках розгалуження до тих пір, доки не відбудеться розщеплення α-1,6-глюкозидних зв'язків, яке каталізується ферментом аміло-1,6-глюкозидазою.
У підручниках з біохімії дається опис складної системи регуляції активності глікогенфосфорилази і переходу неактивної форми фосфорилази (фосфорилази Б) в активну форму (фосфорилазу А) шляхом фосфорилювання (ковалентна модифікація серинових залишків у молекулі фосфорилази Б), а також шляхом зворотнього переходу димерної фосфорилази в тетрамерну. У регуляції беруть участь гормони, циклічна АМФ, іони Ca2+, АТФ, АМФ, глюкозо-6-фосфат і глюкоза. Активація глікогенфосфорилази може приводити до прискорення розщеплення глікогену в кілька сотень і навіть тисяч разів. Глюкозо-1-фосфат, який утворюється під дією фосфорилази, перетворюється при участі фосфоглюкомутази в глюкозо-6-фосфат, який включається в процес гліколізу. Перетворення одного глюкозного залишку глікогену в молочну кислоту супроводжується синтезом чотирьох молекул АТФ також, як і при гліколізі. Але сумарний вихід становить три молекули АТФ, тому що одна молекула АТФ використовується для фосфорилювання фруктозо-6-фосфату.
Розгляд регуляції процесу гліколізу варто почати з фосфофруктокінази - головного ключового ферменту, який визначає сумарну швидкість гліколізу. Фосфофруктокіназа - алостеричний фермент, активність якого залежить від цілого ряду факторів, головним чином від співвідношення між АТФ, АДФ і неорганічним фосфатом. Один з можливих механізмів ефекту Пастера (пригнічення гліколізу подихом) полягає, очевидно, у тім, що високе співвідношення в клітині [АТФ]/[АДФ], характерне для дихального фосфорилювання, приводить до інгібірування фосфофруктокінази і, відповідно, до зниження швидкості гліколізу. У цих умовах накопичується глюкозо-6-фосфат - інгібітор іншого регуляторного ферменту - гексокінази.
Інший механізм пригнічення гліколізу подихом заснований на конкуренції за АДФ між дихальним фосфорилюванням і такими ферментами гліколізу, як фосфогліцераткіназа і піруваткіназа. Можлива конкуренція між дихальним фосфорилюванням і гліколізом за неорганічний фосфат. Якщо через недолік неорганічного фосфату не відбудеться реакція гліколітичної оксидоредукції, яка сполучена з фосфорилюванням, то диоксиацетонфосфат може відновлюватися в гліцерофосфат - попередник ліпідів.
Піровиноградна кислота є проміжним продуктом гліколізу і глікогенолізу. В умовах достатнього постачання тканин киснем (аеробні умови) молочна кислота із неї, як правило, не утворюється. Виключення становлять лише деякі нормальні тканини, які слабко забезпечуються кров'ю, наприклад, кришталик і роговиця ока, і злоякісні пухлини тварин. У білих м'язах риб і домашніх птахів аеробний метаболізм також відносно невеликий, і основним кінцевим продуктом гліколізу є молочна кислота. В умовах великого фізичного навантаження в м'язах виснажуються запаси кисню і накопичується молочна кислота. Незначна частина молочної кислоти надходить у кров і переноситься в печінку, де вона знову окисляється в піровиноградну кислоту, яка у процесі глюконеогенезу перетворюється в глюкозу або глікоген. Глюкоза з токовищем крові вертається в м'язи, де з неї синтезується глікоген. Цикл глюкози й молочної кислоти має назву циклу Корі. Однак у м'язах тварин і людини він здійснюється лише в дуже обмежених масштабах. Установлено, що в стані спокою в м'язах відбувається перетворення молочної кислоти в глікоген. Цикл Корі має значення для тих тканин, де відбувається анаеробний обмін.
Глюконеогенезом називають синтез глюкози і глікогену із сполук невуглеводної природи. Основними субстратами глюконеогенезу служать лактат, гліцерин і амінокислоти. Лактат під дією лактатдегідрогенази перетворюється в піруват, з якого утворюється фосфоенолпіруват. Включення в глюконеогенез гліцерину, який утворюється при розпаді жирів, відбувається через його фосфорилювання і наступне перетворення в гліцерофосфат і далі в гліцеральдегід-3-фосфат і диоксиацетонфосфат. Всі амінокислоти, за винятком лейцину, можуть служити попередниками фосфоенолпіровиноградної кислоти, а отже глюкози і глікогену. Головними попередниками пірувату і фосфоенолпірувату є проміжні продукти циклу трикарбонових кислот (циклу Кребса).
Більшість реакцій глюконеогенезу - це зворотні реакції гліколізу. Однак три реакції гліколізу практично незворотні: піруваткіназна, фосфофруктокіназна і гексокіназна. Обхід піруваткіназної реакції відбувається у два етапи. Спочатку піровиноградна кислота карбоксилюєтся в щавлево-оцтову кислоту (оксалоацетат). Реакція каталізується піруваткарбоксилазаю і супроводжується гідролізом АТФ. В активному центрі ферменту перебуває міцно приєднаний ковалентним зв'язком біотин (вітамін Н). Для активації піруваткарбоксилази тваринних тканин необхідний ацетил-КоА.
1 .
Пируват + СаО2
+ АТФ+Н2О
Оксалоацетат + АДФ + Рнеорг
.
Пируват + СаО2
+ АТФ+Н2О
Оксалоацетат + АДФ + Рнеорг
Потім оксалоацетат під дією фосфоенолпіруваткарбоксикінази декарбоксилюється і фосфорилюється за рахунок ГТФ (гуанозинтрифосфату) або ІТФ (інозинтрифосфату) з утворенням фосфоенолпірувату.
2 .
Оксалоацетат + ГТФ
фосфоенолпіруват + З02
+ ГДФ
.
Оксалоацетат + ГТФ
фосфоенолпіруват + З02
+ ГДФ
Обхід наступних двох реакцій гліколізу досягається шляхом гідролітичного розщеплення фосфорноефірних зв'язків у фруктозо-1,6-дифосфаті і в глюкозо-6-фосфаті під дією специфічних фосфатаз (фруктозодифосфатази і глюкозо-6-фосфатази відповідно). У результаті цих реакцій утворюється неорганічний фосфат, фруктозо-6-фосфат і глюкоза:
 Фруктозо-1,6-дифосфат
+ H2О
Фруктозо-6-фосфат + Рнеорг,
Фруктозо-1,6-дифосфат
+ H2О
Фруктозо-6-фосфат + Рнеорг,
Г люкозо-6-фосфат
+ H2О
Глюкоза + Рнеорг.
люкозо-6-фосфат
+ H2О
Глюкоза + Рнеорг.
Рівняння сумарного процесу глюконеогенезу:
2 Лактат
+ 6АТФ Глюкоза + 6АДФ+ 6Рнеорг.
Лактат
+ 6АТФ Глюкоза + 6АДФ+ 6Рнеорг.
АТФ споживається в реакціях, які каталізуються піруваткарбоксилазою, фосфоенополпіруваткарбоксиназою і фосфогліцераткіназою.
Глюкозо-6-фосфатаза активна в печінці. Глюкоза, яка утворюється із глюкозо-6-фосфату, надходить із печінки в кров і доставляється в інші тканини. Один з механізмів регуляції вмісту глюкози в крові реалізується через інгібірування глюкозо-6-фосфатази продуктом реакції - глюкозою.
У м'язах глюкозо-6-фосфатаза не виявлена. У них відбувається перетворення глюкозо-6-фосфату під дією фосфоглюкомутази в глюкозо-1-фосфат і далі в уридиндифосфатглюкозу, яка служить субстратом для глікогенсинтази:
 УДФ
глюкоза + (І,4-а-D-глюкозил)n
УДФ+(1,4-
а-D-глюкозил)n+1.
УДФ
глюкоза + (І,4-а-D-глюкозил)n
УДФ+(1,4-
а-D-глюкозил)n+1.
Уридинтрифосфат (УТФ) регенерується за рахунок АТФ:
 УДФ
+ АТФ УТФ + AДФ.
УДФ
+ АТФ УТФ + AДФ.
У регуляції активності глікогенсинтази і глікогенфосфорилази в печінці й м'язах бере участь ряд гормонів - адреналін , глюкагон, інсулін, гідрокортизон - і ряд метаболітів.
Звертає на себе увагу центральна роль глюкозо-6-фосфату в обміні вуглеводів. Він утворюється із глюкози або глікогену, і подальші його перетворення можуть протікати за чотирма різними метаболічними шляхами:
1. Шляхом синтезу глікогену через перетворення в глюкозо-1-фосфат;
2. Шляхом гліколізу через перетворення у фруктозо-6-фосфат;
3. Гідроліз до глюкози і фосфорної кислоти під дією глюкозо-6-фосфатази;
4. За пентозофосфатним шляхи через окиснювання в 6-фосфоглюконову кислоту.
Далі варто перейти до розгляду пентозофосфатного шляху перетворення вуглеводів (його також називають фосфоглюконатним шляхом, або гексозомонофосфатним циклом, або пентозним циклом). Для ряду тваринних і рослинних тканин і деяких мікроорганізмів доведена можливість прямого окиснювання глюкозо-6-фосфата з відщіпленням вуглекислого газу й утворенням рибулозо-5-фосфату, який ізомеризується в рибозо-5-фосфат :
1

 .
Глюкозо-6-фосфат
6-фосфоглюконолактон.
.
Глюкозо-6-фосфат
6-фосфоглюконолактон.
НАДФ+ НАДФ Н+
2 .
6-фосфоглюконолактон + H2O
6-фосфоглюконова кислота.
.
6-фосфоглюконолактон + H2O
6-фосфоглюконова кислота.
3

 .
6-фосфоглюконова кислота
Рибулозо-5-фосфат + СО2
.
6-фосфоглюконова кислота
Рибулозо-5-фосфат + СО2
НАДФ+ НАДФ Н+
На цьому закінчується окисний етап пентозофосфатного шляху перетворення вуглеводів. Наступні реакції пентозофосфатного шляху відносяться до неокиснювального етапу:
4. Перетворення однієї молекули рибулозо-5-фосфату в рибозо-5-фосфат під впливом ізомерази і перетворення іншої молекули рибулозо-5-фосфата в ксилулозо-5-фосфат, яке каталізується епімиразою.
5. Перша транскетолазна реакція – перенос глікольальдегідної групи від ксилулозо-5-фосфату на рибозо-5-фосфат. Утворюється гліцеральдегид-3-фосфат і седогептулозо-7-фосфат. Коферментом транскетолази служить тіамінпірофосфат - фосфорильоване похідне вітаміну B1.
6. Фермент трансальдолаза каталізує перенос диоксиацетонової групи від седогептулозо-7-фосфата на гліцеральдегід-3-фосфат з утворенням еритрозо-4-фосфату і фруктозо-6-фосфату відповідно.
7. Друга транскетолазна реакція - перенос глікольальдегідної групи від ксилулозо-5-фосфату на еритрозо-4-фосфат. У результаті цієї реакції утворюється гліцеральдегід-3-фосфат і фруктозо-6-фосфат. На цій стадії пентозофосфатний шлях може перейти в гліколітичний. Перетинання метаболічних шляхів може відбутися й раніше на рівні утворення фруктозо-6-фосфату в трансальдолазній реакції й на рівні першої транскетолазної реакції, коли утворюється гліцеральдегід-3-фосфат - загальний проміжний продукт пентозофосфатного шляху перетворення вуглеводів і гліколізу.
Можливе і повне окиснення глюкозо-6-фосфату ферментами пентозофосфатного шляху: з 6 молекул глюкозо-6-фосфату утворюється 6 молекул рибулозо-5-фосфату і 6 молекул СО2. Потім 6 молекул рибулозо-5-фосфату через ряд проміжних реакцій знову перетворюються в 5 молекул глюкозо-6-фосфату. Рівняння сумарної реакції:
 6Глюкозо-6-фосфат
+ 12НАДФ+
5 Глюкозо-6-фосфат + 6СО2
+
6Глюкозо-6-фосфат
+ 12НАДФ+
5 Глюкозо-6-фосфат + 6СО2
+
12 НАДФ + 12Н+ + Рнеорг.
У підсумку одна молекула глюкозо-6-фосфата повністю окислюється до вуглекислого газу, води і неорганічного фосфату.
Значення пентозофосфатного шляху складається, по-перше, у тім, що утворюються важливі метаболіти, у тому числі рибозо-5-фосфат, необхідний для синтезу нуклеїнових кислот. По-друге, утворюється відновлений НАДФН, використовуваний для процесів біосинтезу жирних кислот, холестерину, стероїдних гормонів і для інших відбудовних процесів. Пентозофосфатний шлях особливо важливий для тих органів і тканин, у яких ці синтези йдуть найбільше активно - для печінки, молочної залози, жирової тканини, кори наднирників, еритроцитів, лімфатичних вузлів і для деяких інших тканин.
У хлоропластах рослин і в деяких бактерій пентозофосфатний шлях функціонує у зворотньому напрямку – відновлюючий пентозофосфатний шлях, відомий за назвою циклу Кальвіна, який складається з реакцій пентозофосфатного і гліколітичного шляхів. Реакції пентозофосфатного шляху є ключовими в процесі фотосинтезу, які приводять до утворення цукрів.
Піровиноградна кислота - проміжний продукт гліколізу і обміну деяких амінокислот, а також гліцерину, який входить до складу жирів, у аеробних умовах окислюється до вуглекислого газу і води. Процес починається з окисного декарбоксилювання піровиноградної кислоти. Реакція каталізується піруватдегидрогеназою - мультиферментним комплексом з молекулярною вагою порядком декількох мільйонів і локалізованим у мітохондріях. До складу комплексу входять три ферменти - піруват декарбоксилаза, ліпоїлтрансацетилаза, ліпоїлгідрогеназа і п'ять коферментів (тіамінпірофосфат, ліпоєва кислота, коензим А, ФАД і НАД).
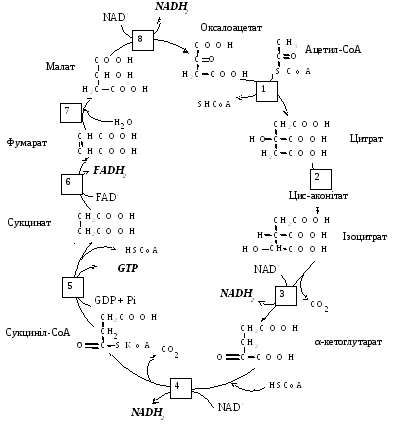
У результаті послідовно протікаючих реакцій, з піровиноградної кислоти утворюються вуглекислий газ і ацетил-КоА, який конденсується із щавлево-оцтовою кислотою й вступає в цикл трикарбонових кислот (цикл Кребсу, лимоннокислий цикл). При одному обороті циклу відбувається повне окиснення однієї ацетильної групи до вуглекислого газу і води.
Використання проміжних продуктів циклу трикарбонових кислот для біосинтезів поповнюється за рахунок анаплеротичних (які відшкодовують, або наповнюють) реакцій. Такою реакцією, найбільш важливої для клітин печінки і нирок, є піруваткарбоксилазна реакція. Піруваткарбоксилаза каталізує карбоксилювання пірувату з утворенням оксалоацетату. Роль потужного алостеричного активатора піруваткарбоксилази грає ацетил-КоА. У його відсутність фермент практично неактивний.
У м'язовій тканині й серці анаплеротичними реакціями служать дві зворотні реакції, які каталізуються фосфоенолпіруваткарбоксилазою (1) і малат-ферментом (2):
1 .
Фосфоенолпіруват + СО2
+ ИДФ Оксалоацетат + ИТФ.
.
Фосфоенолпіруват + СО2
+ ИДФ Оксалоацетат + ИТФ.
2 .
Малат + НАДФ+
Піруват + СО2
+ НАДФН • Н+.
.
Малат + НАДФ+
Піруват + СО2
+ НАДФН • Н+.
Оксалоацетат, який утворюється в анаплеротичних реакціях використовується в циклі трикарбонових кислот, у глюконеогенезі і в утворенні аспарагінової кислоти. З іншого боку, надлишок оксалоацетату в мітохондріях діє як конкурентний інгібітор сукцинатдегідрогенази. Відбувається блокування циклу трикарбонових кислот на етапі окиснення бурштинової кислоти доти, доки приток додаткової кількості ацетил-КоА не приведе до видалення надлишку оксалоацетату в цитратсинтазній реакції.
Цикл трикарбонових кислот займає ключове положення в обміні речовин. Швидкість циклу лімітується активністю ізоцитратдегідрогенази - алостеричного ферменту, специфічним активатором якого служить АДФ, а інгібіторами - АТФ і НАДН.
До регуляторних ферментів циклу трикарбонових кислот відноситься і цитратсинтаза - алостеричний фермент, каталізуючий першу реакцію циклу (конденсації ацетил-КоА із щавлево-оцтовою кислотою). Цей фермент також інгібується кінцевими продуктами циклу - АТФ і НАДН. Інгібірування знімається АДФ і АМФ. Накопичення в мітохондріях цитрату і вихід його в цитоплазму приводить до інгібірування початкових стадій гліколізу (інгібірування фосфофруктокінази) і до прискорення синтезу жирних кислот шляхом активації ацетил-КоА-карбоксилази. Ізоцитрат поряд із цитратом активує ацетил-КоА-карбоксилазу. Надлишок цитрату в цитоплазмі розпадається під дією цитратліази з утворенням оксалоацетату і ацетил-КоА. Останній використовується для синтезу жирних кислот.
Можливі і інші різноманітні механізми регуляції циклу трикарбонових кислот відповідно до енергетичних і біосинтетичних потреб клітини. Складна система регуляції циклу трикарбонових кислот забезпечує необхідний у нормальних умовах баланс надходження і споживання проміжних продуктів циклу, щоб не було ні надлишку, ні недоліку в них. При деяких станах, наприклад, при голодуванні, баланс порушується, тому що в результаті посиленого розпаду жирів у тканинах накопичується ацетил-КоА, з'являється надлишок ацетоацетату й інших "кетонових тіл". Це веде до виникнення патологічного стану, який має назву кетоз. Надмірне зниження змісту вуглеводів у їжі й патологічні порушення вуглеводного обміну (діабет) також приводять до кетозу.
Найбільш важливим для розуміння питань біоенергетики є наступне положення. При окисних перетвореннях окремих членів циклу трикарбонових кислот (ізолімонної, а-кетоглутарової, бурштинової й яблучної кислот) звільняється лише незначна кількість енергії, причому в фосфорильних залишках АТФ вона акумулюється тільки при окисному декарбоксилюванні а-кетоглутарової кислоти. Окиснення ж інших субстратів не супроводжується синтезом АТФ і звільненням помітної кількості енергії. Основна маса енергії звільняється при транспорті протонів і електронів від субстратів, які окислюються, на молекулярний кисень (при тканьовому подиху). Тому, перш ніж закінчити розгляд обміну вуглеводів, рекомендуємо розібратися в сучасній теорії тканьового подиху, викладеного в підручниках.
