
- •Рубежный контроль № 2
- •Лечебно-профилактический, медико-профилактический, педиатрический,
- •19. Кофермент надн участвует в реакциях:
- •20. Какое из перечисленных ниже соединений образуется при взаимодействии пиридина йодистым метилом при нагревании:
- •I. Запишите уравнения химических реакций:
- •II. Составьте цепочки превращений:
- •III. Запишите химические уравнения качественных реакций:
- •IV. Сравните кислотные свойства карбоновых кислот:
- •Основная:
ГОУ ВПО УГМА РОСЗДРАв
кафедра биохимии
“Утверждаю”
Зав. каф. проф., д.м.н.
Мещанинов В.Н.
_____ “ ____________ 2008 г.
Биоорганическая химия
Рубежный контроль № 2
Темы : механизмы реакций, карбоновые кислоты, гетерофункциональные
карбоновые кислоты ( гидрокси-. оксо-. амино-), липиды, белки Факультеты:
Лечебно-профилактический, медико-профилактический, педиатрический,
1 курс. 1 семестр
Для успешной подготовки к рубежному контролю № 2
Студентам надо знать
1. ответы на вопросы, которые входят в программу « Вопросы к экзамену» по биоорганической химии ( см. раздел «Вопросы для подготовки»
2. тривиальные названия и структурные формулы всех нижеперечисленных
соединений, уметь соотнести пары: формула- название, название-формула:
1) Аминокислоты ( 20 наименований, оптические изомеры, разделение на заменимые, незаменимые )
2) Карбоновые кислоты
А).Монокарбоновые : акриловая, уксусная, муравьиная, пропионовая, масляная,
валериановая, пальмитиновая, стеариновая, олеиновая, элаидиновая, линолевая,
линоленовая, арахидоновая, кротоновая, сорбиновая.
Б).Дикарбоновые : щавелевая. малоновая, янтарная,. адипиновая, малеиновая,
фумаровая.
В) Гидроксикислоты: гликолевая, молочная. яблочная, 3-гидроксимасляная,
лимонная изолимонная.
Г) Оксокислоты : пировиноградная , щавелевоуксусная, альфа-кетоглутаровая, бета-
оксомасляная ( в двух таутомерных формах-енольной и кетоновой).
Студенты должны уметь
-
составить формулы триглицеридов в соответствии с приведенным названием, например, 1-олео, 2-пальмитоил, 3-стеарин.
-
составить формулы кефалина и лецитина, содержащих заданный набор высших карбоновых кислот (в соответствии с правилом их расположения в природных фосфатидах- в положении 1- насыщенная кислота, в положении 2 –ненасыщенная кислота).
3. составить формулы трипептидов ( из заданного набора аминокислот) , опре-
делить область рI, заряд в нейтральной, кислой, щелочной среде).
1. ВОПРОСЫ ДЛЯ ПОДГОТОВКИ:
|
1 |
Типы разрыва химической связи и типы реагентов. Классификация механизмов реакции в биоорганической химии. |
|
2 |
Радикалы. Определение понятия Активные формы кислорода.. Свободно-радикальное окисление жирных кислот и его роль в патологии клетки Механизм реакции радикального замещения в ряду алканов. |
|
3 |
Механизмы реакции электрофильного присоединения (AE)- реакции гидратации, гидрогалогенирования, дигалогенированияв ряду алкенов. Влияние электронодонорных и электроноакцепторных заместителей на направленность реакции AE в алкенах. Значение реакции гидратации в биохимических процессах. Механизм реакции электрофильного замещения в ароматических соединениях (бензол и его замещенные) |
|
4 |
Механизм реакций нуклеофильного присоединения к карбонильных соединений (ANU). Нуклеофильные реагенты - вода, спирты, циановодород, тиолы, амины. Электронное строение карбонильной группы. Биологически важные реакции нуклеофильного присоединения в клетке (образование полуацеталей, тиополуацеталей, азометинов). |
|
5 |
Реакции нуклеофильного замещения и элиминирования. Конкурентный характер процессов. Условия реакций дегидратации и дегидрогалогенирования. Значение реакций дегидратации в биохимических процессах .Механизм реакции нуклеофильного присоединения-отщепления в ряду карбоновых кислот. Образование производных карбоновых кислот и их биологическое значение (сложные эфиры, амиды, ангидриды, тиоэфиры - активные формы карбоновых кислот в клетке) АцетилКоА. |
|
6 |
Окисление спиртов, тиоспиртов и альдегидов. Особенности окисления –SH и –ОН групп. Значение SH групп в биологических системах. |
|
7 |
Участие НАД+ в окислительно-восстановительных реакциях. Механизм реакции, гидридный перенос |
|
8 |
Природные аминокислоты. Особенности структурного и пространственного строения. Классификация аминокислот. Заменимые и незаменимые аминокислоты. Кислотно-основные свойства аминокислот. Изоэлектрическая точка нейтральных, кислых и основных аминокислот Образование солей при взаимодействии с кислотами и основаниями. |
|
9 |
Биологически важные реакции аминокислот в клетке: декарбоксилирование, дезаминирование, (переаминирование, окислительное дезаминирование глутаминовой кислоты), образование амидов (глн, асн). Биологическая роль реакций декарбоксилирования на примере аминокислот: гис, три, сер, цис, глу, асп. |
|
10 |
Белки. Определение понятия. Классификация белков. Биологическая роль белка. Современные методы исследования структуры белка. |
|
11 |
Полипептиды: строение, образование. Электронное и пространственное строение пептидной связи. Качественная реакция на пептидную связь. |
|
12 |
Пространственная организация белковой молекулы: первичная, вторичная, третичная структура. Типы связей. Биологическая роль белка. |
|
13 |
Структурные формулы трипептидов, состоящих из природных аминокислот (например: ала-глу-тир). Химическая реакция, доказывающая присутствие аминокислоты тирозина в пептиде. Определение области изоэлектрической точки трипептида. |
|
14 |
Явление денатурации белка. Определение понятия. Факторы, вызывающие денатурацию белка. Механизм денатурации. Медико-биологические аспекты изучения этой проблемы. |
|
15 |
Мочевина. Строение. Химические свойства. Реакция гидролиза. Образование биурета. Качественная реакция обнаружения биурета. Биологическая роль мочевины. |
|
16 |
Липиды. Определение понятия. Классификация липидов. Биологическое значение отдельных представителей. |
|
17 |
Высшие жирные кислоты: насыщенные и ненасыщенные. Строение, свойства, биологическая роль. Заменимые и незаменимые жирные кислоты, витамин F. Содержание в пищевых продуктах. |
|
18 |
Триглицериды: строение, образование. Гидролиз (омыление) триглицеридов. Биологическая роль триглицеридов в клетке. |
|
19 |
Фосфатидилхолины (лецитины): состав, строение, биологическое значение. Гидролиз лецитина. |
|
20 |
Фосфатидилэтаноламин и фосфатидилсерин. Строение. Гидролиз. Биологическое значение. |
|
21 |
Холестерин и его эфиры. Строение. Качественная реакция на холестерин. Биологическая роль холестерина. |
|
22 |
Биологически важные гидрокси- и оксокислоты. Химические свойства. Оптическая изомерия гидроксикислот. Кето-енольная таутомерия оксокислот, строение фосфоенолпирувата, биологическая роль. Биологическое понятие: кетоновые тела. Состав и строение. |
2. ТЕСТОВЫЕ ЗАДАНИЯ
Тестовые задания являются одним из объективных способов оценки знаний и
удобны для самоконтроля и самопроверки усвоения темы.
Обращаем внимание,
что эти тестовые задания были на практических занятиях, поэтому при подготовке к рубежному контролю ответы следует составить самостоятельно
Если нет особого указания, выберите один ответ.
Тема: Механизмы реакций в биоорганической химии. Реакции биологического окисления
1. Распределите карбкатионы в порядке возрастания устойчивости:
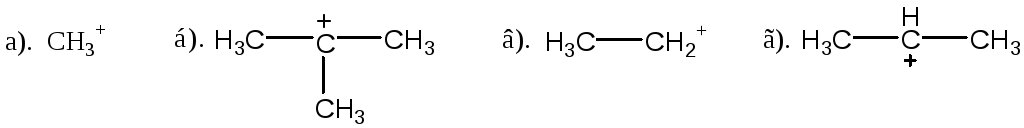
2. Выберите нуклеофилы:
а). С6Н5 б). NH2 в). H2O г). OН- д). H+ е). С2Н6 ж). Cl+ з). NH3
3. Выберите электрофилы:
а). Br- б). RO- в). Br+ г). H3O+ д). SO3 е). C2H4 ж). CN-
4. Устойчивость карбокатиона увеличивается, если в составе иона имеются:
а). заместители, проявляющие +J и +M – эффект;
б). заместители, проявляющие -J и -M – эффект;
в). заместители, проявляющие -J – эффект;
г). любые заместители, независимо от характера эффекта;
д). все суждения неверны
5. Распределите в ряд по увеличению реакционной способности в реакции АЕ вещества:
а). бутен-1 б). пропен в). пропеновая кислота г). этен
6. Одно из пяти веществ гидратируется в растворе на 98%, а остальные значительно меньше. Выберите это вещество:
а). ацетальдегид
б). ацетон
в). формальдегид
г). масляный альдегид
д). бутанон
7. Имины (основания Шиффа) образуются при взаимодействии альдегидов и кетонов с веществом:
а). спиртом
б). галогеноводородом;
в). амином
г). циановодородом;
д). тиолом (меркаптаном)
8. Какие из нижеперечисленных соединений вступают в реакцию АЕ против правил Марковникова?
а). CH2 =CН-CH3
б). CH2 =CН-CООH
в). CH2 =CН-CN
г). CH2 = CH-Сl
9. Напишите уравнения химических реакций, которые относятся к ANU
водн. р-р
а). C2H5J + NaCl → в). C4H7Br + KOH →
б). C2H5-СНО + C2H5ОН → г). C6H5ОNa + CH3J →
10. Какие из перечисленных веществ реагируют с карбонильной группой альдегидов?
а). Н-Cl б). CH3-Cl в). H-OH г). C6H5-NH2 д). H-CN е). C2H5-SH
11. Какие из нижеперечисленных соединений вступают в реакцию АЕ по правилу Марковникова?
а). CH2 =CН–CH3
б). CH2 =CН–CООH
в). CH2 =CН–CN
г). CH2 = CH–С1
12. Выберите тип реакции гидратации пропена:
а). АЕ б). АN в). Е г). SN д). SE
13. Распределите в ряд по уменьшению реакционной способности в реакции АЕ вещества:
а). бутен-2; б). пропен; в). пропеновая (акриловая) г). этен
14. Взаимодействие ацетальдегида с анилином приводит к образованию устойчивого продукта:
а). CH3-СН=N-С6Н5
б). CH3-N=СH-С6Н5
в). CH3-NН-CН(OH)-С6Н5
г). CH3-NН-СH2-С6Н5
д). CH3-N(ОН)–CН2-С6Н5
15. Выберите соединение, которое образуется при взаимодействии ацетона с метанолом:

16. Кофермент НАД+ образован на основе водорастворимого витамина:
а). РР б). Р в). С г). В2 д). В1 е). В6
17. В составе кофермента НАД+ имеется гетероциклическое соединение:
а). пиррол
б). пиримидин
в). пиридин
г). имидазол
д). тиофен
18. Кофермент НАД + участвует в реакциях:
а). дегидрирования
б). гидрирования
в). гидратации
г). гидролиза
д). дегидратации
