- •Кафедра химической технологии переработки
- •Органическая химия
- •Москва, 2007
- •Введение
- •1. Основные теоретические положения органической химии
- •1.1. Классификация органических соединений
- •Органические соединения
- •Важнейшие классы органических соединений.
- •Названия наиболее часто встречающихся радикалов:
- •1.2. Номенклатура
- •1.3. Электронное строение σ- и π- связей Три типа гибридизации атомов углерода
- •1.5 Типы органических реакций
- •1.6. Механизмы химических реакций
- •Рост стабильности радикалов
- •Стабильность третичного иона карбония выше, т.К. Частичный положительный заряд на атоме углерода нейтрализуется индукционным эффектом наибольшего числа радикалов.
- •2. Алканы
- •Химические свойства
- •Алкены Общая характеристика
- •Химические свойства
- •Реакции присоединения (а)
- •4. Диеновые углеводороды (алкадиены или диолефины)
- •Химические свойства дивинила и его гомологов Реакции присоединения
- •Диеновые синтезы (синтезы Дильса-Альдера)
- •Реакции полимеризации
- •5. Алкины (непредельные углеводороды ряда ацетилена )
- •Реакции присоединения
- •Реакции окисления
- •Реакции замещения
- •6. Алициклические соединения
- •6.1 Химические свойства
- •6.2. «Теория напряжения» Байера
- •6.3. Пространственное расположение атомов углерода в циклопарафинах.
- •Оптическая изомерия
- •7. Ароматический ряд. Арены
- •7.1. Строение бензола
- •7. 2. Критерии ароматичности. Определение принадлежности вещества к ароматическим соединениям
- •7.3. Химические свойства бензола
- •Реакции электрофильного замещения se
- •Механизм реакции электрофильного замещения
- •Влияние заместителей I-п рода на реакционную способность кольца и ориентацию при реакциях электрофильного замещения (sе)
- •Заместители I рода орто- и пара-ориентанты
- •Заместители п рода -мета ориентанты
- •8. Галогенопроизводные углеводородов
- •Галогенопроизводные предельных углеводородов (галогеналкилы)
- •Химические свойства
- •Галогенопроизводные непредельных углеводородов
- •Ароматические галогенопроизводные
- •Влияние заместителей в кольце на реакционную способность галогена
- •9. Кислородсодержащие соединения
- •9.1. Спирты Спирты алифатического ряда.
- •Реакции гидроксильного водорода.
- •Реакции гидроксила
- •Окисление
- •Одноатомные непредельные спирты
- •Химические свойства
- •Взаимодействие со щелочами
- •Реакции электрофильного замещения se
- •Влияние заместителей на кислотные свойства фенолов
- •Ароматические спирты
- •9.2 Альдегиды и кетоны
- •Альдегиды и кетоны алифатического ряда Общая характеристика
- •Влияние акцепторных групп
- •Окисление альдегидов и кетонов
- •Реакции конденсации (уплотнения)
- •Механизм реакции
- •Непредельные альдегиды и кетоны
- •Основные химические реакции
- •Ароматические альдегиды и кетоны
- •9.3 Карбоновые кислоты Карбоновые кислоты алифатического ряда Общая характеристика
- •Основные химические реакции
- •Непредельные карбоновые кислоты.
- •Свойства кислот
- •Двухосновные или дикарбоновые кислоты (предельные и непредельные).
- •Ароматические карбоновые кислоты
- •Кислотные свойства
- •Реакция этерификации
- •10. Нитросоединения Нитросоединения алифатического ряда r - nо2
- •Нитросоединения с нитрогруппой в боковой цепи
- •11. Аминосоединеиия
- •Ароматические амины Общая характеристика
- •Влиянение заместителей на основные свойства аминов Акцепторный заместитель уменьшает основность
- •Реакции электрофильного замещения (sе)
- •12. Диазосоединения
- •Реакция диазотирования
- •Реакции солей диазония без выделения азота
- •Реакция сочетания с фенолом и ароматическими аминами
- •Влияние заместителей на реакцию азосочетания
- •13. Азосоединения
- •14. Вопросы для подготовки к зачету
- •Тема 1. Электрофильное и радикальное присоединение и замещение у алкенов. Элиминирование.
- •Тема 2. Нуклеофильные и радикальные (галогенирование, нитрование) реакции у насыщенного атома углерода
- •Тема 3. Окислительно-восстановительный процесс и дегидрирование
- •Тема 4. Электрофильное замещение в ароматических соединениях. Правила ориентации
- •Тема. 5. Нуклеофильное замещение у ароматических соединений. Кислотно-основные свойства органических соединений
- •Тема 6. Полимеризация, конденсация, поликонденсация. Диазосоединения и синтезы на их основе
- •15. Список рекомендуемой литературы Основной
- •Дополнительный
Галогенопроизводные непредельных углеводородов
Галогенопроизводные непредельных углеводородов делят на две группы: первая включает в себя соединения, у которых галоген отделен от атома углерода с двойной связью одним или более атомами углерода CH2=CH–(CH2)n–Cl.
Эти соединения имеют такую же реакционную способность, как и галогенопроизводные предельных углеводородов. Однако в соединениях, где между атомами галогена и углерода при двойной связи стоит только одна группа -СН2 , например:
CH2 = CH – CH2Cl (хлористый аллил), галоген наиболее подвижен. Этот галоген замещается в более мягких условиях, чем в случае галогенопроизводных предельных углеводородов. Такую активность галогена связывают с большой устойчивостью карбкатиона, заряд которого компенсирован π-электронами двойной связи:

Мезомерный карбкатион
Мезомерный карбкатион имеет плоское строение; атака его нуклеофилом возможна с двух сторон плоскости, поэтому реакция нуклеофильного замещения у хлористого аллила протекают по механизму SN1, т.е. значительно легче, чем для третичных и вторичных алкилгалогенидов. Протекание реакции по механизму SN2 в данном случае затруднено, так как π- электронное облако двойной связи мешает молекуле нуклеофила образовать с хлористым аллилом переходное состояние.
Вторая
группа
объединяет соединения, в которых
галоген непосредственно связан с
атомом углерода, имеющим двойную связь.
Например, CH2
=
CHCl
хлористый
винил, хлорбензол
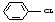 .
.
В таких соединениях галоген очень малоподвижен. Это объясняется взаимным влиянием двойной связи и атома галогена друг на друга. В случае винилхлорида происходит взаимодействие π - электронной системы двойной связи со свободными электронными парами атома галогена, которые смещаются при этом в сторону двойной связи (+М -эффект сопряжения):
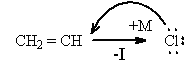
В то же время атом галогена за счет индуктивного эффекта (-I) оттягивает на себя π - электроны соседней связи. Эти два эффекта действуют в противоположных направлениях, и общее распределение электронной плотности в молекуле хлористого винила отражается мезомерной формулой:
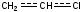
При этом связь между углеродом и галогеном приобретает в известной степени характер двойной связи, ее длина укорачивается (от 1,78 до 1,72 А°). Все это приводит к повышению энергии связи С-Х, уменьшению ее поляризации и понижению реакционной способности атома галогена. Образование карбкатиона затруднено и реакции по механизму SN1, проходить не могут. Реакции, протекающие по механизму SN2, также затруднены, так как затруднен подход нуклеофила к атому углерода в молекуле.
Ароматические галогенопроизводные
Хлор в хлорбензоле можно заменить на ОН- и NН2- группы только в очень жестких условиях (давление, высокая температура). Например:
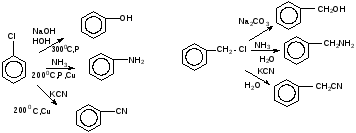
Инертность
галогена, стоящего непосредственно в
ядре, можно объяснить сопряжением
свободных электронов атома хлора с π-
электронами
ароматического кольца. В результате
этого электронная
плотность
в кольце повышается
и
подход (Nu:)
нуклеофильной
частицы
к атому углерода будет
затруднен.
Как
и в хлорвиниле, в хлорбензоле атом хлора
частично двоесвязан с
ядром,
что приводит к укорачиванию связи С–С1
. Проведем сравнение
длины
связи в некоторых соединениях: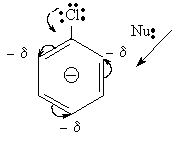
I П Ш

Вывод: если галоген находится непосредственно при двойной связи (I, III) наблюдается укорачивание связи С - С1. Это приводит к более полному перекрыванию облаков, увеличению прочности связи и понижению реакционной способности атома галогена с нуклеофильными реагентами. Механизм реакции в этом случае протекает через стадию образования очень реакционноспособного промежуточного продукта, называемого дегидробензолом :
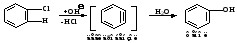
Веским доказательством в пользу именно такого механизма замещения галогена в ароматическом ряду является тот факт, что входящая группа не всегда занимает положение, которое освобождает галоген. Так, например, гидролиз о-хлортолуола дает эквимолекулярную смесь о- и м- крезолов:
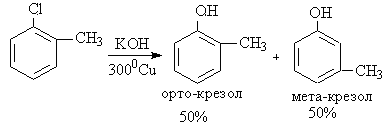
Это можно объяснить возможностью присоединения нуклеофильного реагента к метилдегидробензолу по тройной связи в двух направлениях: