
- •Карбоновые кислоты
- •Классификация карбоновых кислот:
- •Номенклатура. Рациональная: к названию
- •производят от соответствующего углеводорода, добавляя суффикс -овая, атом углерода карбоксильной группы
- •Названия кислот
- •Способы получения
- •-ЖЕСТКОЕ ОКИСЛЕНИЕ боковой
- •- ЖЕСТКОЕ ОКИСЛЕНИЕ СПИРТОВ:
- •2. Гидролиз геминальных трига-
- •3. Гидролиз нитрилов
- •4. Через металлоорганические соединения
- •ФИЗИЧЕСКИЕ СВОЙСТВА С1С9 - бесцветные жидкости.
- •Низшие члены гомологического ряда алифатических монокарбоновых кислот смешиваются с водой в любых пропорциях.
- •Химические свойства
- •Качественная реакция на карбоновые кислоты – реакция с содой → выделение углекислого газа
- •Химические свойства солей карбоновых кислот:
- •б) декарбоксилирование солей карбоновых кислот (см. алканы)
- •в) пиролиз солей Са и Ва
- •2) Реакции с разрывом связи С-ОН идут с образованием функциональных производных
- •1. Получение галогенангидридов.
- •Химические свойства галогенангидридов:
- •2. Получение ангидридов кислот : а) из кислот
- •б) из соли кислоты и галогенангидрида кислоты
- •Химические свойства ангидридов кислот:
- •3. Образование сложных эфиров.
- •б) реакции галогенангидридов кислот со спиртами
- •Химические свойства сложных эфиров – реакции гидролиза
- •4. Образование амидов кислот
- •б) Из ангидридов кислот:
- •Химические свойства амидов кислот:
- •2. Реакции по α-углеродному атому - идут с образованием замещенных кислот.
- •- Реакции по ароматическому кольцу- карбоксильная группа ориентант II рода.
- •Ароматические кислоты Бензойная кислота: содержится в клюкве, бруснике
- •Ненасыщенные кислоты
- •Метакриловая кислота – в
- •Двухосновные кислоты -
- •COOH COOH
- •Химические свойства: 1. Кислотные – образуют с
- •Терефталевая кислота
- •Высшие жирные кислоты Пальмитиновая- С15Н31СООН,
- •Жиры - сложные эфиры глицерина и высших кислот
- •Физические свойства: не имеют определенной Тпл, не растворимы в воде, с водой образуют
- •Химческие свойства:
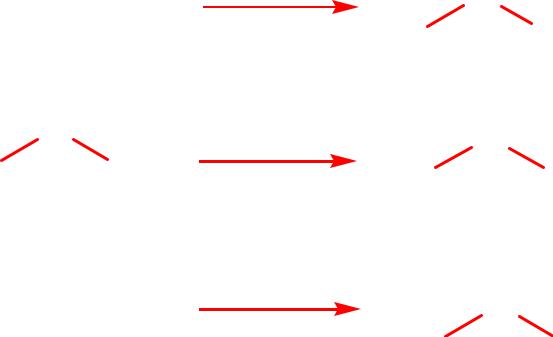
1. Получение галогенангидридов.
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
PBr3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3PO3 |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
С |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
O |
|
|
|
|
R |
Br |
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
PCl5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
С |
|
|
|
|
|
|
|
|
|
|
POCl3 |
|
|
|
HCl |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
R |
OH |
|
|
|
|
R |
Cl |
||||||||||||||||||||||||||
|
|
|
O |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
SOCl2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
SO2 |
|
|
|
|
HCl |
|||||
|
|
|
|
R |
|
|
С |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
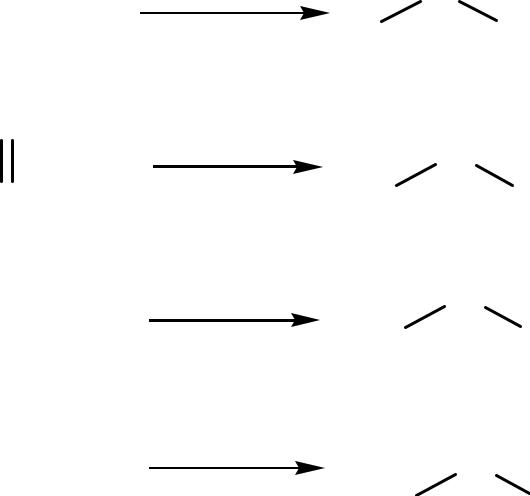
Химические свойства галогенангидридов:
O
R C
C Cl
Cl
аммиак и амины
|
|
|
|
|
|
|
|
O |
|
||||||
|
|
|
HOH |
|
|
|
|
гидролиз |
|||||||
|
|
|
R |
C |
|||||||||||
|
|
|
- HCl |
|
O |
OH |
|||||||||
|
|
|
|
||||||||||||
|
|
|
спирты |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
R'OH |
|
|
|
|
|
|
|
|
|
|||
|
|
|
R |
|
C |
OR' |
|||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
-HCl |
||||||||||||
|
|
соли спирта |
|
|
O |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
C6H5ONa |
|
|
|
|
|
|
||||||
|
|
|
|
|
C |
|
|||||||||
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
OC6H5 |
|
|
|
|
- NaCl |
|
|
|
O |
||||||||
|
|
|
NH3 |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
C |
|
|||||||||
|
|
|
- HCl |
R |
|
|
|
|
NH2 |
||||||
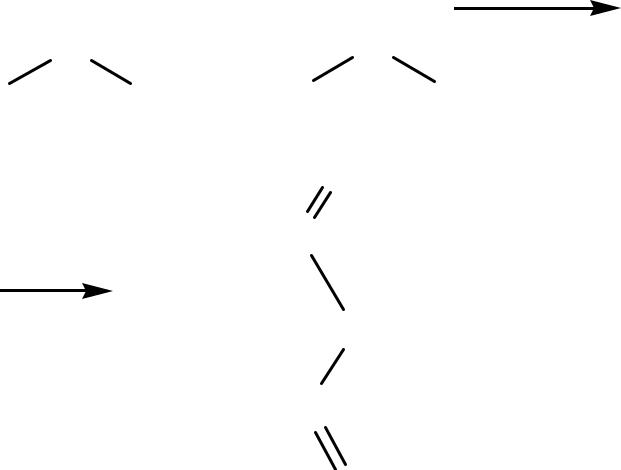
2. Получение ангидридов кислот : а) из кислот
|
O |
|
|
O |
|
P2O5,to |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-H |
O |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
H3C C OH HO C |
||||||||||||||||||
CH32 |
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|||
|
|
|
|
H3C |
|
|
|
C |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|||
|
|
|
|
H3C |
|
|
|
C |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|||
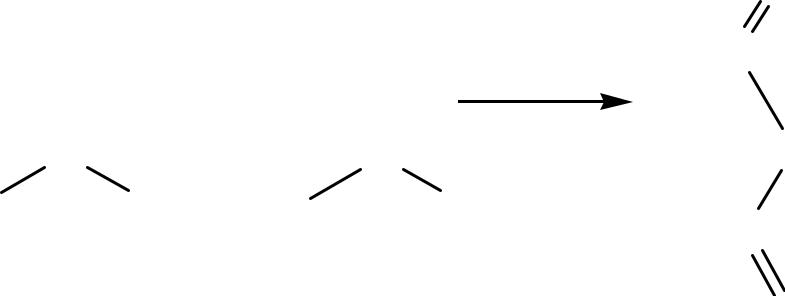
б) из соли кислоты и галогенангидрида кислоты
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
O |
|
|
O |
|
|
R |
|
C |
||||||||
|
|
|
|
|
||||||||||||
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-NaCl |
|
|
|
|
O |
R C ONa Cl |
C |
|
|
|
|
|||||||||||
R' |
|
|
|
|
||||||||||||
R' |
|
|
|
C |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
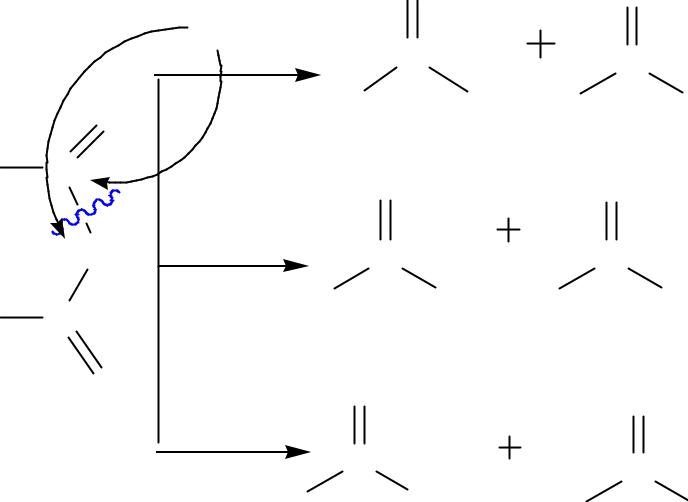
Химические свойства ангидридов кислот:
|
|
|
HOH |
O |
O |
|
|
|
|
|
C |
C |
|
||
|
|
|
|
|
|||
|
|
O |
|
R |
OH R |
OH |
|
R |
C |
|
|
O |
|
Oгидролиз |
|
|
|
O R'OH |
C |
OR' R |
C |
OH |
|
R |
C |
|
R |
||||
|
|
|
алкоголиз |
||||
|
|
O |
|
O |
|||
|
|
NH3 |
|
O |
|
||
|
|
|
C |
|
C |
|
|
|
|
|
R |
NH2 R |
OH |
||
аммонолиз
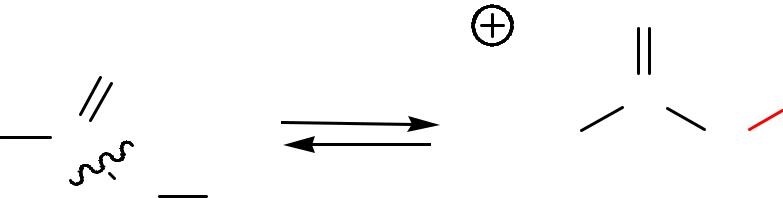
3. Образование сложных эфиров.
а) Реакция карбоновых кислот со спиртами, приводящая к сложным эфирам называется реакцией этерификации:
|
O |
R'OH H |
O |
||
R |
С O R' |
||||
С |
H - H2O |
R |
|||
|
O |
сложный эфир |
|||

б) реакции галогенангидридов кислот со спиртами
O O
R C Cl H OR1 -HCl R C OR1
НАЗВАНИЕ: АЛКИЛАЛКАНОАТ
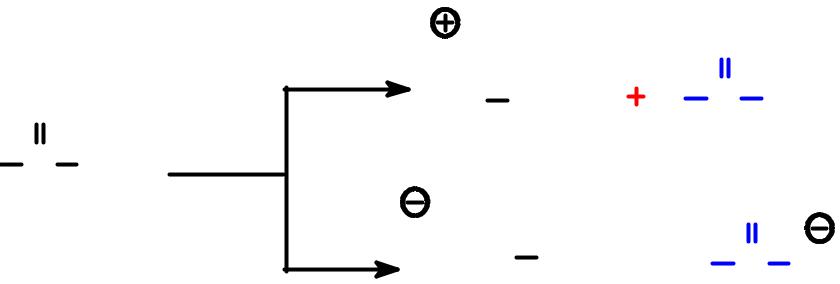
Химические свойства сложных эфиров – реакции гидролиза
|
H2O/H |
|
O |
|
O |
H OR1 |
R C OH |
||
|
||||
R C OR1 |
|
|
O |
|
|
H2O/ OH |
|
||
|
H OR1 + R C O |
|||
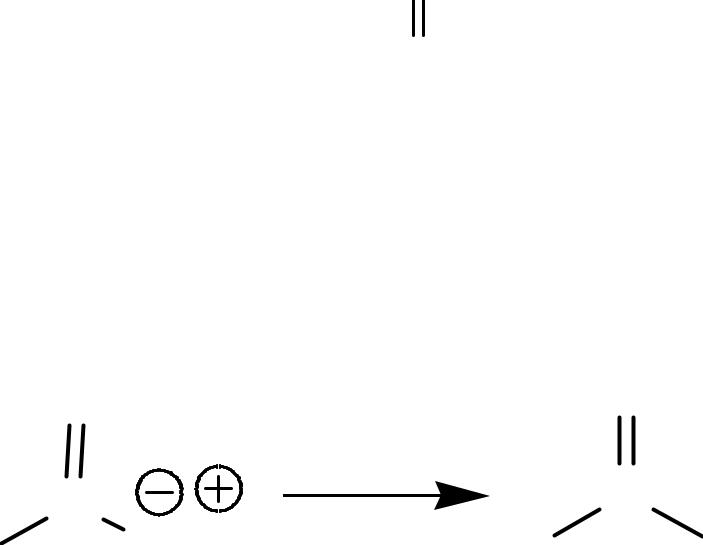
4. Образование амидов кислот
O
R C
C NH2
NH2
Название: амид соответствующей кислоты
а) дегидратация аммонийных солей до амидов (при нагревании)
O |
to |
O |
R C |
|
|
ONH4 - H2O R C NH2 |
||
б) Из ангидридов кислот:
O O
R C Cl2NH3 -NH4ClR C NH2
Cl2NH3 -NH4ClR C NH2
в) Гидролиз нитрилов:
O
R C N H2O/HR C NH2
