
- •54. Обратимые и необратимые процессы, круговой процесс, тепловые двигатели, холодильные машины.
- •55. Цикл Карно. Максимальный кпд тепловой машины.
- •56. Технические циклы.
- •57. Второе начало термодинамики (6 формулировок).
- •58. Энтропия
- •59.Принцип возрастания энтропии
- •60. Определение энтропии неравновесной системы через статистический вес состояния. III начало термодинамики.
- •61. Метод термодинамических потенциалов (характеристических функций).
- •62. Явления переноса. Средняя длина свободного пробега молекул.
- •63. Коэффициент диффузии.
- •64. Теплопроводность. Коэффициент теплопроводности.
- •65. Уравнение теплопроводности.
- •70. Изотермы Ван-дер-Ваальса. Критич. Состояние. Внутр. Энергия реального газа.
- •71. Твёрдые тела.Теплоёмкость кристалла
- •72. Жидкости.Поверхн. Натяж. Жидк.
- •73. Смачивание и капиллярные явления
- •74. Принцип динамич. Отопления
- •75. Элементы физики полимеров
61. Метод термодинамических потенциалов (характеристических функций).
Термодинамическим потенциалом наз функция сост из термодинам-х параметров (p,V,S,T). Каждому набору таких параметров соотв. свой потенциал. Изменение потенциала в ходе прцесса опред либо работу в сис-ме либо тепло получ-мое сис-мой. Приращение любого из потенциалов = полному дифф-лу функции, которой он выраж. Полный дифф-л функции f(x,y) ,будет равен
![]() .
.
Рассм термод-ий потенциал:
1) Внутр энергия
![]() .
Осн. Термод-е тождество:
.
Осн. Термод-е тождество:
![]() ,
,
![]() .
.
IНТ:![]() .
Работа сис-мы в адиобатном процессе
равна убыли внутр энергии сис-мы.
.
Работа сис-мы в адиобатном процессе
равна убыли внутр энергии сис-мы.
2) Свободная энергия или энергия Гельмгольца: F=F(T,V)
IНТ:![]() ;
;![]() ,
если процесс изотерм-ий
,
если процесс изотерм-ий
![]() ,
то
,
то
![]() ;
;
![]() при
при
![]() ,
,![]() т.е.
работа в изотерм-ом прцессе игрант
такую же роль, что и внутр-я энергия в
адиобатном.
т.е.
работа в изотерм-ом прцессе игрант
такую же роль, что и внутр-я энергия в
адиобатном.
![]()
![]()
3) Тепловая функция (Н) или энтальпия:
Н=Н(S,p) - Энтальпия
Если процесс
изобарный т.е. р=const,
тогда IНТ:![]()
4) Потенциал Гиббса
![]() .
Можно показать, что минимум потенц.
Гиббса соотв-т равновесию сис-мы при
р=const.
.
Можно показать, что минимум потенц.
Гиббса соотв-т равновесию сис-мы при
р=const.
62. Явления переноса. Средняя длина свободного пробега молекул.
ТД система находится в неравновесном состоянии, если его ТД-параметры не имеют определенного значения. Время перехода системы из неравновесного состояния в равновесное – время релаксации. Время релаксации может быть различно, но различны параметры, тогда за время перехода берется наибольшее из времен релаксации системы. Вычисляя среднее число столкновения и среднюю длину свободного пробега молекул. Молекулы, находящиеся в тепловом движении непрерывно сталкиваются между собой. Пусть Li проходимость i молекулы между двумя последующими столкновениями наз. длину свободного пробега.
С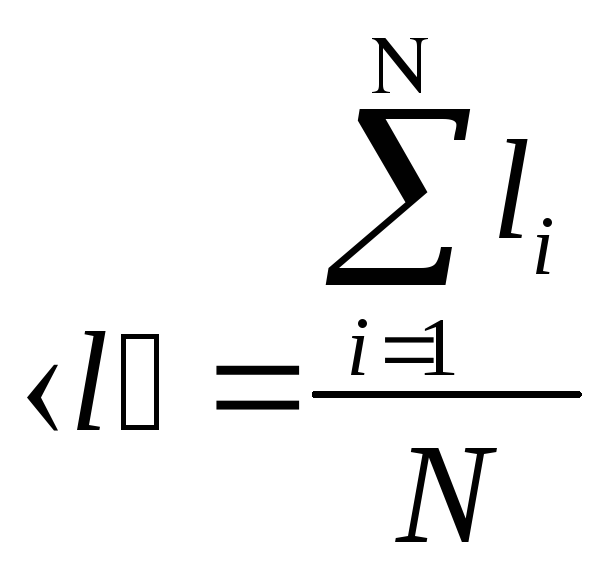 редняя
длина свободного пробега молекул
редняя
длина свободного пробега молекул
Эффективный диаметр молекулы (d) – минимальное расстояние, на которое сближаются при столкновении центры молекул. За 1с молекула проходит в среднем путь равный средней арифметической скорости молекулы. Пусть <z> -- среднее арифметическое число столкновений, испытываемой одной молекулой за 1 секунду, тогда средняя длина свободного пробега молекулы:
Найдем среднее число столкновений z за 1с:
П![]() усть
молекула – шарик с диаметром d
и это молекула движется среди неподвижных
молекул со скоростью <V>,
тогда эта молекула сталкивается со
всеми молекулами, центры которых
находятся от центра молекул на расстоянии
равном или меньшем d,
т.е. лежат внутри ломаного центра R=d.
усть
молекула – шарик с диаметром d
и это молекула движется среди неподвижных
молекул со скоростью <V>,
тогда эта молекула сталкивается со
всеми молекулами, центры которых
находятся от центра молекул на расстоянии
равном или меньшем d,
т.е. лежат внутри ломаного центра R=d.
С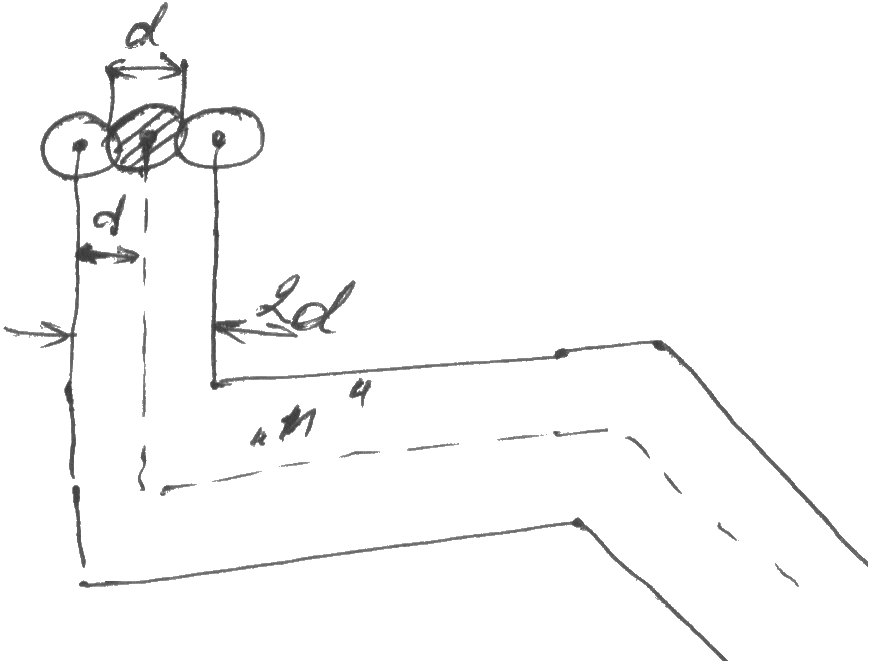 реднее
число столкновений за 1с -- число молекул
в объеме ломаного цилиндра, т.е.
реднее
число столкновений за 1с -- число молекул
в объеме ломаного цилиндра, т.е.
![]()
Объем цилиндра
после его выравнивания равно
![]()
У![]() чет
движения молекул приводит к увеличению
числа столкновений в
чет
движения молекул приводит к увеличению
числа столкновений в
![]() раз.
раз.
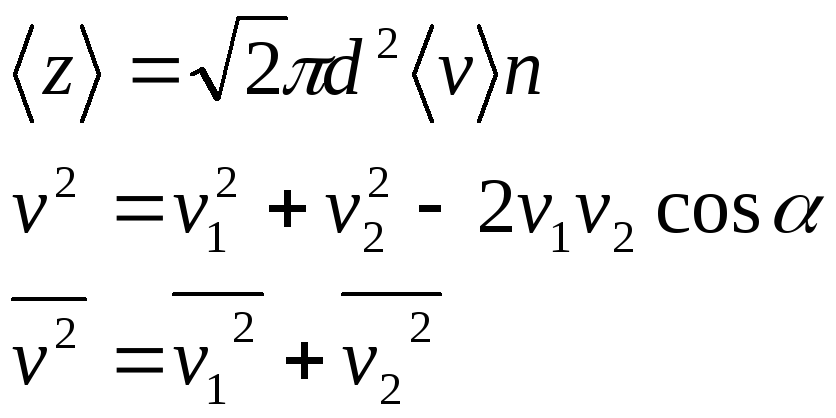
Средняя длина свободного пробега молекул:
![]() ;
;
![]()
Для воздуха при
t=0,
p0=1
атм. средняя длина свободного пробега
![]() ,
эффективный диаметр
,
эффективный диаметр
![]() ,
среднее число столкновений
,
среднее число столкновений
![]() ,
средняя скорость
,
средняя скорость
![]()
