
- •15. Характеристика кератинов, коллагенов, эластинов.
- •24. Необратимые реакции осаждения белков (денатурация).
- •56. Назовите источники витаминов и витаминных препаратов для животных.
- •83. Гормоны передней доли гипофиза и их действие на организм животных.
- •97. Общая характеристика обмена веществ и энергии.
- •124. Распад высших жирных кислот (вжк), β-окисление. Основные этапы и значение.
- •128. Обмен фосфатидов. Значение этой группы липидов для метаболизма клетки и организма в целом. Основные этапы синтеза.
- •Список использованной литературы
15. Характеристика кератинов, коллагенов, эластинов.
24. Необратимые реакции осаждения белков (денатурация).
56.Назовите источники витаминов и витаминных препаратов для животных.
83. Гормоны передней доли гипофиза и их действие на организм животных.
97.Общая характеристика обмена веществ и энергии.
124.Распад высших жирных кислот (ВЖК),β-окисление. Основные этапы и значение.
128. Обмен фосфатидов. Значение этой группы липидов для метаболизма клетки и организма в целом. Основные этапы синтеза.
15. Характеристика кератинов, коллагенов, эластинов.
Структурная функция этих белков заключается в том, что они:
участвуют в образовании практически всех органоидовклеток, во многом определяя их структуру (форму);
образуют цитоскелет, придающий форму клеткам и многим органоидам и обеспечивающий механическую форму ряда тканей;
входят в состав межклеточного вещества, во многом определяющего структуру тканей и форму тела
Кератины -семействофибриллярных белков, обладающих механическойпрочностью, которая среди материалов биологического происхождения уступает лишьхитину. В основном из кератинов состоят роговые производные эпидермиса кожи - такие структуры, какволосы,ногти,роганосорогов,перьяирамфотекаклюва птиц и др. Согласно новой номенклатуре кератинов, в это семейство входят такжецитокератины, образующие наиболее прочные элементы внутриклеточногоцитоскелетаэпителиальных клеток..
Для первичной структуры α-кератинов характерно большое содержание цистеинаи множестводисульфидных связей. Молекулярная масса — от 10 до 50 кДа. Периодичность в чередовании аминокислотных остатков в молекулах отсутствует. В отличие от α-кератинов поперечные дисульфидные связи между соседними полипептидными цепями у β-кератинов отсутствуют. В полипептидной цепи каждый второй элемент -глицин. Для α-кератинов основным структурным компонентом являются цилиндрические микрофибриллы диаметром 75 А, состоящие из спирализованных, скрученных попарно протофибрилл. Характерной особенностью α-кератинов является их полная нерастворимость в воде приpH7,0 и физиологической температуре. Данное свойство частично обусловлено тем, что в состав молекулы входит большой процент гидрофобных аминокислотных остатков (фенилаланин, изолейцин, валин, метионин и аланин). В силу конформации белка R-группы этих остатков направлены к внешней стороне спиралевидной структуры молекулы.
По вторичной структуре белка семейство кератинов разделяется на две группы:
α-кератиныимеют конформацию в виде плотных витков вокруг длинной оси молекулы (α-спираль); эти кератины являются основой волос (включая шерсть), рогов, когтей и копыт млекопитающих. У людей в основном встречаются α-кератины. β-кератины в основном составляют более твёрдые образование, которых почти невозможно найти в теле и в целом, в организме человека.
β-кератины, более твёрдые и имеющие форму несколько зигзагообразных полипептидных цепей (т. н.β-листы); эти кератины обнаружены в когтях и чешуе рептилий, в их панцирях (у черепах), в перьях, клювах и когтях птиц, в иглах дикобразов.
Коллаген -фибриллярный белок, составляющий основусоединительной тканиорганизма (сухожилие,кость,хрящ,дермаи т. п.) и обеспечивающий её прочность и эластичность. Коллаген обнаружен умногоклеточных животных;
отсутствует у растений,бактерий,вирусов,простейшихигрибов. Коллаген основной компонент соединительной ткани и самый распространённыйбелокумлекопитающих, составляющий от 25 % до 35 % белков во всём теле. семейство белков, в теле человека составляют до 25 — 30 % общей массы всех белков. Молекула коллагена представляет собой правозакрученнуюспиральиз трёх α-цепей. Такое образование известно под названиемтропоколлаген.Один виток спирали α-цепи содержит триаминокислотных остатка. Молекулярная масса коллагена около 300 кДа, длина 300нм, толщина 1,5 нм. Коллаген существует в нескольких формах. Основная структура всех типов коллагена является схожей. Коллагеновые волокна образуются путём агрегации микрофибрилл, имеют розовый цвет при окраске гематоксилином и эозином и голубой или зелёный при различных треххромных окрасках, при импрегнации серебром окрашиваются в буро-жёлтый цвет. Кроме структурной функции коллаген выполняет также механическую, защитную, питательную и репаративную функции. Молекула коллагена представляет собой правозакрученную спираль из трёх α-цепей. Всего у человека имеется 28 типов коллагена. Все они сходны по структуре.
Эластин-белок, обладающий эластичностью и позволяющий тканям восстанавливаться, например, при защемлении или порезе кожи. Наличие большого количества гидрофобных радикалов препятствует созданию стабильной глобулы, в результате полипептидные цепи эластина не формируют регулярные вторичную и третичную структуры, а принимают в межклеточном матриксе разные конформации с примерно равной свободной энергией (рис.1).
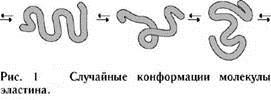
Эластин - белок, отвечающий за упругость соединительных тканей. Он широко используется в косметологии, так как содержит важнейшие аминокислоты (валин,глицин,пролин,аланини др.). В составе эластина также присутствуют уникальные аминокислоты -десмозины. Скрепляя нити эластина, они образуют жесткий каркас. Это обеспечивает эффективное предотвращение образования морщин, увеличение тургора кожи, защиту от растягивания и обвисания. Эластин лучше других веществ увлажняет кожу. Он создает «дышащую» пленку, которая препятствует испарению влаги. В отличие от жиров и масел, традиционно использующихся в качестве увлажнителей, эластин не закупоривает поры. В отличие от коллагена в эластине значительно больше валина и аланина и меньше глутаминовой кислоты и аргинина. В целом характерной особенностью первичной структуры эластина является слишком малое содержание полярных аминокислотных остатков. В основном, эластин состоит изглицина,валина,аланинаипролина. Эластин является специализированным белком с молекулярной массой от 64 до 66 кДа. Эластин синтезируется клеткамифибробластовчерез предшественник — растворимыйтропоэластин, не содержащий поперечных связей. Из множества тропоэластина эластин получается в реакции, катализируемойлизилоксидазой.
В эластине также присутствуют десмозиниизодесмозин, из-за чего эластин может растягиваться в двух направлениях. В поджелудочной железе синтезируется эластаза. Название фермент получил от субстрата эластина, который он гидролизует.
