
- •Комплексные соединения. Комплексообразующая способность s, p, d элементов.
- •Соединения первого порядка (валентно-ненасыщенные)
- •Комплексные соединения – …
- •Теория А. Вернера (1893г.)
- •Теория А. Вернера (1893г.)
- •Строение комплексных
- •Номенклатура комплексных соединений
- •Номенклатура комплексных соединений
- •Классификация комплексных соединений по разным признакам
- •Классификация комплексных соединений по разным признакам
- •Классификация комплексных соединений по разным признакам
- •Классификация комплексных соединений по разным признакам
- •Классификация лигандов
- •Гибридизация – …
- •Типы гибридизации орбиталей центрального иона
- •Спектрохимический ряд
- •Влияние поля лигандов на окраску комплексов
- •Диссоциация КС по внешней сфере
- •Диссоциация КС по внутренней сфере (вторичная диссоциация)
- •Реакции комплексных соединений по внешней сфере
- •Реакции комплексных соединений с разрушением комплекса
- •2. Образование малорастворимого соединения
- •Комплексообразующая способность s, p, d элементов
- •Комплексообразующая способность s,p,d элементов
- •Комплексообразующая способность s,p,d элементов
- •Металлолигандный гомеостаз – …
- •Причины нарушения
- •Причины нарушения
- •Причины нарушения
- •Термодинамические принципы хелатотерапии
- •Детоксиканты хелатотерапии
- •Детоксиканты хелатотерапии
Классификация комплексных соединений по разным признакам
|
3. По природе лигандов |
||||||||||
Аквакомплексы |
|
|
|
|
|
|
|
|
|
||
[Co(H2O)6]SO4 |
|
|
|
|
Цианидные |
|
|
||||
Ацидокомплексы |
|
|
|
|
K4[Со(CN)6] |
|
|
||||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|||
K[Cu(CN)2] |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
Гидроксокомплексы |
|
||||||
|
|
|
|
|
|
K3[Al(OH)6 ] |
|
||||
Разнолигандные |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||
[CoI(NH3)5]Cl2 |
|
|
|
|
|
Карбонилы |
|
||||
NH4[Cr(SCN)4(NH3)2] |
|
|
|
|
|
|
[Fe(CO)5] |
|
|||
|
Аммиакаты |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Карбонатные |
|
|
|
|
||
|
|
Ni(NH3)6 Cl2 |
|
|
|
|
|||||
|
|
|
[Fe(CO3)(NH3)]Cl |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
Классификация комплексных соединений по разным признакам
|
4. По наличию или отсутствию циклов |
|
|
|
|||||||
Простые |
Fe4[Fe(CN)6]3 |
берлинская лазурь |
|
|
|
||||||
|
Циклические |
|
|
|
|
|
|
|
|
|
|
Внутрикомплексные |
|
|
Хелаты |
|
|
|
|||||
соединения |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2+ |
||
|
|
H2C |
|
H2N |
NH |
|
|
|
|
CH2 |
|
|
|
|
2 |
||||||||
|
|
|
|
|
|||||||
|
|
|
|
|
Cu |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2C |
|
H2N |
NH |
|
|
CH2 |
|||
|
|
|
2 |
|
|||||||
|
|
|
|
Хлорид |
|
|
|
||||
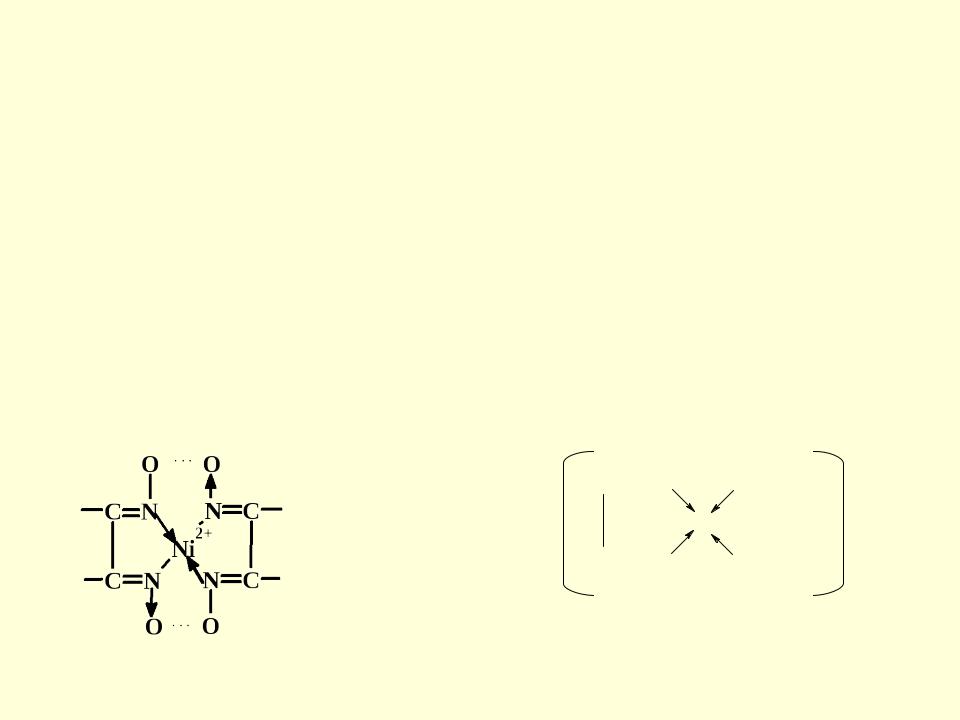
диметилглиоксимат никеля (II) |
[(бис-этилендиамин)медь (II)] |
||||||||||
Классификация лигандов
.. |
.. |
.. |
1. Монодентатные: Н2О, NH3,
..
2. Бидентатные: H2N – CH2 - CH2
..
3. Полидентатные: -OOCCH2
..
CO.
..
– NH2,
..
CH2COO-
..
N-CH2-CH2–N
.. ..
-OOCCH2 CH2COO-
Гибридизация – …
… смешение и выравнивание по форме и энергии орбитали, принадлежащих разным уровням и подуровням.
Заряд комплексо Координацион
образоват ное число еля
1+ 2
4
2+
6
4
3+
6
Тип гибридизации
sp
dsp2 sp3
d2sp3 / sp3d2
dsp2 sp3
d2sp3 / sp3d2
Геометрическая
конфигурация
Линейная
Квадратная
Тетраэдрическая
Октаэдрическая
Квадратная
Тетраэдрическая
Октаэдрическая

Типы гибридизации орбиталей центрального иона
Атом Fe:
Fe0 1s22s22p63s23p6 4s23d6
3
s |
p |
d |
4 
Ион Fe3+:
Fe3+ 1s22s22p63s23p6 4s03d5
3
s |
p |
d |
4 
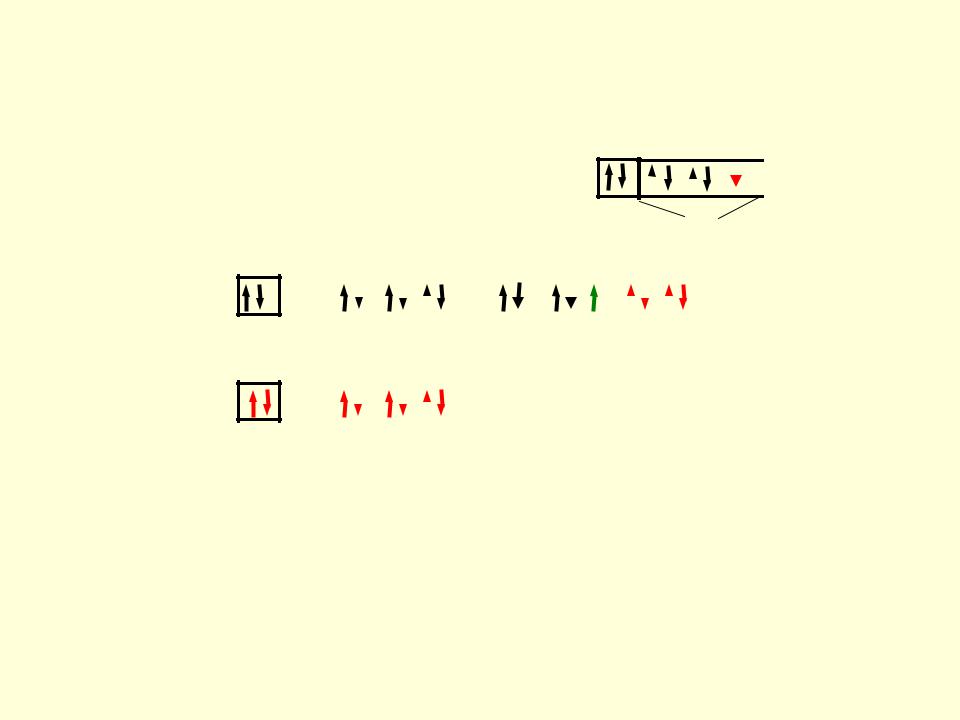
Ион СN :
С 1s22s22р2 |
CN 2s22p5 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
N 1s22s22p3 |
|
p |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
s |
|
||||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
s |
|
|
|
|
p |
|
|
|
d |
|
|
|
|
|
d2sp3 |
|||||||||||
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Внутрисферный комплекс [FeCN6]3–
под действием силы поля лигандов происходит спаривание электронов на d-подуровне.
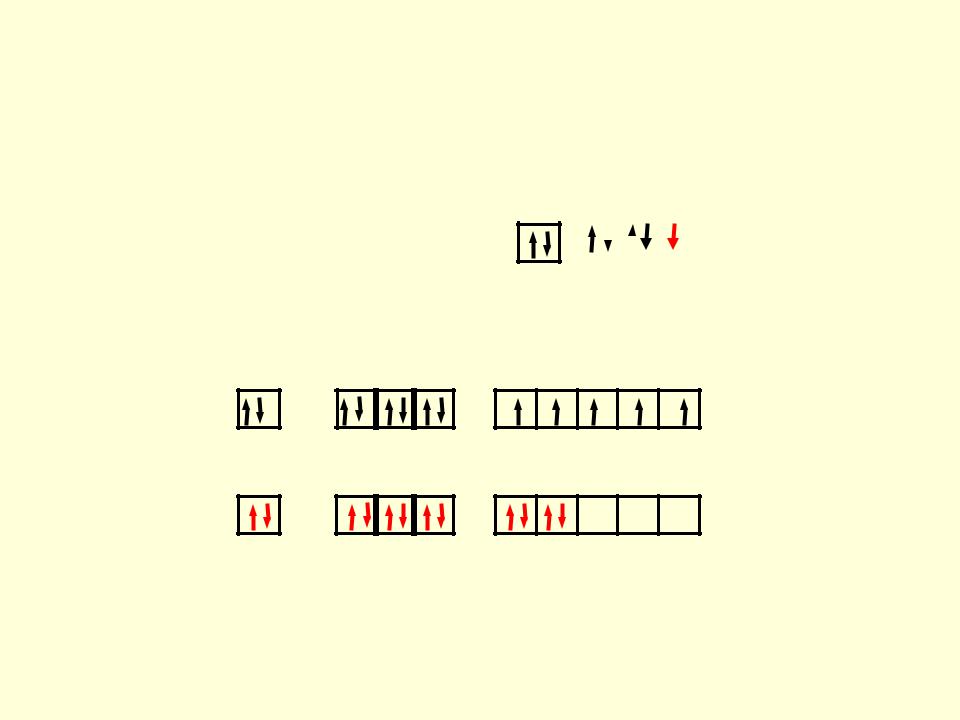
[FeF6]3-
Ион F :
F 1s22s22p5 |
2 |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
||
|
|
|
|
|
||
|
|
|
|
|
||
s |
|
|
|
p |
||
|
|
|
|
|||
3 |
|
|
s |
p |
d |
4 |
|
d2sp3 |
Внешнесферный комплекс [FeF6]3–

Спектрохимический ряд
СO > CN– > NH3 > NO2– > H2O > OH > F > NО3 > SCN
Cl > Br > I
•Сильные обладают способностью спаривать электроны центрального иона. Слабые – никогда.

Влияние поля лигандов на окраску комплексов
[Co(H2O)6]2+ розовый
[Co(CH3COO)2] ярко-розовый
[Co(NO2)6]4- оранжевый
[Co(NH3)6]2+ буро-розовый
 Усиление поля лигандов
Усиление поля лигандов
Диссоциация КС по внешней сфере
(первичная диссоциация)
K [Fe(CN) ] |
|
|
3K+ + [Fe(CN) ]3- |
||
3 |
6 |
|
6 |
||
|
|
|
|
|
|
[Ag(NH |
) ]Cl |
[Ag(NH |
) ]+ + Cl- |
3 |
2 |
3 |
2 |
