
|
|
|
74 |
1) |
ПАВ |
3) |
сильных электролитов |
2) |
света |
4) |
молекул растворителя |
17. Воздух, содержащий частички пыли, относится__________.
1) |
эмульсиям |
3) |
аэрозолям |
2) |
пенам |
4) |
золям |
18. В эмульсиях дисперсная фаза ____, дисперсионная сред_________.
1) |
жидкая, жидкая |
3) |
твердая, жидкая |
2) |
твердая, газообразная |
4) |
газообразная, твердая |
19. Дисперсная система состоит из__________.
1) дисперсной фазы и дисперсионной среды
2) двух растворителей
3) дисперсионной фазы и дисперсной среды
4) растворителя и дисперсионной среды
20. Дисперсностью называется_______.
1) |
величина обратная диаметру частиц 3) |
величина обратная радиусу частиц |
||
2) |
величина обратная объему частиц |
4) |
величина прямо пропорциональная размеру частиц |
|
21. Отметьте свойство, по которому классифицируются дисперсные системы. |
||||
1) |
по растворимости |
3) |
по вязкости |
|
2) |
по степени дисперсности |
4) |
по оптическим свойствам |
|
22. Коллоидные частицы золя, полученного при введении в разбавленный раствор H2SO4
насыщенного раствора BaCl2, имеют _____заряд.
1) |
нескомпенсированный слоем противоионов |
3) |
положительный |
2) |
нулевой |
4) |
отрицательный |
23. Наибольшее коагулирующее действие на золь с отрицательно заряженными
коллоидными частицами оказывает_____.
1)FeSO4 |
2) K3PO4 |
3)KCl |
4) AlCl3 |
24. Коллоидные частицы золя, полученного при добавлении в разбавленный раствор AsCl3
насыщенного раствора Н2S, имеют ____заряд.
1) |
нулевой |
3) |
положительный |
2) |
нескомпенсированный слоем противоионов |
4) |
отрицательный |
Модульная единица 1.3 Низкомолекулярные биорегуляторы и биологически активные высокомолекулярные соединения (строение, свойства, участие в функционировании живых систем)
Занятие 1.3.1
74

75
ТЕМА: Полифункциональные соединения (многоатомные спирты и фенолы, полиамины, двухосновные карбоновые кислоты). Лабораторная работа № 10 «Свойства одно-и- многоатомных спиртов и фенолов» ЦЕЛЬ: Изучить строение, химические свойства многоатомных спиртов, полифенолов, диаминов и
двухосновных карбоновых кислот, которые проявляют выраженное биологическое действие, являются предшественниками биосинтеза ряда физиологически значимых соединений (гормонов, нейтральных и полярных липидов, АТФ).
ЗНАТЬ:
1.Структура многоатомных спиртов: этиленгликоля, глицерола, инозитола, ксилита, сорбита.
2.Особенности химических свойств многоатомных спиртов. Биологическая роль соединений в организме человека.
3.Строение двухатомных фенолов: гидрохинона, катехола, резорцина.
4.Полифенолы ряда катехолов: дофамин (3/, 4/ -дигидроксифенилэтиламин), норадреналин (3/, 4/ - дигидроксифенил, 1-гидроксиэтиламин), адреналин (3/, 4/ -дигидроксифенил, 1-гидрокси, 2-N- метиламиноэтан), биологическая роль.
5.Важнейшие представители флавоноидов. Химические свойства флавоноидов.
6.Р-витаминная активность, антиоксидантное действие флавоноидов.
7.Полиамины: кадаверин, путресцеин, агматин, спермидин, спермин, биологическая роль. Основность двухатомных аминов, химические свойства (алкилирование, ацилирование, образование солей).
8.Двух- и трехосновные карбоновые кислоты: щавелевая, малоновая, янтарная, глутаровая, малеиновая, фумаровая, лимонная.
9.Строение карбоксильной группы, особенности химических свойств двух- и трехосновных карбоновых кислот. Кислотность, образование солей.
10.Сравнительная характеристика кислотно-основных свойств многоатомных спиртов, полифенолов, полиаминов, ди- и трикарбоновых кислот.
УМЕТЬ:
1.Приводить структурные формулы многоатомных спиртов: глицерола, инозитола, ксилита, сорбита; двухатомных фенолов: гидрохинона, катехола, резорцина.
2.Приводить схемы специфических реакций хелатообразования в ряду многоатомных спиртов.
3.По названию представлять структуры полифенолов ряда катехолов.
4.Изображать структуры полиаминов: кадаверина, путресцеина, агматина, спермидина. спермина.
5.Приводить реакции алкилирования, ацилирования полиаминов.
6.Приводить структуры ди-и трикарбоновых кислот: щавелевая, малоновая, янтарная, глутаровая, малеиновая, фумаровая, лимонная.
7.Приводить реакции с участием карбоксильных групп (декарбоксилирования, нуклеофильного замещения, нейтрализации).
8.Сравнивать кислотно-основные свойства многоатомных спиртов, полифенолов, полиаминов, ди- и трикарбоновых кислот.
ВЛАДЕТЬ: экспериментальными навыками качественного обнаружения многоатомных спиртов, двухатомных фенолов, флавоноидов в исследуемом растворе.
Обучающие упражнения
Задание 1. Привести формулы и названия этиленгликоля (I) , глицерола (II), инозитола (III).
Ответ.
1,2-дигидрокси этан 1,2,3-тригидроксипропан гексагидроксициклогексан
75

76
Задание 2. Привести формулы и систематические названия сорбита и ксилита, использующихся в качестве сахарозаменителей в питании людей больных диабетом, ксилит часто применяют при производстве жевательных резинок (например, Дирол с ксилитом и карбамидом (мочевиной)).
Ответ: Ксилит и сорбит представляю собой многоатомные спирты, их получают восстановлением углеводов :ксилозы и глюкозы.
Пентагидроксипентан гексагидроксигексан Задание 3. По систематическому названию привести формулы путресцина (1,4-диамаминобутан), кадаверина (1,5-диаминопентан) и агматина. Указать их биологическую роль.
Ответ.
Путресцин |
кадаверин |
агматин |
||
Путресциин и кадаверин |
образуются при ферментативном |
дезаминировании аминокислот: |
||
аргинина, орнитина и лизина по схеме: |
|
|||
|
|
|
|
|
Аргинин |
агматин |
Орнитин |
|
путресцин |
|
|
|
Лизин |
кадаверин |
Соединения могут образовываться при гниении белков, проявляют высокую основность, поэтому токсичны, обладают неприятным запахом, относятся к трупным ядам. Кадаверин используется организмом для синтеза спермидина и спермина.
Задание 4. Приведите формулы спермидина, спермина, укажите их биологическую роль.
Ответ.
спермидин



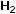












 спермин Спермидин и спермин легко взаимодействуют с нуклеиновыми кислотами, участвуют в поддержании третичной структуры ДНК и РНК.
спермин Спермидин и спермин легко взаимодействуют с нуклеиновыми кислотами, участвуют в поддержании третичной структуры ДНК и РНК.
76

77
Задание 5. Описать схему биосинтеза катехоламинов. Указать биологическое действие норадреналина, адреналина.
Ответ.
Катехоламины образуются в организме в результате метаболизма фенилаланина (гидроксилирования, декарбоксилирования ) в соответствиии со схемой:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
CH |
COOH |
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
CH |
|
COOH |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
||||||
Фенилаланин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тирозин |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
(аминокислота) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(аминокислота) |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
CH |
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
CH |
2 |
NH |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- CO2 |
|
|
|
|
|
|
|
|
|
2 |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ДОФА |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(дигидроксифенилаланин) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
дофамин |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
HO |
|
|
|
|
|
|
CH |
CH2 |
NH2 |
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
CH2 |
NH |
CH3 |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
норадреналин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
адреналин |
|
|
|
|
|
||||||||||||||||||||||||
Дофамин –гормон, нейромедиатор, улучшает доставку кислорода, усиливает силу сердечных сокращений, работу почек, влияет на двигательную активность.
Адреналин является гормоном мозгового слоя надпочечников, дофамин и норадреналин - его предшественники. Адреналин участвует в регуляции сердечной деятельности, обмене углеводов. В стрессовых ситуациях его уровень возрастает мгновенно в 106 раз. Адреналин повышает кровяное давление, в связи с чем стрессы могут способствовать стойкому повышению давления и заболеванию сердечно-сосудистой системы.
Задание 6. На примере глицерола привести химизм качественной реакции на многоатомные спирты.
Ответ: Качественной является реакция многоатомных спиртов со свежеприготовленным раствором Сu(ОН)2, приводящая к образованию комплексного соединения (хелата) интенсивно синего цвета.
Задание 7. Привести реакции, использующиеся для обнаружения флавоноидов (в чае, лекарственных растениях, цветах, плодах цитрусовых).
Ответ: Флавоноиды образуют комплексы желтого цвета с солями свинца (I), в кислой среде превращаются в соли пириллия (II), имеющие окраску от розового до бардового цвета. В слабо щелочной среде фравоноиды приобретают хиноидное строение (III), окраска таких соединений может изменяться от голубого до темно синего и черного цвета. Структуры II и III определяют цвет ягод, плодов, окраску цветов.
77

78
I - желтого цвета
|
III – синего цвета |
|
|
|
II – красногоцвета |
|
|||
|
|
|
|
|
|
|
|
||
Задание 8. Многоатомные фенолы проявляют антиоксидантное действие, обусловленное высокой |
||||
активностью в реакции со свободными радикалами. Приведите взаимодействие флавоноидов с |
||||
гидроксильными (ОН•) и пероксильными радикалами (RO2•), образующимися в организме при |
||||
окислении липидов. |
|
|
||
Ответ: Флавоноиды, способны уничтожать свободные радикалы поэтому являются ингибиторами |
||||
процессов окисления, протекающих с участием радикалов. Обозначаем ингибитор как InH. |
||||
InH + OH• |
In• +HOH |
|
|
InH + RO2• |
In• |
+ ROOH |
|
Радикальные продукты ингибитора In•не активны и не участвуют в дальнейшем в |
|||
радикальных реакциях, |
поскольку электронная |
плотность |
равномерно перераспределяется |
(делокализуется) по всей ароматической системе флавоноидов. |
|
||
Задание 9. Приведите формулы и систематическое название |
щавелевой, малоновой, янтарной, |
||
глутаровой и фумаровой кислот.
Ответ: Формулы и систематические названия кислот приведены ниже. Все кислоты образуются в организме.
O |
O |
O |
|
O |
|
O |
|
|
|
|
O |
|||||||||||
|
C |
|
C |
|
|
C |
|
CH2 |
|
C |
|
C |
|
CH2 |
|
|
CH2 |
|
C |
|||
|
|
|
|
|
|
|
|
|
||||||||||||||
HO |
OH |
HO |
|
OH |
HO |
|
|
|
|
OH |
||||||||||||
щавелевая |
|
|
малоновая |
|
|
янтарная |
|
|
|
|
|
|||||||||||
(этандиовая) |
|
|
(пропандиовая) |
|
|
(бутандиовая) |
|
|
|
|
|
|||||||||||
O |
|
|
O |
|
O |
|
|
|
|
|
|
|
|
O |
|
|||||||
C |
|
(CH2)3 |
|
C |
|
|
|
|
C |
|
CH CH |
|
|
C |
|
|||||||
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
HO |
|
|
OH |
|
HO |
|
|
|
|
|
|
|
|
OH |
|
|||||||
глутаровая |
|
|
|
|
|
|
Фумаровая |
|
|
|
|
|
||||||||||
(пентандиовая) |
|
|
|
|
(транс-бутен-2-диовая)(цис-изомер |
– |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
называется малеиновой кислотой) |
|
||||||||||
Задание 10. Приведите схему образования щавелевой кислоты и ее кальциевых солей (оксалатов), не растворимых в воде и моче. Оксалаты кальция являются причиной образования почечных камней, которые по твердости не уступают костной ткани, травмируют почку, мочеточник, вызывая сильную боль, зачастую являются причиной длительного «безпричинного» крика у младенцев.
78

79
Ответ: Щавелевая кислота в организме может образовываться из молочной, щавелевоуксусной, аскорбиновой кислот в результате их окисления и декарбоксилирования. Ниже приведена реакция образования оксалатов кальция из молочной кислоты.
Молочная кислота гликолевая кислота щавелевая кислота оксалат кальция
Задание 11. Расшифровать цепочку превращений:
Ответ:
Малеиновая кислота |
(А) винная кислота (образуется при изготовлении |
|
вин) |
(В) Виннокислый калий (тартрат калия) |
|
|
|
(С) Комплекс катионов меди с винной |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислотой |
||
|
|
|
|
|
|
|
|
Задания для самостоятельного решения: |
||||||||||
1.Расшифровать цепочки превращений: |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
O2 |
|
|
H O |
Cu(OH)2 |
|
|
|||||||
H2C |
|
CH2 |
|
A |
2 |
|
B |
|
|
|
|
C |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
А—Эпоскиэтан, В – Этиленгликоль, С- хелат |
|
|
|
|
|
|||||||||||||
2. .Расшифровать цепочки превращений: |
|
|
|
|
|
|
||||||||||||
|
HC |
|
CH2 |
Cl2, hV |
|
|
KMnO4 |
|
NaOH, t0 |
3 HNO3 |
||||||||
H3C |
|
|
|
A |
|
|
|
B |
|
|
C |
|
D |
|||||
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H2O
А- 3-хлорпропен-1, В- 3-хлор-пропандиол1,2,
79

80
С- глицерол
D- тринитроглицерол
3.Расшифровать цепочки превращений:
O |
|
|
|
O |
Cl2, hV |
|
|
NaOH, t0 |
|
[O] |
|
2 C2H5OH |
|||||
C H2C |
|
CH2 C |
A |
B |
C |
||||||||||||
|
|
|
|
|
|
|
|
|
D |
||||||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
HO |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
А- 2-хлорбутандиовая кислота; |
|
|
|
|
|
|
|
|
|
|
|||||||
В- 2-гидрокси бутандиовая кислота |
|
|
|
|
|
|
|
|
|
|
|||||||
С- щавелевоуксусная (2-оксобутандиовая) кислота |
|
|
|
|
|
||||||||||||
D- диэтиловый эфир щавелевоуксусной кислоты |
|
|
|
|
|
||||||||||||
4. Расшифровать цепочки превращений: |
|
|
|
|
|
|
|
|
|
||||||||
O |
O |
Ca(HCO3)2 |
|
|
|
|
|
|
|
|
|
|
|||||
C C |
|
|
|
A |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
HO |
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
А- оксалат кальция 5.Расшифровать цепочку превращений:
А- 1,4-бензолдикарбоновая (терефталевая кислота); В- полиэтиленгликольтерефталат (полиэфир, используется в хирургии как шовный материал).
6.По реакции с гидроксидом калия получите соли малоновой кислоты (малонаты), соли лимонной кислоты (цитраты), янтарной кислоты (сукцинаты);
7.Получите соль по реакции кадаверина с хлороводородной кислотой.
8.Напишите реакцию алкилирования и ацилирования кадаверина.
9. Приведите формулы шестиатомных спиртов ( сорбита, инозита.)
Тестовые задания для самостоятельного решения
1. Выбери среди приведенных соединений молекулу адреналина.
а) |
б) |
в)  г)
г) 
 2. Формула какого соединения отвечает кверцетину (3,5,7, 3/,4/-пентагидрокси флавон)?
2. Формула какого соединения отвечает кверцетину (3,5,7, 3/,4/-пентагидрокси флавон)?
80

81
а) |
б) |
в) 
 г)
г)
3. Среди приведенных структур определите соль винной кислоты.
а) |
|
|
|
|
|
б) |
|
|
в) |
|
|
|
|
|
|
г) |
|
4. |
Укажите формулу путресцина (тетраметилендиамина). |
|
||||||
а) |
|
|
|
|
|
б) |
|
|
в) |
|
|
|
|
|
г) |
|
|
5. |
Какие из упомянутых ниже соединений будут взаимодействовать с Cu(OH)2? |
|||||||
а) |
этанол б) |
глицерол |
в) |
молочная кислота |
в) глицин |
|||
6. |
Какое соединение относится к трехатомным спиртам? |
|
||||||
а) |
этиленгликоль |
б) |
сорбитв) |
ксилитг) |
глицерол |
|||
7. |
Какое соединение получают восстановлением глюкозы? |
|
||||||
а) |
ксилит |
|
б) |
гиалуроновую кислоту |
|
|||
г) |
сорбит |
|
в) маннит |
|
|
|
||
8. |
Укажите формулы соединений, относящихся к двухатомным спиртам. |
|||||||
а) |
|
|
|
|
|
б) |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
в) 

 г)
г) 

 9. Какое из предложенных оснований Бренстеда будет более сильным?
9. Какое из предложенных оснований Бренстеда будет более сильным?
81

82
а) |
б) |
в) 
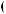



 г)
г)
10. Укажите формулу глицерола (глицерина)?. а) 

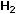


 б)
б)
в) |
г) |
Занятие 1.3.2 ТЕМА: Гетерофункциональные соединения (аминоспирты, гидрокси- и аминокислоты, оксокислоты.
ЦЕЛЬ: Изучить строение, химические свойства гетерофункциональных соединений: аминоспиртов, гидроксикислот, аминокислот, оксокислот, которые проявляют выраженное биологическое действие и являются предшественниками биосинтеза ряда физиологически значимых соединений.
ЗНАТЬ:
1.Классификация и важнейшие представители природных соединений, включающих две и более характеристических групп (аминоспирты, катехоламины, гидрокси-, оксо- и аминокислоты).
2.Классифиция аминооксо- и гидроксикислот в зависимости от взаимного расположения
характеристических групп ( -, -, -, - производные). Биологическое значение аминооксо- и гидроксикислот.
3.Пути биосинтеза некоторых биоорганических соединений: этаноламина (коламина), холина, ацетилхолина, катехоламинов (дофамина, адреналина, норадреналина).
4.Описание центров основности, кислотности у амино- гидрокси-, и оксокислот.
5.Кето-енольная таутомерия (обратимая миграция атома водорода) у пировиноградной, ацетоуксусной кислоты, ацетилКоА.
6.Образование внутренней соли (бетаиновой структуры) у аминокислот.
7.Пространственное строение биоорганических соединений. Основы стереоизомерии амино- и гидроксикислот..
8.Общие и специфические свойства гетерофункциональных соединений.
9.Структура и применение в медицине функциональных производных п-аминофенола, п- аминобензойной кислоты, салициловой и п-аминосалициловой кислот, сульфаниловой кислоты.
УМЕТЬ:
1.Приводить схемы специфических реакций:
-образования лактидов и дикетопиперазинов для -гидрокси- и -аминокислот соответственно;
-элиминирования для -гидрокси- и -аминокислот;
-образования лактонов и лактамов для -гидрокси- и -аминокислот соответственно.
82

83
2.Представлять схему синтеза ацетилхолина, адреналина на основе коламина и фенилаланина соответственно.
3.Определять кислотно-основные центры в гетерофункциональных соединениях.
4.Приводить реакции алкилирования, ацилирования, окислительного гидроксилирования, декарбоксилирования с участием гетерофункциональных соединений.
5.Показывать кето-енольную таутомерию на примере пировиноградной, ацетоуксусной кислоты, ацетилКоА.
6.Осуществлять схемы синтеза синтетических лекарственных препаратов на основе производных бензола.
ВЛАДЕТЬ: навыками проведения специфических реакций с участием гетерофункциональных соединений.
Обучающие упражнения Задание 1 Приведите формулы и систематические названия простейших гидрокси- и аминокислот.
Ответ: Старшей является карбокси-группа, которая определяет нумерацию углеводородной цепи. Младшие группы (гидрокси- и амино-) обозначаются префиксами, перед которыми ставится цифра, обозначающая их положение в цепи. Получаем:
Гликолевая (2-гидроксиэтановая к-та) |
Молочная (2-гидроксипропановая к-та) |
Глицин (2-амино-этановая кислота) |
α-аланин (2-аминопропановая к-та) |
Задание 2. Привести формулы систематические названия этаноламина (коламина) (I) и холина (II). |
|
Этаноламин и холин входят |
в структуру и определяют названия фосфолипидов |
(фосфатидилэтаноламина и фосфатидилхолина). являются предшественниками биосинтеза нейромедиатора - ацетилхолина.
Ответ: Старшей характеристической группой является гидрокси-группа, она определяет нумерацию углеродных атомов в соединении, для ее обозначения используется суффикс –ол. Для обозначения младшей группы используется префикс - амино-, группа называется первой (по алфавиту) с цифрой 2, указывающей ее положение в цепи. Получаем: 2-амино-этанол.
У холина в отличие от этаноламина амино-группа проалкилирована и замещена тремя метильными группами. В этом случае замещенная группа находится в виде соли аммония (является катионом) и обозначается как N,N,N-триметиламино.
(I) 2-аминоэтанол (II) N,N,N-триметиламиноэтанол Задание 3. Привести реакции гликолевой кислоты со спиртом и аммиаком.
Ответ: Взаимодействие происходит как по амино, так и по карбоксильной группе с образованием замещенного сложного эфира и амида.
Этиловый эфир 2-этоксиэтановой к-ты
83

84
Амид 2-аминоэтановой к-ты
Задание 4 Привести реакцию ацилирования гликолевой кислоты.
Ответ. Ацилирование может быть проведено с использованием уксусного ангидрида или хлористого ацетила по схеме:
В условиях организма ацилирование осуществляется с помощью ацетилкоэнзима А или ацетилдифосфата Задание 5. Приведите реакцию дегидратации яблочной кислоты, приводящую к образованию в
организме фумаровой кислоты.
Ответ:
Задание 6. Написать схему синтеза ацетилхолина согласно схеме:
Ответ: Расшифровка цепочки превращений, приводящей к образованию ацетилхолина, приведена ниже. Продукт А- эпоксиэтан, В-этаноламин, С-холин, D- ацетилхолин. Ацетилхолин участвует в проведении нервных импульсов, определяет когнитивные способности организма (способность к обучению, запоминанию).
Задание 7. Приведите последовательность биохимических превращений, приводящих к биосинтезу ацетилхолина.
|
|
|
O |
|
t |
S-аденозилметионин |
|
|
CH3 C |
SKoA |
|
|
|
||
HO CH2 CH COOH |
A |
B |
C |
-СO2
NH2
Ответ:
84

85
S-аденозилметионин
Серин-незаменимая аминокислота.
Этаноламин (коламин) - один из важнейших аминоспиртов - входит в структуру фосфолипидов, лекарственных средств.
Холин - витаминоподобное вещество, регулирующее жировой обмен.
Ацетилхолин - нейромедиатор, участвует в передаче нервного импульса, определяет когнитивные способности организма.
Задание 8. Написать реакции внутри- и межмолекулярной конденсации , и аминокислот.
Ответ:
а) -аминокислоты при нагревании претерпевают межмолекулярную дегидратацию, при этом от двух молекул кислоты отщепляются две молекулы воды:
|
|
|
|
|
O |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
H2N |
|
|
t |
C |
|
|
NH |
|
||||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||
H2C |
|
CH2 |
|
|
H C |
|
|
|
CH |
|
|||
|
|
|
|
|
|
|
|||||||
|
|
- 2H2O |
2 |
|
|
|
|
|
|
|
2 |
||
|
|
|
|
|
|
|
|
|
|
||||
NH2 |
HOOC |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
HN |
|
C |
дикетопиперазин |
|||||||
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||
б) -аминокислоты при нагревании отщепляют аммиак с образованием непредельных кислот:
|
|
|
|
|
|
|
|
|
|
t |
|
|
|
|
|
||
H3C |
|
CH |
CH2 COOH |
|
|
|
|
H3C |
HC |
|
CH COOH |
||||||
|
- NH3 |
|
|||||||||||||||
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
β-аминомасляная кислота |
|
|
|
|
|
кротоновая кислота |
|||||||||||
в) - аминокислоты претерпевают внутримолекулярную дегидратацию: |
|||||||||||||||||
|
|
H2C |
|
|
CH2 |
|
|
t |
H2C CH2 |
|
|||||||
|
|
|
|
|
|
|
|||||||||||
|
H2C |
|
|
|
C |
|
O |
|
|
|
|
|
|
C |
|
||
|
|
|
|
|
|
- H2O |
H C |
|
|
||||||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
N |
|
|
H HO |
|
|
|
|
2 |
N |
O |
|||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
H |
|
||
γ-аминомасляная кислота |
|
|
|
|
|
бутиролактон или пирралидон-2 |
|||||||||||
Задания для самостоятельного решения Задание 1. Выберите среди приведенных ниже кислот одно, - двух, - трехосновные: молочная (2-
гидрокси пропановая), винная (2,3-дигидрокси бутандиовая), лимонная (3-гидрокси-3-карбокси- пентандиовая), пировиноградная (2-оксопропановая), малоновая. Получите сложные эфиры и амиды молочной кислоты Задание 2 . Приведите взаимодействие винной кислоты с гидроксидом меди.
Задание 3. Напишите формулы D- и L-молочной кислоты.
Задание 4. Напишите реакцию декарбоксилирования ацетоуксусной кислоты (отщепление СО2). Задание 5. Получите диэтиловый эфир яблочной кислоты Задание 6. Напишите реакцию дегидратации яблочной кислоты (отщепление Н2О).
Задание 7. Напишите схему биосинтеза адреналина.
Задание 8. Приведите реакцию алкилирования этаноламина, приводящую к образованию холина. Задание 9. Приведите кето-енольную таутомерию ацетилкоэнзима А.
Задание 10. Напишите формулы D- и L-молочной кислоты.
Тестовые задания для самостоятельного решения
85

86
1. Укажите формулу холина:
а) |
б) |
в) 
 г)
г)  2. Выберите из предложенных формул серин (2-амино-3-гидрокси пропановая кислота).
2. Выберите из предложенных формул серин (2-амино-3-гидрокси пропановая кислота).
а) |
б) |
в) 


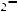

 г)
г)  3. Выберите формулы соединений, включающих в своей структуре остаток этаноламина:
3. Выберите формулы соединений, включающих в своей структуре остаток этаноламина:
а) |
б) |
|
|
|
|
|
|
|
|
в) |
г) |
4.При внутримолекулярной дегидратации какого соединения получают лактоны?
а) |
α-гидроксипропановая кислота |
б) |
γ-аминомасляная кислота |
|
в) |
γ-аминопропановая кислота |
|
в) |
γ-гидроксимасляная кислота |
5. Укажите формулу щавелевоуксусной кислоты. |
|
|||
а) |
б) |
в) |
г) |
6. Укажите, какое соединение относится к кетокислотам
а) |
б) |
86

87
в)  г)
г)  7. Укажите формулу ацетоуксусной (3-оксобутановой) кислоты.
7. Укажите формулу ацетоуксусной (3-оксобутановой) кислоты.
а) |
б) |
в) |
г) |
8. Укажите енольную форму пировиноградной (2-оксопропановой) кислоты
а) |
б) |
в) |
|
|
г) |
|
9. При декарбоксилировании ацетоуксусной кислоты образуется |
||||
а) |
уксусная кислота |
|
б) |
щавелевоуксусная кислота |
в) |
пировиноградная кислота |
г) |
ацетон |
|
10.Какое соединение относится к гидроксикислотам?
а) |
молочная |
б) |
масляная |
в) |
пировиноградная |
г) |
глутаровая |
11.Какое соединение относится к гидроксикислотам?
а) |
яблочная |
б) |
янтарная |
в) |
пировиноградная |
г) |
малоновая |
12. Дикетопиперазин образуется при межмолекулярной дегидратации:
а) |
гидроксикислот |
|
б) |
кетокислот |
в) |
аминокислот |
г) |
дикарбоновых кислот |
|
12. К дикарбоновым гидроксикислотам относится |
||||
а) |
яблочная кислота |
|
б) |
винная кислота |
в) |
фумаровая кислота |
г) |
малеиновая кислота |
|
13. |
Какое соединение выполняет роль нейромедиатора? |
|||
а) |
этаноламин |
|
б) |
холин |
в) |
ацетилхолин |
в) |
путресцин |
|
14. |
Какие пары соединений являются энантиомерами? |
|||
87

88
а) |
б) |
в) |
г) |
Занятие 1.3.3 ТЕМА: Биологически важные ароматические и гетероциклические соединения.
ЦЕЛЬ: Познакомиться с ароматическими гетероциклическими соединениями, входящими в структуру важнейших биологически активных веществ (витаминов, гормонов, ферментов…).
ЗНАТЬ:
1.Классификация ароматических пяти- и шестичленных, одно, двух и полигетероатомных гетероциклов: пиррола, тиофена, фурана, индола, пиридина, хинолина, пиримидина, имидазола, пурина.
2.Признаки ароматичности, устойчивость бензола, тиофена, пиррола, фурана энергия делокализации.
3.Природа пиррольного и пиридинового атомов азота.
3.Структура порфина. Устойчивость гема. Продукты окисления гема. Билирубин.
4.Метаболизм триптофана, схема образования серотонина и мелатонина, их биологическое действие.
5.Структура биотина, его биологическая роль. Биотинзависимые реакции переноса карбоксильных групп.
6.Пиридоксальфосфат: Реакции, происходящие с участием пиридоксальфосфата: декарбоксилирование, переаминирование и рацемизация.
7.Лактим-лактамная таутомерия на примере урацила, цитозина, тимина, характер таутомерных превращений у пурина, гипоксантина, ксантина. Метилированные производные ксантина (кофеин, теофиллин, теобромин)
8.Структура тиамина (витамина В1), его коферментная форма (кокарбоксилаза). Биологическое действие тиамина.
9.Фолиевая кислота. Возможность модификации структуры фолиевой кислоты (подмены остатка ПАБК остатками сульфаниламидных препаратов) для создания лекарственных средств (сульфаниламидных препаратов), способных предотвращать размножение микроорганизмов.
10.Структура рибофлавина (витамина В2) -фактора роста живых организмов. Структура флавинмононуклеотида (ФМН) и флавинадениндинуклеотида (ФАД).
УМЕТЬ:
1.Доказывать наличие ароматической системы в пирроле, тиофене, фуране, индоле, пиридине,
хинолине, пиримидине, имидазоле, пурине.
2.Выделять кислотные и основные центры в молекулах гетероциклических соединений, приводить реакции, доказывающие кислотно-основные свойства.
3.Приводить схемы лактам-лактимной таутомерии для гидроксипроизводных пиримидина и пурина.
88

89
4. Ориентироваться в выборе структур триптофана, серотонина. мелатонина, биотина (витамин Н), пиридоксальфосфата, тиамина (витамин В1), рибофлавина, фолиевой кислоты.
ВЛАДЕТЬ: навыками распознавания ароматических гетероциклов в составе биологически значимых соединений (витаминов, гормонов…).
Обучающие упражнения
Важнейшие биологически значимые гетероциклические и ароматические соединений, их синтезы и биосинтезы
Задание 1. Привести формулы и названия пятичленных гетероциклических соединений.
Ответ.
пиррол |
тиофен |
фуран |
индол |
азол |
тиол |
оксол |
бензазол |
Задание 2. Привести структуру важных производных пятичленных гетероциклов.
Ответ. Триптофан-предшественник гормонов –серотонина и мелатонина.
фурфурол – определяет запах свежеиспеченного хлеба, используется для синтеза антибактериальных средств Задание 3. Привести схему биосинтеза серотонина и мелатонина, указать их биологическую роль.
Ответ.
89

90


 гидроксилирование декарбоксилирование
гидроксилирование декарбоксилирование
триптамин
триптофан
алкилирование |
|
|
|
ацилирование |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
серотонин
мелатонин
Серотонин – синтезируется на свету, является гормоном радости, счастья, локально его концентрация возникает в местах воспаления, ушибов и вызывает боль. Мелатонин синтезируется из серотонина ночью, определяяет сексуальную активность, способствует засыпанию (природное снотворное). Обладает антиоксидантным, геронтологическим, противоопухолевым действием.
Задание 4. Показать схему реакций нитрования бензола, фенола, триптофана. Продукты нитрования окрашены в желтый цвет, в щелочной среде – в оранжевый, поэтому реакция используется как качественная для доказательства ароматической природы соединений.
Ответ.
Для ароматических аминокислот реакция носит название ксантопротеиновой. В реакцию вступают фенилаланин, гистидин, триптофан. По реакции косвенно ценят о качественной ценности белка, содержащего ароматические и гетероциклические аминокислоты.
90

91 |
Задание 5. Привести синтез фурфурола и его производных, обладающих антимикробным |
действием. Ответ: |
фурфурол |
рибоза |
Задание 6. Представить схему окисления гемоглобина с образованием биллирубина, |
определяющего цвет мочи. Уровень биллирубина в моче используется в качестве |
диагностического показателя. |
5-нитрофурфурол
гемоглобин
фурациллин
Ответ.
биллирубин
Задание 7. Привести формулы пятичленных двухгетероатомных циклов и их производных. Указать их биологическую роль.
Ответ:
На основе гистидина (производного имидазола) синтезируется гистамин (отвечает за образование ряда биологических жидкостей (слезы, сопли), высокие уровни гистидина вызывают алергизацию организма.
Пиразол используется для синтеза ряда обезболивающих средств (амидопирин, анальгин).
91
Пиразол (1,2-диазол)
Имидазол (1,3-диазол)

92 |
амидопирин |
анальгин |
Задание 8. Привести шестичленные одно- и двухатомные шестичленные гетероциклы и их |
биологически значимые производные.. |
Ответ. К шестичленным гетероциклам относится пиридин (азин), пиримидин (1,3-диазин), |
пиразин (1,4-диазин). |
Большое значение имеют производные пиридина (никотиновая кислота), витамин В6 (пиридоксальфосфат), а также урацил, тимин, цитозин, входяцие в структуру нуклеиновых кислот.
Никотиновая кислота |
пиридоксальфосфат (витамин В6) |
|
|
Урацил |
цитозин |
тимин |
Соединения могут находиться в фенольной (лактимной) форме или в виде лактамов, последние в структуре нуклеиновых кислот преобладают.
92

93
1.
Лактам-лактимная таутомерия производных пиримидина
Задание 9. Привести гетероциклические соединения с несколькими гетероатомами.
Ответ. К производным пиримидина и тиазола относится витамин В1 (аневрин), который влияет на работу мышц (сердца, кишечника и др.), деятельность нервной системы. При недостатке возникает болезнь бери-бери. Содержится в оболочке злаковых культур, отруби обогащены витаминами группы В.
Производным птеридина является витамин Вс (фолевая кислота), участвующая в синтезе белка и кроветворении.
Производными пурина являются ряд соединений. Некоторые из них (аденин, гуанин) входят в структуру нуклеиновых кислот.
Продуктами окисления пурина являются гипоксантин, ксантин, мочевая кислота. Мочевая кислота не растворяется в воде и биологических жидкостях. При нарушении пуринового обмена мочевая кислота может откладываться в суставах, что приводит к подагре, а также в почках (мочекаменная болезнь).
93

94
К производным пурина относят теофиллин, теобромин, кофеин. Потребление большого количества шоколада, какао, кофе, чая может усугублять болезни, связанные с нарушением пуринового обмена.
II. Задания для самостоятельного решения.
Задание 1. Докажите ароматичность бензола, индола, пиридина, хинолина. Приведите продукты нитрования указанных соединений.
Задание 2 Кислотно-основные свойства азотсодержащих гетероциклов (пиридина, хинолина, имидазола, пурина). Определение кислот и оснований по теории Бренстеда. Ряд основности. Получение солей Задание 3. Напишите основные реакции превращения гистидина в организме человека
(декарбоксилирование, дезаминирование), назовите продукты.
Задание 4. Тиофен. Структура гетероцикла. Биотин (витамин Н) - кофермент, участвующий в переносе карбоксильных групп.
Задание 5. Пиридин. Структура, критерии ароматичности, природа гетероатома. Биологически активные производные пиридина. Пиридоксаль, пиридоксальфосфат (витамин В6).
Задание 6.. Пиримидин. Строение, природа гетероатомов, критерии ароматичности. Производные пиримидина: урацил, цитозин, тимин. Лактим-лактамная таутомерия.
Задание 7. Какой гетероцикл входит в состав гема. Какие ферменты в качестве активного центра содержат порфириновый цикл?
Задание 8. Пурин. Структура, природа гетероатомов. Продукты окисления пурина (гипоксантин, ксантин, мочевая кислота). Таутомерия. Алкалоиды группы пурина (кофеин, теофиллин, теобромин). Применение в медицине.
Задание 9.
Выполнить превращения:
CH3 |
|
|
|
|
|
|
|
|
|
[O] |
A |
NH3 |
|
t |
2 C2H5Cl |
||
|
|
|
B |
|
C |
|
D |
|
|
- H2O |
|
|
|
- H2O |
- 2 HCl |
||
N
Задание 10.
|
Окислительное |
|
|
|
|
|
дезаминирование |
|
А |
– |
β- |
||
|
индолилпировиноградная кислота |
|
|
|||
В |
- |
β- |
индолилуксусная кислота |
Задание 11. |
|
|
|
94

|
|
|
|
|
|
|
95 |
|
|
|
|
|
|
CH2 CH |
COOH |
|
|
|
C |
||
|
|
|
NH2 |
|
|
A |
|
B |
|
|
|
|
|
|
|
|
|
||||
|
N |
гидроксилирование |
- CO2 |
ацилир., алкилир |
||||||
|
|
|
||||||||
|
H |
|
|
|
|
|
|
|
||
А – 5-гидрокситриптофан В – серотони С – мелатонин
Задание 12. Приведите формулы салициловой (I), пара-аминобензойной (II), сульфаниловой кислот (III). Укажите значение этих кислот для организма человека.
Ответ:
I |
II |
III |
Салициловая кислота (I) синтезируется в организме, снижает свертываемость крови, проявляет жаропонижающее и противовоспалительное действие. На ее основе создано ряд препаратов. Пара-аминобензойная кислота (ПАБК) (II) является составной частью фолиевой кислоты, участвующей в кроветворении и синтезе белков. Замещенные производные ПАБК блокируют синтез белков у микроорганизмов и используются в качестве консервантов пищевых продуктов. На основе структуры фолиевой кислоты, включающей модифицированную (измененную) молекулу ПАБК, создана группа антибиотиков и противоопухолевых средств. Сульфаниловая кислота (III) близка по своим размерам ПАБК, на ее основе создана группа сульфаниламидных препаратов, используемых в качестве антибиотиков
Задания для самостоятельного решения.
Задание 1. Докажите ароматичность бензола, индола, пиридина, хинолина. Приведите продукты нитрования указанных соединений.
Задание 2 Кислотно-основные свойства азотсодержащих гетероциклов (пиридина, хинолина, имидазола, пурина). Определение кислот и оснований по теории Бренстеда. Ряд основности. Получение солей Задание 3. Напишите основные реакции превращения гистидина в организме человека
(декарбоксилирование, дезаминирование), назовите продукты.
Задание 4. Тиофен. Структура гетероцикла. Биотин (витамин Н) - кофермент, участвующий в переносе карбоксильных групп.
Задание 5. Пиридин. Структура, критерии ароматичности, природа гетероатома. Биологически активные производные пиридина. Пиридоксаль, пиридоксальфосфат (витамин В6).
Задание 6.. Пиримидин. Строение, природа гетероатомов, критерии ароматичности. Производные пиримидина: урацил, цитозин, тимин. Лактим-лактамная таутомерия.
Задание 7. Какой гетероцикл входит в состав гема. Какие ферменты в качестве активного центра содержат порфириновый цикл?
Задание 8. Пурин. Структура, природа гетероатомов. Продукты окисления пурина (гипоксантин, ксантин, мочевая кислота). Таутомерия. Алкалоиды группы пурина (кофеин, теофиллин, теобромин). Применение в медицине.
Задание 9. Выполнить превращения:
95

|
|
|
|
|
96 |
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
[O] |
A |
NH3 |
|
t |
2 C2H5Cl |
||
|
|
|
B |
|
C |
|
D |
|
|
- H2O |
|
|
|
- H2O |
- 2 HCl |
||
N
Задание 10.
Окислительное
дезаминирование
А – β-индолилпировиноградная кислота В - β-индолилуксусная кислота
Тестовые задания для самостоятельного решения
1.Укажите формулу триптофана
а) |
б) |
в)  г) 2.Укажите формулу индола (бензпиррола).
г) 2.Укажите формулу индола (бензпиррола).
а) |
б) |
в)  г)
г)  3.Предшественником биосинтеза в организме мелатонина является:
3.Предшественником биосинтеза в организме мелатонина является:
а) |
фенилаланин |
б) |
триптофан |
|
в) |
гистидин |
|
г) |
цистеин |
4. Предшественником биосинтеза серотонина является |
||||
а) |
триптофан |
|
б) |
глицин |
в) |
гистидин |
|
г) |
фенилаланин |
5.Укажите формулу фурфурола (фуран-2-карбальдегида).
а) |
б) |
96

97
в)  г)
г)  6. Выберите из предложенных формул никотиновую кислоту (пиридин-3-карбоновую кислоту).
6. Выберите из предложенных формул никотиновую кислоту (пиридин-3-карбоновую кислоту).
а) |
б) |
в)  г) 7.Приведенное ниже соединение является витамином:
г) 7.Приведенное ниже соединение является витамином:
а) |
А |
б) |
В1 |
в) |
Н |
г) |
D |
8. Приведенная ниже формула отражает структуру:
а) |
пурина |
|
б) |
гипоксантина |
в) |
гемоглобина |
г) |
каталазы |
|
9. |
Укажите формулу витамина РР (амида никотиновой кислоты). |
|||
а) |
б) |
в)  г)
г)  10.Укажите формулу пиридоксина (лекарственной формы витамина В6)
10.Укажите формулу пиридоксина (лекарственной формы витамина В6)
97

98
а) |
б) |
в) |
г) |
11.Укажите формулу имидазола (1,3-диазола). |
|
а) |
б) |
в) |
г) |
|
|
|
12. Салициловая кислота является |
|
|
|
|
а) |
п.-сульфобензойной кислотой |
б) |
п.-аминобензойной кислотой |
|
в) |
п.-бензолдикарбоновой кислотой |
г) |
о.-гидроксибензойной кислотой |
|
13. Фолевая кислота в своей структуре содержит остаток: |
||||
а) |
п. –аминобнзойной кислоты |
|
б) |
терефталевой кислоты |
в) |
сульфаниловой кислоты |
г) |
никотиновой кислоты |
|
14. Витамин В1 в своей структуре включает гетероциклы:
а) |
пиридина и тиофена |
б) |
пиримидина и тиазола |
в) |
пурина и имидазола |
г) |
пиперидина и тиазола |
Занятие 1.3.4. ТЕМА: Важнейшие α-аминокислоты, пептиды.
ЦЕЛЬ: Сформировать знания о строении и свойствах важнейших -аминокислот как химических основах структурной организации белковых молекул для дальнейшего изучения биологических функций белков на молекулярном уровне.
ЗНАТЬ:
1. Строение аминокислот. Классификация. Основы стереоизомерии.
98

99
2.Кислотно-основные свойства аминокислот. Биполярный ион, катионная, анионная формы. Изоэлектрическая точка. Показатель кислотности аминокислот.
3.Химические свойства аминокислот:
а) реакции по аминогруппе; б) реакции по карбоксильной группе;
в) специфические и биологически важные реакции аминокислот (трансаминирование, окислительное дезаминирование, элиминирования, декарбоксилирование, окисление тиольных групп); г) реакции в радикалах характеристических группах.
4.Образование, строение и свойства пептидной связи. Дипептиды, трипептиды, первичная структура белка.
5.Важнейшие пептиды: глутатион, карнозин, 6-аминопенициллоновая кислота, инсулин, окситоцин, вазопрессин, метионин - энкефалин, лейцин - энкефалин.
6.Первичная, вторичная, третичная, четвертичная структура белков. Функции белков в организме. Денатурация белков. Протеиды и протеины.
7.Свойства растворов высокомолекулярных соединений (ВМС).
УМЕТЬ:
1.Приводить структуры -аминокислот, их классификацию по характеру бокового радикала.
2.Приводить схемы равновесия катионных, анионных, и диполярных форм для нейтральных,
кислых и основных -аминокислот.
2.Показывать химизм реакций декарбоксилирования, окислительного дезаминирования, элиминирования, окисления тиольных групп -аминокислот.
3.Образовывать дипептиды, трипептиды, тетрапептиды..., уметь их называть, выделять пептидную связь с обозначением электронных эффектов.
4.Приводить схемы гидролиза пептидов.
ВЛАДЕТЬ: Навыками проведения цветных реакций (нингидринная, биуретовая, ксантопротеиновая, «формольное титрование», выявления меркаптогруппы) обнаружения - аминокислот и пептидов с обоснованием результатов .
Обучающие упражнения Задание 1. Один из стереоизомеров 2-амино-3-гидроксибутановой кислоты (треонин) входит в состав белков. Какие стереоизомеры возможны для треонина?
Ответ: в молекуле треонина два центра хиральности
H3C |
|
CH |
CH COOH |
|
|||
|
|
OH |
NH2 |
Изобразим возможные стереоизомеры в виде проекционной формулы Фишера
|
|
|
COOH |
|
|
COOH |
|
|
COOH |
|
COOH |
|||||||||
H2N |
|
|
|
H H |
|
|
|
NH2 |
H |
|
|
NH |
H N |
|
|
|
H |
|||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
|
|
|
|
|
HO |
|
|
|
|
H |
H |
|
|
|
OH |
HO |
|
|
|
H |
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
CH3 |
|
|
CH3 |
|
CH3 |
|||||||||||
|
|
I |
|
|
II |
|
|
|
III |
|
|
IV |
||||||||
L-алло-треонин |
D-алло-треонин |
|
|
D-треонин |
|
L-треонин |
||||||||||||||
Для отнесения амино- и гидроксикислот к стереохимическим рядам, используется так называемый “гидроксильный ключ”, когда рассматривается конфигурация хирального центра с наименьшим номером.
99

100
По этому правилу стереоизомеры I и IV относятся к L ряду, а II и III к D-ряду. В состав белков входит L-треонин IV. Соединения I и II имеют эритроконфигурацию, т.е. заместители находятся в проекции Фишера по одну сторону углеродной цепи, в этом случае еще используется приставка алло-.
Заключение: I и II, III и IV - энантиомеры; I и III; I и IV; II и III; II и IV; диастереомеры. Задание 2. На примере -аланина и триптофана опишите схему образования биполярной структуры. Получите дипептиды образованные этими аминокислотами. Каковы особенности строения пептидной связи?
Ответ: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- H+ |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
H3N |
|
|
|
|
|
CH |
COOH |
|
|
|
|
|
|
|
|
|
|
H3N |
|
|
|
CH |
COO |
|
|
|
|
|
|
|
H N |
|
|
|
CH |
COO |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+H+ |
2 |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|||||||
|
|
|
|
|
|
|
|
pKa1=2,3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
pKa2=9,7 |
|
|
|
||||||||||||
катионная форма |
|
|
|
|
|
|
|
|
|
|
биполярный ион |
|
|
|
анионная форма |
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
В кислой среде -аминокислоты существуют в виде катионной формы, в щелочной в виде |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
анионной и в изоэлектрической точке в виде биполярного иона, т.е. одинаковое количество |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
катионной и анионной форм. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
pJ |
|
pKa1 |
pKa 2 |
,это формула для определения изоэлектрической точки |
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
2 |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
pJ |
|
|
|
|
|
|
|
2,3 9,7 |
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
ала |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- H+ H N |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
H N |
|
|
|
CH |
|
COOH |
- H+ H N |
|
|
CH |
|
COO |
|
|
|
CH |
|
COO |
|
|
|
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+H+ |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
+H |
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
HN |
|
|
|
|
|
|
|
|
|
|
HN |
|
|
|
|
|
|
|
|
HN |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
катионная форма |
|
|
биполярный ион |
|
|
анионная форма |
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
рКа1=2,4 |
|
|
|
|
|
|
|
pJтри=5,9 |
|
|
|
|
|
|
рКа2=9,4 |
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
При взаимодействии триптофана и -аланина могут образовываться четыре дипептида: |
|||||||||||||||||||||||||||||||||||||||||||||
Три-Ала, Ала-Три, Ала-Ала, Три-Три. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
H N |
|
CH |
|
C |
|
OH + H2N |
|
|
CH |
|
C |
|
OH |
|
|
|
H N |
|
|
CH |
|
C |
|
N |
|
|
CH |
|
C |
|
OH |
|||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-H2O |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
CH |
|
CH2 |
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
CH |
||||||||||||||||||||||||||
3 |
|
|
|
|
HN |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
HN |
|
2 |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
аланилтриптофан Ала-Три |
|||||||||||||||||||||
100

101
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2N |
|
|
|
CH |
|
|
C |
|
|
OH |
+ H N |
|
|
|
CH |
|
|
|
C |
|
OH |
|
|
|
|
|
|
H N |
|
|
CH |
|
|
|
C |
|
N |
|
CH |
|
C |
|
OH |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-H2O |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
CH |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
3 |
|
|
|
|
|
|
|
|
CH |
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
аланилаланин Ала-Ала |
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
H N |
|
|
CH |
|
C |
|
|
|
|
OH + |
H N |
|
CH |
|
C |
|
|
|
|
OH |
|
|
|
|
|
|
H2N |
|
|
|
|
|
CH |
|
C |
N |
CH C |
OH |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
CH |
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
2 |
|
|
|
|
H2C |
|
|
||||||||||||||||||||||||
HN |
|
2 |
|
|
|
|
|
|
|
|
|
|
HN |
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HN |
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
триптофанилтриптофан Три-Три
Строение пептидной связи
В составе пептидной (амидной) группы -СО-NH- атом углерода в sp2 гибридном состоянии, атом азота тоже в sp2 состоянии, неподеленная пара электронов атома азота вступает в сопряжение с - электронами двойной связи С=О. Пептидная группа представляет собой трехцентровую - р сопряженную систему, в которой электронная плотность смещена к кислороду, атомы С,О,N находятся в одной плоскости.
H |
H |
N |
N |
C |
C |
O |
O |
Вращение вокруг связи С-N затруднено, поэтому пептидная группа имеет плоскую, жесткую структуру.
Задание 3. Написать реакции внутри- и межмолекулярной конденсации , и аминокислот.
Ответ:
а) -аминокислоты при нагревании претерпевают межмолекулярную дегидратацию, при этом от двух молекул кислоты отщепляются две молекулы воды:
|
|
|
|
|
O |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
H2N |
|
|
t |
C |
|
|
NH |
|
||
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|||
H2C |
|
CH2 |
|
|
H C |
|
CH |
|
|||
|
|
|
|
|
|||||||
|
|
- 2H2O |
2 |
|
|
|
|
|
2 |
||
|
|
|
|
|
|
|
|
||||
NH2 |
HOOC |
|
|
|
|
|
|
|
|
||
|
|
|
HN |
|
C |
|
|||||
|
|
|
|
|
|
|
|||||
O
б) -аминокислоты при нагревании отщепляют аммиак с образованием непредельных кислот:
|
|
|
|
t |
|||
H3C |
|
CH CH2 COOH |
|
|
H3C HC |
|
CH COOH |
|
|
|
|
||||
|
|
|
|||||
|
|
|
|
||||
|
|
|
- NH3 |
||||
|
|
NH2 |
|
|
|
|
|
β-аминомасляная кислота |
|
|
кротоновая кислота |
||||
в) - аминокислоты претерпевают внутримолекулярную дегидратацию:
101

102
H2C |
|
|
CH2 |
|
|
|
t |
H2C CH2 |
|
||||
|
|
|
|
|
|
||||||||
H2C |
C |
|
O |
|
|
|
|
C |
|
||||
|
|
|
|
|
|||||||||
|
|
|
|||||||||||
|
|
- H2O |
H C |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
2 |
|
O |
N H HO |
|
|
|
|
|
|
N |
||||||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
H |
|
||||
γ-аминомасляная кислота |
|
γ-бутиролактон или пирралидон-2 |
|
||||||||||
Задания для самостоятельной работы Задание 1. Напишите основные реакции превращения гистидина в организме человека. Назовите продукты.
Задание 2. Напишите схему метаболизма триптофана в организме человека (окислительное дезаминирование, декарбоксилирование, гидроксилирование), приводящие к образованию - индолилпировиноградной кислоты, -индолилуксусной кислоты, триптамина, серотонина и мелатонина.
Задание 4. На примере фенилаланина напишите уравнения реакций аминокислот с гидроксидом меди, азотной кислотой, формальдегидом. Получите дипептиды фенилаланина с глицином, назовите их.
Задание 5. Напишите реакции, образования дикетопиперазина и дипептида α-аланина. Задание 6. Реакции гидроксилирования, как способ окисления непредельных и ароматических углеводородов. Продукты гидроксилирования фенилаланина, триптамина. Названия продуктов гидроксилирования.
Задание 7. Приведите уравнение реакции, по которой можно определить наличие в белке остатков аминокислот (цистеина, метионина), содержащих атомы серы.
Задание 8. Напишите структурные формулы цистеинилаланина.
Задание 9. Напишите строение трипептидного фрагмента - валил-глицил-аланина. Изобразите электронное строение пептидной группы.
Задание 10. Приведите строение дипептида гистидилаланина.
Задание 11. Напишите схему образования биполярной структуры аминокислот на примере триптофана и -аланина. Получите дипептиды, образованные этими аминокислотами. Задание 12. На пример -аланина напишите уравнения реакций аминокислот с уксусным ангидридом, йодистым метилом, формальдегидом, метанолом(Н+).
Тестовые вопросы
1.Укажите формулу цистеина (2-амино3-меркаптопропановая кислота):
А) HSH2C–(NH2)HC–COOH; Б) (H3C)2HC–(NH2)HC–COOH; В) HОH2C–(NH2)HC–COOH; Г) H2N–CH2–COOH
2.Какие из перечисленных аминокислот относят к ароматическим: А) метионин (2-амино-3-метилтиопропановая кислота); Б) лейцин (2-амино-5-метилпентановая кислота);
В) тирозин (2-амино-3-гидроксифенилпропановая кислота; Г) пролин (2-карбоксипирролидин)
3.Изоэлектрическая точка белка рI=4,8. Какой заряд имеет этот белок в растворе с рН=6,7?
А) положительный -; |
COO- |
|
|
R |
|
Б) отрицательный - |
NH2 ; |
В) нулевой |
|
Г) не имеет заряда 
 4.Какое соединение образуется при декарбоксилировании серина
4.Какое соединение образуется при декарбоксилировании серина
102
