
- •I. Основные понятия и законы химии
- •1. Если числа молекул разных газов одинаковы, то при одних и тех же внешних условиях эти газы занимают одинаковые объёмы.
- •2. Плотность газа (ρ) – величина, численно равная отношению его молярной массы к молярному объёму при н. У.:
- •3. Относительная плотность газа х по газу y () – величина, численно равная отношению молярных масс этих газов:
- •4. Стехиометрические коэффициенты в уравнениях реакций между газами пропорциональны объёмам данных газов.
- •II. Строение атома
- •1. Ядерная модель строения атома. Состав атомных ядер. Атомный номер. Массовое число. Нуклиды. Изотопы. Явление радиоактивности. Воздействие радиоактивного излучения на живую материю.
- •III. Периодический закон и периодическая система элементов д. И. Менделеева
- •IV. Химическая связь и строение веществ
- •H─Cl (степень окисления хлора равна –1, валентность – I),
- •6. Ионная и металлическая связь. Механизм образования ионной связи. Степень ионности связи. Ионные кристаллические решетки. Координационное число иона.
- •9. Молекулярное и немолекулярное строение веществ. Молекулярные, атомные и ионные соединения. Графические и структурные формулы веществ. Газообразное и конденсированное состояния веществ.
- •Алгоритм анализа строения молекулярных частиц
- •Сокращённый вариант записи алгоритма
- •V. Химическая кинетика и термодинамика
- •VI. Растворы
- •VII. Окислительно-восстановительные реакции
- •2. Овр внутримолекулярного типа.
- •1. Оценить окислительно-восстановительные свойства веществ.
- •2. Предсказать принципиальную возможность осуществления реакции в указанном направлении.
- •4. Выбрать наиболее вероятную реакцию из нескольких возможных.
- •5. Рассчитать значение константы химического равновесия данной реакции.
- •6. Оценить влияние различных факторов на направление протекания окислительно-восстановительных реакций
- •4. Коррозия металлов. Основные виды коррозии металлов. Методы защиты металлов от коррозии.
- •VIII. Комплексные соединения
- •IX. Водород и элементы группы viia
- •Простые вещества
- •Водород
- •Галогены и их соединения
- •Бинарные соединения галогенов
- •X. Элементы группы via
- •Простые вещества
- •Взаимосвязь важнейших соединений серы:
- •XI. Элементы группы va
- •Простые вещества
- •4. Получение простых веществ. Получение азота в лабораторных условиях и в промышленности. Общие принципы получения фосфора, мышьяка, сурьмы и висмута.
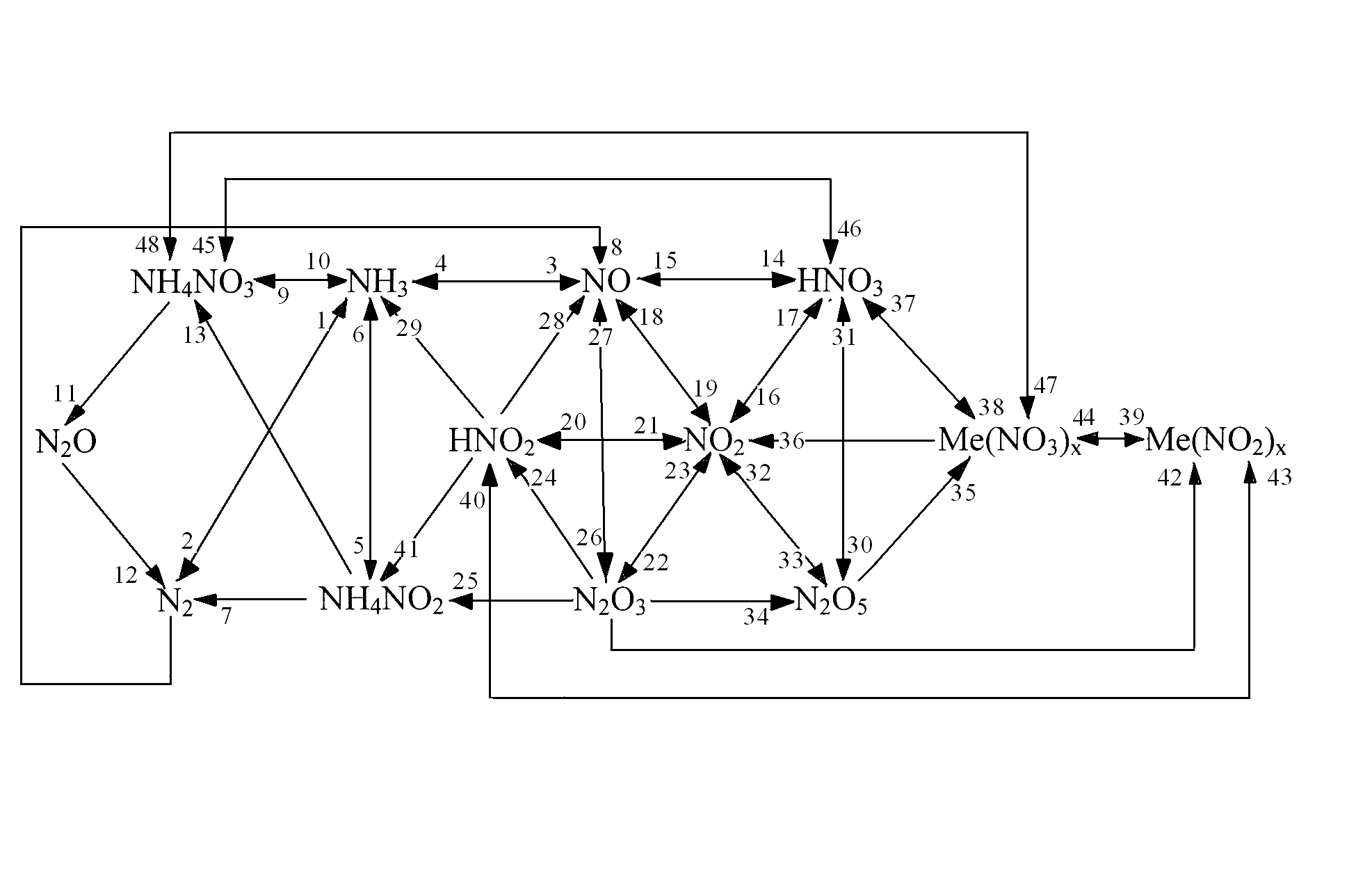
- •Взаимосвязь важнейших соединений азота:
- •Взаимосвязь важнейших соединений фосфора:
- •Хii. Элементы группы IV а
- •Простые вещества
- •Взаимосвязь важнейших соединений углерода:
- •XIII. Металлы
- •Металлы главных подгрупп
- •Взаимосвязь важнейших соединений натрия:
- •Взаимосвязь важнейших соединений кальция:
- •Взаимосвязь важнейших соединений алюминия:
- •4. Подгруппа германия. Общая характеристика элементов. Сопоставление их физических и химических свойств со свойствами углерода и кремния.
- •Взаимосвязь важнейших соединений марганца:
- •Взаимосвязь важнейших соединений железа:
- •Взаимосвязь важнейших соединений меди:
Взаимосвязь важнейших соединений азота:
N
 2
+ 3H2
2
+ 3H2
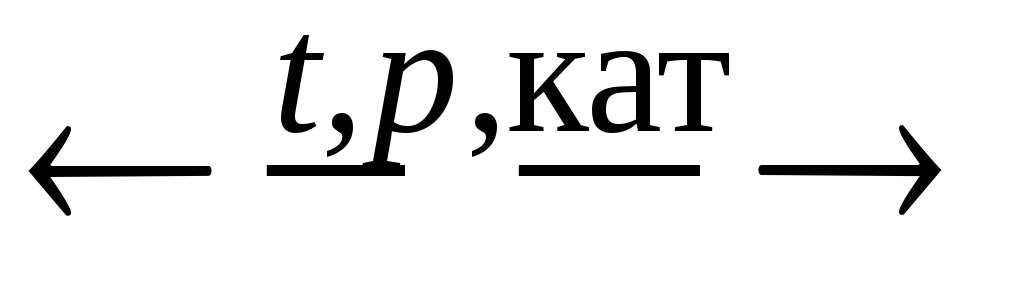 NH3;
NH3;NH3
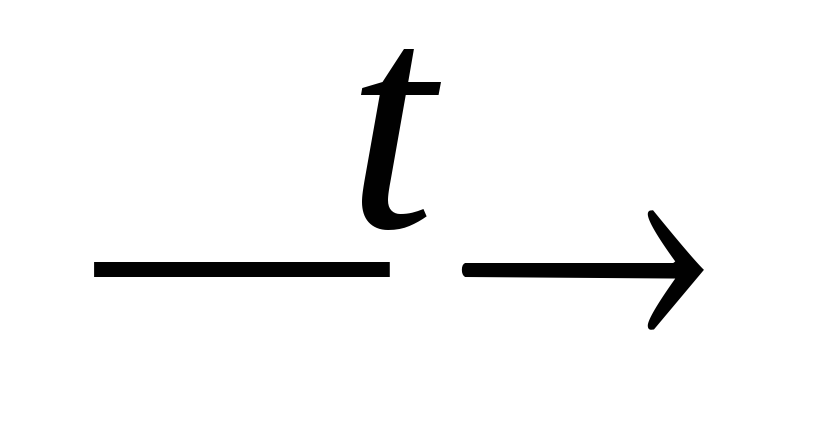 N2
+ H2;
N2
+ H2;NH3 + O2
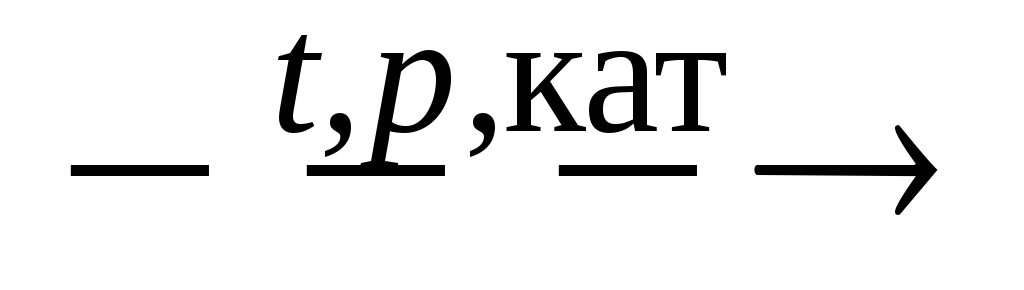 NO + H2O;
NO + H2O;NO + H2
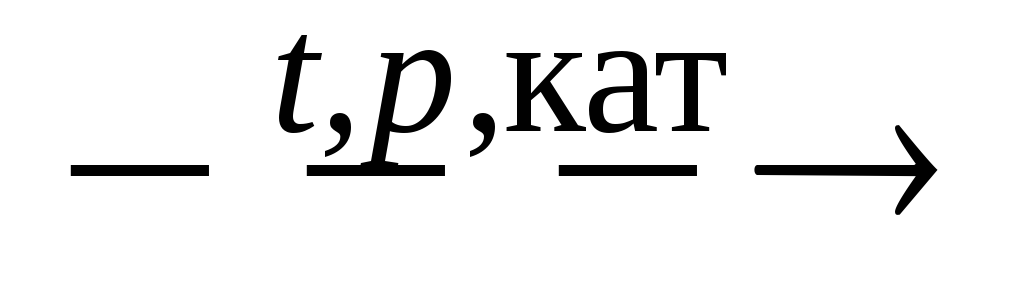 NH3
+ H2O;
NH3
+ H2O;NH3 + HNO2 (охл.р-р) → NH4NO2;
NH4NO2 + KOH
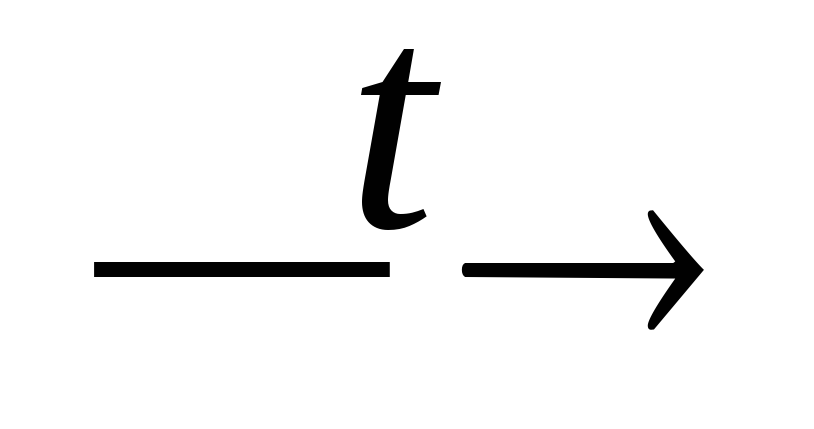 NH3
+
+H2O
+ KNO2;
NH3
+
+H2O
+ KNO2;NH4NO2
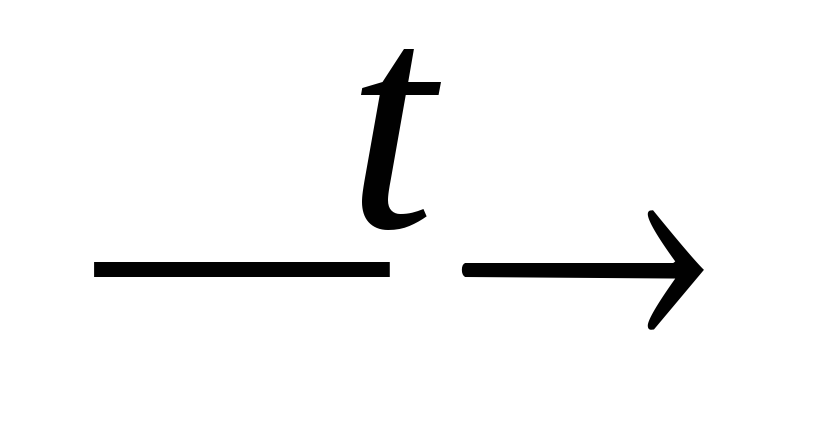 N2
+ H2O;
N2
+ H2O;N2 + O2
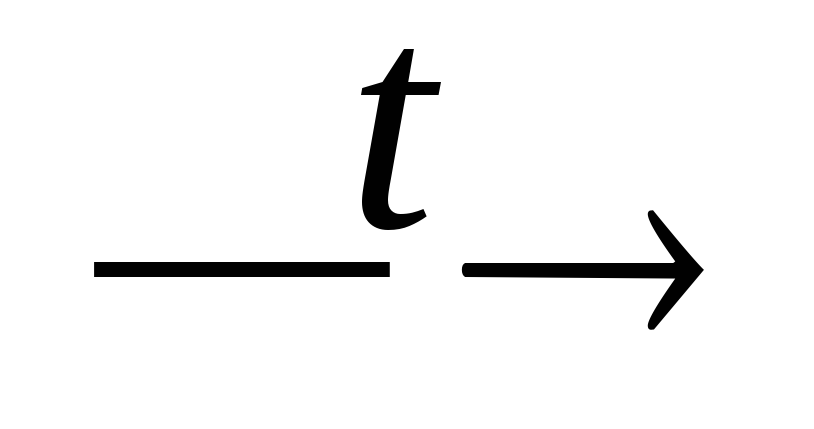 NO;
NO;NH3 + HNO3 → NH4NO3;
NH4NO3 + KOH
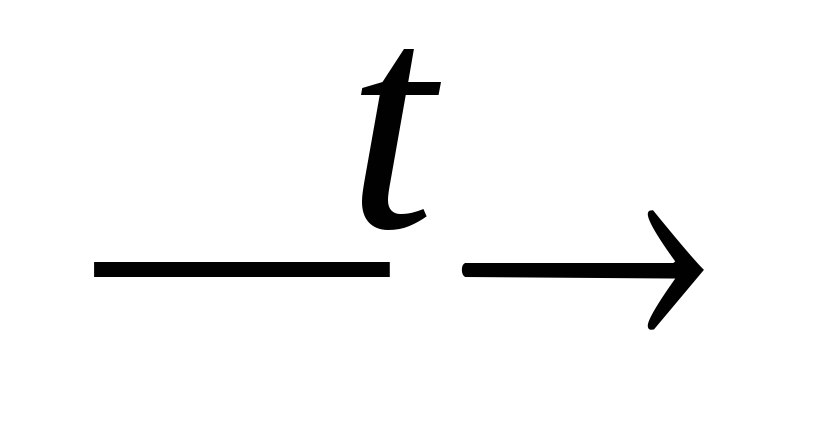 NH3
+ H2O
+ +KNO3;
NH3
+ H2O
+ +KNO3;NH4NO3
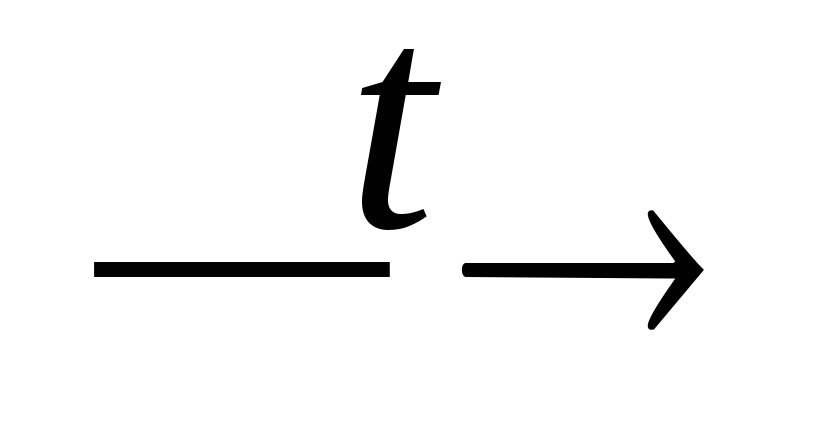 N2O
+ H2O;
N2O
+ H2O;N2O
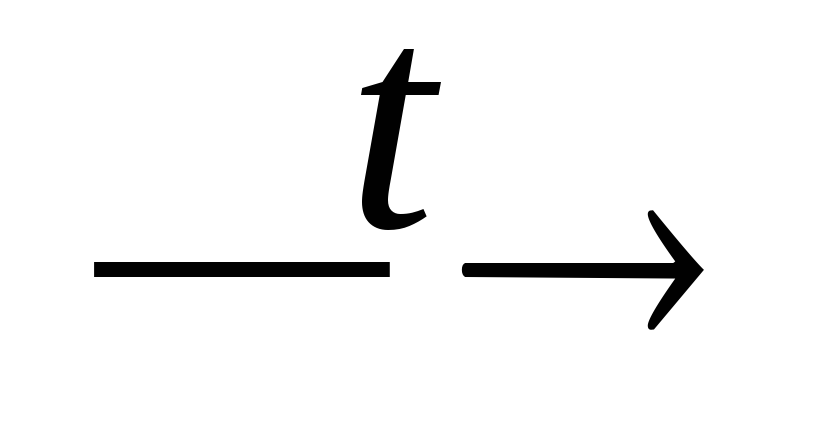 N2
+ O2;
N2
+ O2;NH4NO2 + Br2 + H2O → NH4NO3 + HBr;
NO + KMnO4 + H2SO4 → HNO3 + MnSO4 + K2SO4 + H2O;
HNO3(разб.) + Cu
 NO
+ Cu(NO3)2
+ H2O;
NO
+ Cu(NO3)2
+ H2O;HNO3(конц..) + Cu → NO2 + Cu(NO3)2 + H2O;
NO2 + O2 + H2O → HNO3;
NO2
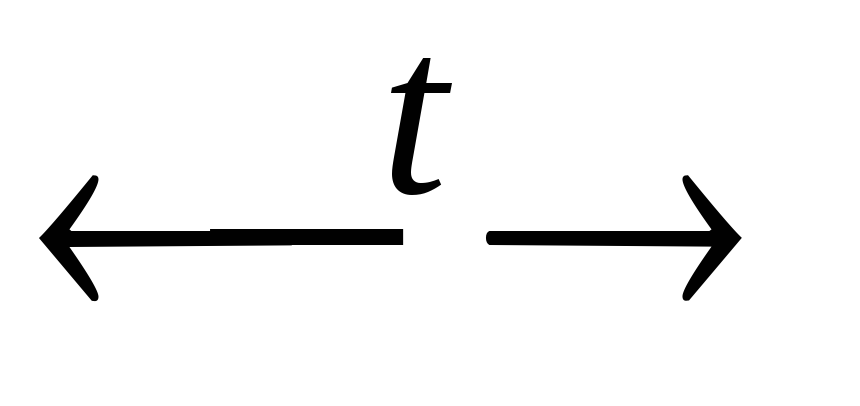 NO + O2;
NO + O2;NO + O2 → NO2;
NO2 + H2O
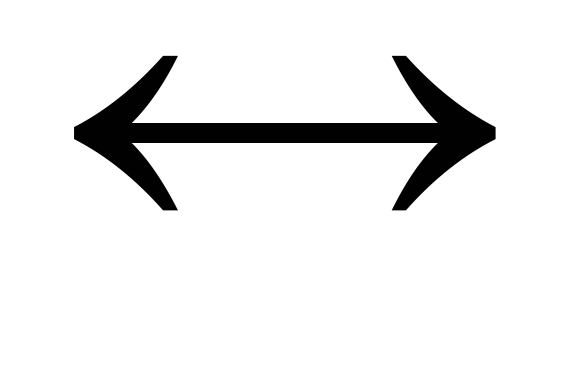 HNO2
+ HNO3;
HNO2
+ HNO3;HNO2(р-р)
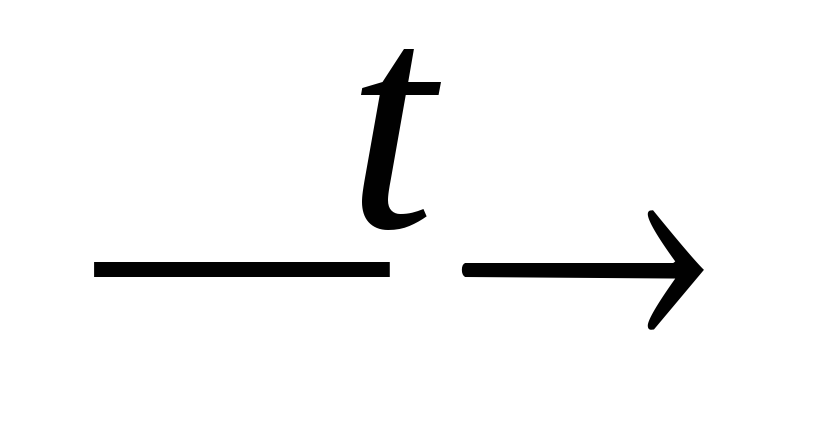 NO2
+ NO↑ + H2O;
NO2
+ NO↑ + H2O;NO2 + NO
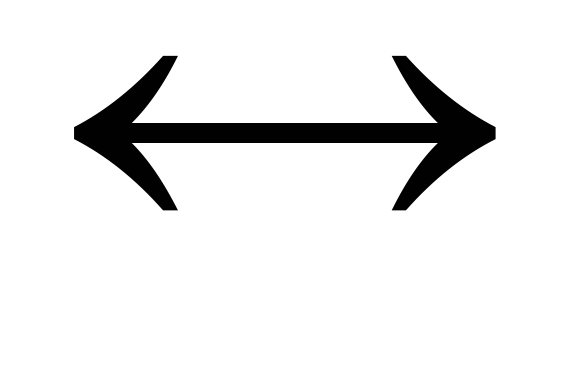 N2O3;
N2O3;N2O3
 NO2
+ NO;
NO2
+ NO;N2O3 + H2O → HNO2;
N2O3 + H2O + NH3 → NH4NO2;
См. № 22;
См. № 23;
См. № 21;
HNO2 + Na[AlH4] + H2O → NH3↑ + Na[Al(OH)4];
HNO3 + P2O5
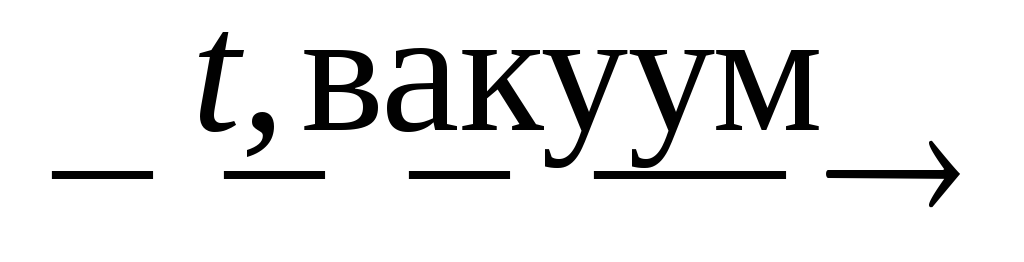 N2O5↑
+ +HPO3;
N2O5↑
+ +HPO3;N2O5 + H2O → HNO3;
N2O5
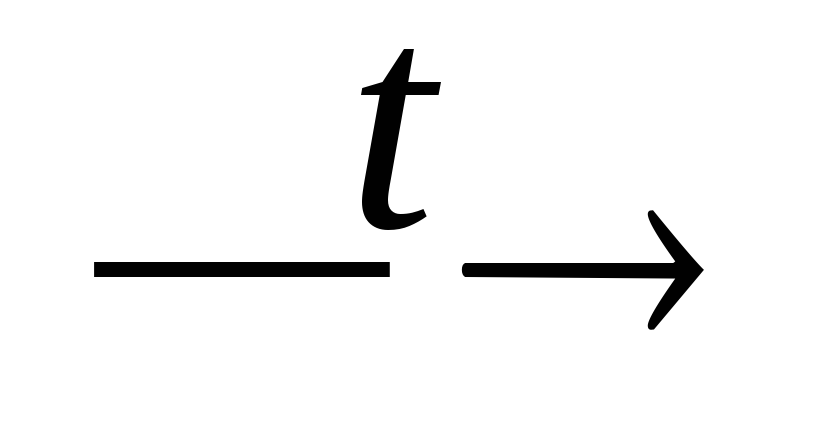 NO2
+ O2;
NO2
+ O2;NO2 + O3 → N2O5 + O2;
N2O3 + O3 → N2O5 + O2;
N2O5 + CuO → Cu(NO3)2;
Cu(NO3)2
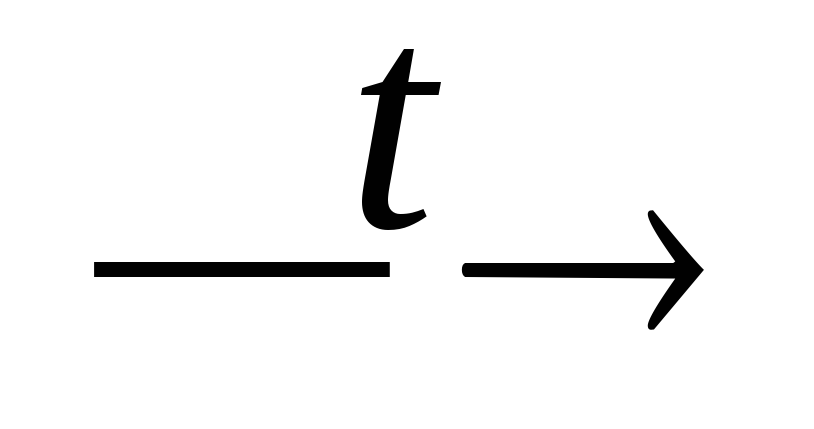 NO2
+ CuO + O2;
NO2
+ CuO + O2;Cu(NO3)2 + H2SO4(конц.)
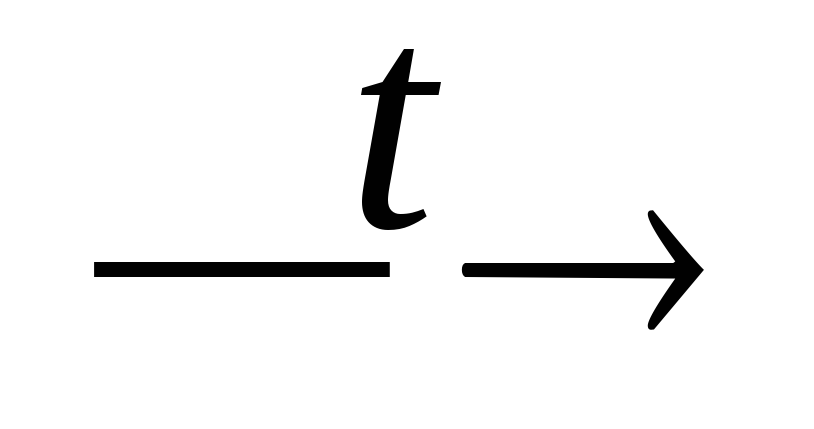 HNO3↑+
CuSO4;
HNO3↑+
CuSO4;HNO3 + KOH → KNO3 + H2O;
KNO3
 KNO2 +
O2;
KNO2 +
O2;KNO2(охл.) + HCl(охл..) → HNO2 + +KCl;
HNO2 + NH3 → NH4NO2;
N2O3 + KOH → KNO2 + H2O;
HNO2 + KOH → KNO2 + H2O;
KNO2 + Cl2 + H2O → KNO3 + НCl;
NH3 + HNO3 → NH4NO3;
NH4NO3 + H2SO4(конц.)
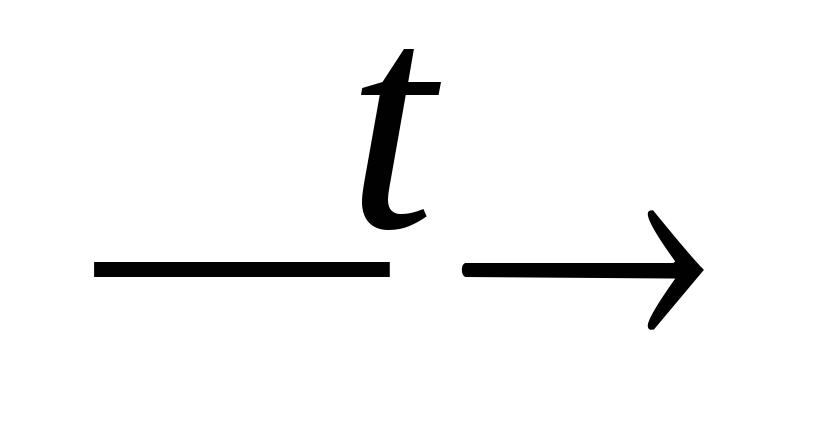 HNO3↑
+ NH4HSO4;
HNO3↑
+ NH4HSO4;NH4NO3 + Ba(OH)2
 NH3↑
+ Ba(NO3)2;
NH3↑
+ Ba(NO3)2;Ba(NO3)2 + (NH4)2CO3 → BaCO3↓ + NH4NO3.
Взаимосвязь важнейших соединений фосфора:
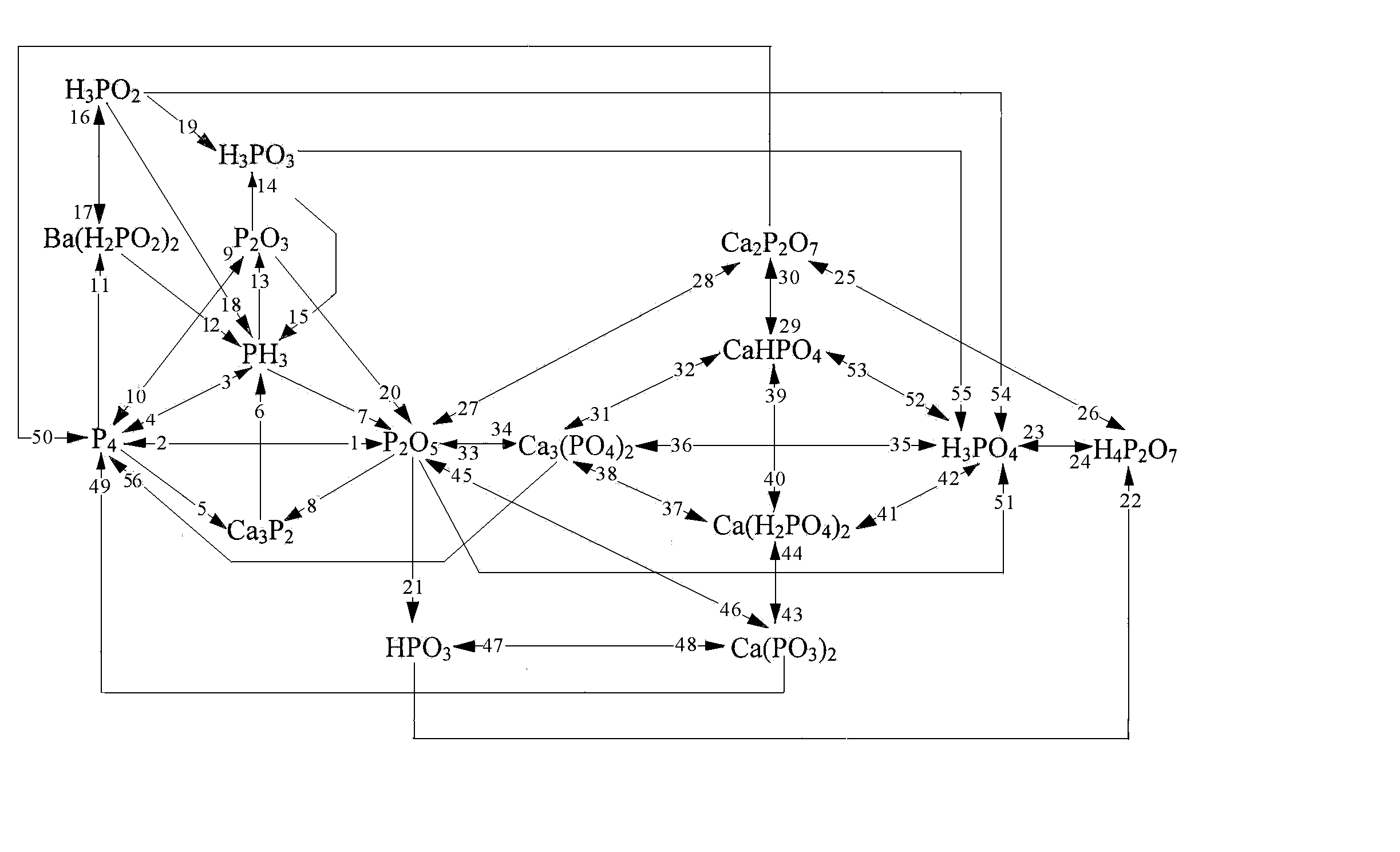
P4 + O2 (изб.)
 P2O5;
P2O5;P2O5 + C
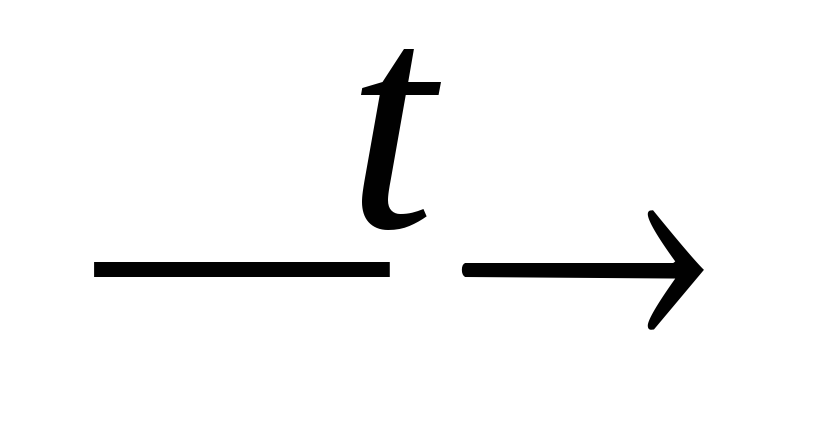 P4
+ CO;
P4
+ CO;P4 + Ba(OH)2 + H2O
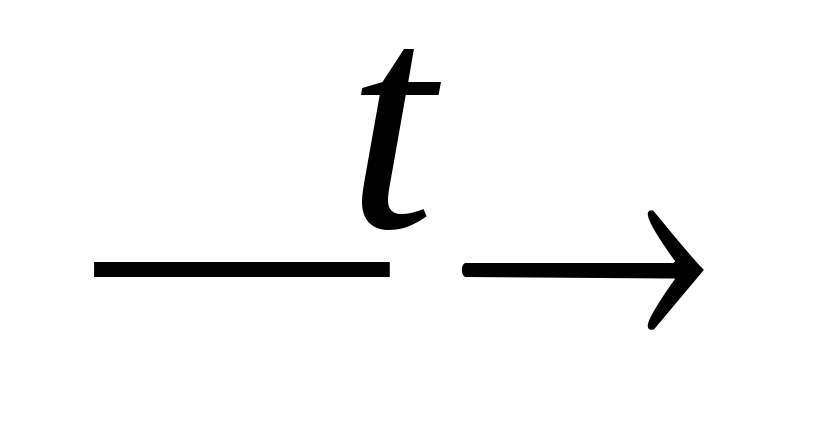 PH3
+ Ba(H2PO2)2;
PH3
+ Ba(H2PO2)2;PH3
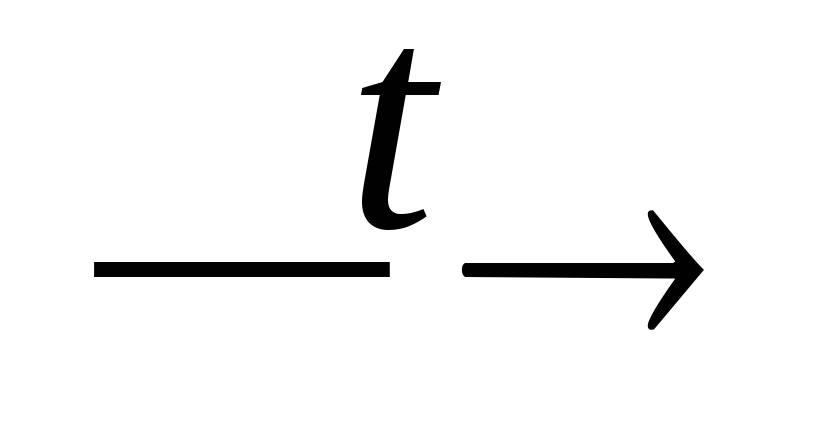 P4
+ H2;
P4
+ H2;P4 + Ca
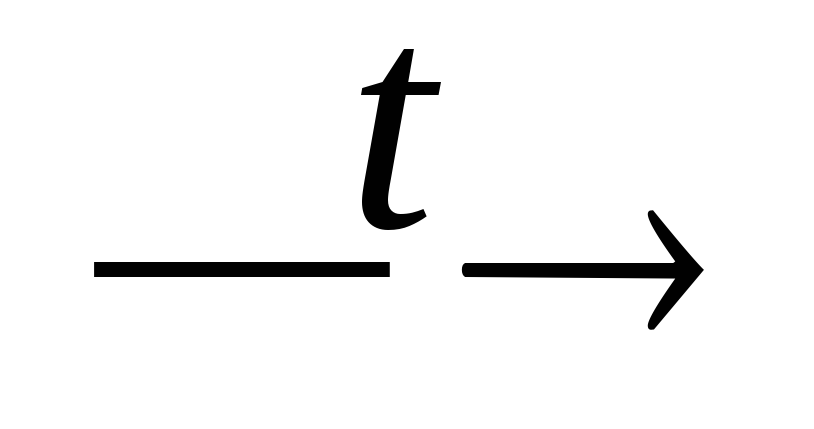 Ca3P2;
Ca3P2;Ca3P2 + HCl → PH3 + CaCl2;
PH3 + O2 (изб.)
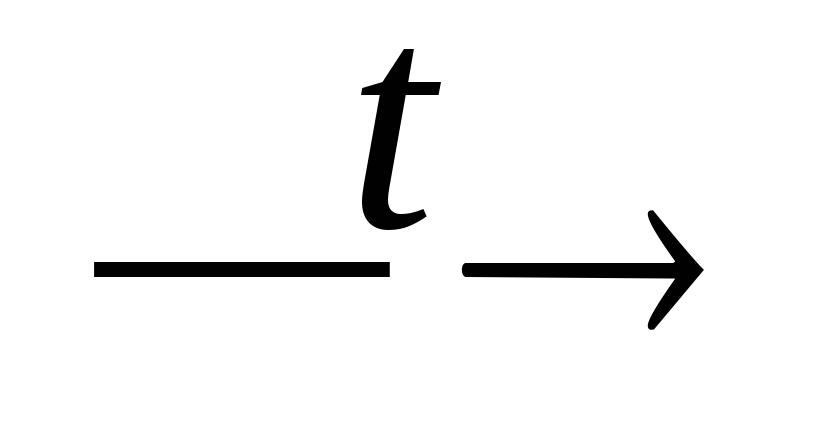 P2O5
+
H2O;
P2O5
+
H2O;P2O5 + Ca
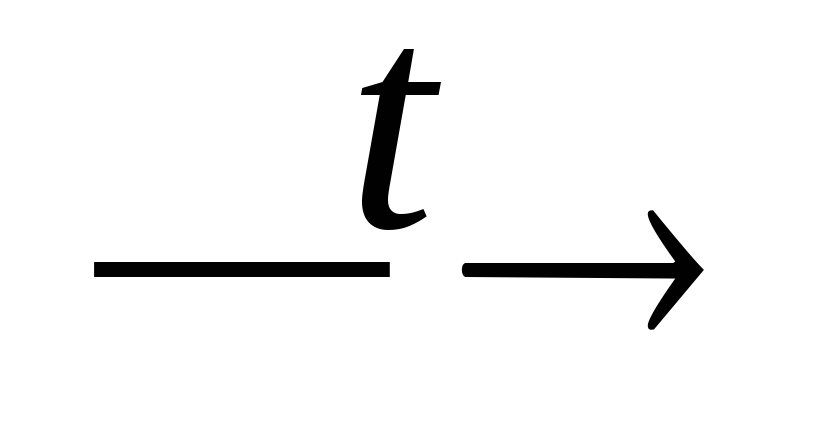 Ca3P2
+ Ca3(PO4)2;
Ca3P2
+ Ca3(PO4)2;
P4 + O2 (нед.)
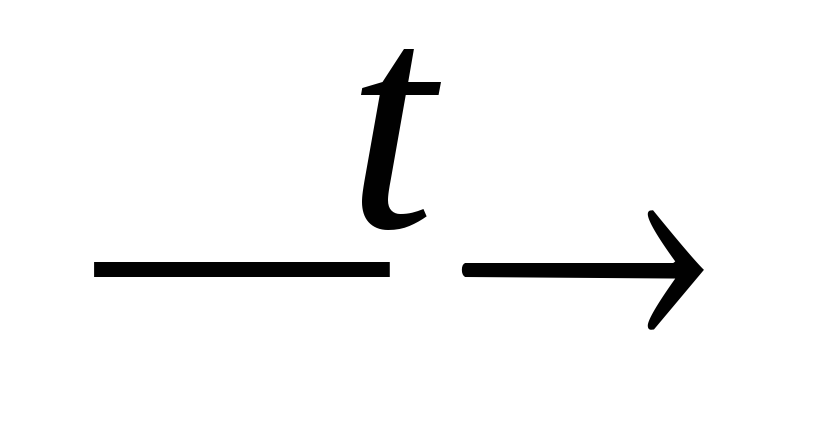 P2O3;
P2O3;P2O3
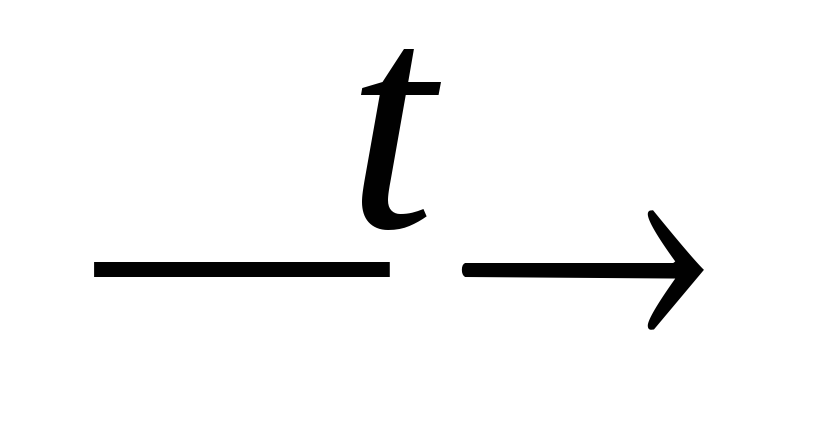 P4
+ P2O5;
P4
+ P2O5;См. № 3;
Ba(H2PO2)2
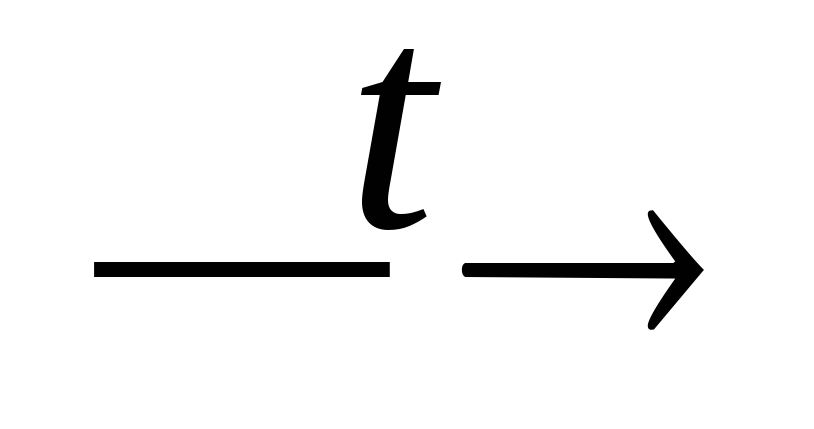 PH3
+ BaHPO4;
PH3
+ BaHPO4;PH3 + O2 (нед.)
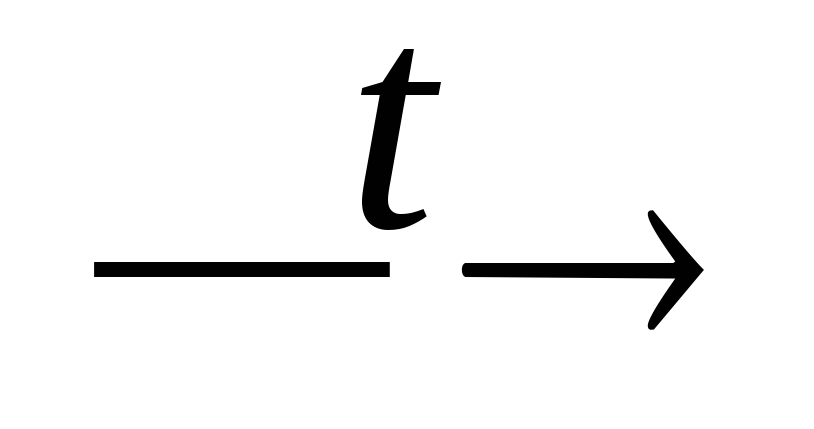 P2O3
+
H2O;
P2O3
+
H2O;P2O3 + H2O (охл.) → H3PO3;
H3PO3
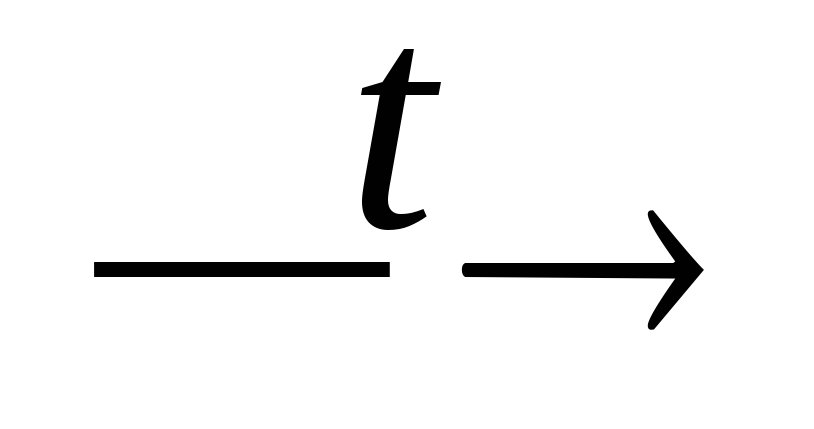 PH3
+ H3PO4;
PH3
+ H3PO4;Ba(H2PO2)2 + H2SO4 → H3PO2 + BaSO4;
H3PO2 + Ba(OH)2 → Ba(H2PO2)2 + H2O;
H3PO2
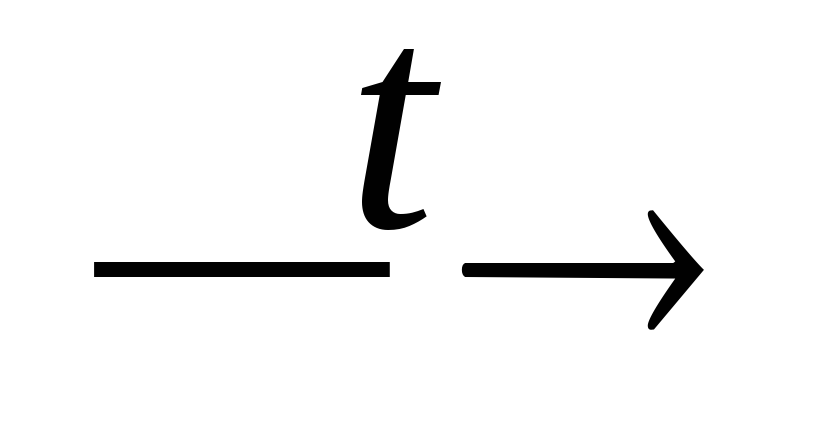 PH3
+ H3PO3;
PH3
+ H3PO3;Cм. № 18;
P2O3 + O2
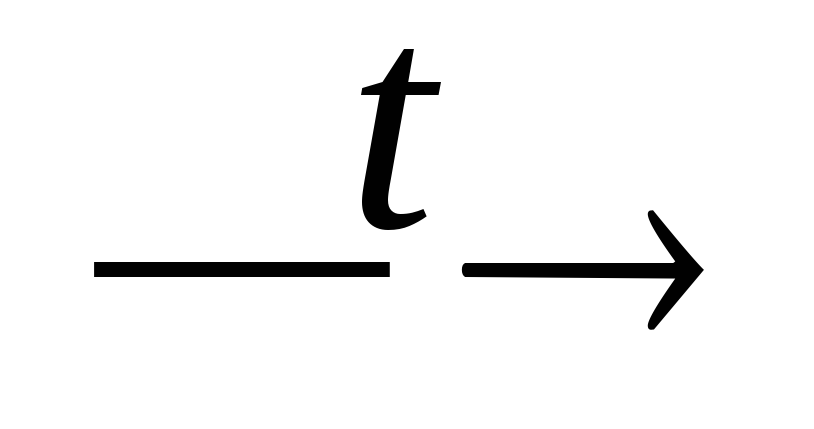 P2O5;
P2O5;P2O5 + H2O (охл.) → HPO3;
HPO3 + H2O
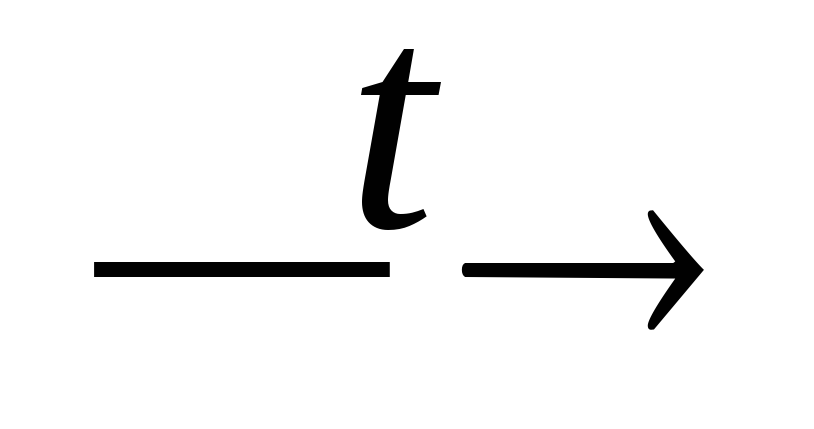 H4P2O7;
H4P2O7;H4P2O7 + H2O
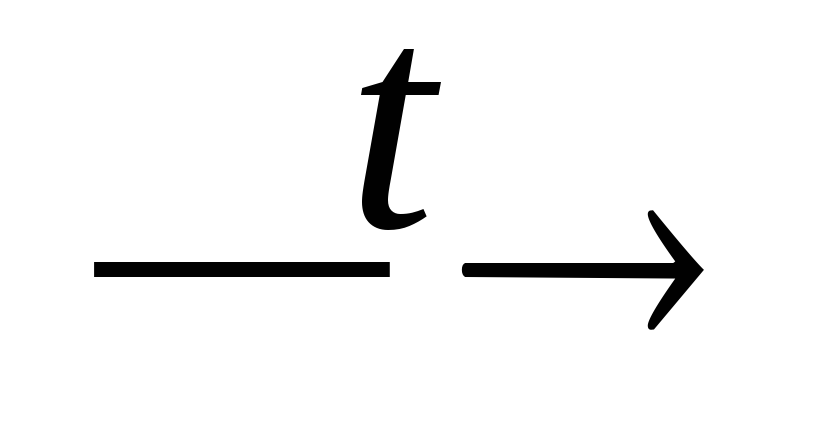 H3PO4;
H3PO4;H3PO4 (распл.)
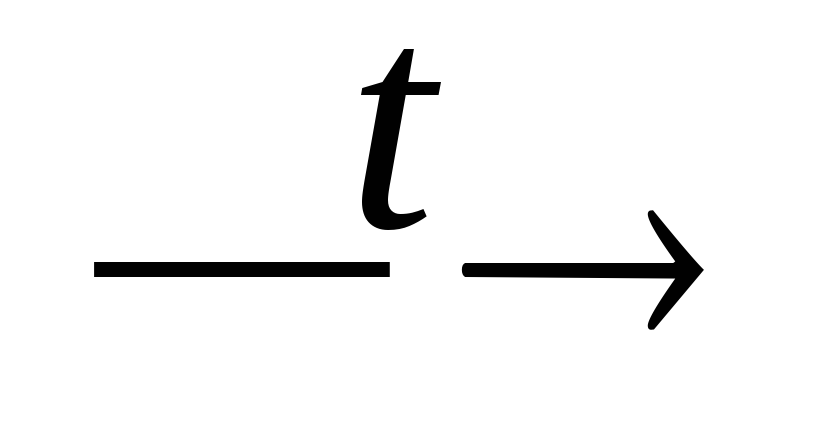 H4P2O7
+ H2O;
H4P2O7
+ H2O;H4P2O7 + Ca(OH)2 → Ca2P2O7 + H2O;
Ca2P2O7 + H2SO4 → H4P2O7 + CaSO4;
Ca2P2O7 + SiO2
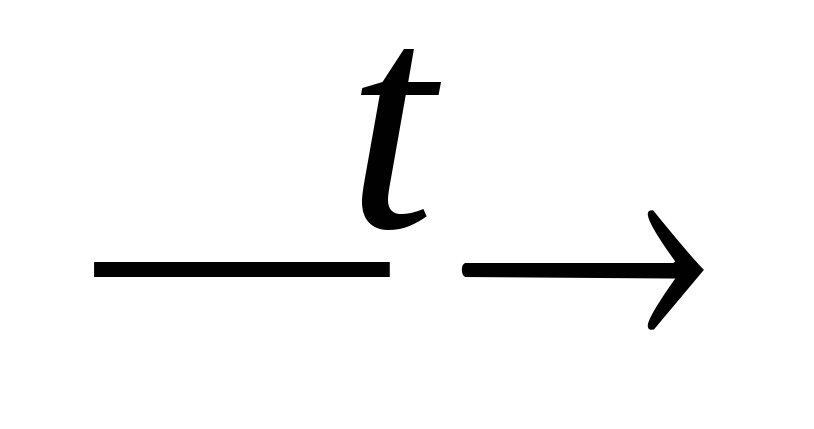 P2O5↑
+ CaSiO3;
P2O5↑
+ CaSiO3;P2O5 + CaO
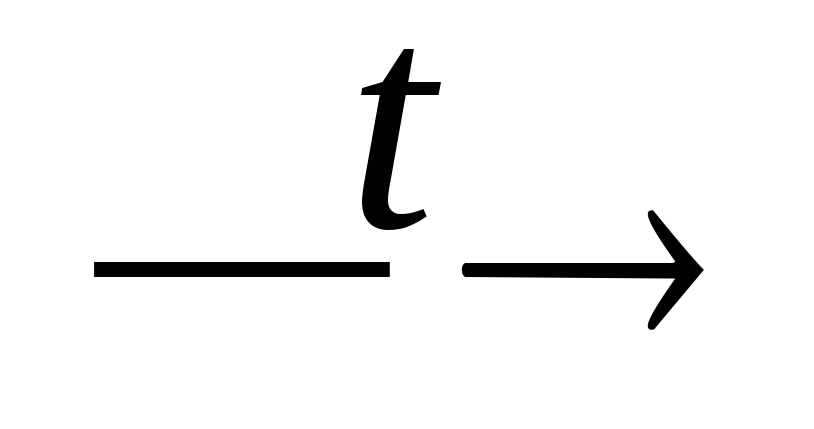 Ca2P2O7;
Ca2P2O7;Ca2P2O7 + H2O
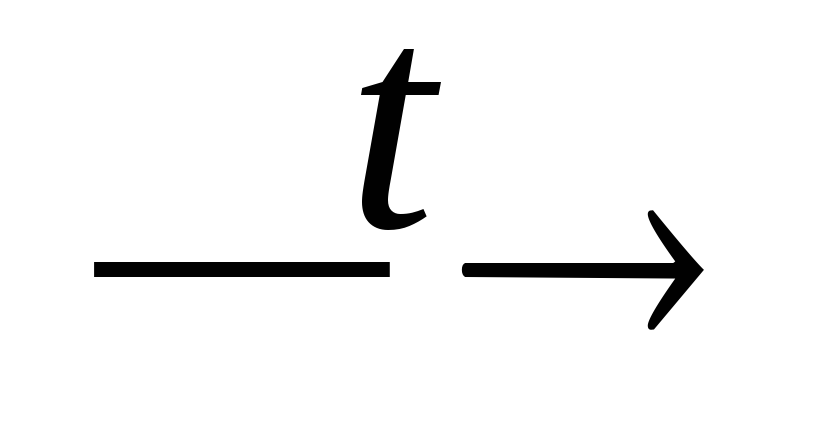 CaHPO4;
CaHPO4;CaHPO4
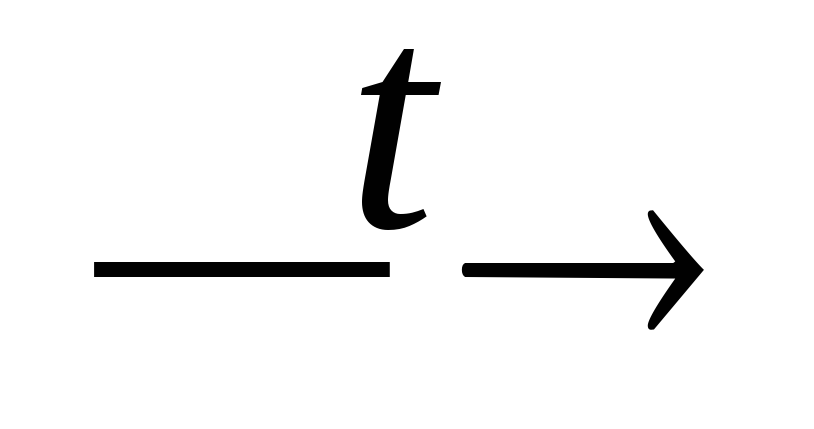 Ca2P2O7
+ H2O;
Ca2P2O7
+ H2O;CaHPO4 + Ca(OH)2 → Ca3(PO4)2 + H2O;
Ca3(PO4)2 + H3PO4 → CaHPO4;
Ca3(PO4)2 + SiO2
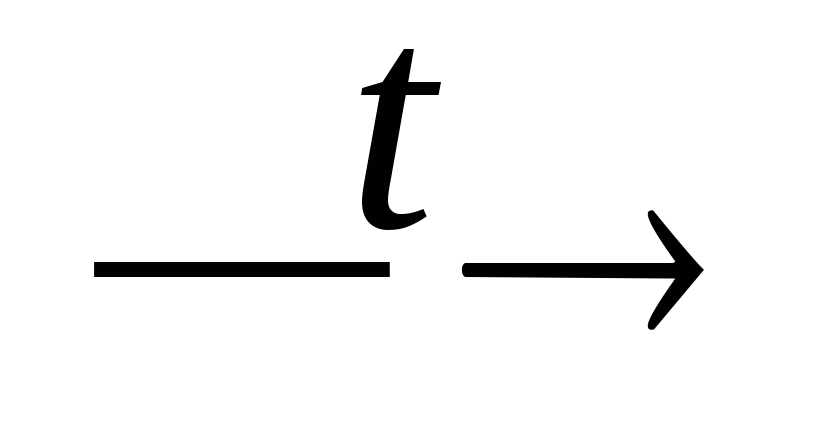 P2O5↑
+ CaSiO3;
P2O5↑
+ CaSiO3;P2O5 + CaO
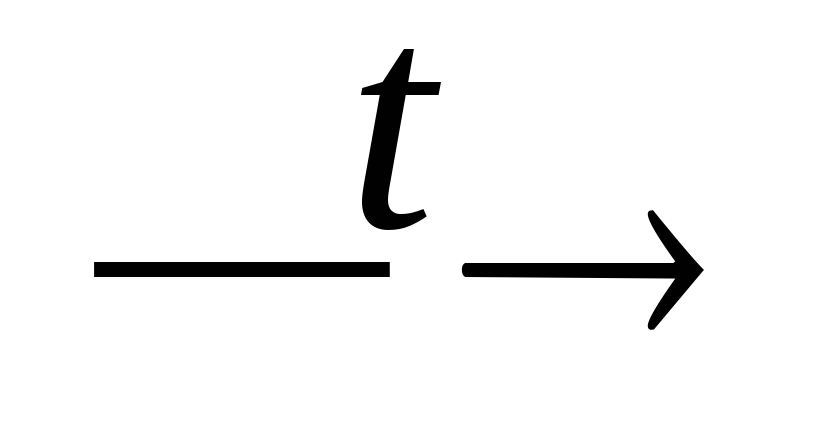 Ca3(PO4)2;
Ca3(PO4)2;Ca3(PO4)2 + H2SO4 → H3PO4 + CaSO4;
H3PO4 + Ca(OH)2 → Ca3(PO4)2 + H2O;
Ca3(PO4)2 + H3PO4 → Ca(H2PO4)2;
Ca(H2PO4)2 + Ca(OH)2 → Ca3(PO4)2 + H2O;
Ca(H2PO4)2 + Ca(OH)2 → CaHPO4 + H2O;
CaHPO4 + H3PO4 → Ca(H2PO4)2;
H3PO4 + Ca(OH)2 → Ca(H2PO4)2 + H2O;
Ca(H2PO4)2 + H2SO4 → H3PO4 + CaSO4;
Ca(H2PO4)2
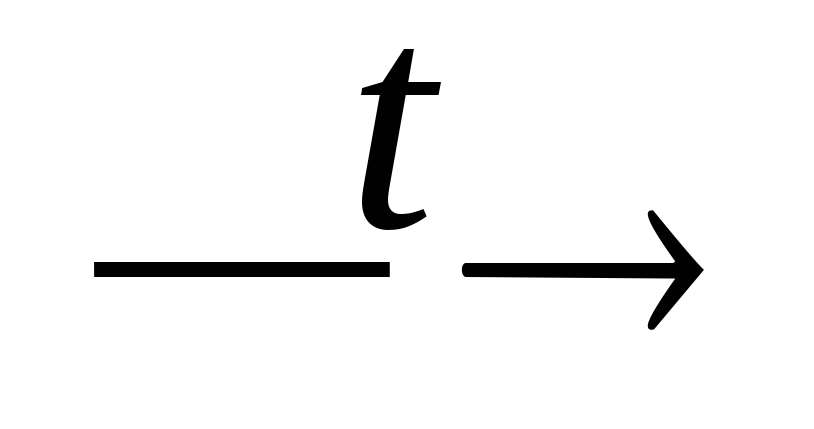 Ca(PO3)2
+ H2O;
Ca(PO3)2
+ H2O;Ca(PO3)2 + H2O
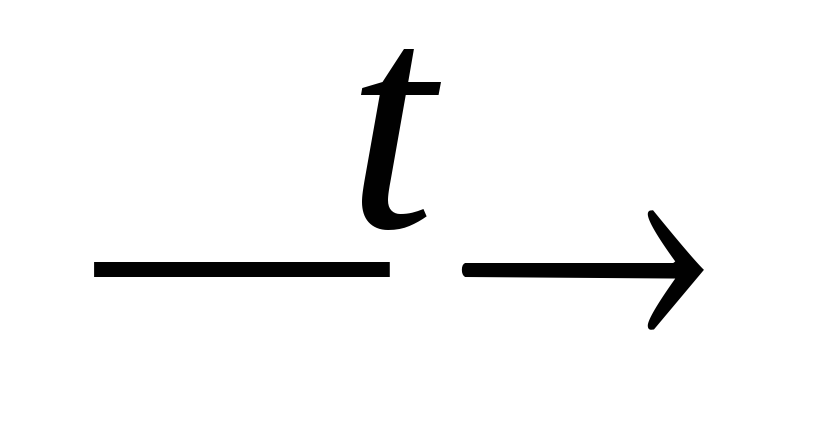 Ca(H2PO4)2;
Ca(H2PO4)2;Ca(PO3)2 + SiO2
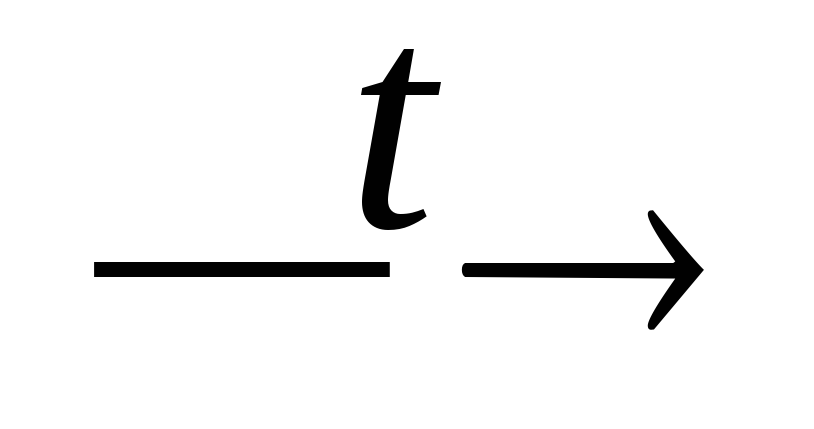 P2O5↑
+ CaSiO3;
P2O5↑
+ CaSiO3;P2O5 + CaO
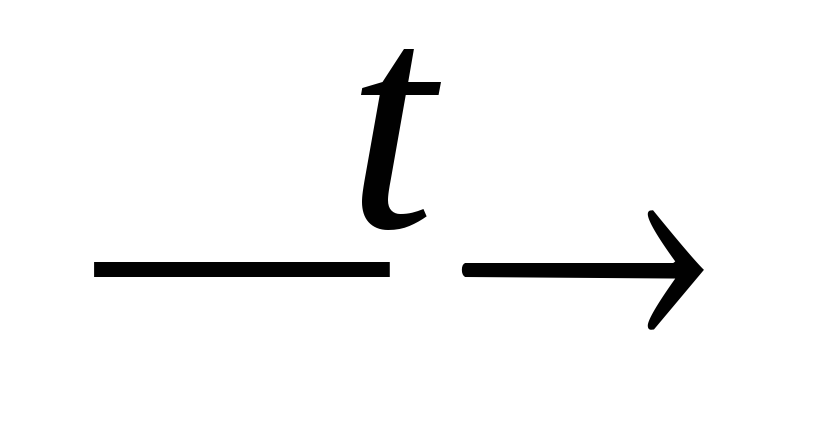 Ca(PO3)2;
Ca(PO3)2;Ca(PO3)2 + H2SO4 (охл.) → HPO3 + CaSO4;
HPO3 + Ca(OH)2 → Ca(PO3)2 + H2O;
Ca(PO3)2 + SiO2 + С
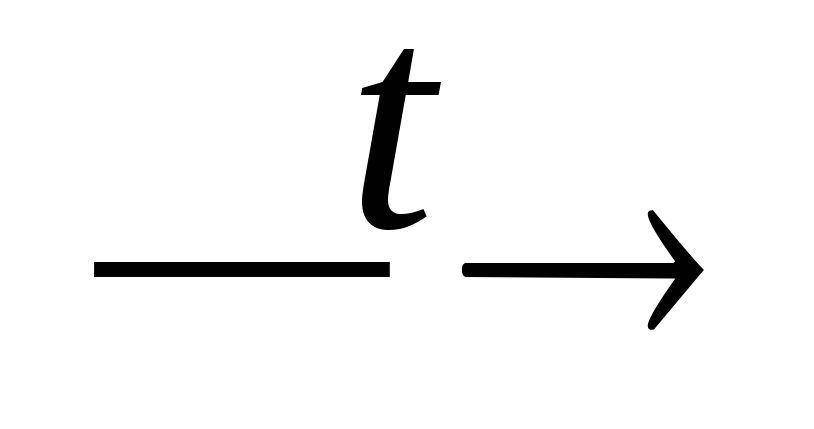 P4↑
+ CaSiO3
+ CO;
P4↑
+ CaSiO3
+ CO;Ca2P2O7 + SiO2 + С
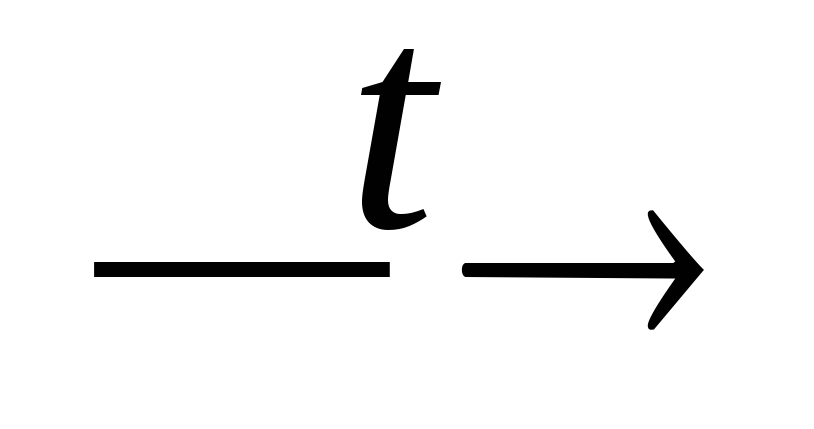 P4↑
+ CaSiO3
+ CO;
P4↑
+ CaSiO3
+ CO;P2O5 + H2O
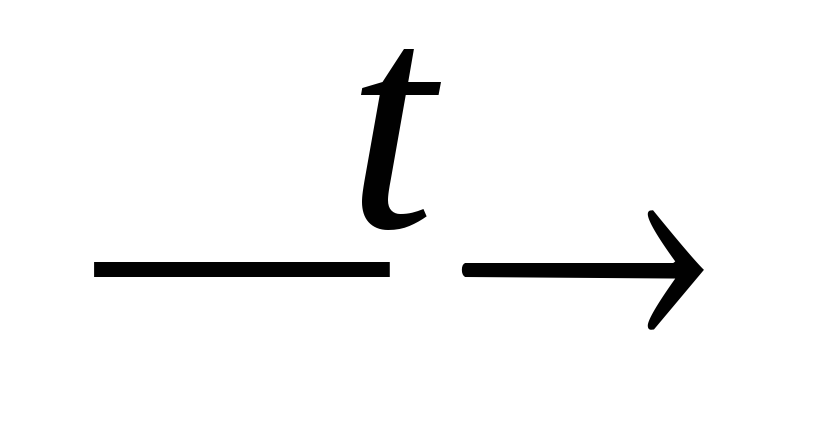 H3PO4;
H3PO4;CaHPO4 + H2SO4 → H3PO4 + CaSO4;
H3PO4 + Ca(OH)2 → CaHPO4 + H2O;
H3PO2
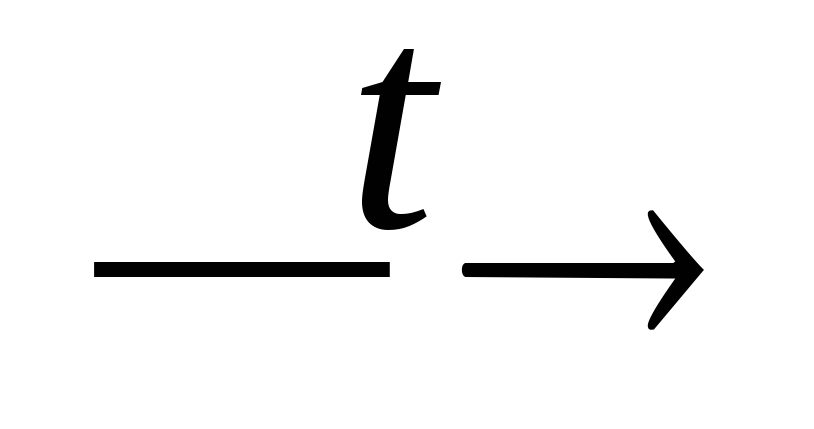 H3PO4
+ PH3;
H3PO4
+ PH3;H3PO3
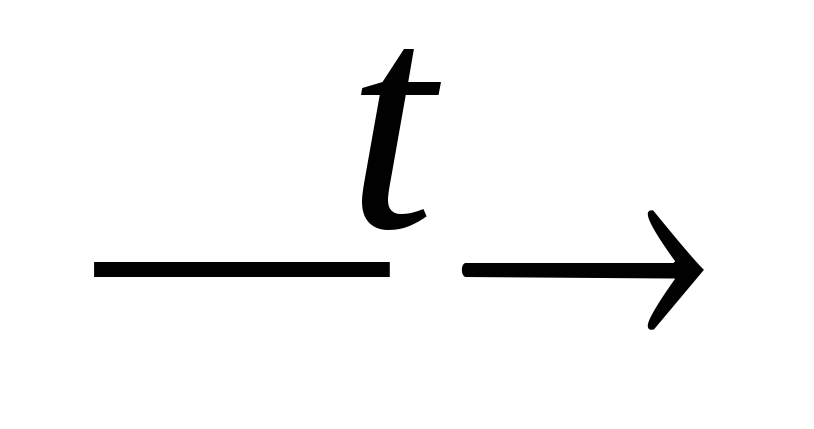 H3PO4
+ PH3;
H3PO4
+ PH3;Ca3(PO4)2 + SiO2 + С
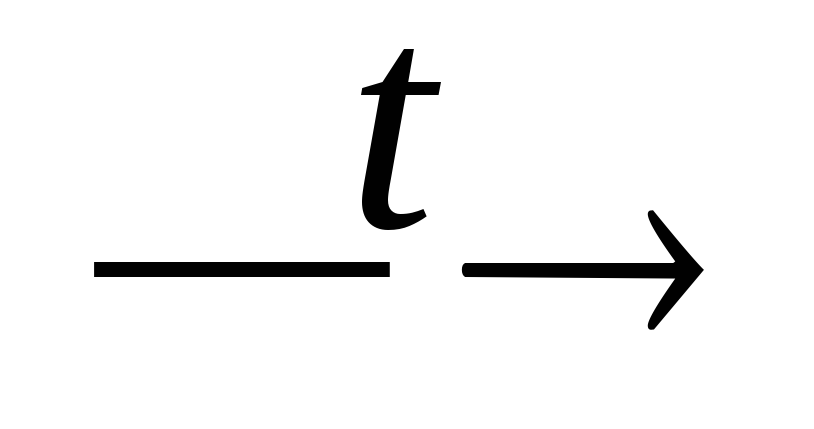 P4↑
+ CaSiO3
+ CO;
P4↑
+ CaSiO3
+ CO;
