1 семестр / Ни́кель
.docxМИНОБРНАУКИ РОССИИ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
«МОСКОВСКИЙ АВИАЦИОННЫЙ ИНСТИТУТ (национальный исследовательский университет)» (МАИ)
Институт №2
«Аэрокосмические конструкции, технологии и системы управления»
Кафедра
«Общая химия, физика и химия композиционных материалов»
РЕФЕРАТ
НИКЕЛЬ
по дисциплине
«ОБЩАЯ ХИМИЯ»
Студент:
Фамилия И.О.
Группа:
Полный номер группы
Преподаватель: Ряховская Е.В.
Фамилия И.О.
Отметка о выполнении (защиты) работы
Дата (защиты работы)
Москва 2016
Оглавление
Положение металла в периодической системе Д.И.Менделеева 3
Проявляемые металлом степени окисления в его соединениях 3
Местоположение металла в электрохимическом ряду напряжений металлов 3
Оценка восстановительной активности металла и окислительно-восстановительной способности его соединений 3
Поведение металла в компактном состоянии в различных средах 3
а)В атмосфере сухого воздуха 3
б) В воде 4
в)Взаимодействие с неокислительными кислотами 4
г)Взаимодействие с окислительными кислотами 5
д)Взаимодействие с растворами и расплавами щелочей 6
Возможные процессы электрохимической коррозии 7
е)Выявить анодный и катодный участники 7
ж)написать уравнения частных анодных и катодных реакций 7
з)ЭДС коррозии 7
и)Итоговый процесс 7
Положение металла в периодической системе Д.И.Менделеева
Никель — элемент десятой группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 28.
Проявляемые металлом степени окисления в его соединениях
Никель образует соединения со степенью окисления +1, +2, +3 и +4. При этом соединения никеля со степенью окисления +4 редкие и неустойчивые
Местоположение металла в электрохимическом ряду напряжений металлов
Электрохимический ряд активности металлов характеризует сравнительную активность металлов в окислительно-восстановительных реакциях в водных растворах.ni располжен слева водорода что означает что он имеет высокую восстановительную способность
Оценка восстановительной активности металла и окислительно-восстановительной способности его соединений
Высокими восстановительными способностями
Поведение металла в компактном состоянии в различных средах
-
В атмосфере сухого воздуха
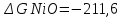
Т.к. энергия Гиббса меньше 0 реакция может протекать самопроизвольно.
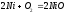
-
В воде
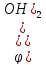
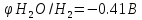
 E<0=>реакция
не протекает
E<0=>реакция
не протекает
-
Взаимодействие с неокислительными кислотами
φNi2+/Ni=-0,25B
φ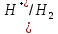 =-0.059PH=-0.059*3=-0.177B
φNi2+/Ni<φ
=-0.059PH=-0.059*3=-0.177B
φNi2+/Ni<φ Значит
реакция возможна
Значит
реакция возможна

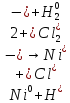
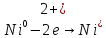
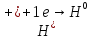
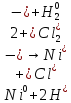
φNi2+/Ni=-0,25B
φ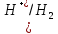 =-0.177B
φNi2+/Ni<φ
=-0.177B
φNi2+/Ni<φ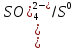 Значит реакция возможна
Значит реакция возможна

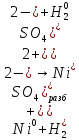



-
Взаимодействие с окислительными кислотами
φNi2+/Ni=-0,339B
φ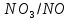 =0.96В
φNi2+/Ni<
φ
=0.96В
φNi2+/Ni<
φ =>реакция
возможна
=>реакция
возможна

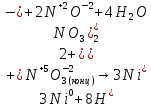
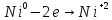
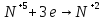


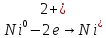
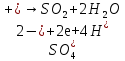
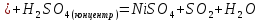
-
Взаимодействие с растворами и расплавами щелочей
В расплавах щелочей: никель устойчив к щелочам
В растворах щелочей:
Возможные процессы электрохимической коррозии
-
Выявить анодный и катодный участники
φNi2+/Ni=-0,339B=>катод φFe2+/Fe=-0,44B=>анод
-
написать уравнения частных анодных и катодных реакций


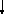



(А)
Fe│H2O,O2
│Ni
(К)
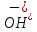
|
Анодный процесс |
Катодный процесс |
|
φFe2+/Fe=-0,44B=>анод |
φNi2+/Ni=-0,339B=>катод |
|
|
|
-
ЭДС коррозии
φk=φ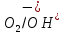 =1.23-0.059*7=0.817B
φa=
φNi2+/Ni=-0.339B
=1.23-0.059*7=0.817B
φa=
φNi2+/Ni=-0.339B
 =
φк-φа=0,817+0,339=1,156В>0=>коррозия
возможна
=
φк-φа=0,817+0,339=1,156В>0=>коррозия
возможна
-
Итоговый процесс