
- •Опыт 4. Изменение окраски крезолового красного при поглощении листом со2.
- •Опыт 5. Фотосенсибилизирующее действие хлорофилла на реакцию переноса водорода (по Гуревич)
- •Б. Изучение фотосенсибилизирующих действий хлорофилла на реакцию переноса водорода по Гуревичу.
- •Влияние света на фотосенсибилизирующее действие хлорофилла
- •Определение содержания хлорофилла на фэКе
- •Реактивы и оборудование
- •Недопустимо отмеривать хромовую смесь пипеткой!
Лабораторная работа № 8
ОБНАРУЖЕНИЕ ПРОЦЕССА ФОТОСИНТЕЗА И ОПРЕДЕЛЕНИЕ КОЛИЧЕСТВА ПИГМЕНТОВ В РАСТЕНИИ
Опыт 1. Обнаружение процесса фотосинтеза (выделение кислорода водными растениями)
Цель работы: обнаружить фотосинтез у водных растений по выделению пузырьков газа и доказать, что этот газ кислород.
Ход
работы: В
один сосуд наливают прокипяченную воду
(вода без СО2),
в другой – 0,5% раствор гидрокарбоната
натрия (вода с СО2).
Отбирают здоровые растения элодеи.
Обновляют под водой срезы. На суженные
концы воронок надевают пробирки,
заполненные тем же раствором, что и в
сосудах. Под воронки помещают растения
(см. рис. 1). Сосуды с растениями устанавливают
под яркий свет. Температура всех жидкостей
в опыте должна достигать 26ºС. В пробирки,
заполненные газом, который выделяют
растения опускают зажженную лучинку.
Горение свидетельствует о присутствии
кислорода. 

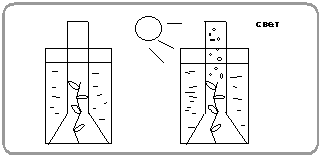
Рис. 1. Влияние углекислого газа на выделение кислорода водными растениями: 1. элодея, 2 – воронки, 3 – сосуд с раствором соды, 4 – пробирка с раствором соды, 5 – сосуд с прокипяченной водой, 6 – пробирка с прокипяченной водой.
Задание: сделать рисунки. Отметить время заполнения каждой из пробирок кислородом и сделать выводы о том, что для фотосинтеза необходим СО2.
Опыт 2. Обнаружение выделенного при фотосинтезе О2 с помощью метиленового синего
Известный краситель – метиленовый синий способен к окислительно-восстановительным превращениям, он может быть как акцептором ионов водорода, так и их донором. В основе данного опыта лежит свойство метиленового синего давать бесцветное соединение при воздействии восстановителя, и переходить снова в окрашенное соединение при воздействии окислителей Н2О2 или О2.
Цель работы: доказать, что растения на свету выедляют кислород.
Ход работы: в три пробирки наливают водопроводную воду и подкрашивают метиленовым синим до ярко-голубой окраски, а затем добавляют по каплям Na2SO3 до обесцвечивания всех трех растворов. Во вторую пробирку наливают пероксид водорода до изменения цвета снова в ярко-голубой, а в третью помещают растение. Все пробирки выставляют на свет и наблюдают за тем, как изменяется в них цвет раствора. Температура среды +26ºС.
Задание: описать опыт; зарисовать пробирки; объяснить причину изменения цвета в пробирках.
Опыт 3. Всплывание на свету инфильтрированных дисков из листьев.
У наземных растений выделяющийся при фотосинтезе кислород накапливается в межклетниках листа. Если межклетники листа заполнены газом, то плотность тканей листа мала и лист плавает на поверхности воды. Если межклетники заполнены водой, то лист оседает на дно. Кислород, выделяющийся при фотосинтезе, вытесняет из межклетников воду, лист становится легче и всплывает на поверхность.
Цель работы: определить интенсивность фотосинтеза по выделению О2 в зависимости от освещенности.
Ход работы: пробочным сверлом из листа делают высечки и инфильтруют их водой, насыщенной СО2. Инфильтрированные высечки помещают по 6 штук в стаканчики с водой, обогащенной СО2. Один из стаканчиков помещают в темноту (контроль), другие выставляют на свет на разные расстояния от его источника и засекают время. Высечки всплывают в разное время в зависимости от интенсивности света (расстояние от лампы 0, 25, 50, 100 см) в результате вытеснения воды из межклетников кислородом, образующимся при фотосинтезе. Высечки, находящиеся в темноте, не должны всплывать. Мерой интенсивности фотосинтеза служит время, прошедшее с момента установки стакана с инфильтрованными высечками на свет до всплывания 50% высечек.
Задание: определить время всплывания высечек в стаканчиках, установленных на разном расстоянии от лампы. Сделать вывод о влиянии интенсивности света на интенсивность фотосинтеза.
Опыт 4. Изменение окраски крезолового красного при поглощении листом со2.
Цель работы: доказать, что живой лист растения поглощает СО2 из воздуха при фотосинтезе. Для этого используют индикатор – крезоловый красный, который меняет свою окраску при изменении рН среды.
Ход работы: в три сосуда наливают водопроводную воду до ½ объема. В I сосуд – воду, содержащую СО2 не более 0,3% (как в воздухе), со значением рН, близким к нейтральной, во II сосуд – прокипяченную воду, остуженную при закрытой пробке (без СО2), со слабощелочной реакцией, в III сосуд – воду, обогащенную СО2 путем 10-ти минутного вдувания через трубочку вдыхаемого воздуха, со слабокислым значением рН, которое обусловлено наличием в воде СО2.
Во все три сосуда добавляют одинаковое количество крезолового красного до окрашивания растворов: в I – до темно-желтого, во II – до красного, в III – до светло-желтого. К пробке III сосуда крепят крючок, на крючок надевают лист и опускают в сосуд. Сосуды выставляют на свет. Спустя 12 часов отмечают изменения, произошедшие с растворами индикатора. В III сосуде лист поглощает НСО3- из раствора, и он изменяет желтую окраску на красную в связи с изменением значения рН до слабощелочного (таблица 1).
Таблица 1
|
Вариант опыта |
Окраска крезолового-красного |
рН среды |
Изменения окраски |
|
СО2 мало |
Темно-желтая |
Нейтральная |
|
|
СО2 отсутствует |
Красная |
Слабощелочная |
|
|
СО2 много+лист |
Светло-желтая |
Кислая |
|
Задание: данные опыта внести в таблицу, объяснить причину изменения окраски.
Опыт 5. Фотосенсибилизирующее действие хлорофилла на реакцию переноса водорода (по Гуревич)
Сущность световой фазы фотосинтеза заключается в окислении воды до молекулярного кислорода с помощью световой энергии, поглощенной хлорофиллом. Освобождающиеся при этом электроны передаются затем через цепь промежуточных переносчиков к НАДФ, который восстанавливается до НАДФ·Н2. Кроме того, при переносе электронов часть энергии расходуется на образование АТФ, т. е. фотосинтетическое фосфорилирование.
Считают, что в переносе электронов воды к НАДФ участвуют последовательно две пигментные системы, которые содержат различные формы хлорофилла а, отличающиеся максимумами поглощения в длинноволновой части спектра. В первую систему входят также каротиноиды, а во вторую- хлорофилл b и ряд других вспомогательных пигментов.
Итак, конечный результат фотоокисления воды - выделение молекулярного кислорода и образование богатых энергией и восстановительной силой соединений - АТФ и НАДФ-Н2, необходимых для последующего восстановления углекислого газа.
Упрощенную схему фотолиза воды можно представить следующим образом:
H2O + HAДФ + АДФ + Н3РО4 (свет, Хл) → НАДФ·Н2 + АТФ + 1/2О2
Как видно из уравнения, хлорофилл выполняет здесь функцию - фотосенсибилизатора, способствующего переносу электрона (водорода) к НАДФ.
Фотосенсибилизирующая роль хлорофилла может быть продемонстрирована в модельных реакциях с выделенным из растений пигментом. Для этого в качестве источника водорода берут аскорбиновую кислоту, а акцептора водорода - метиловый красный, который, присоединяя водород, восстанавливается в неокрашенное лейкосоединение. Аскорбиновая кислота окисляется в дегидроаскорбиновую кислоту по схеме:
АН2 + М + Хл → А + МН2 + Хл,
где АН2 - донор электронов (аскорбиновая кислота);
М - акцептор электронов (метиловый красный);
А - дегидроаскорбиновая кислота;
МН2 - бесцветная лейкоформа метиловый красный,
Хл - хлорофилл.
Цель исследования: установить роль хлорофилла как фотосенсибилизатора в процессах переноса электронов к НАДФ+.
Объекты исследования - спиртовая вытяжка из листьев амариллиса, плюща или других растений.
Реактивы: 85%-ый этиловый спирт, СаСО3, аскорбиновая кислота (кристаллическая), метиловый красный (насыщенный раствор в этиловом спирте), раствор хлорофилла (спиртовая вытяжка из листьев).
Оборудование - пробочные сверла 8-10 мм, ножницы, колбы на 100 мл (2 шт.), воронки (2 шт.), стеклянная палочка, бумажные фильтры, кварцевый песок или толченое стекло, вазелин, колба Бунзена, стеклянный фильтр № 2 или № 3, насос Камовского или водоструйный, градуированные пипетки на 10 мл и на 1 мл, средние пробирки, штатив, электрическая настольная лампа на 300 Вт., стеклянный сосуд с плоскопараллельными стенками.
Схема исследований:
1. Вытяжка хлорофилла + аскорбиновая кислота + метиловый красный + свет (контрольный вариант).
2. Вытяжка хлорофилла + аскорбиновая кислота + метиловый красный + темнота.
3. Вытяжка хлорофилла + метиловый красный + свет.
4. Спирт + аскорбиновая кислота + метиловый красный.
Методика исследований
А. Получение спиртового раствора (вытяжки) пигментов зеленого листа
Из листьев растений (не затрагивая крупных жилок) пробочным сверлом вырезают диски. Из них составляют навеску в 1,0-1,5 г. Для расчета поверхности листьев взятой пробы необходимо сосчитать количество дисков и измерить их диаметр.
Навеску листьев переносят в фарфоровую ступку и растирают с небольшим количеством этилового спирта, прибавив предварительно на кончике ножа СаСОз (для нейтрализации кислот клеточного сока) и чистого кварцевого песка (для лучшего растирания). Носик ступки с наружной стороны смазывают вазелином. После небольшого отстаивания зеленый раствор осторожно (чтобы не потерять ни капли раствора) по палочке сливают в воронку с пористым стеклянным фильтром. С помощью масляного или водоструйного насоса фильтруют вытяжку в колбу Бунзена. Оставшуюся в ступке густую массу снова растирают со спиртом. После отстаивания жидкость переносят на фильтр.
Эту операцию повторяют несколько раз, пока раствор, стекающий из воронки, не будет бесцветен. Переносят спиртовую вытяжку из колбы Бунзена в мерную колбу на 25-50 мл, спиртом доливают до метки и перемешивают. Полученный зеленый раствор содержит следующие пигменты.
1. Зеленые:
хлорофилл «a» C32H30ON4Mg (COOCH3) (СООС20Н39);
хлорофилл «б» C32H28O2N4Mg (СООСНз) (СООС2оН39).
2. Желтые:
каротин С4оН5б; ксантофилл С4оН5бО2.
С полученной вытяжкой производят ряд исследований и определяют количество хлорофилла в ней.
