
Техническая термодинамика
.pdf
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО
ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
БАШКИРСКИЙ ГОСУДАРСТВЕННЫЙ АГРАРНЫЙ УНИВЕРСИТЕТ
Кафедра теплотехники и
энергообеспечения предприятий
Б3.Б.10 ТЕПЛОТЕХНИКА
МЕТОДИЧЕСКИЕ УКАЗАНИЯ к практическим занятиям по разделу «Техническая термодинамика»
Направление подготовки
260800 Технология продукции и организация общественного питания
Профиль подготовки
Технология организации ресторанного дела
Квалификация (степень) выпускника
Бакалавр
Уфа 2012
Методическое указание разработано к.т.н., доцентом Гайсиным Э.М. и ассистентом Шарафеевым А.А.
Методическое указание одобрено и рекомендовано к печати кафедрой теплотехники и энергообеспечения предприятий (протокол №__ от «__» ______
201__г.) и методической комиссией энергетического факультета (протокол №__
от «__»_______ 201__ г.).
Рецензент: д.т.н. Галиуллин Р.Р.
Ответственный за выпуск: зав. кафедрой, к.т.н., доцент Инсафуддинов С.З.
2
|
ОГЛАВЛЕНИЕ |
|
ВВЕДЕНИЕ |
4 |
|
1 |
ОСНОВЫ ТЕХНИЧЕСКОЙ ТЕРМОДИНАМИКИ |
5 |
2 |
СМЕСИ ИДЕАЛЬНЫХ ГАЗОВ |
9 |
|
2.1 Массовый состав смеси |
6 |
|
2.2 Объемный состав смеси |
10 |
3 |
ТЕПЛОЕМКОСТЬ ГАЗОВ |
12 |
4 |
ТЕРМОДИНАМИЧЕСКИЕ ПРОЦЕССЫ ГАЗОВ |
16 |
5 |
ВОДЯНОЙ ПАР. ДИАГРАММА hS ВОДЯНОГО ПАРА. |
|
ИССЛЕДОВАНИЕ ПАРОВЫХ ПРОЦЕССОВ ПО ДИАГРАММЕ hS |
|
|
|
|
20 |
БИБЛИОГРАФИЧЕСКИЙ СПИСОК |
28 |
|
3
ВВЕДЕНИЕ
Настоящее методическое указание предназначено для проведения практических занятий по дисциплине «Теплотехника» со студентами факультета пищевых технологий очного и заочного обучения.
В методические указания включены разделы и задачи, связанные с процессами, протекающими в машинах и аппаратах. Часть задач носит как общетехнический характер, так и теоретический курс.
Все разделы методических указаний начинаются с краткого изложения основных сведений из теории, даны необходимые расчетные уравнения. В каждом разделе приведены решения нескольких характерных и наиболее сложных задач.
4
1 ОСНОВЫ ТЕХНИЧЕСКОЙ ТЕРМОДИНАМИКИ
Параметры состояния термодинамической системы. Уравнение состояния рабочего тела.
В качестве рабочего тела в тепловых машинах используют газы и пары, обладающие способностью легко и быстро расширяться или сжиматься. Физическое состояние рабочего тела определяется время основными параметрами состояния: температурой, давлением и удельным объемом.
Температура характеризует степень нагретости тела и измеряется в градусах. В настоящее время используются три температурные шкалы: абсолютная или термодинамическая шкала – Т, К, практическая международная шкала – t, °С, шкала Фаренгейта – t, °F.
Термодинамическая шкала установлена по температуре абсолютного нуля и тройной точки воды, равной 273,15 К, при которой могут существовать одновременно лед, вода и пар. Эту шкалу называют еще и абсолютной, так как температура измерения по ней не зависит от свойства теплоносителя. Цена деления шкалы в градусах Цельсия совпадает с ценой деления шкалы Кельвина (1
К = 1 °С).
Численные значения температуры, определяемые по этим шкалам связаны соотношением:
Т, К = t°С + 273,15. |
(1.1) |
||||
По шкале Фаренгейта, применяемой в Англии и США, температура плав- |
|||||
ления льда 32 °F и температура кипения воды при нормальных физических ус- |
|||||
ловиях (р 0 =101325 Па, Т0=273,15 К) равна 2120 F следовательно |
|
||||
t°C = |
5 |
∙(t°F-32) , |
(1.2) |
||
|
|||||
9 |
|
|
|
|
|
Давление – это сила, действующая по нормам на единицу поверхности |
|||||
p = |
F |
, |
(1.3) |
||
|
|||||
|
|
|
A |
|
|
где F – сила (в Н), нормальная к поверхности и равномерно распределенная по поверхности площадью А.
Единицей давления в системе СИ является Паскаль (1 Па=1Н/м2). Очень часто в технике для практических измерений используют высоту
столба жидкости. В основном применяется в качестве жидкости вода, спирт или ртуть. Полезно вспомнить, что при 0°C или 273,16 К.
1 мм вод. ст.= 9,81 Па 1 мм рт. ст.= 133,3 Па За параметр состояния в термодинамике принимают абсолютное давле-
ние. Абсолютное давление обычно, подчитывается по показаниям двух приборов. Если давление больше атмосферного, то оно измеряется манометром и абсолютное давление равно
pа=pб+pм, |
(1.4) |
где pб – атмосферное давление, измеренное барометром;
pм – показание манометра, измеряющего избыточное давление, Если pб<pа , то
5
pа=pб-pв, |
(1.5) |
|||
где pв – показание вакуумметра, измеряющего разряжение. |
|
|||
Удельный объем тела |
|
|
||
v |
V |
, |
(1.6) |
|
m |
||||
|
|
|
||
где v- удельный объем, м3/кг; |
|
|
||
V - полный объем, м3; |
|
|
||
m - масса тела, кг.
Величина, обратная удельному объему называется плотностью вещества
|
m |
, |
(1.7) |
|
V |
||||
|
|
|
где - масса единицы, кг/м3.
Уравнение состояние тела устанавливают зависимость между параметрами состояния. Для идеального газа уравнение состояния выражается законом
Клапейрона: |
|
|
Для 1 кг газа |
р v R0∙T, |
(1.8) |
Для m кг газа |
р V т ∙R0∙T. |
(1.9) |
Для моля идеального газа уравнение предложено Менделеевым и имеет |
||
вид |
|
|
|
р V =М∙R0∙Т=R∙T, |
(1.10) |
где Vμ – объем моля газа, м3/кмоль;
R0 – газовая постоянная, Дж/(кгК); М – молекулярная масса, кг/кмоль;
R – универсальная газовая постоянная; её значение для всех газов
8314,3Дж/(кмоль∙К).
При нормальных физических условиях любой килограмм-моль газа занимает объем V=22,4 м3/кмоль. Поэтому для вычисления их удельного объема в м3/кг при этих условиях можно использовать зависимость
v0 |
22,4 |
, |
(1.11) |
|
M |
||||
|
|
|
Газовая постоянная отдельного газа определяется по выражению
R0 |
|
8314, 3 |
, |
(1.12) |
|
M |
|||||
|
|
|
|
Объем газа V, находящегося при произвольных физических условиях (ρ и Т) может быть приведен к нормальным физическим условиям (Ро и То) по формуле
V |
p V T0 |
. |
(1.13) |
|
|||
0 |
P0 T |
|
|
|
|
||
Значения удельной газовой постоянной, молекулярной массы и плотности при нормальных условиях для наиболее распространенных газов приведены в таблице 1.1
Задачи Задача 1.1. Определить абсолютное давление в ресивере компрессорной
установки, если присоединенный к нему манометр показывает 0,3 МПа. Баро-
6
метрическое давление по ртутному барометру составляет 240 мм рт.ст. при температуре ртути 200С.
Решение: Для решения задачи необходимо перевести давление, измеренное по ртутному барометру в давление, выраженное в паскалях, и учесть температурную поправку.
Приведем показания барометра к 00С по следующему соотношению р0=р∙(1-0,000172t),
где р0 - барометрическое давление, приведенное к 00С; р - действительное давление при температуре воздуха 200;
0,000172 – коэффициент объемного расширения ртути.
р0 = 740(1-172·10-6·20)=737,45 мм. рт. ст.=98,3 кПа Тогда абсолютное давление воздуха в ресивере
Ра= р0+ри=98,3+300=398,3 кПа.
Таблица 1.1 Значение М, R0 и ро при нормальных условиях некоторых газов
|
|
Молекулярная |
Удельная газо- |
Плотность |
|
Наименование |
Химическое |
при нормаль- |
|||
газа |
обозначение |
масса |
М, |
вая постоянная |
ных1 |
|
|
кг/кмоль |
|
R0, Дж/(кг∙К) |
3 |
|
|
|
|
|
ф. у. ρ0, кг,м |
Воздух |
- |
28,96 |
|
287,0 |
1,293 |
Кислород |
О2 |
32,00 |
|
259,68 |
1,429 |
Азот2 |
N2 |
28,03 |
|
269,8 |
1,251 |
Аммиак |
NH3 |
17,03 |
|
488,3 |
0,771 |
Аргон |
Az |
39,99 |
|
208,2 |
1,783 |
Атмосферный |
- |
28,16 |
|
(295,3) |
(1,257) |
воздух |
|
||||
|
|
|
|
|
|
Водород |
Н2 |
2,02 |
|
4124,0 |
0,090 |
Водяной пар |
Н 2О |
18,02 |
|
(461,0) |
(0,804) |
Гелий |
На |
4,00 |
|
2078 |
0,179 |
Окись углеро- |
СО |
28,01 |
|
296,8 |
1,260 |
да |
|
|
|
|
|
Двуокись уг- |
СО2 |
44,01 |
|
188,9 |
1,907 |
лерода |
|
|
|
|
|
Сернистый газ |
SО2 |
64,06 |
|
129,0 |
2,926 |
Метан |
СН4 |
16,03 |
|
518,8 |
0,51 |
Этилен |
С 2Н4 |
28,05 |
|
296,6 |
1,251 |
Коксиный газ |
- |
11,50 |
|
721,0 |
0,515 |
Примечание:
1.Приведение водяного пара к нормальному состоянию является условным.
2.Атмосферный азот – углекислый газ, состоящий из азота воздуха вместе с двуокисью углерода и редкими газами, содержащимися в воздухе.
Задача 1.2. Для производства газосварочных работ привезли баллон с кислородом емкостью 40 л. Определить время расхода и массу израсходованного кислорода, если производительность горелки 1280 л/ч при абсолютном давле-
7
нии 100 кПа и температуре 200С, а избыточное давление в баллоне снизилось с
15 до 0,4 МПа.
Решение: Определяем абсолютное давление кислорода в баллоне до и после сварочных работ по формуле Ра =Рб+Ри, так как параметром является только абсолютное давление.
Количество израсходованного кислорода определяется как разность кислорода, которая содержалась в баллоне до начала сварочных работ и после работ
m=m -m = |
p1 V |
|
p2V |
|
V |
|
P p |
|
|
0.04 |
|
15 106 0.4 106 7,67кг. |
||
|
|
|
|
2 |
|
|
||||||||
1 |
2 |
RO |
T |
|
RO Т |
|
RO |
T |
1 |
|
259,8 293 |
|
||
|
|
|
|
|
|
|
|
|||||||
|
|
2 |
|
2 |
|
2 |
|
|
|
|
|
|
||
За 1 час израсходовано
mt= РбVt 100 103 1,28 =1,68 кг/ч RO2 T 259,8 293
Время расхода кислорода
t = m 7,67 =4,5 ч mt 1,68
Задача 1.3. Определить абсолютное давление в молокопроводе доильной установки, если вакуумметр, присоединенный к молокопроводу показывает разряжение 48 кПа, а барометрическое давление атмосферного воздуха 785 мм.рт.ст. при температуре 250С.
Задача 1.4. Для предупреждения испарения ртути из трубки из ртутного манометра над уровнем ртути наливают слой воды. Определить абсолютное давление в сосуде, если высота столба ртути в манометре составляет 560 мм, а высота столба воды над ртутью равна 160 мм. Барометрическое давление равно 750 мм рт.ст.
Задача 1.6. Разряжение на выходе дымохода парового котла измеряется тягомером с углом наклона трубки К горизонту 300. Длина столба воды, отчитанная по шкале тягомера, равно 140 мм. Определить абсолютное давление газа в Мга, если показание барометра равно 750 мм рт.ст.
Задача 1.6. В тормозном ресивере трактора Т-150К находится воздух массой 50 кг, плотностью 15 кг/м3. Определить емкость ресивера и удельный объем воздуха
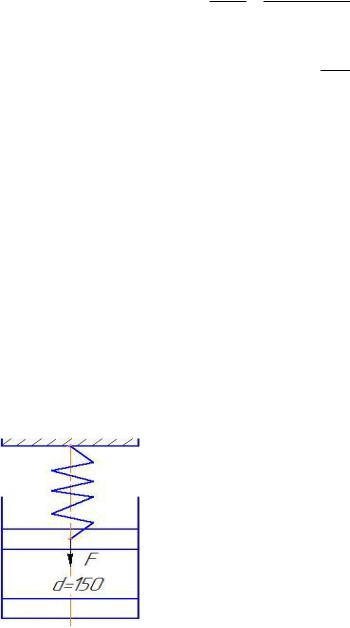
Рисунок 1.1 Рисунок к задаче 1.7
Задача 1.7. Цилиндр, диаметром d=150 мм плотно закрыт подвешенном на пружине поршнем, условно невесомым и скользящим без трения. В цилиндре образован вакуум, составляющий 90% от барометрического давления  б=0,1 МПа. Определить силу натяжения пру-
б=0,1 МПа. Определить силу натяжения пру-
жины, если поршень неподвижен.
Задача 1.8. Определить расход метана в газопроводе диаметром d=600 мм, если скорость истечения газа u=15 м/с при абсолютном давлении 1,6 МПа и температуре 200С.
Задача 1.9. Определить объемную подачу ком-
8
прессора при температуре 250С и барометрическом давлении 750 мм рт.ст., если при нормальных физических условиях она равна 3 м3/мин.
Задача 1.10. Определить площадь поперечного сечения воздуха вода дутьевого вентилятора, если каждую секунду в топку котла требуется подводить 10 кг воздуха плотностью 1,2 кг/м3. Скорость перемещения воздуха по воздуховоду принять равной 8 м/с.
Задача 1.11. В свинарнике площадью 662 м2 и высотой 3,2 м, воздух находится при температуре 200С при барометрическом давлении 98,5 кПа.Какое количество воздуха проникает в помещение при увеличении барометрического давления до 101,3 кПа и понижении температуры до 100С?
Задача 1.12. Определить давление на нижнее днище контейнера ракеты, установленной на подводной лодке, если указанное днище находиться на глубине 15,5 м , а давление атмосферы, измеренное ртутным барометром при тем- пературе-20° C, составляет 755 мм рт.ст.
2 СМЕСИ ИДЕАЛЬНЫХ ГАЗОВ
В практике очень часто приходится встречаться с газовыми смесями. Например, рабочее тело тепловых двигателей, компрессоров, других теплотехнических устройств, дымовые газы представляют собой смесь газов.
При рассмотрении газовых смесей исходят из того, что смесь состоит из идеальных химически не взаимодействующих между собой газов. При этом каждый газ, входящий в состав смеси, ведет себя так, как будто бы он один при данной температуре занимает весь объем смеси и оказывает на стенки сосуда свое давление, называется парциальным.
По закону Дальтона давление смеси рсм равно сумме парциальных давлений газов, входящих в состав смеси
n
Рсм= Р1+Р2+…+Рп= Pi , (2.1)
i 1
где Pi– парциальное давление компонента, входящего в смесь. Состав смеси может, задан одним из следующих способов.
2.1Массовый состав смеси
Вабсолютных единицах массы
n
mсм=m1+ m2+…+ mn= mi , (2.2)
i 1
где m1, m2, mn –массы отдельных компонентов смеси в относительных массовых долях
m1 |
|
m2 |
... |
mn |
=q1+ q2 +…+ qn=1; |
(2.3) |
|
m |
m |
m |
|||||
|
|
|
|
||||
см |
|
см |
|
см |
|
|
|
|
|
|
|
n |
|
|
|
|
|
|
qi 1, |
(2.4) |
|||
i `1
где qi=mi/mсм – массовая доля отдельного компонента смеси.
9
2.2 Объемный состав смеси
Объемный состав смеси можно определить по формуле
n
Vсм=V1+ V2+…+ Vn= Vi , (2.5)
i 1
где V1, V2 и т.д. – приведенные объемы отдельных компонентов смеси, м3; в относительных объемных долях
V1 |
|
V2 |
... |
Vn |
r |
r |
... r |
1 ; |
(2.6) |
|
|
|
|||||||
Vсм |
Vсм |
Vсм |
1 |
2 |
n |
|
|
||
|
|
|
|
|
|||||
|
|
|
n |
|
|
|
|
|
|
|
|
|
ri 1, |
|
|
|
(2.7) |
||
|
|
|
i 1 |
|
|
|
|
|
|
где ri - объемная доля отдельного компонента.
Задание состава смеси числом молей соответствует заданию состава смеси по объему, так как мольная доля компонента равна его объемной доле.
Между массовыми и объемными долями смеси существует следующая зависимость
q j |
|
mi |
|
|
Vi i |
|
|
ri i |
, |
|
|
|
|
|
|
|
|
|
|
(2.8) |
||
mсм |
|
|
см |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
Vсм см |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Следовательно |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ri=qiρсм/ρr |
|
|
|
|
|
|
|
|
|
|
|
(2.9) |
||||||||
На основании следствия закона Авогадро |
|
M СМ |
|
M i |
и |
СМ |
|
M см |
. |
|||||||||||||
|
|
|
||||||||||||||||||||
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
СМ |
|
P |
|
i |
M |
i |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
i |
|
|
|||||||
Соответственно |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
r |
q j M см |
, |
|
|
|
|
|
|
|
|
|
|
|
|
(2.10) |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
i |
|
|
М i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Кажущая молекулярная масса газовой смеси |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
n |
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
см ri i |
|
|
|
|
, |
|
|
|
|
|
|
|
(2.11) |
||||||||
|
n |
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
i 1 |
|
|
qi |
/ М i |
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
i 1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Газовая постоянная смеси может быть определена по составу смеси и газовым постоянным отдельных компонентов
Rсм= |
1 |
|
, |
(2.12) |
|
|
|||
n |
|
|||
|
ri / Ri |
|
|
|
|
i 1 |
|
|
|
n
Rсм= qi Ri , (2.13)
i 1
Или же по кажущейся молекулярной массе и универсальной газовой постоянной
Rсм= |
8314,3 |
, |
(2.14) |
|
|||
|
M см |
|
|
Теплоемкость смеси газов определяется по её составу. Массовая теплоемкость смеси газов
n
ссм=q1с1+ q2с2+∙∙∙∙+qnсn= qiCi , (2.15)
i 1
где С1, С2∙∙∙∙Сn – массовые теплоемкости отдельных компонентов q1, q2∙∙∙∙qn – массовые доли отдельных компонентов.
10
