
- •04205 Задания и методические указания к выполнению контрольной работы по дисциплине
- •Введение
- •Теоретическая часть
- •1.Классификация и правила маркировки железо-углеродистых сплавов Основные определения и понятия
- •1.1.Классификация сталей
- •1.2. Маркировка сталей
- •1.3. Классификация и правила маркировки чугунов
- •А - Работа разрушения
- •4.2. Анализ процессов охлаждения железо углеродистых
- •5. Элементы теории и технологии термической обработки металлов и сплавов
- •5.1. Структурные превращения в сталях
- •5.2. Виды термической обработки
- •5.3. Основы химико-термической обработки
- •6. Современные металлические материалы
- •7. Основы рационального выбора материалов
- •Общая схема выполнения контрольных работ
- •Задания к контрольной работе
- •Приложение 1 Пример анализа кристаллизации сплава
- •«Материаловедение»
А - Работа разрушения
σВ
Временное
сопротивление (предел прочности) –
напряжение, соответствующее наибольшей
нагрузке, предшествующей разрыву
образца.
σТ
Предел
текучести (физический) –
наименьшее напряжение, при котором
начинает развиваться пластическая
деформация и образец деформируется
без заметного увеличения растягивающей
нагрузки.
S,
А tgα=E
tgα=E
Модуль
упругости материала







σуп
Предел
упругости (σуп
= σ0,05)
– напряжение, при котором остаточная
деформация достигает 0,05 % (или меньше)
от первоначальной длины образца.
Sк
Истинное
сопротивление разрыву –
напряжение. Соответствующее наибольшей
нагрузке, предшествующее разрыву
образца.
σ0,2
Предел
текучести (условный) –
напряжение, при котором остаточная
деформация образца составляет 0,2%
σпц
Предел
пропорциональности (условный) –
величина напряжения, при котором
отступление от линейной зависимости
на диаграмме деформации достигает
такой величины, что тангенс угла наклона,
образованного касательной в этой точке
к кривой деформации, увеличивается на
50% своего значения на линейном участке
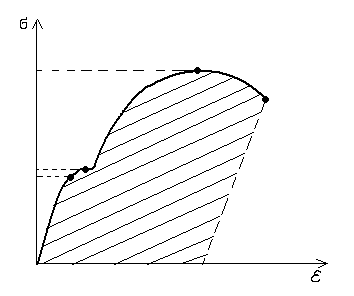
Рис.2. Диаграммы
деформации и характеристики механических
свойств, определяемые по ним
4.ДИАГРАММА СОСТОЯНИЯ ЖЕЛЕЗО-УГЛЕРОД
На диаграмме состояния железо – углерод представлены фазовый состав и структура сплавов с концентрацией по углероду от чистого железа до цементита – химического соединения железа с углеродом при концентрации последнего 6,67 % (вертикальная линия на диаграмме).
Система Fe-Fe3C метастабильна и при определенных условиях цементит может распадаться с образованием железа и чистого углерода в виде графита.
4.1. Компоненты и фазы в железоуглеродистых сплавах
Железо — металл сероватого цвета. Атомный номер 26, атомная масса 55,85, атомный радиус 0,127 нм. Чистое железо, которое может быть получено в настоящее время, содержит 99,999 % Fe, технические сорта 99,8—99,9 % Fe. Температура плавления железа 1539 °С. Железо имеет две полиморфные модификации α и γ. Модификация α - железа существует при температурах ниже 910 °С и выше 1392 °С (рис.1).

Рис.3. Кривая охлаждения чистого железа
В интервале температур 1392 - 1539 °С α - железо нередко обозначают как δ - железо. Кристаллическая решетка α - железа - объемно центрированный куб с периодом решетки 0,28606 нм. До температуры 768 °С α - железо магнитно, (ферромагнитно).
Температуру 768 °С, соответствующую магнитному превращению, т. е. переходу из ферромагнитного состояния в парамагнитное, называют точкой Кюри. Плотность α - железа 7,68 г/см8.
γ - железо существует при температуре 910 - 1392 °С; оно парамагнитно. Кристаллическая решетка -железа гранецентрированная кубическая (а = 0,3645 нм при 910 °С).
Критическую точку превращения α ↔ γ при 910 °С обозначают со ответственно Аc3 (при нагреве) и Аr3 (при охлаждении). Критическую точку перехода γ ↔ α при 1392 °С обозначают Aс4 (при нагреве) и Ar4 (при охлаждении).
Углерод является неметаллическим элементом II периода IV группы периодической системы, атомный номер 6, плотность 2,5 г/см3, температура плавления 3500 °С, атомный радиус 0,077 нм. Углерод полиморфен. В обычных условиях он находится в виде модификации графита, но может существовать и в виде метастабильной модификации алмаза.
Углерод растворим в железе в жидком и твердом состояниях, а также может быть в виде химического соединения - цементита, а в высокоуглеродистых сплавах и в виде графита.
Так как железо, имеет два полиморфных превращения (при температурах 911 и 1392 °С соответственно, а также образует с углеродом химическое соединение Fe3C, то в системе существуют следующие фазы (рис.2):
жидкость – жидкий раствор углерода в железе, существует выше линии ликвидус ABCD и обозначается буквой L;
цементит – химическое соединение Fe3C (карбид железа). В цементите содержится 6,67% углерода. Однофазная область существования цементита представляет собой вертикальную линию DFKL и обозначается в дальнейшем химической формулой или буквой Ц. цементит очень твердая, хрупкая фаза со сплошной ромбической решеткой и твердостью НВ 800 кг/мм2.
феррит – твердый раствор углерода в α- или в -железе с решеткой ОЦК. Соответственно различают низкотемпературный α-феррит с максимальной растворимостью углерода до 0,02% и высокотемпературный δ-феррит с максимальной растворимостью углерода 0,1% при Т = 1499 °С. Область α-феррита в системе железо-углерод расположена левее линии GPQ , а -феррита – левее линии AHN; феррит обозначается буквой Ф, или в виде фаз α, δ. Феррит мягкая эластичная фаза с твердостью НВ 80 кг/мм2.
аустенит – твердый раствор углерода в γ-железе с решеткой ГЦК. Максимальная растворимость углерода в γ-железе 2,14% при Т = 1147 °С.
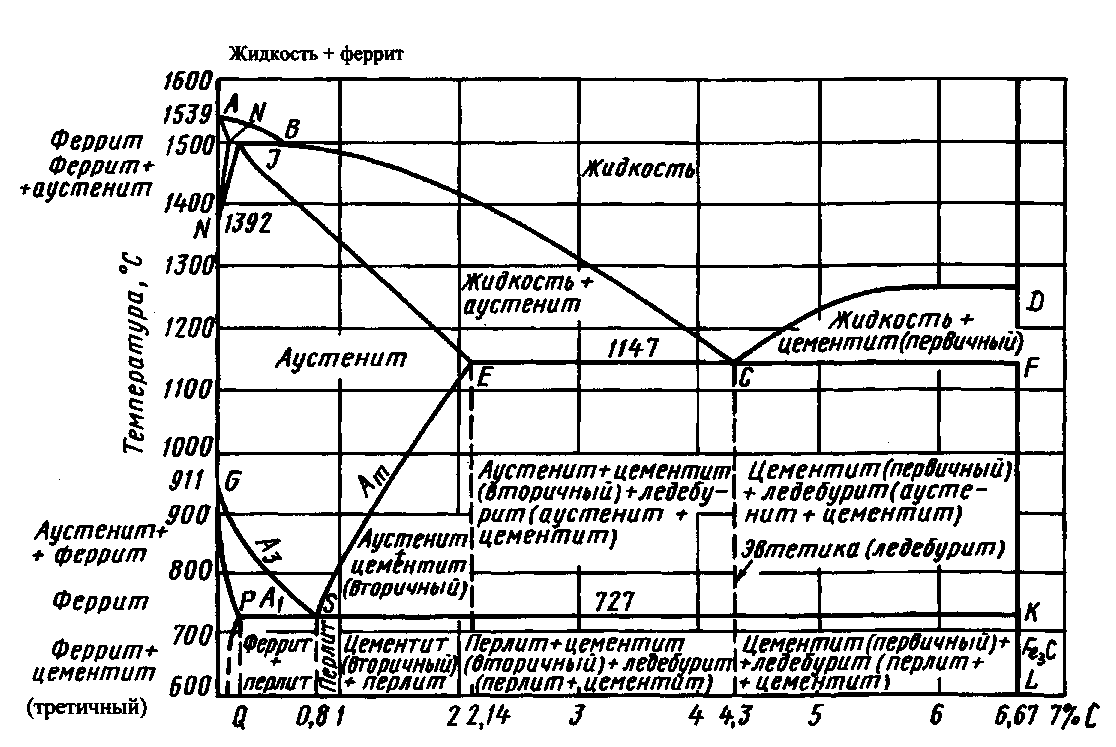

Рис. 4. Диаграмма железо – углерод
