
- •Змістовний модуль 1. Хімія біогенних елементів. Комплексоутворення в біологічних рідинах.
- •Інструкція з техніки безпеки при виконанні лабораторних робіт у хімічній лабораторії
- •1. Загальні положення
- •2. Вимоги безпеки перед початком роботи
- •3. Вимоги безпеки під час роботи
- •4. Вимоги безпеки по закінченню роботи
- •5. Вимоги безпеки в аварійних випадках
- •Теоретичний матеріал. Лабораторне обладнання і його використання
- •Методика проведення експерименту
- •Запис даних досліду
- •Технологічна карта практичного заняття
- •Технологічна карта проведення практичного заняття
- •Виконайте завдання та перевірте вірність їх розв’язання з еталоном відповіді.
- •Технологічна карта проведення практичного заняття
- •Виконайте завдання та перевірте правильність їх розв’язання з еталоном відповіді
- •Технологічна карта проведення практичного заняття
- •Зразки завдань для контролю до першого змістовного модуля
- •Змістовний модуль 2 Кислотно-основні рівноваги в біологічних розчинах
- •Технологічна карта проведення практичного заняття
- •Запис даних досліду
- •Технологічна карта проведення практичного заняття
- •Зразок контрольної роботи до 5-6 заняття.
- •Виконайте завдання та перевірте правильність їх розв’язання з еталоном відповіді
- •Технологічна карта проведення практичного заняття
- •Запис даних досліду
- •Технологічна карта проведення практичного заняття
- •Технологічна карта проведення практичного заняття
- •Зразок контрольної роботи до 9 – 10 заняття.
- •Технологічна карта проведення практичного заняття
- •Виконання досліду
- •Технологічна карта проведення практичного заняття
- •Зразки завдань для контролю до другого змістовного модуля
Виконайте завдання та перевірте правильність їх розв’язання з еталоном відповіді
|
1. Яка комплексна сполука містить йон [BeF4]2-? |
а) [BeF4]F2; б) [BeF4]SO4; в) Cs2[BeF4]; г) інша відповідь |
|
2. Заряд комплексного йона у сполуці Fe3[Fe(CN6)]2 дорівнює: |
а) – 3; б) + 6; в) + 3; г) інша відповідь |
|
3. Ступінь окиснення комплексоутворювача в сполуці Na3[Cr(OH)6] дорівнює: |
а) + 3; б) + 6 ; в) – 6 ; г) інша відповідь. |
|
4. Координаційне число комплексоутворювача в сполуці [Pt(NH3)4ClNO3]Cl дорівнює: |
а) 4; б) 2; в) 6; г) інша відповідь |
|
5. Вкажіть схему вторинної дисоціації комплексної сполуки [Co(NH3)5SO4](OH)
|
а) [Co(NH3)5SO4](OH) → Co3+ + 5NH3 + SO42- + OH-; б) [Co(NH3)5SO4]+ = Co3+ + 5NH3 + SO42-; в[Co(NH3)5SO4]+ = Co3+ + NH3 + SO42-; г) інша відповідь |
|
6. Вкажіть вираз константи нестійкості для K2[Ni(H2O)2(CNS)4]: |
а)
б)
в)
г) інша відповідь |
|
7. Виберіть вірну назву комплексної сполуки [Pt(NH3)4ClNO3]Cl2:
|
а) хлорид нітрохлорогексаамінплатини (ІІ); б) хлорид нітрохлоротетраaмінплатини (ІІ); в) хлорид нітрохлоротетраaмінплатини (ІV); г) інша відповідь |
|
8. Яка формула відображає склад йодида гексааквахрома (ІІІ)?
|
а) Cr[(OH)6]I3; б) [Cr(H2O)6]I3; в) [Cr[(H2O)5I]I2]; г) інша відповідь |
Еталони відповідей: 1в, 2а, 3а, 4в, 5б, 6б, 7в, 8б.
Технологічна карта проведення практичного заняття
|
№ пор. |
Етапи |
Час, хв |
Забезпечення дисципліни |
Місце проведе-ння |
|
1 |
Корекція знань та вмінь студентів шляхом рішення навчальних задач |
40 |
Графологічної структури, набір задач |
Навчальна лабораторія |
|
2 |
Виконання лабораторної роботи і оформлення протоколу |
20 |
Лабораторний посуд, реактиви | |
|
3 |
Тестовий контроль |
15 |
Тести | |
|
4 |
Аналіз і підведення підсумків заняття |
5 |
|
Зразки завдань для контролю до першого змістовного модуля
До якого захворювання призводять забруднення повітря викидами хімічної, металургійної промисловості, виробництво електроенергії?
До якого захворювання може призвести отруєння CO2(концентрація CO2 більш 10%)?
Поясніть токсичну дію CO.
Які біомолекули організму містять фосфор?
Напишіть формулу усіх оксидів азоту. Які оксиди азоту є кислотоутворюючими? Який із оксидів використовується для наркозу?
Яка дія нітратів та нітросполук на організм людини?
Яку властивість озону використовують для стерилізації питної води, води плавальних басейнів?
У чому небезпека хлорування питної води? До утворення яких токсичних речовин може призвести хлорування питної води?
У вигляді яких йонів галогени присутні в організмі?
Яка біологічна роль F,Cl,Br,Iв організмі?
Які неорганічні сполуки F, Cl, Br, I застосовують у медицині?
Який механізм токсичної дії надлишку фторид-іонів на організм?
Чому у медичній практиці використовують розчин йоду з йодидом калію?
Де у живому організмі накопичується F,Br,I?
Чому при отруєнні бромом хворому вводять велику кількість NaCl?
Якими галогенами можна витіснити бром із розчину KBr? Напишіть відповідні рівняння реакцій?
Які солі сульфатної кислоти застосовують у медичній практиці?
Чому сульфурвмісні амінокислоти застосовують для захисту організму під час радіаційних уражень?
Що таке металолігандний ферум гомеостаз? Які чинники зумовлюють порушення металолігандного гомеостазу?
Що таке натрій-калієвий насос? Його дія.
До яких захворювань може призвести надлишок кальцію?
Яка роль Mgу організмі?
Де у організмі концентрується Cu, Zn, Al, As, V, Cd, Hg, Mn, Ba?
Яка хімічна реакція лежить в основі токсичної дії йона Pb2+?
Яке забарвлення мають розчини сполук Mn+4,Mn+6,Mn+7?
У яких ступенях окислення сполуки феруму, кобальту та нікелю найбільш стійкі?
Які особливості електронних структур визначають високі комплексоутворюючі властивості феруму, кобальту та нікелю?
За допомогою яких реакцій можна отримати розчин хлориду заліза (ІІ)? Що відбувається з розчином цієї солі при зберіганні її на повітрі? Напишіть реакції. Чи можна розчин FeCl2 , що довго зберігався, використовувати для отримання лікувальних препаратів двовалентного феруму?
Які функції виконують комплекси заліза в організмі?
Молярна маса гемоглобіну людини дорівнює 4500г/моль. Розрахуйте масову частку феруму в гемоглобіні, якщо в одній молекулі гемоглобіну міститься 4 атоми феруму.
У чому полягає фізіологічна функція гемоглобіну? Який механізм «роботи» гемоглобіну?
Чи змінює ступінь окислення феруму в молекулі гемоглобіну в процесі приєднання і віддачі кисню?
Розрахуйте молярну масу гемоглобіну, якщо в одній молекулі гемоглобіну міститься 4 атоми заліза і масова частка його становить 0,335%.
Які функції в організмі виконує вітамін В12. Назвіть комплексоутворювач В12. Що загального в структурах молекул гемоглобіну і вітаміну В12?
S-елементи групи IA і d-елементи групи 1Б мають на зовнішньому електронному шарі по одному s-електрону. У чому полягає причина того, що елементи цих груп значно відрізняються за хімічними властивостями?
Яку роль виконує Cuу купрумвмісних білках і ферментах?
Які з'єднання срібла застосовують у лікувальних цілях? Який механізм їх дії?
Який механізм токсичної дії розчинних солей купруму, срібла і золота на організм?
Чому Zn, Cd і Hg не проявляють змінної валентності в своїх сполуках?
Запишіть реакції, що характеризують амфотерні властивості цинку.
Напишіть ступінчасту дисоціацію комплексу K2[HgI4]. Запишіть у загальному вигляді константу нестійкої комплексного іона.
Що обумовлює високу токсичність сполук Zn, Cg, Hg?
На чому засновано застосування сполук цинку і ртуті як препаратів зовнішньої дії? Поясніть лікувальну дію на основі хімічних властивостей цих сполук.
На чому засновано застосування комплексонів, як лікувальних препаратів при отруєнні з'єднаннями цинку, камдію і ртуті?
Чому тіолвмісні ферменти необоротно отруюються йонами Cu2+ і Ag+ ?

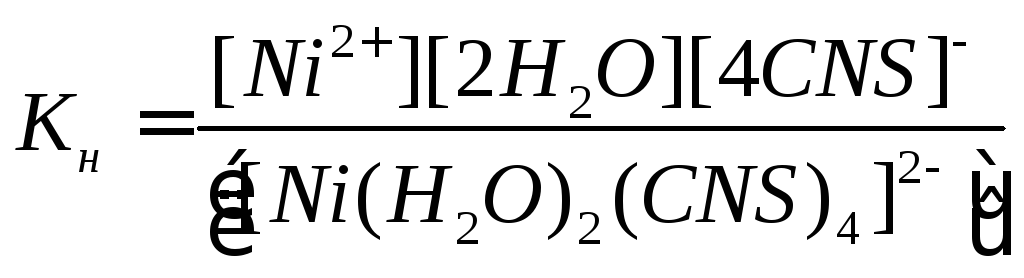 ;
; ;
;