
- •Предисловие
- •Глава 1. Аминокислоты и белки
- •1.1 Общая характеристика
- •1.2 Классификация аминокислот
- •1.3 Модификация аминокислот
- •1.4 Ионизация аминокислот
- •1.5 Пептидная связь
- •1.6 Пептиды и белки
- •1.7 Функции белков
- •1.8 Уровни структурной организации белков
- •А Первичная структура белка
- •Б Вторичная структура белка
- •В Третичная структура белка
- •Д Четвертичная структура белка
- •1.9 Глобулярные и фибриллярные белки
- •А Кератин
- •1.10 Простые и сложные белки
- •1.11 Денатурация и ренатурация белков
- •1.12 Методы работы с белками
- •А Очистка и выделение белка
- •Б Высаливание
- •В Диализ
- •Д Аналитические методы работы с белками
- •Термины
- •Вопросы к семинарскому занятию (1-я часть)
- •Вопросы к семинарскому занятию (2-я часть)
- •Дополнительные вопросы и ключевые слова
- • Аминокислоты
- •Вопросы для самопроверки
- •Глава 2. Ферменты
- •2.1 Общая характеристика
- •2.2 Номенклатура ферментов
- •2.3 Свойства ферментов
- •2.4 Строение фермента
- •2.5 Специфичность ферментов
- •А Модель «ключ-замок»
- •Б Модель индуцированного соответствия
- •2.7 Термодинамика ферментативных реакций
- •2.8 Кинетика ферментативных реакций
- •А Вывод уравнения Михаэлиса-Ментен (по Бергу)
- •В Уравнение Лайнуивера-Берка
- •2.9 Механизмы ферментативного катализа
- •2.10 Влияние факторов среды на скорость протекания ферментативной реакции
- •А Концентрация субстрата
- •2.12 Мультисубстратные реакции
- •А Последовательный механизм
- •2.13 Ингибирование ферментов
- •Б Бесконкурентные ингибиторы
- •В Неконкурентные ингибиторы
- •2.14 Кооперативные взаимодействия внутри молекул ферментов
- •А Параллельная модель
- •2.15 Аллостерическая регуляция активности ферментов
- •2.16 Регуляция активности ферментов с помощью ковалентной модификации
- •2.17 Анти-, мульти- и изоферменты
- •2.18 Ферменты в медицине
- •А Энзимодиагностика
- •Термины
- •Вопросы к занятию (1-я часть)
- •Вопросы к занятию (2-я часть)
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 3. Нуклеиновые кислоты
- •3.1 Общая характеристика
- •3.2 Строение нуклеотида
- •3.3 Первичная структура ДНК
- •3.4 Вторичная структура ДНК
- •3.5 Денатурация и ренатурация ДНК
- •3.6 Третичная структура ДНК
- •3.7 Четвертичная структура ДНК
- •3.8 Виды РНК и их функции
- •3.9 Первичная структура РНК
- •3.10 Вторичная структура РНК
- •3.11 Третичная структура РНК
- •3.12 Четвертичная структура РНК
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 4. Репликация
- •4.1 Общая характеристика
- •4.2 Инициация репликации у прокариот
- •4.3 Элонгация репликации у прокариот
- •Б Механизм ферментативной реакции
- •4.4 Терминация репликации у прокариот
- •4.5 Репликация у эукариот
- •4.6 Проблемы репликации
- •Б Проблема высокой точности процесса
- •4.7 Плазмиды
- •В Типы плазмид
- •Д Механизмы репликации кольцевых плазмид
- •4.8 Репликация вирусов
- •Б Репликация генома РНК-вирусов
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 5. Транскрипция
- •5.1 Организация генетической информации
- •5.2 Общая характеристика транскрипции
- •5.3 Гипотеза Жакоба и Моно
- •5.4 Строение РНК-полимераз
- •5.5 Инициация транскрипции у прокариот
- •5.6 Элонгация транскрипции у прокариот
- •5.7 Терминация транскрипции у прокариот
- •5.8 Инициация транскрипции у эукариот
- •5.9 Элонгация транскрипции у эукариот
- •5.10 Терминация транскрипции у эукариот
- •А Кэпирование
- •Б Полиаденилирование
- •В Сплайсинг
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 6. Трансляция
- •6.1 Общая характеристика
- •6.2 Свойства генетического кода
- •6.3 Основные этапы биосинтеза белка
- •А Этап 1. Активация аминокислот
- •Д Этап 5. Фолдинг и посттрансляционная модификация
- •6.4 Рибосомы
- •6.5 Инициация у прокариот
- •6.6 Инициация у эукариот
- •6.7 Элонгация у прокариот
- •6.8 Элонгация у эукариот
- •6.9 Терминация у прокариот
- •6.10 Терминация у эукариот
- •6.11 Гипотеза «качания»
- •6.12 Фолдинг и посттрансляционная модификация белков
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 7. Регуляция биосинтеза белка
- •7.1 Регуляция экспрессии генов у прокариот
- •В Катаболическая репрессия. Лактозный оперон
- •Д Аттенуация. Триптофановый оперон
- •Е «Сильные» и «слабые» промоторы
- •Ж σ-Субъединица РНК-полимеразы
- •7.2 Регуляция экспрессии генов у эукариот
- •Хроматин-перестраивающие комплексы
- •Архитектурные белки высокомобильной группы
- •Ковалентная модификация гистонов
- •Метилирование ДНК
- •В Регуляция с помощью факторов транскрипции
- •7.3 Регуляция на уровне трансляции у про- и эукариот
- •А Дискриминация мРНК
- •Б Трансляционная репрессия
- •7.4 Другие механизмы регуляции у эукариот
- •Б РНК-интерференция
- •Интерференция с помощью малых интерферирующих РНК
- •Интерференция с помощью микроРНК
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- • Регуляция на уровне транскрипции (прокариоты)
- •Вопросы для самопроверки
- •Глава 8. Мутации и репарация
- •8.1 Мутации
- •8.2 Классификация мутаций по вызвавшим их причинам
- •8.3 Классификация мутаций по степени изменений генома
- •8.4 Классическая классификация
- •8.5 Репарация
- •А Прямая репарация
- •8.6 Эксцизионная репарация оснований (BER)
- •8.7 Эксцизионная репарация нуклеотидов (NER)
- •8.8 Мисметч репарация
- •8.9 Репарация двунитевых разрывов
- •8.10 Негомологичное соединение цепей ДНК при двунитевых разрывах
- •8.11 SOS-репарация (SOS-ответ)
- •8.12 Рекомбинационная репарация
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 9. Иммунитет и антитела
- •9.1 Иммунитет: его виды и элементы
- •9.2 Врожденный (неспецифический) иммунитет
- •В Химические медиаторы врожденного иимунитета
- •Е Классический путь активации комплемента
- •Ж Альтернативный путь активации комплемента
- •З Активация терминальных компонентов комплемента
- •И Как фагоциты отличают чужеродные клетки от «своих»?
- •9.3 Приобретенный (специфический) иммунитет
- •А T-лимфоциты
- •В Антитела
- •Е Вторичный иммунный ответ
- •Ж Активация гуморального иммунитета
- •9.4 Группы крови
- •9.5 Трансфузионные реакции
- •9.6 Правила переливания
- •9.7 Резус-фактор (Rh)
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 10. Биологические мембраны
- •10.1 Строение биомембран
- •В Липиды биомембран
- •10.2 Функции мембран
- •10.3 Мембранный транспорт
- •10.4 Эндо- и экзоцитоз
- •10.5 Трансмембранная передача сигнала
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 11. Энергетический обмен
- •11.1 Энергия в клетке
- •11.2 Дыхательная цепь митохондрий
- •11.3 Сопряжение дыхания и окислительного фосфорилирования
- •11.4 Разобщение дыхания и окислительного фосфорилирования
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 12. Введение в метаболизм
- •12.1 Общая характеристика
- •А Метаболические пути
- •Б Метаболиты
- •В Гомеостаз
- •12.2 Функции метаболических путей
- •А Образование энергии
- •Б Катаболизм органических соединений
- •Переваривание
- •Гликолиз
- •Окисление жирных кислот
- •Катаболизм аминокислот
- •В Синтез органических соединений и предшественников макромолекул
- •Глюконеогенез: синтез глюкозы
- •Синтез жирных кислот
- •Синтез гема
- •Креатинфосфат
- •Гликоген
- •Жиры или триацилглицеролы
- •Д Выведение потенциально опасных соединений
- •Цикл мочевины
- •Синтез желчных кислот
- •Катаболизм гема
- •Е Образование регуляторных молекул
- •12.3 Ключевые положения всех метаболических путей
- •А АТФ — донор энергии для синтеза
- •В Эссенциальные органические соединения
- •Д Взаимосвязи метаболических путей
- •Е Нелинейность метаболических путей
- •Ж Локализация метаболических путей в клетке
- •З Тканеспецифичность метаболических путей
- •И Метаболизм при голодании
- •12.4 Интеграция метаболизма
- •А Основные физиологические состояния организма и роль различных органов в интеграции метаболизма
- •Состояние насыщения
- •Состояние голодания
- •Б Интеграция метаболизма в различных физиологических состояниях
- •Состояние голодания
- •Продолжительное голодание
- •Состояние насыщения
- •Физические нагрузки
- •В Регуляция метаболизма
- •Инсулин
- •Глюкагон
- •Адреналин
- •Гидрокортизон
- •Адипоцитокины
- •Рекомендуемая литература
- •Приложение 1. Аминокислоты и белки
- •Классификация аминокислот
- •Приложение 2. Ферменты
- •Строение химотрипсина
- •Приложение 3. Нуклеиновые кислоты
- •Приложение 4. Репликация
- •Приложение 5. Транскрипция
- •Приложение 6. Трансляция
- •Приложение 7. Регуляция биосинтеза белка
- •Приложение 8. Мутации и репарация
- •Приложение 9. Иммунитет и антитела
- •Приложение 10. Биологические мембраны
- •Приложение 11. Энергетический обмен
- •Оглавление

Энергия в клетке 201
Глава 11. Энергетический обмен
11.1Энергия в клетке
Впростой прокариотической клетке кишечной палочки E. coli происходит более 1000 химических реакций, которые в сумме составляют клеточный метаболизм. Это количество может показаться чересчур большим, однако при детальном рассмотрении становится ясно, что многие из них имеют общий характер или черты. Фактически, примерно 100 молекул играют ключевую роль в жизни всех клеток на нашей планете. И несмотря на то, что количество реакций просто огромно, видов реакций не так уж и много, а их механизмы часто довольно просты. «Энергетической валютой» для всех форм жизни служит аденозинтрифосфат (АТФ) — рибонуклеотид, содержащий 3 остатка фосфорной кислоты, связанных макроэргическими связями. Разрыв этих связей приводит к выделению большого количества энергии, которая используется в анаболизме, то есть АТФ выступает в роли донора энергии в клетках.
Живые организмы нуждаются в притоке свободной энергии для покрытия трёх основных задач:
1.Выполнение механической работы: сокращение мышц и движение клеток;
2.Активный транспорт ионов и молекул;
3.Синтез макромолекул и других биомолекул из простых предшественников.
Фотосинтезирующие микроорганизмы (фототрофы) используют солнечный свет в качестве источника этой энергии. Хемотрофы (например, животные) получают эту энергию, окисляя те соединения, которые синтезируются фототрофами.
Помимо АТФ в роли источников энергии в живых клетках могут выступать и другие соединения:
1.Нуклеозидтрифосфаты (ГТФ, УТФ и ЦТФ);
2.Фосфоенолпируват (участвует в субстратном фосфорилировании АДФ в АТФ);
3.Креатинфосфат (используется в мышцах для регенерации АДФ в АТФ);
4.1,3-Бисфосфоглицерат (участвует в субстратном фосфорилировании АДФ в АТФ).
202Глава 11 Энергетический обмен
11.2Дыхательная цепь митохондрий
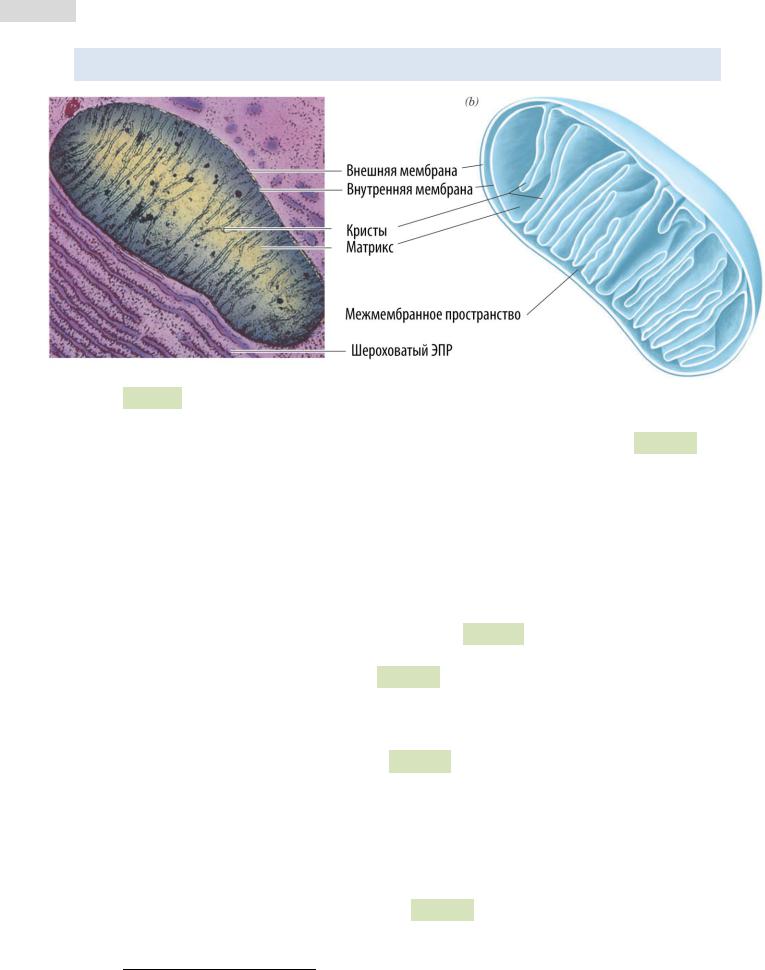
Рис. 118. Митохондрия.
Митохондрии представляют собой двумембранные органеллы (см. Рис. 118 ▲). Внешняя мембрана имеет поры, пропускающие в межмембранное пространство молекулы до 10 кДа (вплоть до небольших белков). Внутренняя мембрана митохондрий очень селективна и содержит множество транспортных систем, переносящих важные соединения из межмембранного пространства в матрикс митохондрий (т.е. во внутреннюю полость).
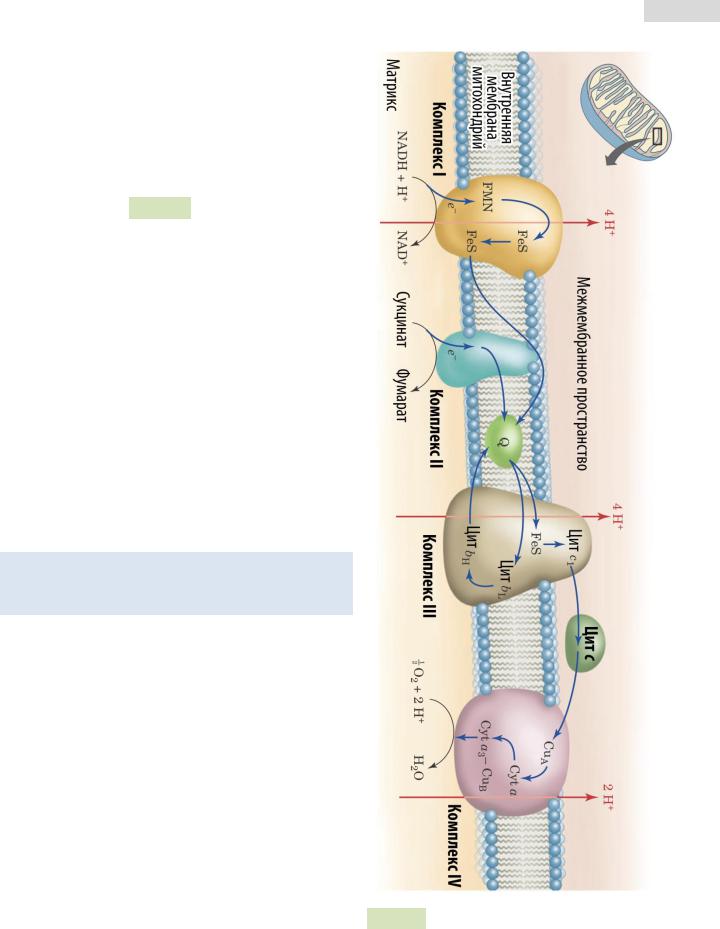
Во внутреннюю мембрану митохондрий встроены белковые комплексы — компоненты дыхательной цепи (цепи переноса электронов или электронтранспортной цепи). Дыхательная цепь митохондрий крайне важна, поскольку отвечает за синтез АТФ в клетке. Компоненты дыхательной цепи (см. Рис. 119 ▼):
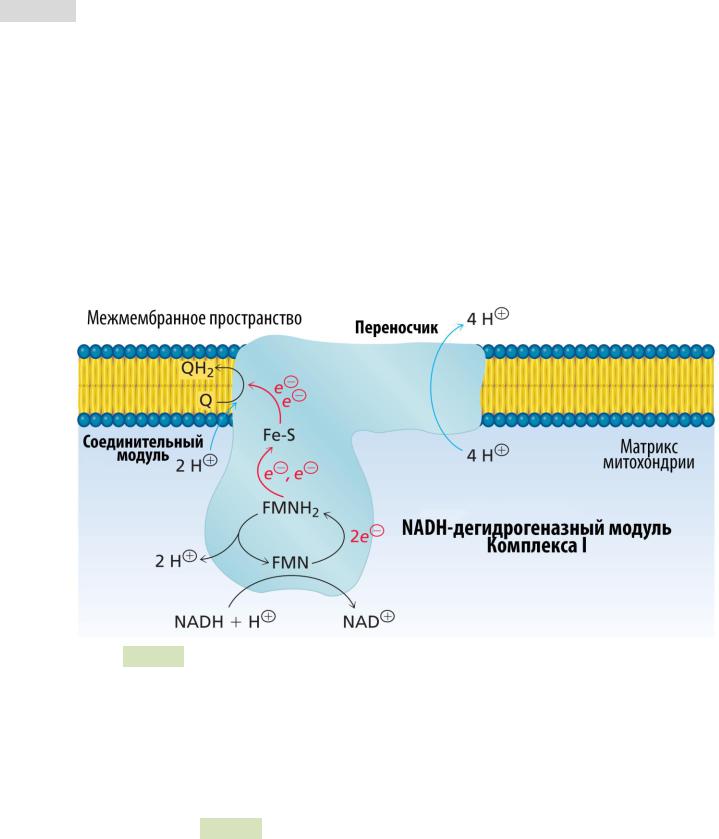
1.Комплекс I (NADH-CoQ 1 оксидоредуктаза; ~900 кДа, 45 уникальных субъединиц) включает (см. Рис. 120 ▼):
а. FMN (флавинмононуклеотид);
б. Ряд Fe-S центров (железистосерные центры).
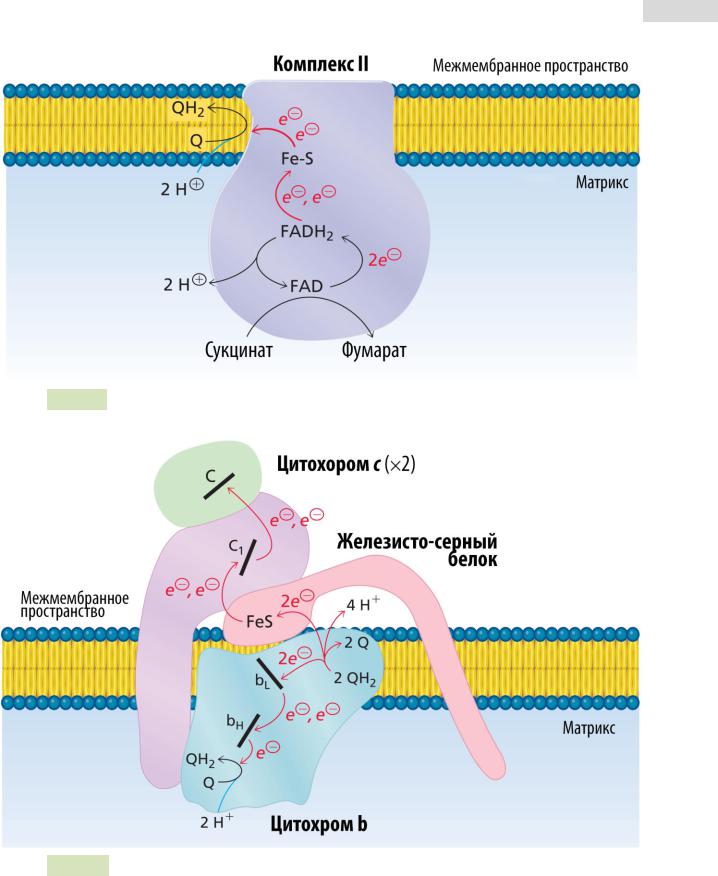
2.Комплекс II (сукцинат-CoQ оксидоредуктаза; ~420 кДа, 4 уникальные субъединицы) включает (см. Рис. 121 ▼):
а. FAD (флавинадениндинуклеотид); б. Ряд Fe-S центров;
в. Гем b560.
3.Кофермент Q (CoQ; единственный небелковый компонент дыхательной цепи).
4.Комплекс III (CoQ-цитохром с оксидоредуктаза; ~450 кДа, 9-11 уникальных субъединиц) включает (см. Рис. 122 ▼):
а. Гем bH (b562)
1 CoQ (англ. coenzyme Q – кофермент Q или просто Q) — убихинон. Может находиться в окисленной (Q) и восстановленной форме (QH2).
Сопряжение дыхания и окислительного фосфорилирования 203
б. Гем bL (b566) в. Fe-S центр; г. Гем c1.
5.Цитохром c («с» чит. как «цэ»).
6.Комплекс IV (цитохром с оксидаза; димер ~410 кДа, 8-13 уникальных субъединиц) включает
(см. Рис. 123 ▼):
а. Гем a;
б. CuA и CuB (медные центры). в. Гем a3.
Сдыхательной цепью связан (но не от-
носится к ней) комплекс V (АТФ-синтаза), непосредственно синтезирующий АТФ.
Переносчиками электронов на дыхательную цепь выступают NADH (никотина- мид-аденин-динуклеотид) и FADH2 (флавин- аденин-динуклеотид). Эти соединения восстанавливаются в ходе разных метаболических путей и циклов (например, в гликолизе, окислительном декарбоксилировании пирувата, ЦТК). Схема переноса электронов изображена на рисунке.
11.3 Сопряжение дыхания и окислительного фосфорилирования
Питер Митчелл предложил хемиосмотическую теорию в 1961 году. Лишь спустя 10 лет его теория получила должное внимание и оценку. В 1978 году ему была вручена Нобелевская премия по химии.
Согласно теории Митчелла, свободная энергия переноса электронов запасается путём переноса протонов H+ из матрикса митохондрий в межмембранное пространство (и тем самым «запасается») и образования таким образом электрохимического градиента протонов H+. Электрохимический протенциал этого градиента протонов используется для синтеза АТФ. В этом и заключается основной смысл со-
пряжения дыхания и окислительного фосфори-
лирования. Некоторые ключевые наблюдения, объясняемые этой теорией:
Рис. 119. Дыхательная цепь митохондрий.
204Глава 11 Энергетический обмен
1.Окислительное фосфорилирование требует интактной митохондриальной мембраны.
2.Внутренняя митохондриальная мембрана непроницаема для ионов (H+, OH–, K+, Cl–), чья диффузия бы нарушила электрохимический градиент.
3.Транспорт электронов сопряжён с переносом протонов из матрикса в межмембранное пространство.
4.Соединения, повышающие проницаемость внутренней митохондриальной мембраны для протонов и тем самым нарушающие электрохимический градиент, не препятствуют транспорту электронов, однако ингибируют синтез АТФ; то есть они «разобщают» процессы переноса электронов и окислительного фосфорилирования.
Рис. 120. Перенос электронов и протонов Комплексом I
Комплексы I, III и IV дыхательной цепи генерируют протонный градиент, транспортируя протоны H+ из матрикса в межмембранное пространство одновременно с переносом электронов. Этот градиент ещё называют протондвижущей си-
лой.
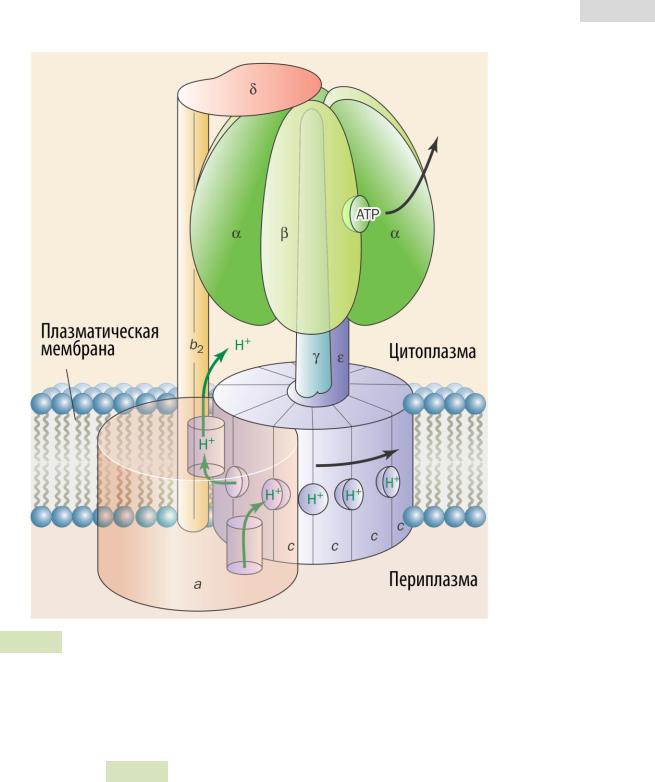
АТФ-синтаза (другие названия: F1F0-синтаза, Комплекс V) представляет собой полисубъединичный трансмембранный белок (фермент) с общей молекулярной массой 450 кДа (см. Рис. 124 ▼). Этот белок состоит из 2 частей:
1.F0 встроен в мембрану и состоит из 8 субъединиц.
2.F1 является периферическим мембранным белком из 5 типов субъеди-
ниц: α3β 3γ δ ε .
Сопряжение дыхания и окислительного фосфорилирования 205
Рис. 121. Перенос электронов Комплексом II
Рис. 122. Перенос электронов и протонов Комплексом III
206 |
Глава 11 |
Энергетический обмен |
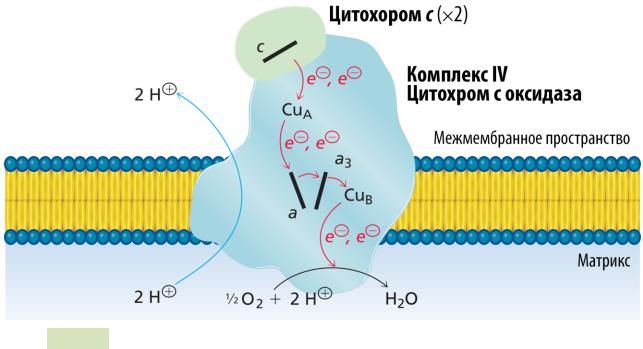
Рис. 123. Перенос электронов и протонов Комплексом IV
Синтез АТФ можно представить в виде трёх фаз:
1.F0 осуществляет транслокацию протонов из межмембранного пространства в матрикс митохондрий.
2.F1 катализирует формирование фосфоангидридной связи (синтез АТФ из АДФ и Фн).
3.Сопряжение рассеяния протонного градиента с синтезом АТФ требует
взаимодействия F1 и F0.
Механизм синтеза — механизм разностного связывания — был предложен Полом Бойером (Paul Boyer). Согласно нему, у компонента F1 есть 3 каталитических протомера (состоящих из αβ -субъединиц), каждый из которых находится в особой конформации:
1.Слабо связывающая субстраты и продукты (L-состояние — англ. loose);
2.Прочно связывающая субстраты и продукты (T-состояние — англ. tight);
3.Свободная конформация, не связанная ни с какими молекулами (O-со- стояние — англ. open).
Сопряжение дыхания и окислительного фосфорилирования 207
Рис. 124. Модель АТФ-синтазы (Комплекса V) кишечной палочки E. coli
Свободная энергия переноса протонов используется для перехода между этими 3 состояниями. Фосфоангидридные связи в АТФ синтезируются только T- протомером, т.е. протомером, находящимся в T-состоянии. Отщепление синтезированной молекулы АТФ осуществляется от протомера в O-состоянии. Эта реакция происходит в 3 этапа (см. Рис. 125 ▼):
1.АДФ и Фн связываются с L-протомером (β DP);
2.Свободная энергия переноса протонов способствует изменению конформации L-сайта в T-сайт и синтезу АТФ в T-сайте (β TP). На этом этапе меняется конформация и других сайтов: T-сайт трансформируется в O- сайт (и происходит диссоциация молекулы АТФ), а O-сайт в L-сайт. Та-
ким образом, в любом момент времени существует 3 протомера (3 сайта, имеющих разную конформацию — T, L и O);
3.АТФ синтезируется в T-сайте, а диссоциирует в O-сайте (β E). Реакция синтеза АТФ находится в равновесии в активном центре фермента. Свободная энергия, обеспечиваемая потоком протонов, способствует от-
