
- •Предисловие
- •Глава 1. Аминокислоты и белки
- •1.1 Общая характеристика
- •1.2 Классификация аминокислот
- •1.3 Модификация аминокислот
- •1.4 Ионизация аминокислот
- •1.5 Пептидная связь
- •1.6 Пептиды и белки
- •1.7 Функции белков
- •1.8 Уровни структурной организации белков
- •А Первичная структура белка
- •Б Вторичная структура белка
- •В Третичная структура белка
- •Д Четвертичная структура белка
- •1.9 Глобулярные и фибриллярные белки
- •А Кератин
- •1.10 Простые и сложные белки
- •1.11 Денатурация и ренатурация белков
- •1.12 Методы работы с белками
- •А Очистка и выделение белка
- •Б Высаливание
- •В Диализ
- •Д Аналитические методы работы с белками
- •Термины
- •Вопросы к семинарскому занятию (1-я часть)
- •Вопросы к семинарскому занятию (2-я часть)
- •Дополнительные вопросы и ключевые слова
- • Аминокислоты
- •Вопросы для самопроверки
- •Глава 2. Ферменты
- •2.1 Общая характеристика
- •2.2 Номенклатура ферментов
- •2.3 Свойства ферментов
- •2.4 Строение фермента
- •2.5 Специфичность ферментов
- •А Модель «ключ-замок»
- •Б Модель индуцированного соответствия
- •2.7 Термодинамика ферментативных реакций
- •2.8 Кинетика ферментативных реакций
- •А Вывод уравнения Михаэлиса-Ментен (по Бергу)
- •В Уравнение Лайнуивера-Берка
- •2.9 Механизмы ферментативного катализа
- •2.10 Влияние факторов среды на скорость протекания ферментативной реакции
- •А Концентрация субстрата
- •2.12 Мультисубстратные реакции
- •А Последовательный механизм
- •2.13 Ингибирование ферментов
- •Б Бесконкурентные ингибиторы
- •В Неконкурентные ингибиторы
- •2.14 Кооперативные взаимодействия внутри молекул ферментов
- •А Параллельная модель
- •2.15 Аллостерическая регуляция активности ферментов
- •2.16 Регуляция активности ферментов с помощью ковалентной модификации
- •2.17 Анти-, мульти- и изоферменты
- •2.18 Ферменты в медицине
- •А Энзимодиагностика
- •Термины
- •Вопросы к занятию (1-я часть)
- •Вопросы к занятию (2-я часть)
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 3. Нуклеиновые кислоты
- •3.1 Общая характеристика
- •3.2 Строение нуклеотида
- •3.3 Первичная структура ДНК
- •3.4 Вторичная структура ДНК
- •3.5 Денатурация и ренатурация ДНК
- •3.6 Третичная структура ДНК
- •3.7 Четвертичная структура ДНК
- •3.8 Виды РНК и их функции
- •3.9 Первичная структура РНК
- •3.10 Вторичная структура РНК
- •3.11 Третичная структура РНК
- •3.12 Четвертичная структура РНК
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 4. Репликация
- •4.1 Общая характеристика
- •4.2 Инициация репликации у прокариот
- •4.3 Элонгация репликации у прокариот
- •Б Механизм ферментативной реакции
- •4.4 Терминация репликации у прокариот
- •4.5 Репликация у эукариот
- •4.6 Проблемы репликации
- •Б Проблема высокой точности процесса
- •4.7 Плазмиды
- •В Типы плазмид
- •Д Механизмы репликации кольцевых плазмид
- •4.8 Репликация вирусов
- •Б Репликация генома РНК-вирусов
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 5. Транскрипция
- •5.1 Организация генетической информации
- •5.2 Общая характеристика транскрипции
- •5.3 Гипотеза Жакоба и Моно
- •5.4 Строение РНК-полимераз
- •5.5 Инициация транскрипции у прокариот
- •5.6 Элонгация транскрипции у прокариот
- •5.7 Терминация транскрипции у прокариот
- •5.8 Инициация транскрипции у эукариот
- •5.9 Элонгация транскрипции у эукариот
- •5.10 Терминация транскрипции у эукариот
- •А Кэпирование
- •Б Полиаденилирование
- •В Сплайсинг
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 6. Трансляция
- •6.1 Общая характеристика
- •6.2 Свойства генетического кода
- •6.3 Основные этапы биосинтеза белка
- •А Этап 1. Активация аминокислот
- •Д Этап 5. Фолдинг и посттрансляционная модификация
- •6.4 Рибосомы
- •6.5 Инициация у прокариот
- •6.6 Инициация у эукариот
- •6.7 Элонгация у прокариот
- •6.8 Элонгация у эукариот
- •6.9 Терминация у прокариот
- •6.10 Терминация у эукариот
- •6.11 Гипотеза «качания»
- •6.12 Фолдинг и посттрансляционная модификация белков
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 7. Регуляция биосинтеза белка
- •7.1 Регуляция экспрессии генов у прокариот
- •В Катаболическая репрессия. Лактозный оперон
- •Д Аттенуация. Триптофановый оперон
- •Е «Сильные» и «слабые» промоторы
- •Ж σ-Субъединица РНК-полимеразы
- •7.2 Регуляция экспрессии генов у эукариот
- •Хроматин-перестраивающие комплексы
- •Архитектурные белки высокомобильной группы
- •Ковалентная модификация гистонов
- •Метилирование ДНК
- •В Регуляция с помощью факторов транскрипции
- •7.3 Регуляция на уровне трансляции у про- и эукариот
- •А Дискриминация мРНК
- •Б Трансляционная репрессия
- •7.4 Другие механизмы регуляции у эукариот
- •Б РНК-интерференция
- •Интерференция с помощью малых интерферирующих РНК
- •Интерференция с помощью микроРНК
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- • Регуляция на уровне транскрипции (прокариоты)
- •Вопросы для самопроверки
- •Глава 8. Мутации и репарация
- •8.1 Мутации
- •8.2 Классификация мутаций по вызвавшим их причинам
- •8.3 Классификация мутаций по степени изменений генома
- •8.4 Классическая классификация
- •8.5 Репарация
- •А Прямая репарация
- •8.6 Эксцизионная репарация оснований (BER)
- •8.7 Эксцизионная репарация нуклеотидов (NER)
- •8.8 Мисметч репарация
- •8.9 Репарация двунитевых разрывов
- •8.10 Негомологичное соединение цепей ДНК при двунитевых разрывах
- •8.11 SOS-репарация (SOS-ответ)
- •8.12 Рекомбинационная репарация
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 9. Иммунитет и антитела
- •9.1 Иммунитет: его виды и элементы
- •9.2 Врожденный (неспецифический) иммунитет
- •В Химические медиаторы врожденного иимунитета
- •Е Классический путь активации комплемента
- •Ж Альтернативный путь активации комплемента
- •З Активация терминальных компонентов комплемента
- •И Как фагоциты отличают чужеродные клетки от «своих»?
- •9.3 Приобретенный (специфический) иммунитет
- •А T-лимфоциты
- •В Антитела
- •Е Вторичный иммунный ответ
- •Ж Активация гуморального иммунитета
- •9.4 Группы крови
- •9.5 Трансфузионные реакции
- •9.6 Правила переливания
- •9.7 Резус-фактор (Rh)
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 10. Биологические мембраны
- •10.1 Строение биомембран
- •В Липиды биомембран
- •10.2 Функции мембран
- •10.3 Мембранный транспорт
- •10.4 Эндо- и экзоцитоз
- •10.5 Трансмембранная передача сигнала
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 11. Энергетический обмен
- •11.1 Энергия в клетке
- •11.2 Дыхательная цепь митохондрий
- •11.3 Сопряжение дыхания и окислительного фосфорилирования
- •11.4 Разобщение дыхания и окислительного фосфорилирования
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 12. Введение в метаболизм
- •12.1 Общая характеристика
- •А Метаболические пути
- •Б Метаболиты
- •В Гомеостаз
- •12.2 Функции метаболических путей
- •А Образование энергии
- •Б Катаболизм органических соединений
- •Переваривание
- •Гликолиз
- •Окисление жирных кислот
- •Катаболизм аминокислот
- •В Синтез органических соединений и предшественников макромолекул
- •Глюконеогенез: синтез глюкозы
- •Синтез жирных кислот
- •Синтез гема
- •Креатинфосфат
- •Гликоген
- •Жиры или триацилглицеролы
- •Д Выведение потенциально опасных соединений
- •Цикл мочевины
- •Синтез желчных кислот
- •Катаболизм гема
- •Е Образование регуляторных молекул
- •12.3 Ключевые положения всех метаболических путей
- •А АТФ — донор энергии для синтеза
- •В Эссенциальные органические соединения
- •Д Взаимосвязи метаболических путей
- •Е Нелинейность метаболических путей
- •Ж Локализация метаболических путей в клетке
- •З Тканеспецифичность метаболических путей
- •И Метаболизм при голодании
- •12.4 Интеграция метаболизма
- •А Основные физиологические состояния организма и роль различных органов в интеграции метаболизма
- •Состояние насыщения
- •Состояние голодания
- •Б Интеграция метаболизма в различных физиологических состояниях
- •Состояние голодания
- •Продолжительное голодание
- •Состояние насыщения
- •Физические нагрузки
- •В Регуляция метаболизма
- •Инсулин
- •Глюкагон
- •Адреналин
- •Гидрокортизон
- •Адипоцитокины
- •Рекомендуемая литература
- •Приложение 1. Аминокислоты и белки
- •Классификация аминокислот
- •Приложение 2. Ферменты
- •Строение химотрипсина
- •Приложение 3. Нуклеиновые кислоты
- •Приложение 4. Репликация
- •Приложение 5. Транскрипция
- •Приложение 6. Трансляция
- •Приложение 7. Регуляция биосинтеза белка
- •Приложение 8. Мутации и репарация
- •Приложение 9. Иммунитет и антитела
- •Приложение 10. Биологические мембраны
- •Приложение 11. Энергетический обмен
- •Оглавление

Регуляция экспрессии генов у эукариот 139
«позволяет» или «не позволяет» РНК-полимеразе связаться с нужным промотором. Если связывания с промотором не произошло, то белок с гена, контролируемого данным промотором, синтезироваться не будет. Распространена гипотеза сменных σ- субъединиц: в зависимости от того, к какому промотору следует присоединиться РНКполимеразе, в коровой части фермента будет присутствовать σ-субъединица то одного, то другого типа (так же, как мы меняем насадки миксера или пылесоса при выполнении разной работы). Нуклеотидные последовательности промоторов, опознаваемых разными σ-субъединицами, существенно различаются и, как правило, не могут быть распознаны более чем одной σ-субъединицей. Например, у бактерии Bacillus subtilis один тип σ-субъединиц распознает последовательность TTGACA, расположенную в положении –35 и последовательность TATAAT в положении –10. Для распознавания другим типом σ-субъединиц этой же бактерии указанные последовательности должны быть ATATT и ATACA соответственно.
Транскрипцию практически всех жизненно важных генов, обеспечивающих гомеостатические клеточные процессы (репликацию ДНК, транскрипцию, трансляцию и т.д.), обеспечивают σ-субъединицы, называемые основными. Остальные процессы требуют альтернативных σ-субъединиц, которых в настоящее время описано не менее десяти. Например, у E. coli при резком повышении температуры (тепловом шоке) начинает синтезироваться альтернативная субъединица σ32 (с молекулярной массой 32 кДа). Ее присутствие придает РНК-полимеразе способность находить промоторы генов, кодирующие защитные белки — белки теплового шока.
7.2Регуляция экспрессии генов у эукариот
АОбщая характеристика
Общий принцип регуляции экспрессии генов у прокариот применим и к эукариотам: экспрессия отдельных генов может быть ингибирована или активирована с помощью особых белков, которые способны связываться с ДНК или РНК. Как и у прокариот, большинство регуляторных механизмов действуют на уровне транскрипции. Однако эукариотические организмы имеют значительно более сложную регуляцию экспрессии генов, чем прокариотические. Основные отличия связаны в первую очередь со строением ДНК:
1.Эукариотическая ДНК имеет огромные размеры по сравнению с прокариотической. К примеру, кишечная палочка E. coli имеет одну кольцевую хромосому (4 миллиона нуклеотидных пар), а самый примитивный эукариотический организм — Saccharomyces cerevisiae — имеет 16 хромосом, и длина его ДНК — 16 миллионов нуклеотидных пар.
2.Генотип у эукариот в большинстве случаев диплоидный.
3.Эукариотическая ДНК связана с белками гистонами и образует хроматин. Хроматин состоит из повторяющихся элементов — нуклеосом (см. тему 3). Каждая молекула гистона в нуклеосоме имеет N- терминальный «хвост», который может ковалентно модифицироваться. Именно эта модификация гистонов играет значимую роль в регуляции экспрессии эукариотических генов.
140Глава 7 Регуляция биосинтеза белка
4.Эукариотические гены не организованы в опероны. Гены, кодирующие белки, участвующие в одном метаболическом пути, часто находятся в разных частях генома. Однако у эукариот существует кластеризация генома — некоторые гены объединены в кластеры.
5.Жизненный цикл у эукариот сложнее и продолжительнее, чем у прокариот.
6.Процессы транскрипции и трансляции у эукариот разделены в пространстве и во времени.
Некоторые особенности регуляции экспрессии генов у эукариот:
1.У эукариот большинство генов «выключено», т.е. транскрипция на них не идёт, поэтому регуляция очень часто направлена на их «включение». Постоянно транскрибируется не более 7-10% генов.
2.Регуляция осуществляется очень «гибко». Возможна различная интенсивность синтеза белка (низкая или высокая).
3.Транскрипционный аппарат состоит из множества белковых факторов, комбинирование которых делает регуляцию более разнообразной.
4.Эукариоты активно нарабатывают мРНК заранее и используют их «по потребности».
БСтруктура хроматина и регуляция экспрессии генов
Большая часть ДНК в многоклеточных организмах не экспрессируется: к ней относятся участки, не кодирующие белок или РНК, а также гены, чья экспрессия в клетках определённого типа нежелательна. Несмотря на то, что все клетки организма содержат одинаковый набор молекул ДНК, их экспрессия тканеспецифична. Например, многие клетки поджелудочной железы синтезируют и секретируют пищеварительные ферменты, при этом островковые клетки поджелудочной железы синтезируют инсулин или глюкагон.
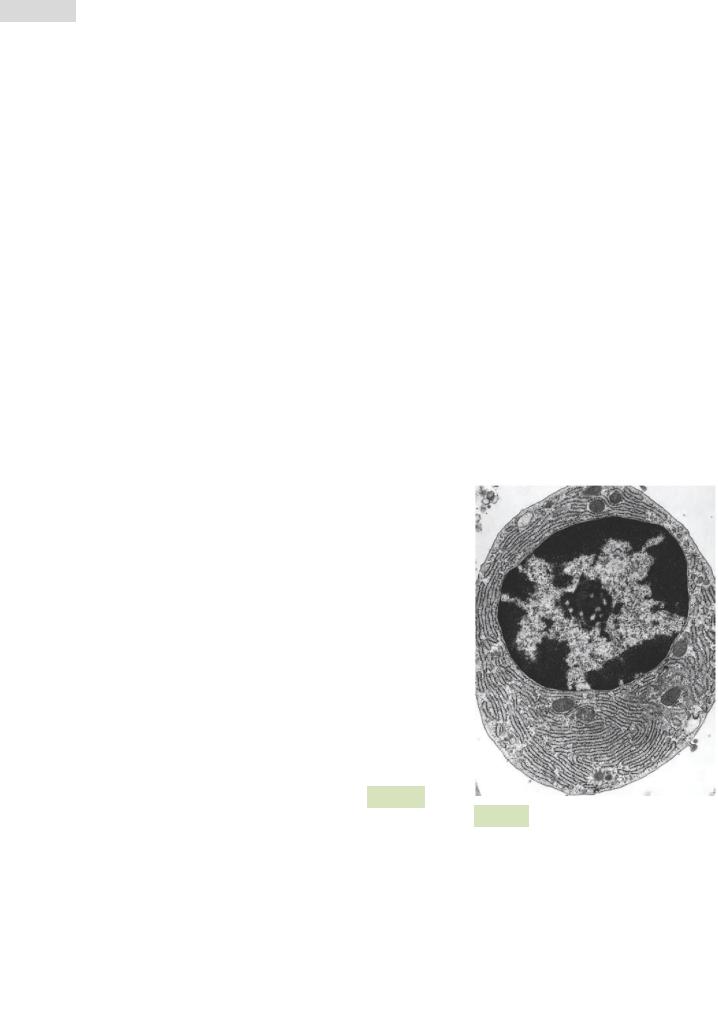
Неэкспрессируемая ДНК — гетерохроматин — обычно высокоспирализована и потому недоступна для РНК-полимераз (см. Рис. 93 ). Транскрипционно активная форма ДНК — эухроматин — имеет меньшую степень спирализации.
Для того, чтобы экспрессировать генетическую информацию ДНК, транскрипционный аппарат клетки должен получить «доступ» к ДНК, которая упакована в нуклеосомную нить гистоновыми белками. Нуклеосомы не являются фиксированными структурами — они могут подвергаться перестройке. Например, гистоны способны ковалентно модифицироваться.
Рис. 93. Электронная микрофотография B-лимфоцита. Значи-
тельную часть клетки занимает ядро, где темные участки — гетерохроматин (неактивная ДНК), а светлые — эухроматин (активная ДНК). В центре ядра — ядрышко. Обратите внимание на обилие шероховатого эндоплазматического ретикулума в клетке.

Регуляция экспрессии генов у эукариот 141
Хроматин-перестраивающие комплексы
В ходе матричных процессов — транскрипции и репликации — полимеразные белки и белковые факторы должны иметь возможность присоединяться к цепи ДНК. Однако практически вся ДНК у эукариот связана с гистонами и образует нуклеосомную нить. В середине 90-х годов стало известно, что хроматин содержит комплексы,
перестраивающие нуклеосомы и использующие энергию АТФ. Эти комплексы разры-
вают связи между ДНК и гистонами, благодаря чему ДНК становится доступной для других белков, а гистоновый октамер «скользит» вдоль цепи ДНК или даже перено-
сится на другую цепь. Таким образом, хроматин-перестраивающие комплексы
придают хроматину «плавающую» структуру, не меняя общую степень упаковки ДНК. Хроматин-перестраивающие комплексы состоят из множества субъединиц, организованных в комплекс SWI/SNF (~11 субъединиц) и комплекс RSC. Донором энергии служат молекулы АТФ. Предполагаемый механизм действия этих комплексов заключается во внесении локальных изгибов в цепь ДНК, благодаря созданию «волн», которые постепенно разрывают связи между ДНК и гистонами. В результате нуклеосомный кор «соскальзывает» с нужного участка ДНК, приоткрывая его для бел-
ков-ферментов.
Архитектурные белки высокомобильной группы
Среди негистоновых белков, связанных с ДНК, самыми распространенными являются белки высокомобильной группы (HMG-белки). Они были названы так потому, что обладают высокой электрофоретической мобильностью в полиакриламидном геле (электрофорез). Эти белки имеют малую массу ~30 кДа и необычный аминокислотный состав: ~25% осно́вных и 30% кислых аминокислот.
HMG-белки способны изменять конформацию ДНК, вызывая скручивание, выпрямление, разматывание цепи или формирование петель.
Ковалентная модификация гистонов
Гистоны способны посттрансляционно модифицироваться:
—Ацетилирование по определённым остаткам лизина (присоединение ацетильной группы —CH3CO).
—Метилирование определённых остатков лизина и аргинина (присоединение метильной группы —CH3).
—Фосфорилирование определенных остатков серина и треонина (присоединение остатка фосфорной кислоты —PO4 3–).
—Убиквитинилирование определённых остатков лизина.
Все модификации за исключением метилирования снижают заряд гистонов (он становится отрицательным), поэтому их взаимодействие с ДНК нарушается (ДНК заряжена отрицательно, а гистоны в норме — положительно). Гистоны отщепляются от ДНК, и транскрипция начинается.
Метилирование гистонов H3 и H4 по остаткам лизина и аргинина выключает экспрессию генов, вызывая формирование гетерохроматина.
