
- •Предисловие
- •Глава 1. Аминокислоты и белки
- •1.1 Общая характеристика
- •1.2 Классификация аминокислот
- •1.3 Модификация аминокислот
- •1.4 Ионизация аминокислот
- •1.5 Пептидная связь
- •1.6 Пептиды и белки
- •1.7 Функции белков
- •1.8 Уровни структурной организации белков
- •А Первичная структура белка
- •Б Вторичная структура белка
- •В Третичная структура белка
- •Д Четвертичная структура белка
- •1.9 Глобулярные и фибриллярные белки
- •А Кератин
- •1.10 Простые и сложные белки
- •1.11 Денатурация и ренатурация белков
- •1.12 Методы работы с белками
- •А Очистка и выделение белка
- •Б Высаливание
- •В Диализ
- •Д Аналитические методы работы с белками
- •Термины
- •Вопросы к семинарскому занятию (1-я часть)
- •Вопросы к семинарскому занятию (2-я часть)
- •Дополнительные вопросы и ключевые слова
- • Аминокислоты
- •Вопросы для самопроверки
- •Глава 2. Ферменты
- •2.1 Общая характеристика
- •2.2 Номенклатура ферментов
- •2.3 Свойства ферментов
- •2.4 Строение фермента
- •2.5 Специфичность ферментов
- •А Модель «ключ-замок»
- •Б Модель индуцированного соответствия
- •2.7 Термодинамика ферментативных реакций
- •2.8 Кинетика ферментативных реакций
- •А Вывод уравнения Михаэлиса-Ментен (по Бергу)
- •В Уравнение Лайнуивера-Берка
- •2.9 Механизмы ферментативного катализа
- •2.10 Влияние факторов среды на скорость протекания ферментативной реакции
- •А Концентрация субстрата
- •2.12 Мультисубстратные реакции
- •А Последовательный механизм
- •2.13 Ингибирование ферментов
- •Б Бесконкурентные ингибиторы
- •В Неконкурентные ингибиторы
- •2.14 Кооперативные взаимодействия внутри молекул ферментов
- •А Параллельная модель
- •2.15 Аллостерическая регуляция активности ферментов
- •2.16 Регуляция активности ферментов с помощью ковалентной модификации
- •2.17 Анти-, мульти- и изоферменты
- •2.18 Ферменты в медицине
- •А Энзимодиагностика
- •Термины
- •Вопросы к занятию (1-я часть)
- •Вопросы к занятию (2-я часть)
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 3. Нуклеиновые кислоты
- •3.1 Общая характеристика
- •3.2 Строение нуклеотида
- •3.3 Первичная структура ДНК
- •3.4 Вторичная структура ДНК
- •3.5 Денатурация и ренатурация ДНК
- •3.6 Третичная структура ДНК
- •3.7 Четвертичная структура ДНК
- •3.8 Виды РНК и их функции
- •3.9 Первичная структура РНК
- •3.10 Вторичная структура РНК
- •3.11 Третичная структура РНК
- •3.12 Четвертичная структура РНК
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 4. Репликация
- •4.1 Общая характеристика
- •4.2 Инициация репликации у прокариот
- •4.3 Элонгация репликации у прокариот
- •Б Механизм ферментативной реакции
- •4.4 Терминация репликации у прокариот
- •4.5 Репликация у эукариот
- •4.6 Проблемы репликации
- •Б Проблема высокой точности процесса
- •4.7 Плазмиды
- •В Типы плазмид
- •Д Механизмы репликации кольцевых плазмид
- •4.8 Репликация вирусов
- •Б Репликация генома РНК-вирусов
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 5. Транскрипция
- •5.1 Организация генетической информации
- •5.2 Общая характеристика транскрипции
- •5.3 Гипотеза Жакоба и Моно
- •5.4 Строение РНК-полимераз
- •5.5 Инициация транскрипции у прокариот
- •5.6 Элонгация транскрипции у прокариот
- •5.7 Терминация транскрипции у прокариот
- •5.8 Инициация транскрипции у эукариот
- •5.9 Элонгация транскрипции у эукариот
- •5.10 Терминация транскрипции у эукариот
- •А Кэпирование
- •Б Полиаденилирование
- •В Сплайсинг
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 6. Трансляция
- •6.1 Общая характеристика
- •6.2 Свойства генетического кода
- •6.3 Основные этапы биосинтеза белка
- •А Этап 1. Активация аминокислот
- •Д Этап 5. Фолдинг и посттрансляционная модификация
- •6.4 Рибосомы
- •6.5 Инициация у прокариот
- •6.6 Инициация у эукариот
- •6.7 Элонгация у прокариот
- •6.8 Элонгация у эукариот
- •6.9 Терминация у прокариот
- •6.10 Терминация у эукариот
- •6.11 Гипотеза «качания»
- •6.12 Фолдинг и посттрансляционная модификация белков
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 7. Регуляция биосинтеза белка
- •7.1 Регуляция экспрессии генов у прокариот
- •В Катаболическая репрессия. Лактозный оперон
- •Д Аттенуация. Триптофановый оперон
- •Е «Сильные» и «слабые» промоторы
- •Ж σ-Субъединица РНК-полимеразы
- •7.2 Регуляция экспрессии генов у эукариот
- •Хроматин-перестраивающие комплексы
- •Архитектурные белки высокомобильной группы
- •Ковалентная модификация гистонов
- •Метилирование ДНК
- •В Регуляция с помощью факторов транскрипции
- •7.3 Регуляция на уровне трансляции у про- и эукариот
- •А Дискриминация мРНК
- •Б Трансляционная репрессия
- •7.4 Другие механизмы регуляции у эукариот
- •Б РНК-интерференция
- •Интерференция с помощью малых интерферирующих РНК
- •Интерференция с помощью микроРНК
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- • Регуляция на уровне транскрипции (прокариоты)
- •Вопросы для самопроверки
- •Глава 8. Мутации и репарация
- •8.1 Мутации
- •8.2 Классификация мутаций по вызвавшим их причинам
- •8.3 Классификация мутаций по степени изменений генома
- •8.4 Классическая классификация
- •8.5 Репарация
- •А Прямая репарация
- •8.6 Эксцизионная репарация оснований (BER)
- •8.7 Эксцизионная репарация нуклеотидов (NER)
- •8.8 Мисметч репарация
- •8.9 Репарация двунитевых разрывов
- •8.10 Негомологичное соединение цепей ДНК при двунитевых разрывах
- •8.11 SOS-репарация (SOS-ответ)
- •8.12 Рекомбинационная репарация
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 9. Иммунитет и антитела
- •9.1 Иммунитет: его виды и элементы
- •9.2 Врожденный (неспецифический) иммунитет
- •В Химические медиаторы врожденного иимунитета
- •Е Классический путь активации комплемента
- •Ж Альтернативный путь активации комплемента
- •З Активация терминальных компонентов комплемента
- •И Как фагоциты отличают чужеродные клетки от «своих»?
- •9.3 Приобретенный (специфический) иммунитет
- •А T-лимфоциты
- •В Антитела
- •Е Вторичный иммунный ответ
- •Ж Активация гуморального иммунитета
- •9.4 Группы крови
- •9.5 Трансфузионные реакции
- •9.6 Правила переливания
- •9.7 Резус-фактор (Rh)
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 10. Биологические мембраны
- •10.1 Строение биомембран
- •В Липиды биомембран
- •10.2 Функции мембран
- •10.3 Мембранный транспорт
- •10.4 Эндо- и экзоцитоз
- •10.5 Трансмембранная передача сигнала
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 11. Энергетический обмен
- •11.1 Энергия в клетке
- •11.2 Дыхательная цепь митохондрий
- •11.3 Сопряжение дыхания и окислительного фосфорилирования
- •11.4 Разобщение дыхания и окислительного фосфорилирования
- •Термины
- •Вопросы к занятию
- •Дополнительные вопросы и ключевые слова
- •Вопросы для самопроверки
- •Глава 12. Введение в метаболизм
- •12.1 Общая характеристика
- •А Метаболические пути
- •Б Метаболиты
- •В Гомеостаз
- •12.2 Функции метаболических путей
- •А Образование энергии
- •Б Катаболизм органических соединений
- •Переваривание
- •Гликолиз
- •Окисление жирных кислот
- •Катаболизм аминокислот
- •В Синтез органических соединений и предшественников макромолекул
- •Глюконеогенез: синтез глюкозы
- •Синтез жирных кислот
- •Синтез гема
- •Креатинфосфат
- •Гликоген
- •Жиры или триацилглицеролы
- •Д Выведение потенциально опасных соединений
- •Цикл мочевины
- •Синтез желчных кислот
- •Катаболизм гема
- •Е Образование регуляторных молекул
- •12.3 Ключевые положения всех метаболических путей
- •А АТФ — донор энергии для синтеза
- •В Эссенциальные органические соединения
- •Д Взаимосвязи метаболических путей
- •Е Нелинейность метаболических путей
- •Ж Локализация метаболических путей в клетке
- •З Тканеспецифичность метаболических путей
- •И Метаболизм при голодании
- •12.4 Интеграция метаболизма
- •А Основные физиологические состояния организма и роль различных органов в интеграции метаболизма
- •Состояние насыщения
- •Состояние голодания
- •Б Интеграция метаболизма в различных физиологических состояниях
- •Состояние голодания
- •Продолжительное голодание
- •Состояние насыщения
- •Физические нагрузки
- •В Регуляция метаболизма
- •Инсулин
- •Глюкагон
- •Адреналин
- •Гидрокортизон
- •Адипоцитокины
- •Рекомендуемая литература
- •Приложение 1. Аминокислоты и белки
- •Классификация аминокислот
- •Приложение 2. Ферменты
- •Строение химотрипсина
- •Приложение 3. Нуклеиновые кислоты
- •Приложение 4. Репликация
- •Приложение 5. Транскрипция
- •Приложение 6. Трансляция
- •Приложение 7. Регуляция биосинтеза белка
- •Приложение 8. Мутации и репарация
- •Приложение 9. Иммунитет и антитела
- •Приложение 10. Биологические мембраны
- •Приложение 11. Энергетический обмен
- •Оглавление
64 |
Глава 2 |
Ферменты |
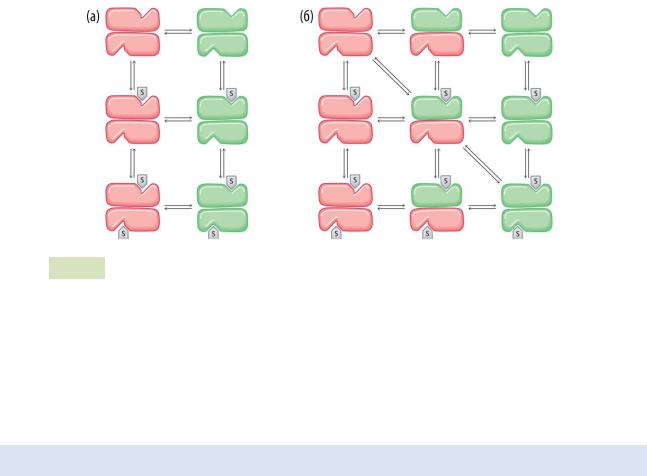
Рис. 45. Две модели кооперативных взаимодействий при связывании субстрата с ферментом: а) параллельная модель; б) последовательная модель.
Существует явление отрицательной кооперативности ферментов: связывание субстрата с одной субъединицей делает невозможным связывание таких же молекул субстрата с остальными субъединицами фермента. Например, связывание тирозина с одной субъединицей тирозил-тРНК-синтетазы ингибирует связывание тирозина с другими субъединицами.
2.15 Аллостерическая регуляция активности ферментов
Аллостерические ферменты регулируются молекулами, которые называют эффекторами. Они связываются с ферментом в аллостерическом центре и изменяют свойства ферментов: сродство к субстрату (прочность его связывания с ним) и максимальная скорость катализа.
Эффекторы могут быть положительными и отрицательными (позитивными и негативными). Положительные эффекторы — активаторы — повышают активность ферментов, а отрицательные эффекторы — ингибиторы — снижают её. Кроме того, эффекторы классифицируют на:
1.Гомотропные эффекторы — это молекулы самого субстрата фер-
мента. Чаще всего регуляция происходит по позитивному механизму: субстрат повышает сродство фермента и активность его каталитических субъединиц. Однако не исключается и негативная регуляция.
2.Гетеротропные эффекторы — это молекулы, отличные от субстрата — т.е. какие-либо другие соединения. Регуляция может быть как позитивной, так и негативной, но чаще всего она негативная: связывание гетеротропного эффектора (ингибитора) снижает сродство фермента к субстрату и влияет на его каталитические свойства.

Регуляция активности ферментов с помощью ковалентной модификации 65
2.16 Регуляция активности ферментов с помощью ковалентной модификации
Регуляция работы фермента может осуществляться и по механизму ковалентной модификации. Одна из наиболее частых модификаций фермента — его фосфорилирование / дефосфорилирование — присоединение / отщепление остатка фосфорной кислоты к молекуле. Как правило, фосфорилированию подвергаются остатки серина (см. Рис. 46 ▼), тирозина и треонина. Белки, которые осуществляют эти реакции называют протеинкиназами. Донором фосфатных остатков являются молекулы АТФ.
Рис. 46. Фосфорилирование серина.
Стоит заметить, что фосфорилирование не всегда активирует фермент. Нельзя точно предсказать, как скажется фосфорилирование на активности белка без проверки обеих гипотез (активация / ингибирование) на практике. Например, гликогенфосфорилаза в фосфорилированном состоянии активна, а гликогенсинтаза — неактивна.
2.17 Анти-, мульти- и изоферменты
Антиферменты — это соединения, например, антитела или ингибирующие ферменты, способные снизить или нарушить активность фермента. Примером антифермента является α -1-антитрипсин (его ещё называют α -1-ингибитор протеаз), который защищает ткани от ферментов иммунных клеток, участвующих в неспецифическом иммунном ответе (в реакциях воспаления). Антитрипсин ингибирует эластазу нейтрофилов, которая расщепляет фибриллярный белок эластин. Другие при-
меры: α -1-антихимотрипсин, каллистатин, васпин, антитромбин, нейросерпин.
Мультиферменты представляют собой комплексные ферментные системы (комплексы из нескольких белковых субъединиц), последовательно катализирующие взаимосвязанные реакции одного метаболического пути или реакции, имеющие общие метаболиты. Примеры: Комплексы I и IV (дыхательная цепь митохондрий), синтаза жирных кислот, глициндекарбоксилазный комплекс, α -кетоглутаратдегидроге- назный комплекс, сахаразо-изомальтазный комплекс, пируватдегидрогеназный комплекс.
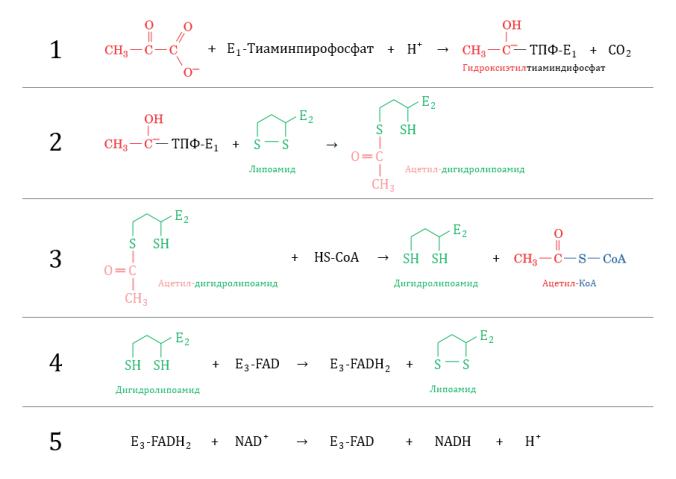
К примеру, рассмотрим пируватдегидрогеназный комплекс. Он состоит из субъединиц трёх типов в разном количестве — 45 E1 + 60 E2 + 9 E3:
66 |
Глава 2 |
Ферменты |
—E1 (пируватдегидрогеназа) — примерно 45 гетеротетрамеров;
—E2 (дигидролипоилтрансацетилаза) — 60 субъединиц;
—E3 (дигидролипоилдегидрогеназа) — 9 гомодимеров.
Каждая из субъединиц представляет собой полипептидную цепь и обладает ферментативной активностью. В целом этот комплекс осуществляет 5 последовательных превращений. При этом в трёх из них участвует E2:
У организации ферментов в мультиферментные комплексы есть ряд преимуществ:
1.Ферментативные реакции ограничены той частотой, с которой молекулы фермента и субстрата «сталкиваются» и взаимодействуют. Если реакции осуществляет мультиферментный комплекс, то расстояние, которое субстрат должен преодолеть, попадая из одного активного центра в другой (т.е. от одной субъединицы к другой) резко снижается, а значит, скорост реакции повышается (фермент меньшее количество времени «ждёт» субстрат).
2.Перенаправление продуктов реакций между субъединицами мультиферментного комплекса снижает вероятность их нежелательного взаимодействия с другими соединениями.
3.Мультиферментный комплекс регулируется скоординированно. Изоферменты (или изозимы) — это ферменты, отличающиеся по аминокис-
лотной последовательности, но при этом катализирующие одну и ту же химическую реакцию. Иными словами, изоферменты — это разные варианты одного и того же фермента. Обычно у этих ферментов разные кинетические показатели (константа
