
- •И. В. Мозговой, г. М. Давидан, л.Н. Олейник
- •Предисловие
- •Тема 1.
- •1.1. Краткая история нефтепереработки
- •1.2. Происхождение нефти
- •1.3. Мировые запасы нефти
- •1.4. Добыча нефти
- •1.5. Добыча природных газов
- •Контрольные вопросы
- •2.2. Химический состав нефти
- •2.3. Классификация нефтей
- •Контрольные вопросы
- •Тема 3.
- •3.1. Фракционный состав нефтей
- •3.2. Плотность
- •3.3. Молекулярная масса
- •3.4. Вязкость
- •3.5. Низкотемпературные свойства нефти и нефтепродуктов
- •3.6. Пожароопасные и взрывоопасные свойства нефтепродуктов
- •3.7. Оптические свойства нефти и нефтепродуктов
- •3.8. Электрические свойства нефтепродуктов
- •3.9. Тепловые свойства нефтепродуктов
- •Контрольные вопросы
- •Тема 4.
- •4.1. Газообразные алканы
- •4.2. Жидкие алканы
- •4.3. Твердые алканы
- •4.4. Физические свойства алканов
- •4.5. Химические свойства алканов
- •Контрольные вопросы
- •Тема 5.
- •5.1. Физические свойства циклоалканов
- •5.2. Химические свойства циклоалканов
- •5.3. Получение циклоалканов
- •5.3.2. Получение циклогептана
- •5.3.4. Получение циклододекана
- •Контрольные вопросы
- •Тема 6.
- •6.1. Типы аренов и концентрация их в нефтях и их фракциях
- •6.2. Физические свойства аренов
- •6.3. Химические свойства
- •6.3.3. Окисление
- •6.4. Применение аренов в нефтехимии
- •Контрольные вопросы
- •Тема 7.
- •7.1. Сернистые соединения
- •7.2. Азотистые соединения
- •7.3. Кислородсодержащие соединения
- •7.4. Асфальто-смолистые вещества
- •7.5. Микроэлементы
- •Контрольные вопросы
- •Тема 8.
- •8.1. Введение в теорию
- •8.2. Кинетика и механизм термических процессов
- •8.3. Термические превращения углеводородов в газовой фазе
- •8.4. Пиролиз (высокотемпературный крекинг)
- •8.5. Коксование
- •8.6. Промышленные термические процессы
- •Контрольные вопросы
- •Тема 9.
- •9.1. Основные понятия о катализе и катализаторах
- •9.2. Реакции карбкатионов
- •9.3. Каталитический крекинг
- •9.4. Катализаторы каталитического крекинга
- •9.5. Макрокинетика процесса
- •9.6. Промышленный каталитический крекинг
- •Контрольные вопросы
- •Тема 10.
- •10.1. Химизм процесса
- •10.2. Катализаторы процесса
- •10.3. Промышленная реализация процесса
- •Контрольные вопросы
- •Тема 11.
- •11.1. Алкилирование изоалканов алкенами
- •2,2,3-Триметилпентан
- •11.2. Изомеризация алканов с4 – с5
- •11.3. Полимеризация алкенов
- •11.4. Применение сжиженных газов и кислородсодержащих органических веществ в получении карбюраторных топлив
- •Контрольные вопросы
- •Тема 12.
- •12.1. Гидроочистка
- •12.1.3. Реакции кислородных соединений
- •12.2. Гидрокрекинг
- •Контрольные вопросы
- •Тема 13.
- •13.1. Нефтяные топлива
- •13.2. Нефтяные масла
- •13.3. Присадки к маслам
- •13.3. Пластичные смазки
- •13.5. Консервационно-смазочные материалы
- •13.6. Смазочно-охлаждающие технологические жидкости
- •13.7. Нефтяные растворители, ареновые углеводороды, керосины осветительные
- •13.8. Масла белые, вакуумные, технологические, теплоносители
- •13.9. Разные продукты
- •Контрольные вопросы
- •Тема 14.
- •14.1. Автомобильный бензин
- •14.2. Дизельное топливо
- •14.3. Авиационное топливо
- •Контрольные вопросы
- •Тема 15.
- •Контрольные вопросы
- •Библиографический список
- •Содержание
9.2. Реакции карбкатионов
9.2.1. Изомеризация может протекать при переносе как гидрид-иона, так и метил-аниона:
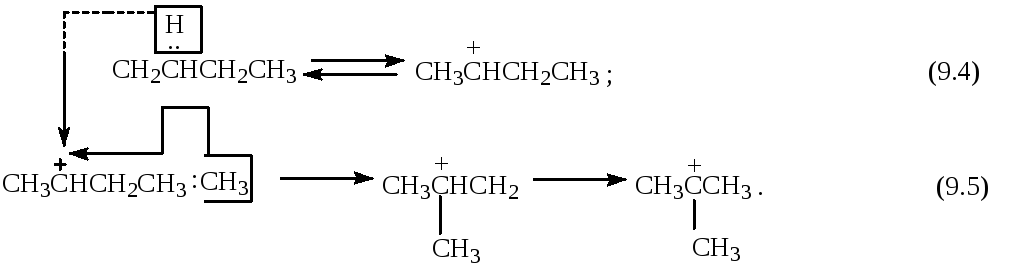 Реакция
изомеризации протекает с небольшим
тепловым эффектом (
Реакция
изомеризации протекает с небольшим
тепловым эффектом (![]() Н
реакции (9.4) равен – 79 кДж/моль,
Н
реакции (9.4) равен – 79 кДж/моль,![]() Н
реакции (9.5) составляет – 59 кДж/моль).
Н
реакции (9.5) составляет – 59 кДж/моль).
9.2.2.
Распад по
![]() -связи.
Расщепление карбкатионов обычно идет
по ослабленной
-связи.
Расщепление карбкатионов обычно идет
по ослабленной
![]() -связи
С – С.
Эта реакция эндотермическая:
-связи
С – С.
Эта реакция эндотермическая:
+ +
 СН2(СН2)6СН3
СН2
= СН2
+ СН2(СН2)4СН3
– 92
кДж/моль.
(9.6)
СН2(СН2)6СН3
СН2
= СН2
+ СН2(СН2)4СН3
– 92
кДж/моль.
(9.6)
Вероятность
распада по
![]() -связи
С – С
снижается при переходе от первичного
иона ко вторичному и третичному. Для
распада вторичного октильного катиона
требуется уже 176 кДж/моль энергии, вместо
92 кДж/моль для первичного катиона. В то
же время распад первичных катионов
возрастает, когда в процессе образуются
вторичные и третичные карбкатионы.
-связи
С – С
снижается при переходе от первичного
иона ко вторичному и третичному. Для
распада вторичного октильного катиона
требуется уже 176 кДж/моль энергии, вместо
92 кДж/моль для первичного катиона. В то
же время распад первичных катионов
возрастает, когда в процессе образуются
вторичные и третичные карбкатионы.
+ +


 СН3СН2СНСН2ССН2СН3
СН2СН=СН2
+С(СН3)2СН2
– 21 кДж/моль (9.7)
СН3СН2СНСН2ССН2СН3
СН2СН=СН2
+С(СН3)2СН2
– 21 кДж/моль (9.7)

 Н3С
СН3
СН3
СН3
СН3
СН3
Н3С
СН3
СН3
СН3
СН3
СН3
Из сравнения термодинамики распада и изомеризации карбкатионов следует, что в большинстве случаев распаду предшествует изомеризация.
9.2.3. Присоединение карбкатионов к алкенам и аренам. Эти реакции являются обратными распаду карбкатионов:
+ +
 (СН3)3С
+ СН2
= С(СН3)2
(СН3)3ССН2С(СН3)2
; (9.8)
(СН3)3С
+ СН2
= С(СН3)2
(СН3)3ССН2С(СН3)2
; (9.8)



 Н
Н


 (СН3)3С
+
+
+. (9.9)
(СН3)3С
+
+
+. (9.9)
 (СН3)3С
(СН3)3С
Реакции (9.8) и (9.9) идут с тепловыми эффектами, равными по абсолютной величине с реакциями распада, но противоположными по знаку.
9.2.4. Передача протона молекуле алкена или аниону катализатора осуществляется, например, в реакции:
+ +
С Н2СНСН3+СН3СН=СН2
СН2=ССН3+СН3СНСН2СН3
+73 кДж/моль. (9.10)
Н2СНСН3+СН3СН=СН2
СН2=ССН3+СН3СНСН2СН3
+73 кДж/моль. (9.10)


СН3 СН3
Термодинамически наиболее вероятны те реакции, в которых протон отщепляется от первичного карбкатиона, а в результате образуется третичный карбкатион. При передаче протона катализатору цепь обрывается.
9.2.5. Отрыв гидрид-иона от молекулы углеводорода оуществляется, например, в реакции:
+
С Н3СНСН2СН3+СН3СН(СН3)2
СН3(СН2)2СН3+
С(СН3)3+41кДж/моль.
(9.11)
Н3СНСН2СН3+СН3СН(СН3)2
СН3(СН2)2СН3+
С(СН3)3+41кДж/моль.
(9.11)
– Н+
Таким путем осуществляется передача цепи. Активность карбкатиона при реакции отрыва гидрид-иона от молекулы изменяется так:
R+перв. > R+втор. > R+трет.
Карбкатионные реакции протекают либо в жидкой фазе, либо на поверхности твердого катализатора. Сольватация в растворе и адсорбция на поверхности твердого катализатора изменяют тепловые эффекты реакций. При этом теоретические соотношения тепловых эффектов реакций разных карбкатионов реально могут значительно отличаться от расчетных соотношений.
