
Marri_i_dr_-_Biokhimia_cheloveka_tom_1
.pdf
Глава 14
Физиологически важные углеводы
Литер Мейес
ВВЕДЕНИЕ |
КЛАССИФИКАЦИЯ УГЛЕВОДОВ |
Углеводы широко представлены в растениях |
в химическом плане углеводы можно определить |
и животных, где они выполняют как структурные, |
как альдегидные или кетонные производныс полиа |
так и метаболические функции. В растениях в про |
томных (содержащих более одной ОН-группы) спир |
цессе фотосинтеза из углекислого газа и воды синте |
тов или как соединения, при гидролизе которых |
зируется глюкоза, которая далее запасается в виде |
образуются эти производные. |
крахмала или превращается в целлюлозу |
1) моносахаридыуглеводыы' которые не могут |
структурную основу растений. Животные способны |
Бы1ь гидролизованы до более простых форм. Их мо |
синтезировать ряд углеводов из жиров и белков, но |
жно подразделить на триозы. тетрозы, пентозы,. ге |
большая часть углеводов поступает с пищей расти |
ксозы, гептозы и октозы в зависимости от числа со |
тельного происхождения. |
держащихся в их молекуле атомов углерода; их мо |
|
жно разделить также на альдозы и кетозы в зависи |
|
мости от присутствия альдегидной или кетонной |
БИОМЕДИЦИНСКОЕ ЗНАЧЕНИЕ
Знания о структуре и свойствах физиологически
важных углеводов необходимы для понимания их
фундаментальной роли в материальном и энергети
ческом обеспечении жизни млекопитающих. Наибо
лее важным углеводом является шестиуглеродный
сахар глюкоза. Именно в форме глюкозы поступает
в кровь основная масса углеводов из пищи; в глю
козу же превращаются углеводы в печени и из
клюкозы могут образовываться все остальные углеводы в организме. Глюкоза используется как основной вид топлива в тканях млекопи
тающих (исключение составляют жвачные живот
ные) и служит универсальным топливом в период эмбрионального развития. Она превращается в
другие углеводы, выполняющие высокоспеци
фичные функции-в гликоген, являющийся формой
хранения энергии, в рибозу, содержащуюся в нуклеи
новых кислотах, в галактозу, которая входит в со
став лактозы молока. Некоторые углеводы входят
в состав сложных липидов и образуют вместе с бел ками гликопротеины и протеогликаны. С наруше
нием обмена углеводов тесно связан ряд заболева
ний-сахарный диабет, галактоземия, нарушения
в системе запасания гликогена, нетолерантность
к молоку.
группы. Примерами могут служить
|
Альдозы |
Кетсзы |
|
Глицероза |
Дигидроксиаuе |
|
|
тон |
Тетрозы (С4НнО4) |
Эритроза |
Эритрулоза |
Пентозы (CsHIOOs) |
Рllбоза |
Рибулоза |
Гексозы (С6Н,2О6) |
Глюкоза |
Фруктоза |
2) Дисахариды при гидролизе дают две молеку лы моносахарида (одинаковых или различных).
Примерами служат сахароза, лактоза и мальтоза.
3) Олигосахариды при гидролизе щtют 3--6 мо носахаридов. Примером может служить мальто
триоза 1.
4) Полисахариды дают при гидролизе более
6 молекул моносахаридов. Они могут быть линей ными или разветвленными. Примерами служат крахмал и декстрины. Иногда их называют гексоза
нами или пентозанами, а также гомополисахарида ми или гетерополисахаридами - в зависимости от
I Это не триоза, а трисахарид, содержащий три остат
ка а-глюкозы.
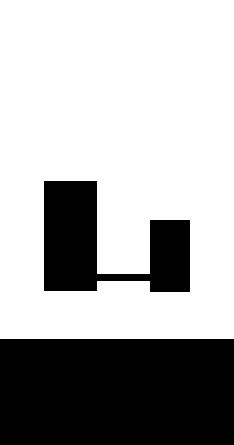
Физиологически ваЖllые углеводы
того, идентичные или неидентичные моносахариды
образуются при их гидролизе.
МОНОСАХАРИДЫ
Структура глюкозы
Линейная формула глюкозы (альдогексоза, рис.
14.1, А) может объяснить ряд ее свойств. но в термо
динамическом отношении более предпочтительна циклическая формула, которая полностью объяс няет химические свойства глюкозы. Для большин
ства целей структурную формулу глюкозы можно
изображать в виде простого кольца с передачей пер спективы, как это предложил Хеуорс (рис. 14.1, Б).
По данным рентгеноструктурного анализа шестич
ленное кольцо, содержащее один атом кислорода,
вдействительности имеет конформацию кресла (рис.
14.1.В).
о
11
IС-Н
I
H()~C -Н
1
3СН2ОН
L-ГлицеРОЗ8
(L-Глицеральдегид)
о
11
IС-Н
1
НО- 2С-Н
1 .
Н- 3С -ОН
1
НО- 4С -Н
1
HO-sС -Н
141
о
11
С-Н
I
Н-С -он
1
СН2ОН
DГлицеРОЗ8 (~Гпицеральдегид)
о
11
С-Н
I
Н-С -ОН
I
НО-С -Н
I
Н-С -ОН
1·
Н-С -он
Изомерия сахаров
Соединения. имеющие одну и ту же структурную
формулу. но различающиеся по пространственной конфигурации, называются стереоизомерами. Обра
зование таких изомеров оказывается возможным
А
Б
~---o
в Н ОН
1 |
I |
IIСН2ОН |
СН2ОН |
L-ГЛЮКОЗ8 |
[).Глюкоза |
Рис. 14.2. D- и L-изомеры Г.lицерозы и ГЛЮКОЗЫ.
при вхождении в состав молекулы асимметрических
атомов углерода (к которым присоединены четыре различных атома или группы). Число возможных
изомеров данного соединения зависит от числа
асимметрических атомов углерода (п) и равно 2".
Глюкоза с четырьмя асимметрическими атомами
углерода имеет. следовательно. 16 изомеров. Ниже
указаны наиболее важные типы изомеров глюкозы.
1. D и L: обозначение изомера как D-формы или как L-формы. являющейся ее зеркальным отображе
нием. основано на сравнении пространственной кон
фигурации изомера с конфигурацией «родительско
го» соединения углеводного семейства -
трехуглеродного сахара глицеральдегида (глицеро
зы). L- и D-формы этого сахара изображены на рис. 14.2 вместе с соответствующими изомерами глюко зы. Принадлежность к D- или L-ряду определяется
ориентацией групп -Н и -ОН при атоме углерода,
соседнем с концевым атомом углерода, содержащим
первичную спиртовую группу (в молекуле глюко
зы - ориентацией групп -Н и -ОН при атоме угле
рода 5). Если группа -ОН при этом углероде нахо
дится справа (как показано на рис. 14.2), сахар при надлежит к D-ряду, если же она стоит слева, сахар относится к L-ряду. Большинство моносахаридов
нв организме млекопитающих имеют о
конфигурацию - именно к этой конфигурации спе
цифичны ферменты. ответственные за их метабо
Рис. 14.1. а-D-глюкозз. |
лизм. |

142 |
|
|
|
Глава /4 |
|
|
|
||
Присутствие асимметрических атомов углерода |
|
|
I |
||||||
|
|
ноеН2 |
|||||||
является |
причиной |
оптической активности соедине |
|
|
|||||
J ---- Q |
|||||||||
ния. Если пучок плоскополяризованного света про |
|||||||||
|
|
|
|||||||
ходит через раствор оптического изомера, плоскость |
|
|
|
||||||
поляризации света |
поворачивается |
либо |
вправо |
|
|
|
|||
(правовращающий изомер. +). либо влево (левовра |
4 |
|
|
||||||
щающий изомер, -). Соединение обозначают О( - |
), |
|
|
|
|||||
|
|
|
|||||||
|
|
|
|||||||
D( +), L( -) или L( +); это обозначение показывает |
|
|
н |
||||||
наличие |
структурного родства с |
D- |
или |
L- |
a-D-Фруt<топираНОЗ8 |
||||
глицеральдегидом, но не обязательно тот же знак |
|||||||||
|
|
|
|||||||
оптического вращения. Например, природной фор |
|
|
|
||||||
мой фруктозы является О( - )-изомер. |
|
|
|
|
|
|
|||
Если D- и L-изомеры присутствуют в равных ко |
|
|
|
||||||
личествах, их смесь не проявляет оптической актив |
|
|
|
||||||
ности - |
активности |
изомеров компенсируют одна |
|
|
|
||||
другую. Такие смеси называют рацемическими (или
DL-смесями). Соединения, получаемые синтетиче
ским путем, оказываются рацемическими, поскольку
в этом случае вероятности образования каждого из
изомеров одинаковы.
2. Пиранозные и фуранозные кольцевые структу |
a-[)"ФРуt<тофураНОЗ8 |
|
ры. Эта терминология основана на существовании |
||
|
двух устойчивых кольцевых структур моносахари
дов, сходных со структурами пирана или фурана
(рис. 14.3). Кольцевую структуру могут принимать
икетозы (например, D-фруктофураноза или D- фруктопираноза; рис. 14.4). В растворе глюкозы бо
лее 99% молекул находится в пиранозной форме
именее 1% - в фуранозной форме.
3.а- И Р-аномеры. Кольцевая структура альдо зы - полуацетальная. так как она образуется в резу льтате взаимодействия альдегидной и спиртовой
групп (рис. 14.5), кольцевая структура кетозы полукетальная. Кристаллическая глюкоза является
-----о |
(:) |
||
|
|
|
|
|
Пиран |
ФУР8Н |
|
|
|
|
ноеН2 |
1 ---- 0 |
|
I |
|
|
неон |
||
нон
a-D1пюt<опираНОЗ8 a-[)..ФРУt<ТОфураноза
Рис. 14.3. Пиранозная и фуранозная формы глюкозы.
. Рис. 14.4. Пиранозная и фуранозная формы фруктозы.
глюкопиранозоЙ. Циклическая структура сохраняе тся и в растворе, но при этом происходит образова ние изомеров относительн~ положения 1, которое занимает карбонильный или аномерный атом углеро да, что приводит к образованию смеси а глюкопиранозы (36%) и ~-глюкопиранозы (63%);
~оставшийся 1% представлен в основном а- и ~ аномерами глюкофу~анозы. Описанное выше уста
новление равновесия сопровождается так называе
мой мутаротацией: полуацетальное кольцо раскры
вается и вновь замыкается, при этом может изменя
ться положение групп --Н и -ОН при углероде 1. Предполагают, что в ходе этого процесса образуется
промежуточная гидратированная линейная (ацикли
ческая) молекула, хотя по данным полярографии на
долю ациклической формы глЮкозы приходится все
го 0.0025%. В растворе глюкоза является правовра щающей; этим объясняется еще одно ее название-
декстроза (декстро - правый), част() употребляемое
вклинической практике.
4.Эпимеры. Изомеры. различающиеся по конфи гурации положением групп -Н и --он при втором.
третьем и четвертом атомах углерода. на·Jываются
эпимерами. Биологически наиболее важными 1пиме рами глюкозы являются манноза и галактоза, обра
зующиеся путем эпимеризации при атомах углерода
2 и 4 соответственно (рис. 14.6).
5. Альдо-кето-изомеризация. Фруктоза имеет ту же химическую формулу, что и глюкоза, но отличае
тся по структурной формуле, поскольку фруктоза со
держит потенциальную кетонную группу в положе
нии 2. а глюкоза - потенциальную альдегидную группу в положении 1 (рис. 14.3 и 14.4).
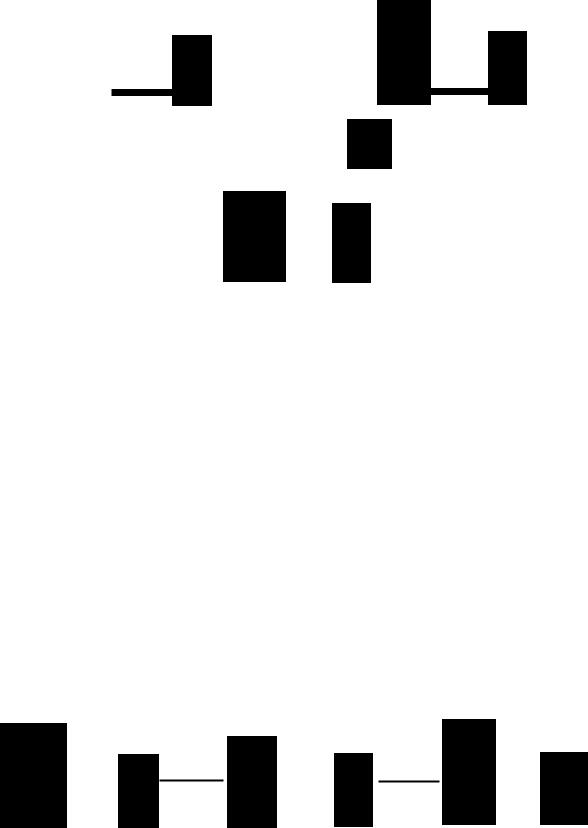
Физиологически важные углеводы |
143 |
~---O |
J ... ---- О |
н |
он |
н |
он |
a-D-Гnюкonир8НО.. '\ .. 13-D-rлюкопираноэа
НОСН2
он
|
|
|
|
|
Ациклическая |
|
|
|
|
|
альдегидная |
|
|
|
|
|
|
|
|
|
|
|
форма |
|
|
н |
он |
||
|
Рис. 14.5. Мутаротация глюкозы. |
||||
Физиологически важные моносахариды |
D-глюкуронат (компонент глюкуронидов и гликоза |
||||
В ходе метаболической деградации глюкозы при |
миногликанов) и его метаболические производные р |
||||
гликолизе образуются |
производные |
различных |
L-идуронат (компонент гликозаминогликанов, рис. |
||
триоз. Метаболические |
превращения |
глюкозы по |
14.9) и L-гулонат (участвует в метаболизме уроно |
||
пентозофосфатному пути приводят к образоваНИIQ |
вой кислоты, см. рис. 21.1). |
||||
|
|
||||
производных триоз, тетроз и пентоз, а также к обра
зованию семиуглеродного сахара (седогептулозы).
Пятиуглеродные моносахариды, пентозы, являются
важными компонентами нуклеотидов, нуклеиновых
кислот и многих коферментов (табл. 14.1). Из гексоз наиболее важное физиологическое значение имеют глюкоза, галактоза, фрукт<)за и манноза (табл. 14.2).
Структура биологически важных альдосахаров показана на рис. 14.7. Пять кетосахаров, играющих важную роль в метаболизме, представлены на рис.
14.8. |
. |
. Самостоятельное значение имеют производные
глюкозы, содержащие карбоксильную группу: а-
HOCH~
Гликозиды
Гликозиды- это соединения, образующиеся пу тем конденсации моносахарида (или моносахарид ного остатка в составе более сложного сахара) с гид роксильной группой другого соединения, которым может быть другой моносахарид или вещество не углеводной природы (тогда его называют aг~нкo ном). Гликозидную связь называют ацетальнои, так
как она образуется в результате реакции между по
луацетальной группой (образующейся при взаимо действии альдегида с -ОН-группой) и другой -
ОН-группой. Если полуацетальная группа принадле-
}----:.- О |
|
}----о |
|
J ---- O |
||||||
|
|
.. |
• |
|
|
• |
• |
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
н |
|
н |
н |
|
он |
|
н |
он |
|
|
|||
|
|
|
|
|
|
|||||
a-ОоГалактоза |
|
|
a-ОоГлюкоза |
|
а-[)'Манноза |
|||||
Рвс. 14.6. Эпимеризация ГЛЮКОЗbl.

144 |
|
Глава J4 |
|
Таблица 14.1. Физиологически важные пентозы |
|
|
|
|
|
|
|
Сахар |
Местонахождение |
Биохимическое значение |
Клиническое значение |
|
|
|
|
D-Рибоза |
Нуклеиновые кислоты |
Структурный элемент нуклеиновых кислот и ко |
|
|
|
ферментов (например: АТР, NAD, NADP, |
|
|
|
флавопротеинов). Является промежуточным |
|
|
|
соединением пентозофоофатного пути |
|
D-Рибулоза |
Образуется в ходе метаболиз |
Промежуточное соединение пентозофосфатного |
|
|
ма |
пути |
|
D-Арабиноза |
Гуммиарабик, сливовая и виш |
Компонент гликопротеинов |
|
|
невая мякоть |
|
|
D-Ксилоза |
Древесная смола, протеоглика |
Компонент гликопротеинов |
|
|
ны, гликозаминогликаны |
|
|
D-Ликсоза |
Сердечная мышца |
Компонент ликсофлавина, выделяемого из сер- |
|
|
|
дечной мышцы человека |
|
L-Ксилулоза |
Промежуточное соединение метаболизма уроновой кислоты |
Обнаруживается |
|
в моче при
пентозурии
жит глюкозе, образующееся соединение называют Дезоксисахара
ГЛЮКОЗИДОМ, если галактозе - галактозидом и т. д.
Гликозиды найдены в составе многих лекарств и пряностей, они являются также компонентами жи
вотных тканей. Агликонами могут быть метанол,
глицерол, какой-либо стерол или фенол. Гликозиды,
имеющие важное медицинское значение, а именно
влияющие на работу сердца (сердечные гликозиды),
содержат в качестве агликонового компонента сте
роиды; так, из наперстянки и строфанта выделен гликозид уабаинингибитор Na+ /К+-АТРазы кле
точных мембран. К числу гликозидов относится ряд антибиотиков, в частности стрептомицин (рис. 14.10).
Таблица 14.2. Физиологически важные rексозы
у дезоксисахаров одна из гидроксильных групп,
присоединенных к кольцевой структуре, замещена на атом Boд~poдa. Они образуются при гидролизе ряда
соединений, играющих важную роль в биологиче ских процессах. Примером служит дезокснрибоза
(рис. 14.11), входящая в состав нуклеиновых кислот
(ДИК).
Другими примерами дезоксисахаров являются L-
фукоза (рис. 14.17) - компонент ряда гликопротеи
нов и 2-дезоксиглюкоза- инrибитор ме:rаболизма
глюкозы.
Сахар Источник Биологическая роль Клиническое значение
D-Глюкоза |
Фруктовые соки. Гид |
«Сахар» организма. Переносится |
Появляется в моче (гликозурия) у |
|||
|
ролиз |
крахмала, |
кровью, эффективно используе |
больных сахарным диабетом из |
||
|
тростникового са |
тся тканями |
за повышенного содержания |
|||
|
хара, |
мальтозы |
и |
|
глюкозы в крови (гиперглике |
|
|
лактозы |
|
|
|
мия) |
|
D-Фруктоза |
Фруктовые соки. Мед. |
Может превращаться в глюкозу в |
Наследственная нетолерантность к |
|||
|
Гидролиз |
трост |
печени и кишечнике, с после |
фруктозе приводит к накоплению |
||
|
никового сахара и |
дующим использованием в |
фруктозы и ГИПОI ликемии |
|||
|
инулина (из иеру |
этой форме |
|
|||
|
салимских |
арти |
|
|
||
|
шоков) |
|
|
|
|
|
D-Галактоза |
Гидролиз лактозы |
|
Может превращаться в глюкозу в |
Нарушение метаболических прсвра |
||
|
|
|
|
|
печени и затем использоваться |
щений галактозы приводит к раз |
|
|
|
|
|
в процессах метаболизма. Син |
витию галактоземии и образова |
|
|
|
|
|
тезируется в молочных желе |
нию катаракты |
|
|
|
|
|
зах, входит в состав лактозы |
|
|
|
|
|
|
молока. Компонент гликолипи |
|
|
|
|
|
|
дов и гликопротеинов |
|
D-Манноза |
Гидролиз |
раститель- |
Компонент многих гликопротеинов |
|
||
|
ных |
маннанов |
и |
|
|
|
камедей

|
|
|
|
|
ФиЗllологически важ'uые углеводы |
|
145 |
|||||
|
|
|
|
|
|
сно |
|
|
|
|
|
|
|
|
|
|
|
|
I |
|
|
|
|
|
|
|
|
|
|
|
|
н-с-он |
|
|
|
|
|
|
|
|
|
|
|
|
I |
|
|
|
|
|
|
|
|
|
|
|
|
сн2он |
|
|
|
|
|
|
|
|
|
|
|
~Глицероза(~,лицерал~егид) |
|
|
|
|
|||
|
|
|
t |
|
|
|
|
|
|
|
t |
|
|
|
сно |
|
|
|
|
|
|
СНО |
|||
|
|
I |
|
|
|
|
|
|
|
I |
||
|
|
но-с-н |
|
|
|
|
|
|
н-с-он |
|||
|
|
I |
|
|
|
|
|
|
|
I |
||
|
|
н-с -он |
|
|
|
|
|
|
н-с -он |
|||
|
|
|
I |
|
|
|
|
|
|
|
I |
|
|
|
СН2 |
ОН |
|
|
|
|
|
|
сн2он |
||
|
|
~Треоза |
|
|
|
|
|
|
~Эритроза |
|||
|
|
, |
|
t |
|
|
|
|
, |
|||
|
|
|
|
|
|
|
||||||
t |
|
|
|
t |
|
|
|
t |
||||
сно |
|
сно |
|
|
сно |
|
|
сно |
||||
|
I |
|
I |
|
|
I |
|
|
|
I |
||
но-с -н |
|
н-с -он |
|
|
но-с-н |
|
|
н-с -ОН |
||||
НО-С -Н |
|
I |
|
|
I |
|
|
|
I |
|||
|
но-с -Н |
|
|
Н-С-ОН |
|
|
Н-С -он |
|||||
|
I |
|
I |
|
|
I |
|
|
|
I |
||
н-с -он |
|
н-с -он |
|
|
н-с -ОН |
|
|
н-с -ОН |
||||
|
I |
|
I |
|
|
I |
|
|
|
I |
||
сн2он |
|
сн2он |
|
|
СН2 |
ОН |
|
|
сн2он |
|||
~Ликсоза |
|
D-Ксилоза |
t |
D-Арабиноза |
|
|
D-Рибоэа |
|||||
|
t |
|
|
I |
|
t |
||||||
|
сно |
|
|
|
|
|
|
|
||||
|
|
|
СНО |
|
сно |
|||||||
|
I |
|
|
I |
|
|
I |
|||||
|
н-с-он |
|
|
но-с-н |
Н-С-ОН |
|||||||
|
I |
|
|
I |
|
|
I |
|||||
|
НО-С-н |
|
|
HO~C-H но-с-н |
||||||||
|
I |
|
|
I |
|
|
I |
|||||
|
но-с-н |
|
|
н-с-он н-с -он |
||||||||
|
I |
|
|
I |
|
|
, |
|
||||
|
н-с-он |
|
|
н-с -ОН Н-С-ОН |
||||||||
|
I |
|
|
I |
|
|
, |
|
||||
|
сн2он |
|
|
сн2он |
сн2он |
|||||||
|
~Галактоза |
|
|
D-Манноза |
D-Глюкоза |
|||||||
Рис. 14.7. С, руктурные соотношения между аЛЬJ].озами D-ряда. о-Треоза фИЗИОJl0гической цеННОСl и не прелстаR.lяет. По строение РЯJЩ основано на добавлении СН2О-сдиниц к - eHO-группе сахар:!.
|
|
|
|
сн2он |
|
|
|
сн2он |
I |
|
|
|
с=о |
|
|
сн2он |
сн2он |
I |
I |
|
с=о |
но-с-н |
||
|
I |
I |
I |
I |
|
с=о |
с=о |
НО-с-н |
н-с -он |
|
I |
I |
I |
I |
сн2он |
но-с-н |
н-с-он |
н-с -он |
н-с -он |
I |
I |
I |
I |
I |
с=о |
н-с -ОН |
н-с -ОН |
н-с-он |
н-с -ОН |
I |
I |
, I |
I |
I |
сн2он |
сн2он |
сн2он |
СН2ОН |
сн2он |
Дигидроксиацетон |
~Ксилулоза |
~Рибулоза |
[).фруктоза |
D-Седогептулоза |
Рис. 14.8. Кетозы (ряд примеров).
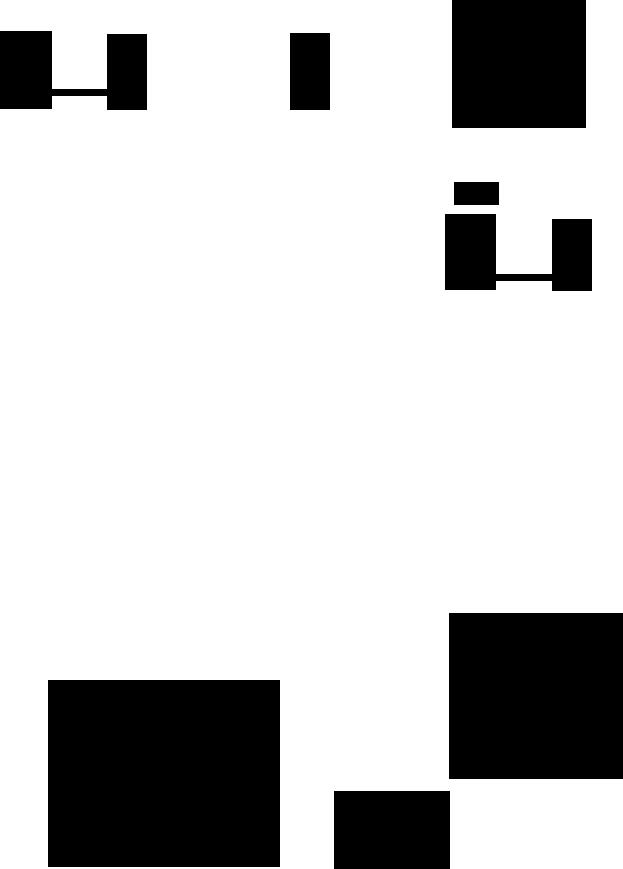
146 |
Глава J4 |
соо- |
н |
J ---- O |
~---o |
н |
он |
н |
он |
н |
|
|
|
|
|
Рис. 14.9. а-D-Глюкуронат (слева) и J3-L-ИДУРОНё1Т (справа I |
Рис. 14.11. 2-Дезокси-D-рибофураноза (J3-форма). |
|||
Аминосахара (гексозамииы)
Примерами аминосахаров служат D-глюкозамин
(рис. 14.(2), D-галактозамин и D-маннозамин-все
эти вещества обнаружены в природе. Глюкозамин является компонентом гиалуроновой кислоты. Га лактозамин (хондрозамин) входит в состав хондрои тина (см. гл. 54).
Ряд антибиотиков (эритромицин, карбомицин)
содержит в своем составе аминосахара. Считается,
что аминосахара вносят существенный вклад в био логическую активность этих антибиотиков.
ДИСАХАРИДЫ
Дисахариды представляют собой сахара, состоя
щие из двух моносахаридных остатков, соединенных
гликозидной связью (рис. 14.13). Их химическое на
звание отражает название составляющих их моноса
харидов. Физиологически важными дисахаридами
являются мальтоза. сахароза. лактоза и трегалоза
(табл. 14.3).
Гидролиз сахарозы приводит к образованию
смеси, которую называют <<инвертированным саха
ром)): в ней преобладает сильно левовращающая фруктоза, которая инвертирует (меняет на обрат ный) знак врашения правовращающего раствора
исходной сахарозы.
|
|
|
|
|
|
|
он |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
о |
|
|
|
|
|
|
сн,он |
O~ |
|
|
|
|
|
|||
|
|
H,CNH |
ОН |
|
HNCNHz |
||||
|
|
|
|
|
|
|
1. |
||
|
|
|
|
|
|
|
|||
NH
ОН
J ----- O
н+ t1
Рис. 14.12. Глюкозамин (2-амино-D-ГЛЮJCопираноза) (а
форма). Галактозамин - 2-амино-D-галаJCтопираноза.
И глюкозамин. и галактозами" в виде N-ацетильных про
изводных входят в состав более сложных углеводов, в част-
ности, в составе гликопротеинов.
ПОЛИСАХАРИДЫ
К полисахаридам относятся следующие физио
логически важные углеводы.
Крахмал. Моносахаридные остатки соединены в крахмале Q-ГЛЮКОЗИДНЫМИ связями. Соединение такой структуры, образованное только остатками
глюкозы, является гомополимером, его. называют
глюкозаном или глюканом. Это наиболее важный
""--0
оон
ОН он
Рис. 14.10. СтреПТОМ!"fЦИН (слева) и уабаин (справа).

|
|
|
|
|
|
|
|
Физиологически важные углеводы |
|
|
|
|
147 |
|||||
|
|
|
|
|
Мальтоза |
|
|
|
|
|
|
Трегалоза |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
н |
ОН |
||
1 ---- 0 |
Joo----O |
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
О |
|
|
|
|
|
|
|
|
О |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
н ' |
|
|
|
|
|
|
|
|
|
|
|
||
н |
|
|
ОН |
ОН |
н |
ОН |
|
|
н |
|||||||||
().a-D-rлюкопираНОIИЛ- (1 - |
4) .cz-о.глюкопираноза |
().a-D-rлюкопиранозил- (1 -1) -а-о.глюкопиранозид |
||||||||||||||||
|
|
|
|
|
Сахароза |
|
|
|
|
|
|
ЦеллоБИОЗ8 |
|
|
||||
J ----- O |
|
|
|
|
|
1 ----- 0 |
....--- 0 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
3 |
|
|
|
|
|
|
|
|
|
ОН |
|
|
|
|
|
|
|
|
|
|
||
н |
|
ОН |
н |
н |
ОН |
н |
ОН |
|||||||||||
().а-о.Глюкопиранозиn- (1 - 2) -13-[).фРУКТОфуранозид |
0-13-D-rлюкопиранозил- (1 - |
4) -fj-o.r люкопираноза |
||||||||||||||||
|
|
|
|
|
Лактоза |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 ---- 0 |
J ----- О |
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
Рис. 14.13. Структура ряда важных дисахаридов. а- и 13- |
|||||||
|
|
|
|
|
|
|
|
|
|
|
форма различаются конфигурацией при аномерном aTo~e |
|||||||
|
|
|
|
|
|
|
|
|
|
|
углерода (отмечен звездочкой). Если в ГJ1ИКОЗИДНОЙ связи |
|||||||
|
|
|
|
|
|
|
|
|
|
|
участвует аномсрный углерод второго сахарного остатка, |
|||||||
|
|
|
|
|
|
|
|
|
|
|
этот остаток называют гликозидом (фураназидом или пи- |
|||||||
н |
|
|
он |
н |
|
|
ОН |
|
|
|
ранозидом). . |
|
|
|||||
Таблица 14.3. Дисахариды
Сахар ИСТОЧНИК Клиническое значение
Мальтоза |
Продукт распада крахмала (при переваривании |
|
|
амилазой или гидролизе). Проростки злаков, |
|
|
солод |
|
Лактоза |
Молоко. В период беременности может содержа |
При понижении активности лактазы усвоение лак |
|
ТЬСJl в моче |
тозы нарушается, что приводит к диарее и ме |
|
|
теоризму |
Сахароза |
Тростниковый и свекловичный сахар. Сорго, ана |
При понижении активности сахаразы усвоение са |
|
нас, морковь |
харозы нарушается, и в связи с этим наблю |
|
|
даЮТСJl диарея и метеоризм |
Трегалоза |
Грибы и дрожжи. Главный сахар в гемолимфе на |
|
секомых
148 |
Глава /4 |
Б
о
Рис. 14.14. Структура крахмала. А - амилоза с характерной для нее спиральной структурой; Б -- амилопектин. образую
щий в точках ветвления связи типа 1-6.
А
НАРУЖНЫЕ УЧАСТКИ
Б
I
~?H' o~~
.. |
СН2 |
О |
. 1 |
|
наСН2 |
а |
~----------------------------~ |
арн |
|
.. |
fH2 |
1 О |
R |
а |
|
I |
|
Рис. 14.15. Молекула гликогена. А ---:увеличенное изображение структуры в окрестности точки ветвления. Б-структура
молекулы. Цифрами обозначены участки, образующиеся на эквивалентных стадиях роста макромолекулы. R-первый остаток глюкозы. Обычно ветвление носит более разнообразный характер, чем 'Это показано на рисунке; отношение числа связей типа 1~4 к числу связей типа 1-6 колеб!JСТСЯ от 12 до 18

ФllЗllОllО?UЧt'СКll ва.ЖIlЫС уг.lевоОЫ
вид пищевых углеводов; он содержится в злаках, |
ХИТИН |
картофеле, бобовых и в других растениях. Двумя
Г:1аВНЫМИ компонентами крахмала являются амило
за (15-20%), имеющая неразветвленную спираль ную структуру (рис. 14.14), и амилопектин (80-85%),
образованный разветвленными цепями, каждая |
|
ветвь состоит из 24-30 остатков глюкозы, соеди |
|
ненных (l - 4)-связями [в точках ветвления остатки |
|
соединены (1 - 6)-связями]. |
~Дцетилглюкозамин |
Гликоген (рис. 14.15)-полисахарид, в виде кото |
|
149
n
~Дцетилглюкозамин
рого углеводы запасаются в организме животного.
Его часто называют животным крахмалом. Глико |
гиалуроновая кислота |
|
|
ген характеризуется более разветвленной структу |
HOCHz |
рой, чем амилопектин, линейные отрезки цепи вклю |
|
чают 11-18 остатков а-О-глюкопиранозы [соеди |
|
ненных u(l - 4)-гликозидными связями], В точках |
|
ветвления остатки соединены nО - 6)-гликозид |
'о |
ными связями.
Инулин - полисахарид, содержащийся в клубнях и корнях георгинов, артишоков и одуванчиков. При его гидролизе образуется фруктоза, следовательно он представляет собой фруктозан. Этот полисахарид в отличие от картофельного крахмала легко раство
ряется в теплой воде; его используют в физиологиче
ских исследованиях для определения скорости клу
бочковой фильтрации в почках.
Декстринами называют вещества, образующиеся при гидролизе крахмала. Название «остаточные дек стрины» получили продукты, образующиеся на
определенной стадии гидролиза.
Целлюлоза- главный компонент структурной основы растений. Она нерастворима в обычных ра створителях и состоит из а-О-глюкопиранозных зве
ньев, соединенных 13(1 - 4)-связями и образующих
длинные вытянутые цепи, стабилизированные попе речными водородными связями. Многие млекопи
нон
I3-Глюкуроновая ~Дцетилглюкозамин
кислота
Хондроитин-4-сульфат
(встречается также 6-сулЬфат)
n
I3-Глюкуроновая I"+Дцетилгалактоз
кислота аминеульфат
тающие, в том числе человек, не способны перевари
вать целлюлозу, так как их пищеварительная систе
ма не содержит гидролаз, расщепляющих Р-связи. Поэтому целлюлозу можно рассматривать как зна чительный неиспользуемый пищевой резерв. В ки
шечнике жвачных и других травоядных животных
имеются микроорганизмы, способные к фермента тивному расщеплению J3-связей, и для этих живот
ных целлюлоза является важным источником пище вых калорий.
Хитин- важный структурный полисахарид бес позвоночных. Из него, в частности, построен нару жный скелет ракообразных и насекомых. Структуру хитина составляют N-ацетил-О-глюкозаминовые
звенья, соединенные В (1 - 4)-гликозидными связями
(рис. 14.16).
Глнкозаминоглнканы (мукополисахариды) состо
ят из цепей сложных углеводов, содержащих амино
сахара и уроновые кислоты. Если эти цепи присоеди
нены к белковой молекуле, соответствующее соедине-
Гепарин
Н
'о
нNH.SO:J-
Сульфатированный СулЬфатированная n
глюкозамин |
идуроновая кислота |
Рис. 14.16. Структура некоторых СЛОЖНblХ полисах<tРJЩОR
ние называю,{ протеогликаном. Гликозамино
гликаны как основное скрепляющее вещество свя
заны со структурными компонентами, входящими в
состав костей, а также с эластином и коллагеном. Их функция состоит в удержании большой массы
воды и в заполнении межклеточного пространства.
Они служат смягчающим и смазочным материалом
для разного рода тканевых структур; выполнению
