
- •21. Основной закон релятивистской динамики.
- •22. Закон взаимосвязи массы и энергии покоя.
- •23. Частицы с нулевой массой.
- •24. Модель идеального газа. Уравнение состояния.
- •25. Основное уравнение мкт газов.
- •26. Давление газа на стенки сосудов.
- •27. Средняя кинетическая энергия поступательного движения молекул идеального газа.
- •28. Распределение Максвелла. Виды скоростей молекул и их физический смысл.
- •29. Распределение Больцмана. Барометрическая формула.
- •30. Закон равного распределения энергии по степеням свободы. Внутренняя энергия.
- •31. Первое начало термодинамики.
- •32. Работа газа при изменении его объёма.
- •33. Теплоёмкость газа.
- •34. Применение первого начала к изопроцессам.
- •35. Адиабатический процесс. Уравнение адиабаты (Пуассона). Коэффициент Пуассона.
- •Адиабата Пуассона
- •36. Политропические процессы. Уравнение политропы.
- •37. Понятие энтропии. Свойства энтропии. Второе начало термодинамики.
- •38. Изменение энтропии при обратимых и необратимых процессах.
- •39. Третье начало термодинамики (теорема Нернста).
- •40. Принцип работы тепловой машины. Кпд.
- •41. Цикл Карно. Теорема Карно.
- •42. Реальные газы. Уравнение Ван-дер-Ваальса.
- •43. Экспериментальные изотермы.
- •44. Фазовые переходы.
- •45. Строение твёрдых тел. Классификация кристаллов.
- •46. Физические типы кристаллических решёток.
- •47. Дефекты в кристаллах.
- •48. Теплоёмкость твёрдых тел.
- •49. Диаграмма состояния. Тройная точка.
- •50. Физическая кинетика. Явления переноса. Диффузия. Закон Фика.
- •51. Теплопроводность. Внутреннее трение (вязкость).
- •52. Диффузия, теплопроводность и вязкость газов.
- •53. Закон Кулона. Напряженность электрического поля. Принцип суперпозиции.
- •54. Поток вектора. Теорема Гаусса. Расчёт электростатических полей.
- •55. Работа сил электростатического поля.
- •56. Потенциал. Градиент потенциала. Циркуляция вектора. Эквипотенциальные поверхности.
38. Изменение энтропии при обратимых и необратимых процессах.
Изменение энтропии в результате обратимого процесса записывается:
∆S
=
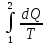 ,
где
,
где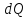 – теплота, передаваемая системе
при температуре Т.
– теплота, передаваемая системе
при температуре Т.
Изменение энтропии в результате необратимого процесса записывается:
dS
>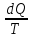
39. Третье начало термодинамики (теорема Нернста).
Третье начало термодинамики (теорема Нернста) — физический принцип, определяющий поведение энтропии при приближении температуры к абсолютному нулю.
Теорема
Нернста утверждает, что всякий
термодинамический процесс, протекающий
при фиксированной температуре T в сколь
угодно близкой к нулю, ![]() ,
не должен сопровождаться изменением энтропии S,
то есть изотерма
,
не должен сопровождаться изменением энтропии S,
то есть изотерма ![]() совпадает
с предельной адиабатой
совпадает
с предельной адиабатой ![]() .
.
40. Принцип работы тепловой машины. Кпд.
Всякий двигатель можно представить как систему, совершающую многократно круговой процесс (цикл). Пусть в ходе цикла рабочее вещество сначала расширяется до объёма V2, а потом сжимается до объёмаV1. Чтобы работа за цикл была положительной, давление в процессе расширения должно быть больше, чем при сжатии. Для этого рабочему веществу в ходе расширения нужно сообщать дополнительное количество энергииQ1. А при сжатии забирается энергияQ2. Совершая цикл, рабочее вещество возвращается в исходное состояние. Изменение внутренней энергииdU=0. Работа, совершаемая за цикл: А=Q1-Q2.
Периодически
действующий двигатель, совершающий
работу за счёт получаемого из вне тепла,
называется тепловой машиной. КПД такой
машины определяется, как отношение
работы к полученному из вне количеству
теплоты. ŋ=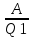
41. Цикл Карно. Теорема Карно.
Для работы теплового двигателя необходимо наличие двух тепловых резервуаров нагревателя с температурой Т1 и охладителя с температурой Т2, где Т1>Т2. Будем считать. Что теплоёмкость резервуаров бесконечна. Это значит, что отдача или забор теплоты не меняет его температуры.
Диаграмма цикла Карно.
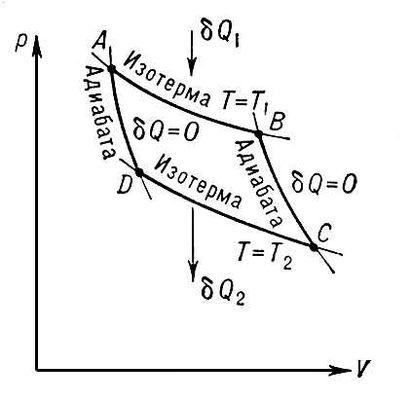
Найдём КПД цикла: совершив цикл, система возвращается в исходное состояние. Значит, полное изменение энтропии за цикл равно нулю. На участке АВ изменение энтропии равно Q1/T1. На участкеCD–Q2/T2. На участкеADи ВС изменение энтропии равно нулю.
Полное
изменение: ∆S=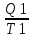 -
- = 0 ==>
= 0 ==>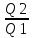 =
=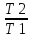
КПД тепловой
машины ŋ =
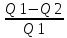
ŋ = 1-
ŋ = 1-
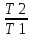
Это и есть запись КПД цикла Карно, откуда следует теорема Карно: КПД тепловой машины, работающей по циклу Карно, не зависит от состояния рабочего вещества и определяется только температурой нагревателя и охладителя.
42. Реальные газы. Уравнение Ван-дер-Ваальса.
Поведение реальных газов хорошо удовлетворяет модели идеального газа при уравнении Менделеева-Клапейрона только при малых плотностях. Малые плотности газа реализуются только при малых давлениях и высоких температурах. С ростом давления при постоянной температуре левая часть уравнения должна оставаться постоянной, однако при давлениях порядка в 100 атмосфер наблюдается заметное отклонение от равенства. Для описания поведения газа в широком интервале давлений и температур записывается уравнение Ван-дер-Ваальса:
![]()
где
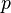 — давление,
— давление,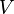 — молярный
объём,
— молярный
объём, —
абсолютная температура,
—
абсолютная температура,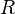 — универсальная
газовая постоянная.
— универсальная
газовая постоянная.
Коэффициенты aиb- есть константы Ван-дер-Ваальса, имеющие разные значения для различных газов.
Анализ
формулы показывает, что
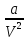 - есть добавка к внешнему давлению,
которое обусловлено взаимным притяжением
молекул друг к другу. Их взаимодействие
существенно на небольших расстояниях,
определяемыхRмолекулярного
действия.
- есть добавка к внешнему давлению,
которое обусловлено взаимным притяжением
молекул друг к другу. Их взаимодействие
существенно на небольших расстояниях,
определяемыхRмолекулярного
действия.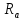 =
=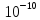 .
.
Коэффициент «b» определяет объём молекул в сосуде.
Внутренняя
энергия 1 моля газа: U
=
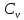 T
+
T
+
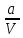
Уравнение Ван-дер-Ваальса представляет собой уравнение третьей степени относительно объёма. Это уравнение имеет три вещественных корня.
