
- •Вопрос 2,3. Конец
- •Вопрос 4.
- •Вопрос 4. Продолжение
- •Вопрос 4. Продолжение
- •Вопрос 4. Конец
- •Вопрос 6, 7.
- •Вопрос 6, 7. Конец
- •I. Реакции присоединения
- •Вопрос 10 продолжение1.
- •Вопрос 10 продолжение2.
- •Вопрос 10 конец.
- •Вопрос 12 продолжение1.
- •Вопрос 12 продолжение2.
- •Вопрос 15 конец.
- •Сложные эфиры
- •Вопрос 19 конец.
- •Вопрос 21 конец.
- •Вопрос 23 конец.
- •Вопрос 24 конец.
Вопрос 15 конец.
7) при взаимодействии кислот с основными оксидами и основаниями образуются соли (пропионат натрия):
СН3-СН2-COOH + NaOH -> СН3-СН2-COONa + Н2О.
Способы получения.
1. Окисление альдегидов и первичных спиртов — общий способ получения карбоновых кислот. В качестве окислителей применяются KМnО4 и K2Сr2О7.
|
|
[O] |
|
[O] |
|
|
R-CH2-OH |
→ |
R-CH=O |
→ |
R-CO-OH |
|
Спирт |
альдегид |
Кислота | ||
2. Гидролиз галогензамещенных углеводородов, содержащих, три атома галогена у одного атома углерода. При этом образуются спирты, содержащие группы ОН у одного атома углерода — такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:
|
|
ЗNаОН |
|
|
|
|
R-CCl3 |
→ |
[R-C(OH)3] |
→ |
R-COOH + Н2О |
|
|
-3NaCl |
|
|
|
3. Получение карбоновых кислот из цианидов (нитрилов) СН3-Вr + NaCN → CH3 - CN + NaBr. Образующийся нитрил уксусной кислоты (метилцианид) при нагревании легко гидролизуется с образованием ацетата аммония: CH3CN + 2Н2О → CH3COONH4. При подкислении раствора выделяется кислота: CH3COONH4 + HCl → СН3СООН + NH4Cl. 5. Гидролиз сложных эфиров 6. Гидролиз ангидридов кислот
Вопрос№16 Простые эфиры Простыми эфирами называют производные спиртов, образованные в результате замещения водорода гидроксильной группы спирта на углеводородный остаток. Эти соединения можно рассматривать и как производные воды, в молекуле которой углеводородными остатками замещены оба атома водорода:
R—O—H H—O—H R—O—R
Спирт вода простой эфир
Простые эфиры рассматриваются как производные спиртов. Названия этих соединений состоят из названий радикалов и слова эфир (название класса). Для симметричных эфиров ROR используется приставка ди перед названием радикала, а в названиях несимметричных эфиров ROR' радикалы указываются в алфавитном порядке. Например, CH3OCH3 – диметиловый эфир; C2H5OCH3 – метилэтиловый эфир[2].
Сложные эфиры
Сложные эфиры — производные кислот, у которых кислотный водород заменён на алкильные (или вообще углеводородные) радикалы Среди сложных эфиров особое место занимают природные эфиры — жиры и масла,
Способы получения эфиров
Простые эфиры
Простые эфиры в природе не встречаются. Их получают синтетическим путем.
1. Взаимодействием галогеналкилов с алкоголятами (синтез Вильямсона):
2. Дегидратацией спиртов под влиянием минеральных кислот (например, серной):
Сложные эфиры
Реакция этерификации — взаимодействие кислоты и спирта в присутствии минеральной кислоты. Механизм реакции этерификации можно представить в таком виде:
Кислород карбонильной группы, присоединяя протон минеральной кислоты(катализатор), образует карбониевый ион (I), который подвергается нуклеофильной атаке молекулой спирта. В результате этого образуется неустойчивый промежуточный комплекс (II), распадающийся сразу же с выделением молекулы воды. Возникший карбкатион сложного эфира (III), отщепляя протон, дает сложный эфир (IV).
Реакция этерификации обратима. Скорость этой реакции зависит от строения кислот и спиртов. При одной и той же кислоте скорость этерификации первичных спиртов в два раза выше, чем вторичных, и во много раз выше, чем третичных.
Взаимодействие ангидридов кислот со спиртами:
Взаимодействие галоидангидридов кислот со спиртами.
Вопрос№17 Жиры — это смесь сложных эфиров глицерина и высших жирных кислот (ВЖК). Классификация Чем больше в жирах содержание ненасыщенных кислот, тем ниже температура плавления жиров.
|
Агрегатное состояние жиров |
Различия в химическом строении |
Происхождение жиров |
Исключения |
|
Твёрдые жиры |
Содержат остатки насыщенных ВКК |
Животные жиры |
Рыбий жир(жидк. при н/у) |
|
Смешаные жиры |
Содержат остатки насыщенных и ненасыщенных ВКК | ||
|
Жидкие жиры(масла) |
Содержат остатки ненасыщенных ВКК |
Растительные жиры |
Кокосовое масло, какао масло(твёрд. при н/у) |
Номенклатура
По
тривиальной номенклатуре глицериды
называют, добавляя окончание -ид к
сокращенному названию кислоты и
приставку, показывающую, сколько
гидроксильных групп в молекуле глицерина
проэтерифицировано.
Химические
свойства жиров
1. Гидролиз, или омыление,
жиров происходит под
действием воды, с участием ферментов
или кислотных катализаторов(обратимо)
, при
этом образуются спирт - глицерин и смесь
карбоновых кислот: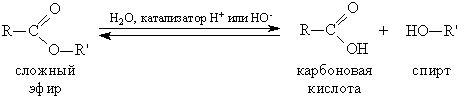 или
щелочей (необратимо). При
щелочном гидролизе образуются соли
высших жирных кислот, называемые мылами. Мыла
получаются при гидролизе жиров в
присутствии щелочей:
или
щелочей (необратимо). При
щелочном гидролизе образуются соли
высших жирных кислот, называемые мылами. Мыла
получаются при гидролизе жиров в
присутствии щелочей: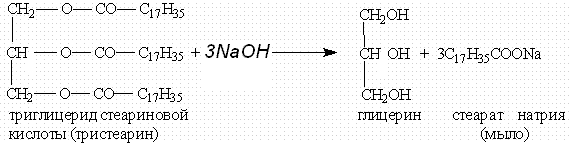 Мыла
—
это
калиевые и натриевые соли высших
карбоновых кислот.
2.Гидрирование
жиров –
превращение
жидких растительных масел в твердые
жиры –
имеет
большое значение для пищевых целей. Продукт
гидрогенизации масел –
твердый
жир (искусственное сало, саломас). Маргарин –
пищевой
жир, состоит из смеси гидрогенизированных
масел (подсолнечного, кукурузного,
хлопкого и др.), животных жиров, молока
и вкусовых добавок (соли, сахара,
витаминов и др.).
Так
в промышленности получают маргарин:
Мыла
—
это
калиевые и натриевые соли высших
карбоновых кислот.
2.Гидрирование
жиров –
превращение
жидких растительных масел в твердые
жиры –
имеет
большое значение для пищевых целей. Продукт
гидрогенизации масел –
твердый
жир (искусственное сало, саломас). Маргарин –
пищевой
жир, состоит из смеси гидрогенизированных
масел (подсолнечного, кукурузного,
хлопкого и др.), животных жиров, молока
и вкусовых добавок (соли, сахара,
витаминов и др.).
Так
в промышленности получают маргарин: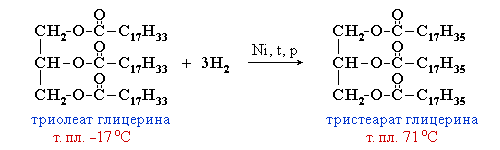
Вопрос №18. Углеводы содержатся в клетках растительных и животных организмов и по массе составляют основную часть органического вещества на Земле. Эти соединения образуются растениями в процессе фотосинтеза из углекислого газа и воды. Строение углеводов
По своему строению углеводы являются многоатомными спиртами с альдегидной или кетоновой группой (полигидроксиальдегиды и полигидроксикетоны). Наиболее известные углеводы (крахмал, глюкоза, гликоген) обладают эмпирической формулой (CH2O)6. Другие представителя класса не соответствуют данному соотношению, и даже могут включать атомы азота, серы, фосфора.
Классификация углеводов
По способности к гидролизу углеводы делятся на простые — моносахариды и сложные — полисахариды.
Применение. 1.Пищевая промышленность( сахар, хлеба – булочные изделия,картофель,для диабетического питания) 2. В медицине.( растворы глюкозы ,витаминные сиропы, оболочка таблеток ,лекарственные препараты) 3. Сельскохозяйственные корма. 4. Биотехнология и микробиология. 5.Химическая промышленность(множество продуктов, в том числе на основе целлюлозы) 6. Строительство(древесина,клея,обои,краски) 7.Топливо
Вопрос №19.
Моносахариды- органические соединения, одна из основных групп углеводов; самая простая форма сахара; являются обычно бесцветными, растворимыми в воде, прозрачными твердыми веществами. Некоторые моносахариды обладают сладким вкусом. Химические свойства. Для моносахаридов характерны реакции, свойственные спиртам, альдегидам и кетонам.При взаимодействии моносахаридов с различными веществами реакции могут протекать: по карбонильной группе, гидроксильным группам либо с изменением углеродного скелета молекулы. 1. Альдегидная группа моносахаридов окисляется до карбоксильной группы с образованием альдоновых кислот. 2. При нагревании моносахаридов с концентрированными кислотами происходит дегидратация молекулы. Из пентоз образуется фурфурол, из гексоз – оксиметилфурфурол:
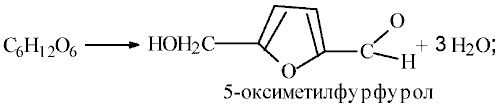
3. Моносахариды
D-ряда (глюкоза, фруктоза, манноза)
расщепляются при каталитическом
действии ферментов дрожжей.
Способы
получения.
1.
Гидролиз ди- и полисахаридов,
который происходит под действием кислот
или ферментов, водные растворы щелочей
не способствуют гидролизу:
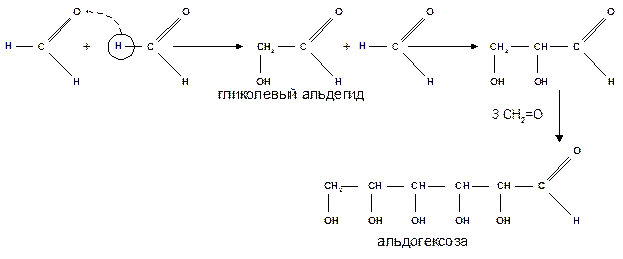
2.Альдольная
конденсация формальдегида –
первый
синтез сахаров был произведен еще А.М.
Бутлеровым, в качестве катализатора
используют гидроксид кальция
 3.
Метод укорачивания цепи основан
на окислении моносахаридов, содержащих
на один атом углерода больше, чем в
нужном моносахариде. Например, при
окислении альдогексозы H2O2 в
присутствии ацетата железа(III) образуется
альдоновая кислота, которая затем
декарбоксилируется с
3.
Метод укорачивания цепи основан
на окислении моносахаридов, содержащих
на один атом углерода больше, чем в
нужном моносахариде. Например, при
окислении альдогексозы H2O2 в
присутствии ацетата железа(III) образуется
альдоновая кислота, которая затем
декарбоксилируется с
