
- •Качественные реакции обнаружения катионов.
- •Определение растворимости лекарственных веществ
- •2. Определение температуры плавления лекарственных веществ
- •Методика определения.
- •3. Определение кислотности или щелочности растворов лекарственных препаратов
- •4. Определение рН раствора лекарственного препарата колориметрическим методом
- •1. Приготовление эталонных растворов
- •Натрия гидрокарбонат
- •Натрия сульфат
- •Тема 4: определение качества воды очищенной, воды для инъекций, кислорода, перекисных соединений Вопросы для самоконтроля
- •Раствор водорода перекиси
- •Магния перекись
- •Таблетки гидроперита
- •Вода очищенная (фс)
- •Вода для инъекций (фс).
- •Образец оформления протокола анализа качества неорганического лекарственного средства.
- •Тема 5: определение качества натрия тиосульфата, натрия нитрита, натрия гидрокарбоната, лития карбоната. Вопросы для самоконтроля
- •Натрия тиосульфат
- •Натрия гидрокарбонат
- •Натрия нитрит
- •Лития карбонат
- •Тема 6: определение качества лекарственных средств из группы производных галогенов Вопросы для самоконтроля
- •Йод (растворы йода спиртовые)
- •Натрия иодид
- •Калия иодид
- •Натрия фторид
- •Раствор кальция хлорида
- •Магния оксид
- •Магния сульфат
- •Цинка оксид
- •Цинка сульфат
- •Бария сульфат для рентгеноскопии
- •Тема 8: определение качества лекарственных средств из группы соединений бора, висмута, алюминия, железа, меди и серебра Вопросы для самоконтроля
- •Кислота борная
- •Натрия тетраборат
- •Висмута нитрат основной
- •Алюминия гидроксид
- •Алюминия фосфат
- •Железа сульфат
- •Серебра нитрат
- •Меди сульфат
- •Тема 9: функциональный анализ органических лекарственных веществ Блок информации
- •Идентификация спиртового гидроксила
- •Реакции окисления (индофеноловая проба)
- •Реакции конденсации с альдегидами
- •Сочетание с солями диазония
- •Реакции замещения (с бромной водой и азотной кислотой)
- •Идентификация кето-группы
- •Идентификация гидроксиацетильной группы
- •Идентификация карбоксильной группы
- •Идентификациясложноэфирнойгруппы
- •Реакция кислотного или щелочного гидролиза
- •Гидроксамовая проба
- •Идентификация простой эфирной группы
- •Идентификация первичной ароматической аминогруппы
- •Реакция образования азокрасителя
- •Реакции окисления
- •Реакции конденсации с альдегидами
- •Идентификация первичной алифатической аминогруппы
- •Идентификация вторичной аминогруппы
- •Идентификация третичной аминогруппы
- •Идентификация амиднои и n-замещенной амидной группы
- •Идентификация гидразидной группы
- •Идентификация ароматической нитрогруппы
- •Идентификация сульфгидрильной группы
- •Идентификация сульфамидной группы
- •Реакция образования солей с тяжелыми металлами
- •Реакция минерализации
- •Идентификация соединений, содержащих двойную связь
- •Реакция с уксусным ангидридом
- •Тема 10: определение качества лекарственных средств из группы спиртов, альдегидов, их производных и углеводов Вопросы для самоконтроля
- •Раствор формальдегида
- •Гексаметилентетрамин
- •Хлоралгидрат
- •Спирт этиловый (гф х)
- •Глюкоза
- •Сахароза
- •Лактоза
- •Галактоза
- •Крахмал
- •Образец оформления протокола анализа качества органического лекарственного средства.
- •Тема 11: определение качества лекарственных средств из группы карбоновых кислот Вопросы для самоконтроля
- •Калия ацетат
- •Кальция лактат
- •Кальция глюконат
- •Натрия цитрат для инъекций
- •Натрия вальпроат
- •Тема 12: определение качества лекарственных средств производных лактонов ненасыщенных полигидроксикислот, статинов, кислоты дитиокарбаминовой и аминокислот Вопросы для самоконтроля
- •Кислота аскорбиновая
- •Таблетки «тетурам»
- •Кислота глутаминовая
- •Кислота аминомасляная (аминалон)
- •Цистеин
- •Ацетилцистеин
- •Метионин
- •Пеницилламин
- •Раствор тетацина-калыция (натрия кальция эдетата) 10% для инъекций
- •Кислота аминокапроновая
- •Каптоприл
- •Образец оформления протокола анализа качества неизвестного лекарственного вещества.
- •Тема 13. Определение качества лекарственных средств из группы бета-лактамидов: пенициллинов, цефалоспоринов, ингибиторов бета-лактамаз Вопросы для самоконтроля
- •Общие реакции определения подлинности лекарственных средств из группы бета-лактамидов
- •1. Гидроксамовая реакция
- •2. Образование комплексных солей
- •3. Взаимодействие с реактивом Марки
- •4. Реакция обнаружения серы
- •Ампициллина тригидрат
- •Тема 1: определение качества лекарственных средств группы терпенов Вопросы для самоконтроля:
- •Терпингидрат
- •Валидол
- •Камфора
- •Бромкамфора
- •Масляный раствор ретинола ацетата (3,44%; 6,88%; 8,60%)
- •Раствор сульфокамфокаина 10% для инъекций
- •Тема 2: определение качества лекарственных средств,
- •Производных циклопентанопергидрофенантрена:
- •Витаминов группы d, карденолидов, аминостероидных миорелаксантов.
- •Вопросы для самоконтроля.
- •Масляный раствор эргокальциферола
- •Строфантин к
- •Таблетки дигитоксина
- •Таблетки дигоксина.
- •Раствор коргликона 0,06% для инъекций
- •Тема 3: определение качества лекарственных средств из группы кортикостероидов. Вопросы для самоконтроля
- •Таблетки дезоксикортикостерона ацетата
- •Раствор дезоксикортикостерона ацетата в масле для инъекций
- •Таблетки кортизона ацетата
- •Таблетки преднизолона
- •Мазь флуоцинолона ацетонида
- •Тема 4: определение качества лекарственных средств из группы производных циклопентанопергидрофенантрена: андрогенов и анаболиков; антиандрогенов. Вопросы для самоконтроля
- •Раствор тестостерона пропионата в масле
- •Таблетки метилтестостерона
- •Таблетки метиландростендиола
- •Таблетки метандростенолона
- •Раствор нандролона деканоата (ретаболила) для инъекций или раствор нандролона фенилпропионата (феноболина) для инъекций.
- •Таблетки ципротерона ацетата (андрокур) по 0,05 г.
- •Тема 5: определение качества лекарственных средств,
- •Производных циклопентанопергидрофенантрена:
- •Эстрогенов и гестагенов, антиэстрогенов.
- •Вопросы для самоконтроля
- •Эстрадиола гемигидрат
- •Таблетки этинилэстрадиола
- •Идентификация эстрогенов методом тсх
- •Прогестерон
- •Раствор прогестерона для инъекций.
- •Таблетки норэтистерона (норколут)
- •Суспензия медроксипрогестерона ацетата для инъекций (депо-провера)
- •Таблетки тамоксифена цитрата
- •Тема 6: определение качества лекарственных средств из группы производных фенола. Вопросы для самоконтроля
- •Резорцин
- •Таблетки синэстрола
- •Таблетки диэтилстильбэстрола
- •Тема 7: определение качества лекарственных средств из группы производных хинонов и тетрациклинов Вопросы для самоконтроля
- •Раствор витамина к, для инъекций. (раствор фитоменадиона для инъекций)
- •Таблетки витамина к (фитоменадиона)
- •Раствор викасола 1% для инъекций
- •Таблетки викасола (по 0,015 г)
- •Таблетки тетрациклина или тетрациклина гидрохлорида
- •Таблетки окситетрациклина или окситетрациклина гидрохлорида
- •Таблетки или капсулы доксициклина гидрохлорида
- •Таблетки или капсулы метациклина гидрохлорида
- •Тема 8: определение качества лекарственных средств из группы производных пара- и мета-аминофенола, диалкиламиноацетанилида, ароматических кислот и их солей Вопросы для самоконтроля
- •Парацетамол
- •Таблетки парацетамола
- •Прозерин (неостигмина метилсульфат)
- •Раствор прозерина 0,05% для инъекций
- •Раствор лидокаина гидрохлорида (ксикаина) для инъекций
- •Кислота бензойная
- •Кислота салициловая
- •Натрия бензоат
- •Натрия салицилат
- •Тема 9: определение качества лекарственных средств, производных салициловой, фенилуксусной, фенилпропионовой кислот и бутирофенона. Вопросы для самоконтроля.
- •Оксафенамид
- •Таблетки оксафенамида
- •Кислота ацетилсалициловая
- •Таблетки кислоты ацетилсалициловой
- •Натрия пара-аминосалицилат
- •Ибупрофен
- •Таблетки ибупрофена
- •Диклофенак-натрий
- •Галоперидол
- •Раствор галоперидола для инъекций
- •Тема 10: определение качества лекарственных средств, производных пара-аминобензойной кислоты и близких по структуре местных анестетиков. Вопросы для самоконтроля.
- •Бупивакаина гидрохлорид
- •Раствор бупивакаина гидрохлорида для инъекций
- •Анестезин
- •Новокаин
- •Раствор новокаина для инъекций
- •Новокаинамид
- •Метоклопрамида гидрохлорид
- •Раствор метоклопрамида для инъекций
- •Таблетки метоклопрамида
- •Раствор артикаина гидрохлоридл для инъекций
- •Тема 11: определение качества лекарственных средств из группы арилалкиламинов гидроксифенилалкиламинов и их производных. (занятие 1) Вопросы для самоконтроля
- •Допамина гидрохлорид
- •Раствор адреналина гидрохлорида 0,1 % или адреналина гидротартрата 0,18% для инъекций
- •Раствор норадреналина гидротартрата 0,2% для инъекций
- •Раствор изопреналина гидрохлорида (изадрина) для инъекций
- •Фенотерола гидробромид
- •Аэрозоль сальбутамола
- •Таблетки верапамила гидрохлорида.
- •Таблетки леводопы
- •Таблетки метилдопы
- •Тема 12: определение качества лекарственных средств из группы арилалкиламинов, гидроксифенилалкиламинов и их производных. (занятие 2). Вопросы для самоконтроля
- •Эфедрина гидрохлорид
- •Таблетки эфедрина гидрохлорида
- •Таблетки анаприлина
- •Таблетки атенолола
- •Таблетки тимолола
- •Левомицетин
- •Таблетки левомицетина стеарата
- •Левомицетина сукцинат растворимый
- •Таблетки бромгексина
- •Таблетки амброксола
- •Общие реакции идентификации сульфаниламидных препаратов
- •Частные реакции идентификаци сульфаниламидных препаратов
- •Раствор сульфацила-натрия 10%, 20% или 30%
- •Таблетки «ко-тримоксазол»
- •Таблетки фуросемида
- •Таблетки дихлотиазида
- •Таблетки карбутамида
- •Таблетки глибенкламида
- •Таблетки метформина
- •Тема: анализ лекарственных средств производных фурана производные 5-нитрофурана Вопросы для самоконтроля
- •Рекомендуемая литература
- •Гризеофульвин
- •Амиодарон
- •Тема: анализ лекарственных средств, производных бензопиранаи индана Вопросы для самоконтроля
- •Рекомендуемая литература
- •Токоферола ацетат
- •Таблетки неодикумарина
- •Фенилин
- •Тема: анализ лекарственных средств, производных бензопирана и тиофена Вопросы для самоконтроля
- •Рекомендуемая литература
- •Рутин, кверцетин
- •Дигидрокверцетин
- •Кромолин натрия (интал)
- •Тема: анализ лекарственных средств, производных пиррола Вопросы для самоконтроля
- •Рекомендуемая литература
- •Пирацетам
- •Линкомицин и клиндамицин
- •Тема: анализ лекарственных средств, производных индола Вопросы для самоконтроля
- •Рекомендуемая литература
- •Резерпин
- •Индометацин
- •Таблетки индометацина по 0,025 г
- •Таблетки винпоцетина по 0,005 г
- •Арбидол
- •Тема: анализ лекарственных средств, производных пиразола, тиазола и 1,2,4-триазола Вопросы для самоконтроля
- •Рекомендуемая литература
- •Антипирин
- •Анальгин
- •Бутадион
- •Пропифеназон
- •Тема: анализ лекарственных средств, производных имидазола (1) Вопросы для самоконтроля
- •Рекомендуемая литература
- •Пилокарпина гидрохлорид
- •Метронидазол
- •Тема: анализ лекарственных средств, производных имидазола (2) Вопросы для самоконтроля
- •Рекомендуемая литература
- •Дибазол
- •Нафтизин
- •Ксилометазолин (галазолин)
- •Дибазол (таблетки по 0,02 г и растворах 1% и 2% для инъекций)
- •Тема: анализ лекарственных средств, производных пиперидина и пиперазииа Вопросы для самоконтроля
- •Рекомендуемая литература
- •Фентанил
- •Циннаризин
- •Циклодол
- •Циннаризин в таблетках по 0,025 г
- •Тема: анализ лекарственных средств, производных тропана Вопросы для самоконтроля
- •Рекомендуемая литература
- •Атропина сульфат
- •Тропацин
- •Гоматропина гидробромид, скополамина гидробромид
- •Тема: анализ лекарственных средств, производных пиридина Вопросы для самоконтроля
- •Рекомендуемая литература
- •Пиридоксина гидрохлорид
- •Пиридоксальфосфат
- •Пармидин
- •Тема: анализ лекарственных средств, производных дигидропиридина и пиридин-з-карбоновой кислоты Вопросы для самоконтроля
- •Рекомендуемая литература
- •Никотиновая кислота
- •Никотинамид
- •Диэтиламид никотиновой кислоты
- •Пикамилон
- •Тема: анализ лекарственных средств, производных пиридин-4-карбоновой кислоты Вопросы для самоконтроля
- •Рекомендуемая литература
- •Изониазид
- •Фтивазид
- •Ниаламид
- •Рекомендуемая литература
- •Хингамин
- •Тема: анализ лекарственных средств, производных хинолина, фторхинолона и хиназолина Вопросы для самоконтроля
- •Рекомендуемая литература
- •Нитроксолин
- •Ломефлоксацина гидрохлорид
- •Гранулы хлорхинальдола (0,06 г в 1г) .
- •Тема: анализ лекарственных средств, производных изохинолина Вопросы для самоконтроля
- •Рекомендуемая литература
- •Папаверина гидрохлорид
- •Тема: анализ лекарственных средств, производных пиримидина Вопросы для самоконтроля
- •Рекомендуемая литература
- •Метилурацил
- •Гексамидин
- •Фторафур
- •Зидовудин
- •Тема: анализ лекарственных средств, производных пиримидина, гидантоина и 1,2-бензотиазина Вопросы для самоконтроля
- •Рекомендуемая литература
- •Общегрупповые реакции
- •Барбитал
- •Фенобарбитал
- •Тиопентал-натрий
- •Дифенин
- •Пироксикам
- •Барбитал, фенобарбитал и бензонал
- •Гексенал
- •Тема: анализ лекарственных средств, производных пиримидино-тиазола Вопросы для самоконтроля
- •Рекомендуемая литература
- •Тиамина бромид или тиамина хлорид
- •Фосфотиамин
- •Тема: анализ лекарственных средств производных ксантина Вопросы для самоконтроля
- •Рекомендуемая литература
- •Теобромин
- •Теофиллин
- •Эуфиллин
- •Темисал
- •Пентоксифиллин
- •Тема: анализ лекарственных средств, производных пурина Вопросы для самоконтроля
- •Рекомендуемая литература
- •Аллопуринол
- •Меркаптопурин
- •Азатиоприн
- •Рибоксин
- •Анализ ацикловира в таблетках 0,2 или 0,4
- •Тема: анализ лекарственных средств, производных птеридина Вопросы для самоконтроля
- •Рекомендуемая литература
- •Фолиевая кислота
- •Рибофлавин
- •Рибофлавина мононуклеотид
- •Рекомендуемая литература
- •Аминазин
- •Тема: анализ лекарственных средств, производных бензодиазепина Вопросы для самоконтроля
- •Рекомендуемая литература
- •Количественное определение оксазепама в таблетках
- •Анализ раствора сибазона (диазепам) 2% для инъекций
- •Анализ нитразепама в таблетках
- •Мезапам
- •Алпразолам
- •Тема: анализ лекарственных средств, производных 1,5-дибензодиазепина, бензотиазепина, иминостильбена, 10,11-дигидродибензоциклогептена Вопросы для самоконтроля
- •Рекомендуемая литература
- •Таблетки азалептина 0,025 и 0,1
- •Амитриптилина гидрохлорид
- •Карбамазепин
- •Тема: титрованные растворы. Установка титра и поправочного коэффициента.
- •Вопросы для самоконтроля
- •Рекомендуемая литература
- •Тема: использование метода неводного титрования в анализе лекарственных средств
- •Вопросы для самоконтроля
- •Рекомендуемая литература
- •Тема: анализ сложных лекарственных форм с использованием рефрактометрии
- •Вопросы для самоконтроля
- •Рекомендуемая литература
- •Методики анализа лекарственных форм с использованием рефрактометрии
- •Количественное определение
- •Тема: применение рефрактометрии для определения концентрации спирта в спиртовых лекарственных формах
- •Вопросы для самоконтроля
- •Рекомендуемая литература
- •Методики анализа водно-спиртовых растворов
- •Раствор кислоты борной спиртовой 0,5;1,0;2,0 и 3,0% фс 42-1512-99
- •Литература:
- •Тема: анализ лекарственных форм с применением условного и среднего ориентировочного титров
- •Титр средний ориентировочный (суммарный)
- •Титр условный
- •Рекомендации, которые следует соблюдать при аналитических расчетах:
Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
БЕЛГОРОДСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
Фармацевтический факультет
Кафедра фармацевтической химии и фармакогнозии
МЕТОДИЧЕСКИЕ УКАЗАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ И ВЫПОЛНЕНИЯ ЛАБОРАТОРНО-ПРАКТИЧЕСКИХ РАБОТ ПО ФАРМАЦЕВТИЧЕСКОЙ ХИМИИ
Для студентов 3 - 5 курсов специальности «Фармация»
Белгород - 2009
TЕMA 1: ТЕХНИКА БЕЗОПАСНОСТИ РАБОТА С НОРМАТИВНОЙ ДОКУМЕНТАЦИЕЙ, УЧЕБНИКАМИ, ПРАКТИКУМАМИ, УЧЕБНЫМИ ПОСОБИЯМИ КАФЕДРЫ, СПРАВОЧНИКАМИ. ПОРЯДОК ОФОРМЛЕНИЯ РАБОТ. ОБЩИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ КАЧЕСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ НЕОРГАНИЧЕСКОГО ПРОИСХОЖДЕНИЯ: ИСПЫТАНИЕ НА ПОДЛИННОСТЬ.
Вопросы для самоконтроля
1. Основные правила техники безопасности при работе в химической лаборатории.
2. Основные приемы оказания первой медицинской помощи при химических, термических ожогах, поражениях электротоком, порезах, ингаляционных воздействиях токсикантов.
3. Фармацевтическая химия как наука, фармацевтическая терминология: лекарственное средство, лекарственная форма, лекарственный препарат.
4. Структура Государственной фармакопеи XиXIизданий, их значение для оценки качества лекарственных средств.
5. Нормативная документация (НД), фармакопейные статьи предприятий (ФСП), регламентирующие качество лекарственных средств.
6. Опишите пробы и реакции идентификации катионов калия, натрия, аммония, магния, кальция, железа, цинка, свинца, висмута, ртути, серебра, меди (реактивы, условия, эффекты реакций). Напишите соответствующие уравнения химических реакций.
7. Опишите реакции идентификации анионов: хлоридов, бромидов, иодидов, сульфатов, фосфатов, нитритов, нитратов, боратов, карбонатов и гидрокарбонатов (реактивы, условия, эффекты реакций). Напишите соответствующие уравнения химических реакций.
БЛОК ИНФОРМАЦИИ
Среди лекарственных веществ встречаются соединения, водные растворы которых являются электролитами (кислоты, основания, соли). Основными свойствами электролитов (в отличие от неэлектролитов) является их способность вступать в реакции двойного обмена с другими электролитами. Такие реакции протекают быстро, и части молекул, которыми обмениваются при этих реакциях электролиты, реагируют независимо одна от другой. В реакцию как бы вступают части молекул, которые образуют продукт реакции с определённой частью молекулы реагента. Например, при прибавлении к раствору бариевой соли (хлорида, нитрата, ацетата) раствора любой сернокислой соли образуется один и тот же продукт – сульфат бария:
Ba(NO3)2 + Na2SO4 BaSO4 + 2NaNO3
BaCl2+Na2SO4BaSO4+ 2NaCl
Ba(CH3COO)2+Na2SO4BaSO4+ 2CH3COONa
Эти реакции объясняются тем, что молекулы химических соединений, растворы которых способны проводить электрический ток, во время растворения вещества распадаются на ионы (электролитическая диссоциация).
Большая часть кислот, оснований и солей являются ионогенными, и реакции электролитов представляют реакции ионогенного типа.
Анализ минеральных веществ основывается на реакциях отдельных ионов. В результате этих реакций возможны следующие случаи:
Образование недиссоциированного соединения в виде осадка:
Са2++ С2О4СаС2О4
Образование малодиссоциированного соединения с появлением характерного окрашивания:
Fe3+ + 3(SCN)- Fe(SCN)3
Выделение недиссоциированного газообразного вещества, распознаваемого по характерным признакам (цвет, запах):
SO32- + 2H+ H2O + SO2
Образование малодиссоциированного комплексного соединения:
Ag+ + 2(CN)- [Ag(CN)2]-
Качественные реакции обнаружения катионов.
КАЛИЙ
1. Окрашивание пламени. Соли щелочных и щелочноземельных металлов окрашивают пламя горелки. Это объясняется их восстановлением в пламени горелки до нейтральных атомов, малым потенциалом ионизации s1– электрона и его способностью легко возбуждаться и переходить на возбуждённые уровни. При обратном переходе электрон испускает квант света.
При внесении солей, содержащих ионы калия в приветное пламя горелки, происходит окрашивание пламени в фиолетовый цвет.
2. К 2 мл раствора KClприбавляют 1 мл раствора винной кислоты и 1 мл раствора натрия ацетата. При охлаждении и потирании стеклянной палочкой о стенки пробирки выпадает белый кристаллический осадок.
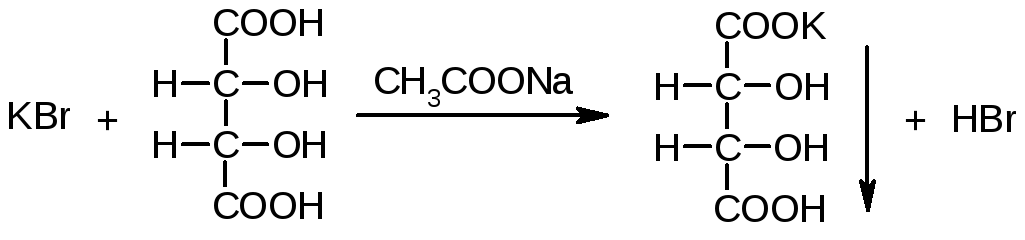
Осадок растворим в кислотах (образование винной кислоты) и в щелочах (образование средних солей). Образование осадка может быть ускорено добавлением спирта или уксусной кислоты.
НАТРИЙ
Окрашивание пламени. Бесцветное пламя горелки окрашивается солями натрия в желтый цвет.
АММОНИЙ
1. Разложение при нагревании. К 3 каплям раствора аммония хлорида прибавляют 4 капли раствора натрия гидроксида и осторожно нагревают. Выделяется аммиак, обнаруживаемый по запаху или по посинению красной лакмусовой бумажки.
NH4++NaOHNH3+Na++H2O
2. К 3 каплям раствора хлорида аммония прибавляют 2 - 3 капли реактива Несслера - появляется осадок красно-бурого цвета или желто-бурое окрашивание.

МАГНИЙ
1. К 1 мл раствора соли магния прибавляют 1 мл раствора аммиака и хлорида аммония и по каплям раствор натрия гидрофосфата. Выпадает белый кристаллический осадок.
Mg2++PO43– +NH4+NH4MgPO4
белый
Реакцию проводят в присутствии аммония хлорида во избежание выпадения в щелочной среде осадка Mg(OH)2. ПрисутствиеNH4Clпрепятствует выпадению такого осадка вследствие связыванияOH-- иона аммоний-ионами. При большом избыткеNH4Clосаждение магний-аммоний фосфата не наступает, потому что образуются комплексные ионы трихлормагния и тетрахлормагния.
2. К 1 мл раствора соли магния прибавляют по каплям раствор 8-оксихинолина - появляется зеленовато-желтый осадок оксихинолята магния.
КАЛЬЦИЙ
1. К раствору препарата прибавляют 1 мл раствора аммония оксалата. Образуется белый осадок.
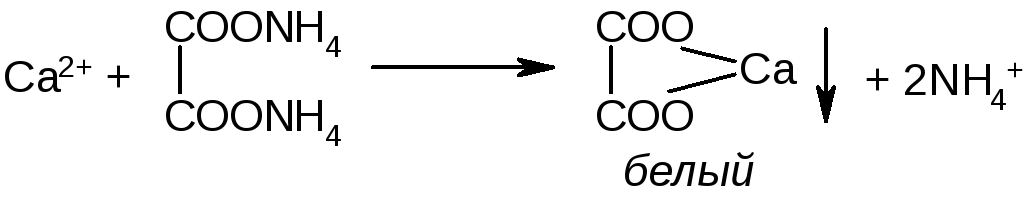
Осадок нерастворим в уксусной кислоте (отличие от оксалатов бария и стронция) и растворе аммиака, растворим в растворах сильных кислот (образование щавелевой кислоты). Реакцию лучше проводить в слабокислой среде (рН = 6,0 – 6,5).
ЦИНК
1. К 2 мл раствора соли цинка прибавляют 0,5 мл раствора натрия сульфида образуется осадок белого цвета, нерастворимый в уксусной кислоте и растворимый в разведённой хлороводородной кислоте:
Zn2++S2– ZnS
белый
ZnS+ 2HClZnCl2+ Н2S
2. К 2 мл раствора соли цинка прибавляют 0,5 мл кислого раствора калия ферроцианида - образуется белый студенистый осадок, нерастворимый в разведённой соляной кислоте:
Zn2++K4[Fe(CN)6]K2Zn[Fe(CN)6]+ 2K+
белый
СВИНЕЦ
1. К 1 мл раствора соли свинца прибавляют -4-5 капель раствора калия иодида, выпадает желтый осадок, растворимый в избытке реактива с образованием бесцветного комплекса. PbI2растворим в горячей воде и в уксусной кислоте. При охлаждении раствора выпадает осадок в виде золотых чешуек.
2. К 3 каплям раствора соли свинца прибавляют несколько капель раствора натрия сульфида, образуется черный осадок.
СЕРЕБРО
1. К раствору серебра нитрата прибавляют раствор аммиака (до растворения образующегося осадка), 2 - 3 капли формалина и нагревают. На стенках пробирки образуется налет металлического серебра (реакция «серебряного зеркала»).
2. Ионы серебра образуют осадки с хлоридами, бромидами, иодидами. Образующиеся галогениды различают по растворимости в растворе аммиака. К 1 мл раствора соли серебра прибавляют 2 - 3 капли раствора натрия хлорида или разведенной кислоты хлороводородной - образуется белый творожистый осадок, растворимый в растворе аммиака, с образованием бесцветного комплексного соединения хлорида диамминсеребра:
AgCl+ 2NH3[Ag(NH3)2]Cl
Хлорид диамминсеребра взаимодействует с азотной кислотой выделяя осадок AgCl.
Осадок бромида серебра светло-жёлтого цвета малорастворим в аммиаке:
Ag++Br– AgBr
светло-желтый
Жёлтый осадок йодида серебра нерастворим в растворе аммиака:
Ag++I– AgI
желтый
МЕДЬ.
1. Раствор аммиака сначала осаждает из растворов солей меди (II) осадок основных солей меди голубовато-зелёного цвета, который растворим в избытке реактива с образованием тетраамминмедь (II) – иона синего цвета.
К 1 мл раствора сульфата меди прибавляют по каплям раствор аммиака - выпадает синий осадок, который растворяется в избытке реактива с образованием раствора темно-синего цвета.
2CuSO4 + 2NH3 + 2H2O Cu(OH)2SO4 + (NH4)2SO4
Cu(OH)2SO4 + (NH4)2SO4 + 6NH3 2[Cu(NH3)4]2+ + 2SO42- + 2H2O
2. К нескольким каплям раствора меди сульфата прибавляют раствор ферроцианида калия до образования красно-бурого осадка.
ЖЕЛЕЗО (II)
1. К 1 мл раствора железа (П) сульфата прибавляют 1 мл 2М кислоты хлороводородной и 1 мл раствора калия феррицианида; выпадает осадок синего цвета.
Fe2++K3[Fe(CN)6]KFe[Fe(CN)6]+ 2K+
синий
Соединение КFe3+[Fe2+(CN)6] носит тривиальное название турнбулевой сини и по данным рентгеноструктурных исследований идентично берлинской лазури КFe3+[Fe2+(CN)6]. Реакция проводится в кислой среде.
ЖЕЛЕЗО (III)
1. К 1 мл раствора хлорида железа (III) прибавляют 2-3 капли 2М кислоты хлороводородной и 2-3 капли раствора калия ферроцианида - образуется темно-синий осадок.
Fe3++K4[Fe(CN)6]KFe[Fe(CN)6]+ 3K+
синий
2. К 1 мл раствора анализируемого вещества прибавляют 1 мл разведенной кислоты хлороводородной и 4-5 капель раствора аммония тиоцианата - появляется винно-красное окрашивание.
Fe3++ 3SCN– Fe(SCN)3
КАЧЕСТВЕННЫЕ РЕАКЦИИ ОБНАРУЖЕНИЯ АНИОНОВ.
ХЛОРИДЫ, БРОМИДЫ, ИОДИДЫ.
1. К 2 мл раствора испытуемого вещества прибавляют 0,5 мл разведенной кислоты азотной и 0,5 мл раствора серебра нитрата выпадают творожистые осадки белого (AgCl), слегка желтоватого (AgBr), и жёлтого (Agl) цветов. Все осадки нерастворимы в разведенной азотной кислоте и имеют различную растворимость в растворе аммиака (проверить растворимость!).
2. Окисление до элементарного галогена (для бромидов и йодидов). Бромиды идентифицируют по реакции выделения брома в результате окислительно-восстановительной реакции между бромидом и хлорамином в кислой среде. Выделяющийся в результате реакции молекулярный бром извлекают хлороформом. Хлороформный слой окрашивается при этом в желто-бурый цвет.
Йодиды являются выраженными восстановителями. Поэтому слабые окислители выделяют молекулярный йод из йодидов. Йод окрашивает крахмал в синий цвет; раствор йода в хлороформе окрашен в фиолетовый цвет. Сильные окислители переводят йодиды в бесцветные гипойодиты (IO−) или йодаты (IO3−), поэтому выбор окислителя и его концентрация имеет большое значение. ГФ рекомендует использовать для окисления йодидов растворы железа (III) хлорида или натрия нитрита.
В качестве окислителя ГФ предлагает также применять кислоту серную концентрированную, при действии которой на йодиды при нагревании выделяются фиолетовые пары йода.
К 1 мл раствора испытуемого вещества прибавляют 1 мл разведенной кислоты хлороводородной, 0,5 мл раствора хлорамина Б и 1 мл хлороформа. Взбалтывают. Выделившийся бром окрашивает хлороформ в желто-бурый, а иод - в фиолетовый цвет.

2KBr + Cl2 → Br2 + 2KCl
СУЛЬФАТЫ
1. К 1 мл раствора анализируемого вещества прибавляют 0,5 мл раствора бария хлорида: появляется белый кристаллический осадок, нерастворимый в растворах минеральных кислот.
ФОСФАТЫ
1. К 1 мл раствора анализируемого вещества прибавляют несколько капель раствора серебра нитрата - образуется желтый осадок, растворимый в разведенной азотной кислоте и растворе аммиака.
3Ag++PO43– Ag3PO4
2. К 1 мл раствора соли фосфата прибавляют 1 мл раствора аммония хлорида. 1 ил раствора аммиака, 0,5 мл раствора магния сульфата - образуется белый кристаллический осадок.
БОРАТЫ
Несколько кристалликов борной кислоты смешивают с 1-2 мл этанола, прибавляют 1 каплю концентрированной серной кислоты и поджигают - пламя имеет окрашенные в зеленый цвет края.

КАРБОНАТЫ И ГИДРОКАРБОНАТЫ
1. К 0.2 г препарата прибавляют 0,5 мл разведенной минеральной кислоты (хлороводородной или серной) - выделяются пузырьки углекислого газа.
CO32– + 2HCl CO2 + H2O + 2Cl–
HCO3– + HCl CO2 + H2O + Cl–
2. К 2 мл раствора анализируемого вещества прибавляют 5 капель насыщенного раствора сульфата магния: карбонаты образуют белый осадок при комнатной температуре, гидрокарбонаты - при кипячении.
ОБРАЗЕЦ ОФОРМЛЕНИЯ ПРОТОКОЛА ЗАНЯТИЯ ПО ОБЩИМ
МЕТОДАМ ОПРЕДЕЛЕНИЯ КАЧЕСТВА ЛЕКАРСТВЕННЫХ
СРЕДСТВ НЕОРГАНИЧЕСКОГО ПРОИСХОЖДЕНИЯ. РЕАКЦИИ
НА ПОДЛИННОСТЬ.
ДАТА................................................................................................................
ТЕМА ЗАНЯТИЯ............................................................................................
|
N пп/п
|
Катион/ анион
|
Испытуемое лекарственное средство |
Краткая методика идентификации |
Уравнение химической реакции |
Наблюдаемый эффект |
ТЕМА 2. ОБЩИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ КАЧЕСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ. ОПРЕДЕЛЕНИЕ РАСТВОРИМОСТИ, ТЕМПЕРАТУРЫ ПЛАВЛЕНИЯ И КИПЕНИЯ, КИСЛОТНОСТИ, ЛЕТУЧИХ ВЕЩЕСТВ, ВОДЫ, ЗОЛЫ. ИСПОЛЬЗОВАНИЕ ФИЗИКО-ХИМИЧЕСКИХ КОНСТАНТ В ОЦЕНКЕ ДОБРОКАЧЕСТВЕННОСТИ ЛЕКАРСТВЕННЫХ СРЕДСТВ.
Вопросы для самоконтроля
1. Назовите источники и причины недоброкачественности лекарственных средств.
2. Приведите основные типы реакций, приводящих к изменению лекарственных веществ под воздействием факторов окружающей среды.
3. Опишите природу и характер примесей. Специфические и неспецифические (общие) примеси. Допустимые и недопустимые примеси.
4. Дайте определение показателей «описание» и «растворимость» согласно ГФ XI, их значение для оценки качества лекарственных средств. Условные термины растворимости.
5. Дайте определение понятиям: температура плавления и затвердевания, температура кипения. Опишите способы их определения.
6. Опишите определение кислотности, летучих веществ, золы и воды в лекарственных средствах. Напишите уравнение химической реакции титрования воды по методу К.Фишера.
7. Опишите возможность использования физико-химических констант в оценке доброкачественности лекарственных средств. Дайте определения понятиям: Rf,Rs, удельный и молярный показатели поглощения, показатель преломления, удельное вращение. Напишите формулы для их расчета.
