
ЛАБОРАТОРНАЯ РАБОТА 6
.docЛабораторная работа № 6
Свойства липидов
Опыт 1. Эмульгирование жира.
Принцип метода. При взбалтывании жира с водой, раствором желчи, белка, мыла, соды образуется эмульсия. Вода с жиром дает нестойкую, а остальные растворы стойкую эмульсию.
Это обусловлено тем, что поверхностно – активные частицы желчных кислот, белка, мыла обволакивают капельки жира и препятствуют их слиянию. Эмульгирование жира содой обусловлено образованием мыла в результате взаимодействия углекислого натрия с присутствующими в жире свободными жирными кислотами.
Порядок выполнения работы.
В 4 пробирки наливают по 1 мл: в первую – дистиллированной воды, во вторую – 1% раствора яичного белка, в третью – 1% раствора мыла, в четвертую – 1% раствора углекислого натрия Na 2 CO 3 •10H 2 O. В каждую пробирку добавляют по 2 капли растительного масла и тщательно взбалтывают.
Результаты работы заносят в таблицу:
|
Вода+растительное масло |
Белок+растительное масло |
Мыло+растительное масло |
Сода+растительное масло |
|
Степень эмульгирования жира |
|||
|
|
|
|
|
Примечание: Степень эмульгирования выражают знаком плюс (+),
Отсутствие эмульгирования выражают знаком минус (–).
Опыт 2. Омыление жиров (гидролиз).
В результате гидролиза происходит расщепление связей в молекулах глицеридов при действии воды, причем элементы воды присоединяются по месту возникающих свободных валентностей с образованием двух структурных элементов жиров — жирных кислот и глицерина. Участвующая в реакции вода диссоциирует на водород и гидроксил. Водород присоединяется к кислотному остатку, а гидроксил — к спиртовому радикалу. Практически процесс распада триглицеридов протекает последовательно, с образованием промежуточных продуктов реакции – моно- и диглицеридов:
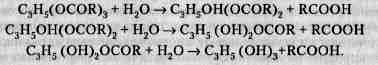
Глубина гидролитического распада определяется содержанием свободных жирных кислот и характеризуется величиной кислотного числа жира (КЧ).
Скорость гидролитического расщепления жиров находится в прямой зависимости от концентрации водородных ионов, которые, как и ионы гидроксила, являются катализаторами этой реакции. Процесс гидролиза протекает значительно быстрее в присутствии некоторых металлов или их оксидов, например Zn, ZnO, CaO, MgO.
Низкомолекулярные кислоты сильно меняют вкус и запах жира. По этим изменениям и определяется пищевая порча жира. Из-за гидролиза особенно сильно изменяются органолептические показатели коровьего и кокосового масел, имеющих в своем составе низкомолекулярные летучие жирные кислоты. Высокомолекулярные жирные кислоты вкуса и запаха не имеют, а потому увеличение их содержания при гидролизе не изменяет органолептических показателей жира.
Принцип метода. Омыление – это гидролиз сложных эфиров под действием щёлочи. При этом получается соль органической кислоты (мыло, т. е. смесь солей высших жирных кислот) и спирт (глицерин – трёхатомный спирт)
Омыление жиров производится в автоклавах, щелочью или ферментативным путем (фермент липаза). Быстрее омыление происходит в водно-спиртовом растворе и спиртово-щелочном растворе.
Схема омыления жира:
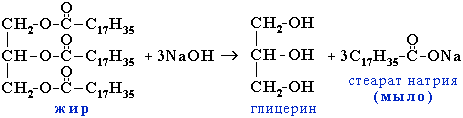
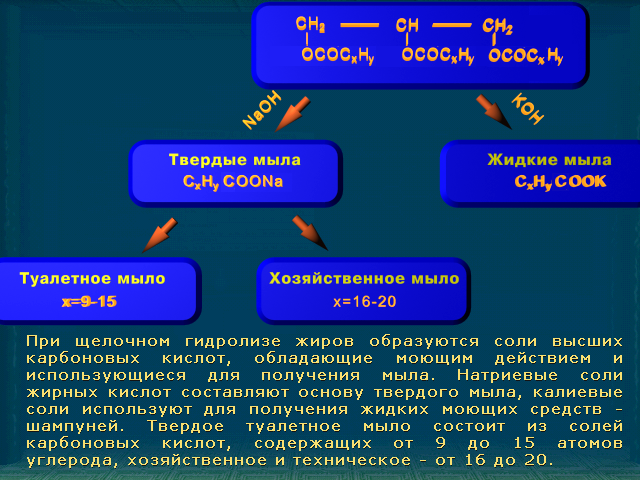
Порядок выполнения работы.
В пробирку отвешивают 2 г. жира и приливают 5 мл. 1%-ного спиртового раствора щелочи. Пробирку закрывают пробкой со стеклянной трубой (холодильником) и ставят в водяную баню на 10-12 мин. при (t=80oC). После окончания омыления (образуется однородный раствор мыла) смесь выливают в фарфоровую чашку, добавляют воду и при нагревании на водяной бане удаляют спирт.
Полученный раствор мыла используют для определения составных частей жира.
Оформление опыта: результат опыта и уравнение реакции записывают в тетрадь.
Опыт 3. Гидролиз жира и открытие в гидролизате его составных частей.
Гидролиз жира.
В широкую пробирку пипеткой налейте 20 капель подсолнечного масла и мерным цилиндром 2 − 3 мл 1%-ного спиртового раствора KOH. Пробирку поместите в кипящую водяную баню на 15 − 20 минут до образования однородного раствора. Напишите уравнение реакции гидролиза триглицерида.
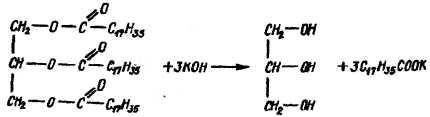
жир глицерин стеарат калия
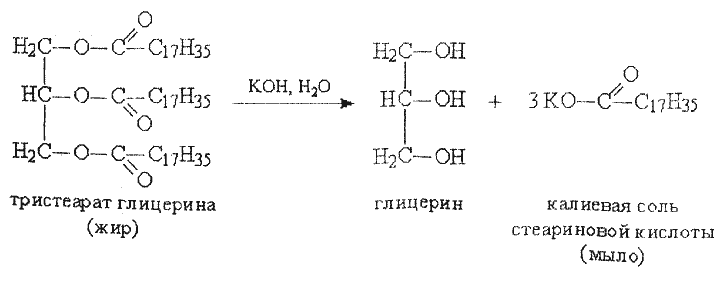
К гидролизату мерным цилиндром прилейте 6 − 8 мл воды, взболтайте и используйте для открытия глицерина и жирных кислот.
Принцип метода. Качественная реакция на определение наличия глицецерина в растворах проводится с раствором сульфата меди (II) и раствором гидроксида натрия. Таким образом, происходит получение глицерата меди – комплексного соединения сине-василькового цвета.
Химический эксперимент проводится так: к раствору сульфата меди (II) приливается раствор гидроксида натрия. Раствор окрашивается в синий цвет – это выпал осадок гидроксида меди (II). Далее добавляется несколько мл гидролизата или глицерина и раствор перемешивается. Наблюдается растворение осадка – образуется комплексное соединение цвета индиго - глицерат меди. Получение его записывается в уравнении:
CH2OH-CHOH-CH2OH + Cu(OH)2--> Cu(-O-CH2-CH-O-)-CH2OH
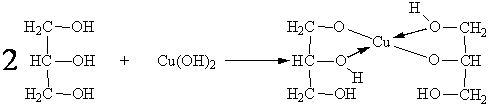
глицерин глицерат меди
При взаимодействии серной или соляной кислоты с гидролизатом или мылом выделяются свободные жирные кислоты, которые всплывают на поверхность жидкости. Реакция идет по следующему уравнению:
2C17H35COOK + H2SO4 →2C17H35COOH + K2SO4
стеариновая кислота
Кальциевые, магниевые соли жирных кислот нерастворимы в воде.
Химизм реакции:
C 17H35COOK
+ СаCl2
→(C17H35COO)2Са
+ 2KCl
17H35COOK
+ СаCl2
→(C17H35COO)2Са
+ 2KCl
Открытие глицерина.
Порядок выполнения работы.
В чистую пробирку мерным цилиндром налейте 2-3 мл разбавленного гидролизата, добавьте равный объем 10 %-ного раствора NaOH и 2 − 3 капли 2 %-ного раствора CuSO4. Смешайте. Наблюдайте появление характерного для глицерата меди окрашивания раствора. Напишите уравнение реакции образования глицерата меди
Оформление опыта. Записать: как окрашивается гидролизат жира, содержащий глицерин, при взаимодействии с гидроксидом меди (II)? Объясните ход реакции и напишите уравнение реакции.
Открытие жирных кислот.
Порядок выполнения работы.
Оставшийся гидролизат разлейте поровну в две пробирки. В первую мерным цилиндром прибавьте равное количество 10 %-ного раствора H2SO4 и поместите её в кипящую водяную баню до образования на поверхности раствора жидкого слоя свободных жирных кислот. Во вторую пробирку пипеткой прибавьте 5 − 6 капель 10 %-ного раствора CaCl2. Встряхните. Наблюдайте появление осадка нерастворимых солей высших жирных кислот (нерастворимого кальциевого мыла).
Оформление опыта. Сделать вывод и написать уравнение реакции.
Опыт 4. Проба на непредельные жирные кислоты.
Принцип метода. Непредельные жирные кислоты способны присоединять галоиды по месту двойных связей.
Остатки непредельных кислот в жирах сохраняют свойства алкенов. Учитель обращается к классу: какие качественные реакции на алкены вы знаете? В первую очередь, это обесцвечивание бромной воды (реакция присоединения) и раствора перманганата калия (реакция окисления). При добавлении к 2 мл растительного масла равного объема бромной воды или раствора КМnO4 происходит обесцвечивание водного слоя, несмотря на то что масло и вода не смешиваются.
олеиновая кислота

Порядок выполнения работы.
В пробирки наливают 1-2 мл масла, растворяют его в 2—3 мл диэтилового эфира или хлороформа, прибавляют 1—2 капли бромной воды и взбалтывают. Бромная вода – тяжёлая едкая жидкость красно-бурого цвета с сильным неприятным запахом. Молекула брома двухатомна (формула Br2).
Бромная вода представляет собой разведенный водой бром. Ее в уравнениях реакции принято записывать через такую формулу - Br2, хотя она в растворе находится в виде смеси двух кислот - HBrO (бромноватистая кислота) и HBr (бромоводородная кислота). Данное соединение имеет желто-оранжевый цвет и довольно низкую температуру замерзания. Является сильным окислителем, который способен в щелочной среде окислять катионы таких металлов - Сг+3, Мп+3, Fe+2, Co +2, Ni+3. Добавление Br2 уменьшает водородный показатель раствора (рН), т.к. бромная вода содержит свободные кислоты.
Буровато-желтая окраска бромной воды исчезает, что указывает на присутствие непредельных кислот.
Результат опыта и реакцию занести в тетрадь.
Опыт 5. Открытие лецитина в яичном желтке.
Принцип метода. Лецити́ны находятся в тканях животных и растений, яичных желтках, и состоят из: ортофосфорной кислоты, холина, жирных кислот и глицерина. Из этих компонентов и состоят фосфолипиды, отличающиеся друг от друга составом жирных кислот.
Лецитины относятся к группе жироподобных фосфорсодержащих веществ, называемых фосфатидами. Лецитины являются смешанными глицеридами жировых кислот (пальмитиновой, стеариновой, олеиновой) и фосфорной кислоты, причем из трех гидроксилов фосфорной кислоты один образует эфир глицерина, а второй – сложный эфир с гидроксилом холина (или моноэтаноламина). Таким образом, предполагаемая формула строения лецитинов имеет вид:
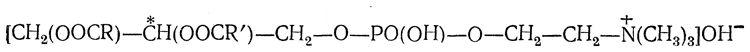
Поэтому лецитины, относятся к группе фосфолипидов, не растворяются в воде и ацетоне, но хорошо растворяются в этиловом спирте, эфире и хлороформе.
Вследствие этого они могут быть выделены из раствора добавлением ацетона или воды. Ацето́н (диметилкето́н, 2-пропано́н) – органическое вещество, имеющее формулу CH3—C(O)—CH3 или С3Н6О, простейший представитель насыщенных кетонов. Своё название ацетон получил от лат. Acetum – уксус.
Порядок выполнения работы.
В две пробирки мерным цилиндром налейте по 1 мл спиртового раствора яичного желтка. В одну пробирку добавьте равное количество воды (при смешивании образуется устойчивая эмульсия), в другую − ацетона (выпадает белый осадок). Наблюдайте образование эмульсии лецитина в первой пробирке и его осаждение во второй.
Оформление работы: сделайте заключение о наличии лецитина в желтке куриного яйца, напишите структурную формулу лецитина и сделайте вывод о его растворимости.
Контрольные вопросы.
1. Какие вещества являются растворителями, а какие эмульгаторами жиров?
2. Как определяются составные части жира?
3. Какие жирные кислоты называются насыщенными и ненасыщенными?
4. Укажите различия в структуре и свойствах насыщенных и ненасыщенных жирных кислот. Приведите пример.
5. Напишите уравнение реакции гидролиза жира.
Самостоятельная работа.
1. Назвать условия кислородного обеспечения организма, необходимые для окисления жира в организме человека.
2. Особенности энергетического катаболизма и конструктивного метаболизма жиров в организме человека.
3. Что такое кетоновые тела? Из чего и при каких условиях они образуются?
