- •Избранные лекции по токсикологической химии
- •Содержание
- •Введение в токсикологическую химию
- •Особенности химико-токсикологического анализа.
- •Организационная структура судебно-медицинской и судебно-химической экспертизы в рф
- •Правовые и методологические основы судебно-химической экспертизы
- •Правила производства судебно-химической экспертизы вещественных доказательств в схо смл Бюро смэ органов здравоохранения
- •Помещения лаборатории
- •Порядок проведения судебно-химической экспертизы Основные правила судебно-химического анализа (сха)
- •Документация при производстве судебно-химической экспертизы
- •Яд. Общая характеристика токсического действия. Формирование токсического эффекта как фактор взаимодействия яда, организма и окружающей среды. Понятие «яд», «отравление»
- •Классификация отравлений
- •Общая характеристика и классификация веществ, вызывающих отравление
- •2. Токсические вещества неорганической природы:
- •Токсикокинетика чужеродных соединений
- •Всасывание чужеродных соединений
- •Факторы, влияющие на абсорбцию чужеродных соединений
- •Распределение. Факторы, влияющие на распределение чужеродных веществ в организме.
- •Метаболизм чужеродных соединений
- •2. Восстановление:
- •Выделение чужеродных соединений
- •Группа веществ, изолируемых дистилляцией
- •(«Летучие яды»)
- •5.Сложные эфиры алифатического ряда
- •Объекты судебно-химического исследования. Пробоподготовка
- •Одноатомные спирты
- •Этиловый спирт в химико-токсикологическом отношении
- •Токсикологическое значение спиртов
- •Токсикокинетика спиртов
- •Объекты исследования и пробоподготовка
- •Правила отбора проб для исследования
- •Экспертиза алкогольного опьянения.
- •Клиническая диагностика
- •Химические свойства спиртов. Методы анализа в судебно-химической экспертизе отравлений и экспертизе алкогольного опьянения.
- •Количественное определение спиртов
- •Теоретические предпосылки метода
- •Основные газохроматографические параметры
- •Относительное время удерживания является величиной более постоянной, так как на него меньше влияют условия проведения хроматографического процесса.
- •Аппаратурное оформление метода гжх
- •Определение этанола методом гжх
- •Оценка результатов количественного определения этанола в крови человека
- •Группа веществ, изолируемых из биологического материала экстракцией и сорбцией.
- •(Подгруппа «Лекарственные средства»)
- •Номенклатура и классификация.
- •Теоретические основы метода изолирования
- •Факторы, влияющие на эффективность изолирования «нелетучих» ядов из биоматериала.
- •Общие и частные методы изолирования
- •Изолирование этанолом, подкисленным щавелевой кислотой (метод Стаса-Отто)
- •Выход 20-30%
- •3 Раза
- •(Основания алкалоидов)
- •Изолирование водой, подкисленной щавелевой кислотой (метод Васильевой)
- •3 Раза
- •(Молекулярные формы кислот,
- •Выход 30-40%
- •(Основания алкалоидов)
- •Частные методы изолирования :
- •(Кислотные формы барбитуратов)
- •2 Раза по 2 часа
- •(Основания алкалоидов)
- •Выход 50-70%
- •(Вещества кислого и нейтрального характера)
- •(Вещества основного характера)
- •Очистка изолируемых веществ от сопутствующих компонентов биоматериала.
- •Аналитический скрининг лекарственных веществ, имеющих токсикологическое значение.
- •Хроматографические скрининговые методы
- •Тонкослойная хроматография (тсх)
- •Газожидкостная хроматография (гжх)
- •Высокоэффективная жидкостная хроматография (вэжх)
- •Спектральные скрининговые методы
- •Абсорбционная спектроскопия
- •Иммунохимические методы в скрининге лекарственных веществ. Иммунохимический анализ (иха)
- •Производные барбитуровой кислоты
- •В химико-токсикологическом отношении
- •Лактим-лактамная таутомерия барбитуратов.
- •Токсикокинетика барбитуратов (всасывание, распределение, метаболизм, выделение)
- •Токсикодинамика (развитие отравлений).
- •Алкалоиды в химико-токсикологическом отношении
- •Токсикологическое значение алкалоидов
- •3. Идентификация выделенных алкалоидов.
- •Экспресс - анализ интоксикаций
- •Экспресс-метод определения лекарственных веществ на основе хроматографического скрининга (хтс)
- •Группа веществ, изолируемых экстракцией неполярными растворителями. Пестициды
- •Пестициды как химические загрязнители
- •Питания
- •Токсикологическая характеристика и судебно-химическое значение пестицидов
- •3. Классификация пестицидов
- •II. Органические пестициды
- •Классификация по назначению (по объектам применения):
- •Классификация в зависимости от путей проникновения в организм насекомых:
- •- Контактные – убивающие насекомых при соприкосновении с любой частью тела
- •Классификация гербицидов в зависимости от характера действия:
- •Контактного действия – действуют только на те участки растений, куда попали (органические соединения ртути, цианиды, кислота серная, медный купорос).
- •Классификация по формам применения пестицидов:
- •4. Изолирование и очистка
- •5.Анализ пестицидов
- •6.Основные группы пестицидов
- •Изолирование
- •Метод газожидкостной хроматографии (гжх) в анализе фоп
- •Группа веществ, изолируемых минерализацией
- •(«Металлические яды»)
- •Общая характеристика группы
- •Металлические загрязнения
- •Марганец
- •Методы минерализации
- •Методы “мокрой минерализации”
- •Методика изолирования металлических ядов из биологического материала общим методом минерализации
- •Дробный метод анализа «металлических ядов»
- •Маскировка ионов в дробном анализе
- •Применение органических реагентов в дробном анализе
- •Применение диэтилдитиокарбаминовой кислоты и её солей
- •Свойства ддтк металлов
- •Применение дитизона
- •Свойства дитизонатов
- •Методы количественного определения
- •Группа токсикологически важных веществ, изолируемых экстракцией водой (минеральные кислоты, щёлочи и их соли)
- •Группа токсикологически важных веществ, требующих особых методов изолирования (соединения фтора)
- •Группа веществ, не требующих особых методов изолирования. Вредные пары и газы. Оксид углерода (II)
- •Литература
Применение диэтилдитиокарбаминовой кислоты и её солей
Диэтилдитиокарбаминовая кислота – соединение, неустойчивое в водных растворах, поэтому в аналитической практике используют её соли, натриевая, аммониевая, свинцовая. Эти реагенты образуют более чем с 20 металлами внутрикомплексные соединения – диэтилдитиокарбаминаты (ДДТК металлов). В большинстве случаев они используются для целей селективной экстракции катионов из минерализата.
Свойства ддтк металлов
ДДТК металлов, за исключением ДДТК натрия, нерастворимы в воде, но хорошо растворяются в органических растворителях (хлороформ).
Большинство ДДТК металлов – бесцветные соединения. Окраску имеют только некоторые растворы комплексных соединений в хлороформе: ДДТК меди имеет яркое желто-коричневое окрашивание, ДДТК висмута, кадмия, сурьмы – бледно-желтое, хрома – бледно-зеленое.
ДДТК металлов образуются при строго определенных значениях рН среды. В щелочной среде образуются комплексы цинка (рН 8,5), кадмия (рН 12,5), висмута (рН 14). Оптимальным значением рН для образования ДДТК меди является рН равное 3, однако этот комплекс устойчив в интервале рН от 4 до 11. Таким образом, регулируя рН раствора, можно избирательно изолировать из минерализата тот или иной катион.
4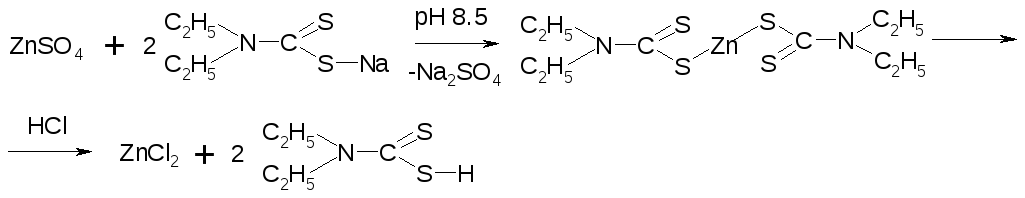 .
Устойчивость ДДТК металлов также связана
с рН среды. Те комплексы, которые
образуются в щелочной среде – неустойчивы
в кислой и разрушаются под действием
кислот. Это свойство используется для
реэкстракции металлов из их комплексов
и переведения в водную фазу с целью
проведения подтверждающих реакций.
Например, ДДТК цинка и кадмия можно
разрушить действием хлористоводородной
кислоты, а ДДТК висмута – азотной.
.
Устойчивость ДДТК металлов также связана
с рН среды. Те комплексы, которые
образуются в щелочной среде – неустойчивы
в кислой и разрушаются под действием
кислот. Это свойство используется для
реэкстракции металлов из их комплексов
и переведения в водную фазу с целью
проведения подтверждающих реакций.
Например, ДДТК цинка и кадмия можно
разрушить действием хлористоводородной
кислоты, а ДДТК висмута – азотной.
5.Для тех ДДТК металлов, которые устойчивы в широком интервале рН (медь), выделение катиона в водную фазу основано на использовании правила рядов среди диэтилдитиокарбаминатов. Согласно этому правилу каждый предшествующий катион, находящийся в водной фазе, вытесняет последующие катионы из их комплексов, растворенных в хлороформе.
Ряд ДДТК токсикологически важных катионов можно представить следующим образом:
Hg > Ag > Cu > Ni > Co > Pb > Bi > Cd > Tl > Sb > Zn > Mn > Fe
Например, Hg2+ способна вытеснять Cu из (ДДТК)2Cu, в свою очередь Cu2+ вытесняет Pb из (ДДТК)2Pb.
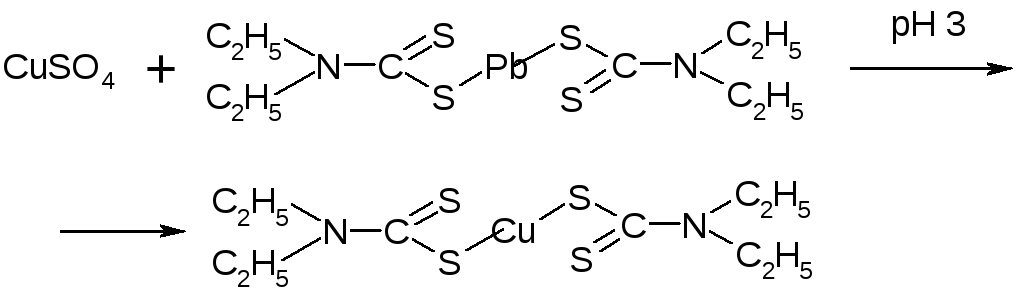
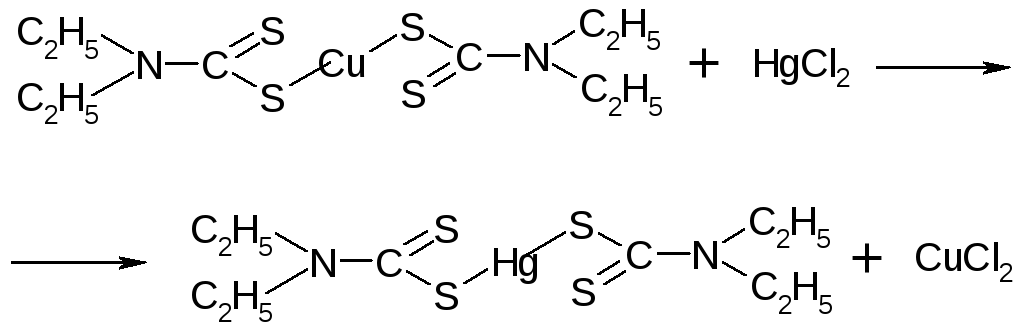
Катионы цинка, кадмия, висмута и меди называют экстракционными катионами и их анализ проводят по следующей схеме:
Выделение из минерализата в виде комплекса с ДДТКК при определенном рН раствора и экстракция в органическую фазу.
Разрушение комплексов кислотами или по правилу рядов – реэкстракция – переведение катионов в водную фазу.
Обнаружение и количественное определение.
Применение дитизона
Дитизон (дифенилтиокарбазон), введен в аналитическую практику в 1957 г. Фишером, который предписывает следующую структуру органического реагента. В зависимости от рН среды, дитизон может существовать в двух таутомерных формах: в кислой среде – в кетоформе, в щелочной среде – в енольной форме.