
- •Избранные лекции по токсикологической химии
- •Содержание
- •Введение в токсикологическую химию
- •Особенности химико-токсикологического анализа.
- •Организационная структура судебно-медицинской и судебно-химической экспертизы в рф
- •Правовые и методологические основы судебно-химической экспертизы
- •Правила производства судебно-химической экспертизы вещественных доказательств в схо смл Бюро смэ органов здравоохранения
- •Помещения лаборатории
- •Порядок проведения судебно-химической экспертизы Основные правила судебно-химического анализа (сха)
- •Документация при производстве судебно-химической экспертизы
- •Яд. Общая характеристика токсического действия. Формирование токсического эффекта как фактор взаимодействия яда, организма и окружающей среды. Понятие «яд», «отравление»
- •Классификация отравлений
- •Общая характеристика и классификация веществ, вызывающих отравление
- •2. Токсические вещества неорганической природы:
- •Токсикокинетика чужеродных соединений
- •Всасывание чужеродных соединений
- •Факторы, влияющие на абсорбцию чужеродных соединений
- •Распределение. Факторы, влияющие на распределение чужеродных веществ в организме.
- •Метаболизм чужеродных соединений
- •2. Восстановление:
- •Выделение чужеродных соединений
- •Группа веществ, изолируемых дистилляцией
- •(«Летучие яды»)
- •5.Сложные эфиры алифатического ряда
- •Объекты судебно-химического исследования. Пробоподготовка
- •Одноатомные спирты
- •Этиловый спирт в химико-токсикологическом отношении
- •Токсикологическое значение спиртов
- •Токсикокинетика спиртов
- •Объекты исследования и пробоподготовка
- •Правила отбора проб для исследования
- •Экспертиза алкогольного опьянения.
- •Клиническая диагностика
- •Химические свойства спиртов. Методы анализа в судебно-химической экспертизе отравлений и экспертизе алкогольного опьянения.
- •Количественное определение спиртов
- •Теоретические предпосылки метода
- •Основные газохроматографические параметры
- •Относительное время удерживания является величиной более постоянной, так как на него меньше влияют условия проведения хроматографического процесса.
- •Аппаратурное оформление метода гжх
- •Определение этанола методом гжх
- •Оценка результатов количественного определения этанола в крови человека
- •Группа веществ, изолируемых из биологического материала экстракцией и сорбцией.
- •(Подгруппа «Лекарственные средства»)
- •Номенклатура и классификация.
- •Теоретические основы метода изолирования
- •Факторы, влияющие на эффективность изолирования «нелетучих» ядов из биоматериала.
- •Общие и частные методы изолирования
- •Изолирование этанолом, подкисленным щавелевой кислотой (метод Стаса-Отто)
- •Выход 20-30%
- •3 Раза
- •(Основания алкалоидов)
- •Изолирование водой, подкисленной щавелевой кислотой (метод Васильевой)
- •3 Раза
- •(Молекулярные формы кислот,
- •Выход 30-40%
- •(Основания алкалоидов)
- •Частные методы изолирования :
- •(Кислотные формы барбитуратов)
- •2 Раза по 2 часа
- •(Основания алкалоидов)
- •Выход 50-70%
- •(Вещества кислого и нейтрального характера)
- •(Вещества основного характера)
- •Очистка изолируемых веществ от сопутствующих компонентов биоматериала.
- •Аналитический скрининг лекарственных веществ, имеющих токсикологическое значение.
- •Хроматографические скрининговые методы
- •Тонкослойная хроматография (тсх)
- •Газожидкостная хроматография (гжх)
- •Высокоэффективная жидкостная хроматография (вэжх)
- •Спектральные скрининговые методы
- •Абсорбционная спектроскопия
- •Иммунохимические методы в скрининге лекарственных веществ. Иммунохимический анализ (иха)
- •Производные барбитуровой кислоты
- •В химико-токсикологическом отношении
- •Лактим-лактамная таутомерия барбитуратов.
- •Токсикокинетика барбитуратов (всасывание, распределение, метаболизм, выделение)
- •Токсикодинамика (развитие отравлений).
- •Алкалоиды в химико-токсикологическом отношении
- •Токсикологическое значение алкалоидов
- •3. Идентификация выделенных алкалоидов.
- •Экспресс - анализ интоксикаций
- •Экспресс-метод определения лекарственных веществ на основе хроматографического скрининга (хтс)
- •Группа веществ, изолируемых экстракцией неполярными растворителями. Пестициды
- •Пестициды как химические загрязнители
- •Питания
- •Токсикологическая характеристика и судебно-химическое значение пестицидов
- •3. Классификация пестицидов
- •II. Органические пестициды
- •Классификация по назначению (по объектам применения):
- •Классификация в зависимости от путей проникновения в организм насекомых:
- •- Контактные – убивающие насекомых при соприкосновении с любой частью тела
- •Классификация гербицидов в зависимости от характера действия:
- •Контактного действия – действуют только на те участки растений, куда попали (органические соединения ртути, цианиды, кислота серная, медный купорос).
- •Классификация по формам применения пестицидов:
- •4. Изолирование и очистка
- •5.Анализ пестицидов
- •6.Основные группы пестицидов
- •Изолирование
- •Метод газожидкостной хроматографии (гжх) в анализе фоп
- •Группа веществ, изолируемых минерализацией
- •(«Металлические яды»)
- •Общая характеристика группы
- •Металлические загрязнения
- •Марганец
- •Методы минерализации
- •Методы “мокрой минерализации”
- •Методика изолирования металлических ядов из биологического материала общим методом минерализации
- •Дробный метод анализа «металлических ядов»
- •Маскировка ионов в дробном анализе
- •Применение органических реагентов в дробном анализе
- •Применение диэтилдитиокарбаминовой кислоты и её солей
- •Свойства ддтк металлов
- •Применение дитизона
- •Свойства дитизонатов
- •Методы количественного определения
- •Группа токсикологически важных веществ, изолируемых экстракцией водой (минеральные кислоты, щёлочи и их соли)
- •Группа токсикологически важных веществ, требующих особых методов изолирования (соединения фтора)
- •Группа веществ, не требующих особых методов изолирования. Вредные пары и газы. Оксид углерода (II)
- •Литература
Аппаратурное оформление метода гжх
Прибор для определения спиртов и других «летучих» ядов состоит из следующих блоков:
2 -
устройство ввода пробы
-
устройство ввода пробы
3- хроматографическая колонка (разделение веществ)
4- детектор (регистрация сигналов веществ)
5- самописец (хроматограмма)
В качестве газа-носителя используется инертный газ (азот, гелий, аргон), находящийся в баллоне под большим давлением, выполняющий роль подвижной фазы. К нему предъявляются следующие требования:
газ-носитель должен быть инертен к материалу колонки, твердому носителю и неподвижной жидкой фазе, к исследуемым веществам,
газ должен обладать малой сорбируемостью на неподвижной жидкой фазе,
газ должен обеспечивать хорошее разделение веществ,
газ должен соответствовать чувствительности и принципу работы детектора,
газ должен обладать высокой теплопроводностью, быть достаточно чистым и доступным.
В химико-токсикологическом анализе в качестве газа – носителя чаще всего используются азот и гелий.
Хроматографические колонки представляют из себя V-образные или спиралевидные трубки из инертных материалов (металлические, стеклянные, полимерные) с внутренним диаметром 2-6 мм, длиной 2-6 метров. Основное требование к материалу колонки – инертность по отношению к газу-носителю, твердому носителю и неподвижной жидкой фазе, к исследуемым веществам.
Набивка колонки состоит из твердого носителя (т.н.) и неподвижной жидкой фазы (н.ж.ф.), которая в виде тонкой пленки наносится на гранулы т.н.
Большинство твердых носителей готовят из диатомитовой (диатомовой) земли, представляющей из себя разновидность окислов кремния, а также из огнеупорного кирпича (инзенский кирпич), который по свойствам близок к диатомитовой земле. В настоящее время существует большое количество синтетических т.н. различных марок. Чаще всего используется хроматон, хромосорб, полисорб, целит и др.
Основные требования к твердому носителю:
должен обеспечивать равномерное распределение на его поверхности н.ж.ф. (должен ею смачиваться),
должен иметь большую удельную поверхность (на 1г т.н. должна приходиться площадь от 1 до 20 кв.метров),
должен быть инертным к материалу колонки, н.ж.ф., анализируемым веществам,
должен быть термостабильным при температуре опыта,
должен быть механически прочным, гранулы не должны ломаться при пересыпании.
В качестве неподвижной жидкой фазы обычно используют жидкие высокомолекулярные вещества (ВМС), имеющие высокую температуру кипения. Н.ж.ф. наносят тонким слоем на гранулы т.н. в количестве от 5 до 30% от его веса, чтобы не было слипания частиц т.н. К ВМС такого типа относятся полиэтиленгликоли ( полиэтиленгликоль с молекулярной массой 1000-1500, триэтиленгликоль), эфиры полиэтиленгликолей, смеси углеводородов, различные высококипящие масла и ряд других веществ (около 400 наименований). Характеристики различных н.ж.ф. приводятся в справочной литературе.
Требования к н.ж.ф.:
низкая летучесть (высокая температура кипения),
термостабильность,
химическая инертность к материалу колонки, т.н., к веществам,
должна обеспечивать четкое разделение хроматографируемых веществ, т.е. вещества должны иметь в этой н.ж.ф. различные коэффициенты распределения и различные времена удерживания.
Детектор представляет из себя устройство, которое регистрирует выходящие из колонки вещества и измеряет их количество. Главное требование, предъявляемое к детектору, - высокая чувствительность к определяемым веществам. Чаще всего в химико-токсикологическом анализе используют детектор по теплопроводности (ДТП), или катарометр, и пламенно-ионизационный детектор (ПИД).
Катарометр. Схема устройства.
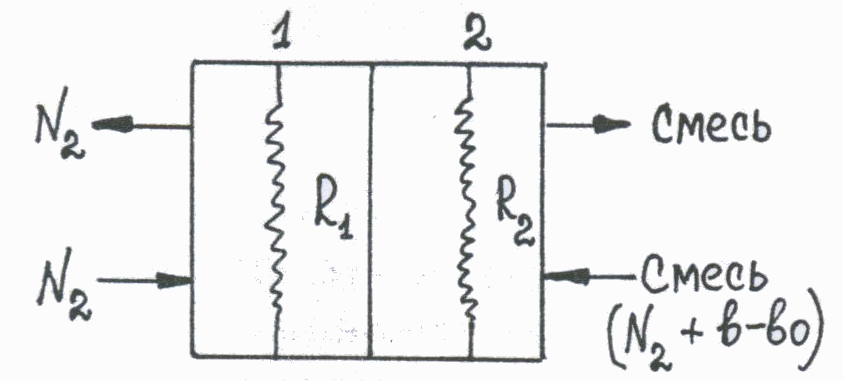
-
На схеме:
1- сравнительная камера
2- измерительная камера
R1 и R2 - нити сопротивления
Принцип действия катарометра состоит в измерении разности теплопроводностей чистого газа-носителя, поступающего в сравнительную камеру детектора, и смеси газа с анализируемым веществом, выходящей из колонки в измерительную камеру. Чем больше эта разница, тем выше чувствительность детектора. Самой большой теплопроводностью обладает гелий, поэтому при работе с ним достигается наиболее высокая чувствительность детектора. При использовании в качестве газа-носителя азота чувствительность снижается.
Нити сопротивления R1 и R2 в сравнительной и измерительной камерах детектора одинаковы. Если в обе камеры поступает чистый газ-носитель, одинаково охлаждающий сопротивления R1 и R2, тока в цепи детектора не возникает, так как эти сопротивления являются плечами моста Уитстона.
 На
схеме моста Уитстона
На
схеме моста Уитстона
R3 и R4 – уравновешивающие сопротивления,
G- гальванометр.
В этом случае самописец вычерчивает прямую линию (сигнал от газа-носителя, нулевая линия на хроматограмме). Когда в газовом потоке появляется вещество (в измерительной камере), меняется теплопроводность газа, что приводит к изменению сопротивления R2, разбалансировке моста и возникновению тока в цепи детектора. Сигнал с детектора поступает на самописец, который вычерчивает хроматографический пик. Величина пика (т.е. высота и площадь) пропорциональна сигналу детектора и количеству вещества в пробе, на чем и основано количественное определение.
Катарометр является универсальным детектором, он реагирует на все вещества (органические и неорганические), теплопроводность которых отличается от теплопроводности газа-носителя.
Чувствительность определения составляет 10-3 - 10-5 г.
Ионизационно-пламенный детектор (ПИД). Схема устройства.

В настоящее время ПИД является наиболее распространенным в газовой хроматографии. Принцип работы ПИД основан на том, что выходящий из колонки газ смешивается с водородом и сжигается в атмосфере воздуха или кислорода. Образующиеся в присутствии исследуемого вещества ионы и электроны ионизируют пламя, в результате чего возникает ионный ток между электродами детектора, находящимися под напряжением. Сигнал детектора (ионный ток) поступает на самописец, вычерчивающий хроматограмму.
Чувствительность ПИД на несколько порядков выше чувствительности катарометра и составляет 10-9-10-12 г/сек. (количество органического вещества, поступающего в камеру ПИД в единицу времени).
ПИД чувствителен ко всем органическим соединениям и проявляет к ним селективность. Мало чувствителен по отношению к воде, окиси и двуокиси углерода, аммиаку, окислам азота и ряду других веществ. Низкая чувствительность ПИД к воде делает его особенно удобным при анализе биологических жидкостей.
