
_2_1_2014_doc
.pdf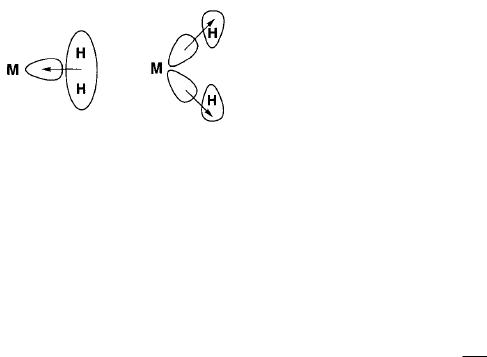
104
3.3. МЕХАНИЗМЫ РЕАКЦИЙ, КАТАЛИЗИРУЕМЫХ КОМПЛЕКСАМИ ПЕРЕХОДНЫХ
МЕТАЛЛОВ. [1-17].
3.3.1.ГИДРИРОВАНИЕ
Строение молекулы водорода.
Атомы в молекуле водорода связаны прочной -связью с энергией диссоциации 103 ккал/моль. Электроны, образующие эту связь
расположены на связывающей МО. Разрыхляющая -орбиталь молекула водорода не заполнена электронами и не рассматривалась, как важный фактор строения молекулы до тех пор пока не было установлено ее важное значение в катализе:
Рис. Образование связи метал-водород в 2-Н2 комплексе. Донорная связь с передачей электронов от связывающей орбитали Н2 на свободные
орбитали металла (слева). Обратное -связывание за счет донирования электронов с заполненных орбиталей металла на незаполненную разрыхляющую орбиталь Н2-лиганда.
Молекула водорода легко вступает в радикально-цепные реакции. Однако гидрирование ненасыщенных соединений протекает весьма трудно и требует либо очень высоких температур, либо применение катализаторов.
Классические металл-гидридные и неклассические 2-Н2 комплексы
Достаточно долго считалось, что водородные лиганды в комплексах переходных металлах существуют только в виде гидрид-анионов.
Сенсацией стало открытие Кубасом (Kubas) в 1984 году неклассической координации молекулы водорода в координационной сфере переходных металлов [15]. Объектом изучения были комплексы Mo(CO)3(PPri3)2 и W(CO)3(PPri3)2. В этих комплексах 18-электронное состояние центрального атома достигается за счет агостического взаимодействия металла с С-Н связью одного из изопропильного заместителя в фосфиновом лиганде. При взаимодействии этих комплексов с молекулой водорода агостическая связь заменяется на связь центрального атома с молекулой водорода за счет взаимодействия не заполненной орбитали центрально атома с электронами связывающей МО
водорода. Это приводит к образованию неклассического 2-Н2 лиганда.
105
Лиганд 2-Н2 занимает одно координнационное место в октаэдрической координационной сфере комплекса.
Расстояние Н-Н в таком состоянии составляет 0,82 А, что не многом больше межатомного расстояние в свободной молекуле водорода (0,74 А). Для сравнения: расстояние между гидридными лигандами в классических дигидридных косплексах находится на уровне 1,8 А.
Последующие за этим открытиям исследования позволили пересмотреть строение некоторых комплексов. Так, комплекс RuH4(PPh3)3 считался классическим тетрагидридным комплексом с редким координнационным числом 7. Теперь установлено, что это дигидридный,
2-Н2 комплекс с октаэдрической геометрией.
Это важное открытие с точки зрения механизма катализа реакций с участием молекулярного водорода. Дело в том, что обратное -
связывание в 2-Н2 комплексах приводит к ослаблению связи Н-Н в молекуле водорода и к понижению энергии активации ее диссоциации.
Например, для свободной молекулы водорода pKa составляет 35, а в 2- Н2 комплексах от 10 до -2.
Увеличение электронной плотности на центральном атоме приводит
к усилению обратного -связывание в 2-Н2 комплексах, что значительно облегчает окислительное присоединения водорода.
Комплексы практически всех переходных металлов проявляют каталитическую активность в реакциях гидрирования. Но наибольшей активность отличаются комплексы металлов VIII группы. Они эффективно
катализируют присоединение водорода по кратным связям (C=C, C C,
C=O, C N) в достаточно мягких условиях. Подбором металла и его лигандного окружения можно добиваться высокой селективности
гидрирования (например, селективное гидрирование связи C C до C=C; или гидрирование C=C в непредельных альдегидах не затрагивая связь C=O и пр.).
Для протекания реакции гидрирования водород должен войти в координационную сферу металла в виде гидрида. Введение гидрида может протекать по двум рассмотренным ранее механизмам: гетеролитическое и окислительное присоединение (гомолитическое присоединение).
Механизмы с окислительным присоединением водорода.
Окислительное присоединение сопровождается увеличением степени окисления металла и вхождением в координационную сферу гидридных лигандов. Следовательно, центральный атом должен иметь не высшую степень окисления, комплекс должен быть электронно-ненасыщенным а также иметь свободные координационные места. Поэтому наиболее активны в этой реакции плоскоквадратные d8-комлексы.
Например, для комплекса Вилкинсона RhI(PPh3)3Cl характерно окислительное присоединене водорода, сопровождающееся последующей диссоциацией одного трифенилфосфинового лиганда:
|
|
|
|
|
|
H |
- PPh3 R3P |
H |
|
||||||
R3P |
Cl |
H2 |
|
R3P |
|
H |
|
|
H |
|
|||||
|
|
|
|||||||||||||
|
Rh |
|
|
|
|
Rh |
|
|
|
|
Rh |
|
|||
|
|
|
|
|
|
|
|
|
|
||||||
R3P |
PPh3 |
|
|
|
R3P |
|
Cl |
|
|
|
R3P |
|
|
Cl |
|
|
16e |
|
|
|
|
PPh3 |
|
|
|
|
|
|
16e |
(3.33) |
|
|
|
|
|
|
18e |
|
|
|
|
|
|
||||
106
Образующийся в результате 16-электронный координационноненасыщенный гидридный комплекс является активным катализатором реакции гидрирования. После этого следует каталитический цикл (3.34).
Каталитический цикл проходит через стадии: координирования олефина, внедрения олефина по связи Rh-H (как правило, лимитирующая), восстановительного элиминирования продукта гидрирования, и, снова, окислительного присоединения водорода (регенерация катализатора).
|
18e |
|
H |
|
|
|
L3ClRhIII |
|
|
||
Диссо циация |
|
H |
|
||
|
+ L |
- L |
|
|
|
- L |
|
|
H |
|
|
О кислительн о е |
|
III |
|
||
|
|
|
|||
ï ðèñî åäèí åí èå |
L2ClRh |
|
Ï ðèñî åäèí åí èå |
||
16e |
H |
||||
H2 |
|||||
|
|
|
|
||
|
|
|
L2ClRhIII |
H |
|
16e L3ClRhI |
|
|
18e |
||
|
|
|
H |
||
|
L2ClRhIII |
H |
|
||
|
Вн едрен ие |
||||
|
|
|
|||
Во сстан о вительн о е |
|
|
|
|
|
ýëèì èí èðî âàí èå |
|
|
|
(3.34) |
|
+ L |
|
16e |
|
||
|
|
|
|||
На региоселективность гидрирования диенов до моноолефинов может влиять концентрация лигандов в реакционной массе. Рассмотрим пример гидрирования бутадиена при катализе комплексным ионом пентацианокобальтатом.
Гидридный комплекс образуется по реакции гомолитического присоединения [10]:
2[Co(CN)5]3- + H2 2[HCo(CN)5]3- |
(3.34.1) |
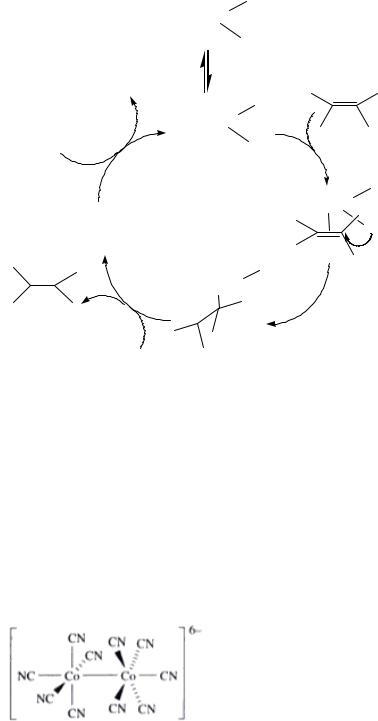
Исходный анион устойчив как в виде моноядерного комплекса |
|
(например K3[Co(CN)5]), так и в виде биядерного комплекса. |
И тот и |
другой имеют геометрию тетрагональной пирамиды [10]: |
|

107
Далее через стадии координирования бутадиена в координационную сферу и стадию внедрения его по связи Со-Н (сопровождающееся диссоциацией и последующим обратным координированием CNлиганда для соблюдения правила 16/18 электронов) образуется аллильный лиганд (С4Н7):
[HCo(CN)5]3- + С4Н6 [Co(CN)5(С4Н7)]3-
Продукт гидрирования образуется по реакции восстановительного элиминирования (обратной гомолитическому присоединению) при взаимодействии гидридного и аллильного комплексов:
[H-Co(CN)5]3- |
[H--- |
|
Co(CN)5]3- |
|
|||
|
|
|
2[Co(CN)5]3- + С4Н8 |
|
|
||
|
|
||
[(С4Н7)-Co(CN)5]3- |
[(С4Н7)--- |
|
Co(CN)5]3- |
|
|||
Каталитический цикл завершается по реакции (3.34.1). |
|||
Оказалось, что при |
высоком избытке цианид-ионов в растворе |
||
(CN-/Co = 10) с селективностью 90% образуется бутен-1, при низком избытке цианид-ионов (CN-/Co = 5) с селективностью 85% образуется транс-бутен-2.
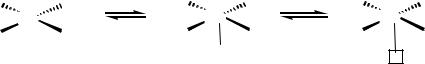
Это объясняется смещением , -равновесия комплекса в результате обратимой диссоциации цианид-иона:
CH3 |
|
|
|
H |
CH3 |
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
C |
|
|
|
|
|
|
|
|
CH3 |
|
|
|||
HC |
|
|
|
|
+CN - |
|
|
|
|
|
|
H2C |
|||||
|
|
(CN)4Co |
|
|
CH |
(CN) |
Co |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
CHCH=CH |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
||||||||||
CH |
|
|
|
|
|
|
-CN - |
5 |
|
|
|
|
2 |
|
CH |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
H C |
|
|
|
H2C |
|
|
|
|
|
|
|
H2C |
|||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
При низком избытке CN/Co в координационной сфере находится |
|||||||||||||||||
четыре CN- |
лиганда и |
-аллильный лиганд |
имеет возможность |
||||||||||||||
изомеризоваться в -аллильный, занимающий 2 координнационных места. На стадии восстановительного элиминирования из него получается бутен-2. При большом избытке цианид-ионов, равновесие смещается в сторону пяти-цианированного комплекса. В таком комплексе остается только одно координнационное место и, соответственно, углеводородный
лиганд может существовать только в виде -лиганда. Такой лиганд приводит к образованию только бутена-1.
Механизмы с гетеролитическим присоединением водорода.
Такой механизм гидрирования характерен, когда в системе имеются «основные центры», принимающие протон при гетеролитическом разрыве молекулы водорода.
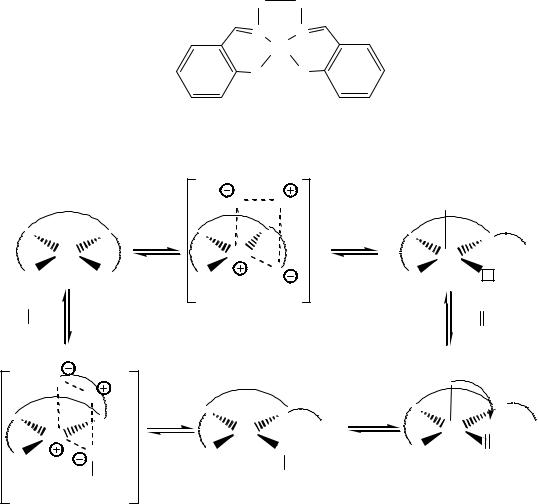
Например, в комплексе Pd(salen) таким центром является фенольный кислород лиганда, а механизм гидрирования схож с действием природного фермента гидрогеназы.
Pd(salen)
N,N’-этиленбис(салицилимин)
108
H2C |
CH2 |
N |
N |
|
Pd |
OO
Вупрощенном виде механизм гидрирования может быть представлен следующим каталитическим циклом:
|
|
|
|
H |
H |
|
H |
|
|
|
N |
N |
+ H2 |
N |
N |
|
N |
N |
|
|
|
|
OH |
||||||
|
Pd |
O |
|
Pd |
O |
|
Pd |
|
|
|
O |
|
O |
|
O |
|
|
||
- |
CHR2 |
|
|
|
|
|
|
CR2 |
|
CHR2 |
|
|
|
|
|
|
+ CR2 |
|
|
|
O |
H |
|
|
|
|
H |
|
|
N |
|
|
N |
N |
|
N |
N |
|
|
|
N |
|
|
OH |
|||||
|
|
OH |
Pd |
CR2 |
|||||
|
Pd |
|
|
Pd |
|
|
|||
O |
CR2 |
|
O |
CR2 |
|
O |
CR2 |
|
|
|
|
|
|
||||||
|
|
|
CHR2 |
|
|
||||
|
|
CHR2 |
|
|
|
|
|
||
Молекула водорода гетеролитически, через четырехцентровое переходное состояние, присоединяется к комплексу Pd(salen). При этом гидридный лиганд входит в координационную сферу комплекса, а протон присоединяется к фенолятной группе хелатного лиганда. Образовавшаяся фенольная группа теряет связь с центральным атомом. На свободное координационное место присоединяется алкен, который далее по механизму миграционного внедрения взаимодействует с гидрирдом, образуя этильный лиганд. Заканчивается каталитический цикл присоединением протона фенольной группы хелатного лиганда к алкильному лиганду, а фенолятной группы к центральному атому (гетеролитическое присоединение ОН группы через четырехцентровое переходное состояние).
Факторы, влияющие на эффективность катализатора.
В реакциях гидрирования, как правило, лимитирующей стадией является стадия внедрения ненасыщенного лиганда по связи металл-
гидрид. |
мягких катализаторов (то есть комплексов |
В присутствии |
металлов d8 – d10 в низших степенях окисления) в мягких условиях селективно гидрируются мягкие субстраты (олефины, диены, ацетилены),
а более жесткие непредельные группы (СН=О, СООН, С N) не затрагиваются.
Если лимитирующей стадией каталитического цикла является нуклеофильная атака гидрид-анионом на атом, находящийся при кратной
109
связи, то лигандое окружение, повышающее электронную плотность на Н-, приводит к увеличению скорости реакции. Так, для комплекса RhL3Cl наблюдается следующий ряд активности комплекса в зависимости от природы L:
L:I- > Br- > Cl-
рост скорости
рост мягкости L
От хлорида к йодиду увеличивается мягкость лиганда, т.е. его электроно-донорные свойства. Это приводит к повышению нуклеофильности Н- и увеличивает скорость реакции.
В ряде случаев лимитирующей стадией может быть окислительное присоединение. Например, при гидрировании циклогескена на фосфиновом комплексе родия Rh(L)3Cl был получен следующий ряд относительной активности [13, 14]:
L: Относительная активность
Повышение активности комплекса с повышением электроно-донорных
свойств лигандов связывают с увеличением скорости |
лимитирующей |
|||
стадии – окислительного присоединения водорода. |
|
|||
Однако, следует отметить, что в предыдущем примере такое же |
||||
электронное |
влияние |
лигандов |
(галоген-анионов) |
объяснялось |
лимитированием реакции стадией внедрения. Это говорит о том, что в реакциях гидрирования электронное влияние заместителей до конца не выяснено.
Заместители в субстрате, понижающие электронную плотность кратной связи (т.е. увеличивающие электрофильность внедряемого лиганда), также способствуют увеличению скорости. Например, аллилацетат гидрируется легче, чем 1-гексен из-за электроноакцепторного влияния сложноэфирной группы.
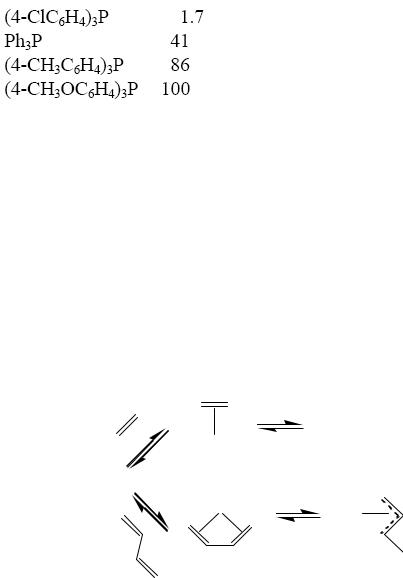
Концепция ЖМКО хорошо объясняет влияние природы лигандов на селективность в конкурирующем восстановлении олефинов и диенов:
LnPt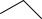
HPtLn
HPtLn
HPtLn |
LnPt |
(3.35)
Гидрирование олефинов протекает через промежуточное образование-алкильного лиганда (более жесткое основание), а гидрирование диена
110
- через образование -аллильного (более мягкое основание). Поэтому наличие мягких лигандов, таких как PR3, CO, [SnCl3]- и др., в координационной сфере катализатора, приводит к повышению селективности гидрирования диенов в присутствии моноолефинов.
Энантиоселективное гидрирование.
Чем крупнее лиганд, тем сильнее его пространственное влияние на другие лиганды комплекса. На этом основано применение оптическиактивных замещенных фосфиновых лигандов, характеризующихся высокими значеними конусного угла (или угла захвата – для бидентантных лигандов), для энантиоселективного гидрирования прохиральных соединений. Так, например, используя в качестве катализатора комплекс родия(I) с лигандом 1,5-гексадиеном и двумя хиральными фосфиновыми лигандами следующего строения (L):
Кат ализат о р: |
|
L Rh |
|
|
|
+ |
- |
L: |
*P |
|
CH |
|
|
|
|
|
|||||||||
|
|
|
||||||||||
|
|
|
|
|
BF4 |
|
||||||
|
|
|
|
|
|
|||||||
|
|
|
|
|
||||||||
|
2 |
|
|
|
|
|
|
3 |
||||
OCH3
Нойлесу (Knowles) и сотр. удалось прогидрировать , -ненасыщенную N-
ацилированную -аминокислоту стереоспецифически и получить L-форму продукта с 80-90% селективностью:
|
|
|
|
|
|
|
H |
|
|
COOH |
H2 |
|
|
|
|
|
|
|
|
|
|
|
H2 |
* |
COOH |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
AcO |
|
|
|
|
C |
|
C |
|
|
|
|
AcO |
|
|
|
|
|
|
|
|
C |
|
|
CH |
|
|
||||||
|
|
|
|
|
|
|
Катализато р |
|
|
|
|
|
NHCOR |
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
NHCOR |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
H3CO |
|
|
|
|
|
|
|
|
||||||||||||
H CO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
3 |
|
|
|
|
I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2 |
* |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
C |
|
|
CH |
NHCOR |
(3.36) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-DOPA |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Данная |
|
реакция имеет |
очень |
большое |
практическое значения в |
|||||||||||||||||||||||||||
технологии тонкого органического синтеза, а именно в процессе производства L-DOPA (3,4-диоксифенил-L-аланин) - лекарства для
лечения болезни Паркинсона. |
|
|
|
|
||
|
Наиболее эффективным на сегодняшний день является процесс |
|||||
получения |
L-DOPA, разработанный |
фирмой |
«Monsanto». |
Авторы этого |
||
изобретения Уильям Нойлес, Рьойи Нойори и |
Барри Шарплесс получили |
|||||
за |
него |
Нобелевскую |
премию |
2001 |
года. |
Катализатором |
энантиоселективного гидрирования в данной технологии является катионный родиевый комплекс, содержащий хиральный фосфиновый лиганд DIPAMP следующего строения:

111
OMe
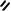 P P
P P
MeO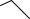

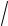
(S)-(2-метоксифенил)-[2-[(2- метоксифенил)-фенилфосфанил]этил]-фенилфосфан
Этот катализатор обеспечивает высокую селективность образования желаемого оптически активного продукта гидрирования (соотношение L
(S) и D (R) изомеров составляет 98:2). Благодаря наличию в комплексе ассиметричного хелатного лиганда при координировании субстрата образуются два диастереомера:
II |
III |
|
Следует отметить важную роль ацетамидной группы, которая |
||
участвует в образовании донорно-акцепторной связи |
наряду с |
|
олефиновой группой. |
стереоизомеры комплекса с субстратом |
образуются |
При этом R и S |
||
в соотношении 9 к 1. Но, не смотря на такой большой концентрационный избыток «ненужного» комплекса, целевой стереоизомер продукта (L(S)- DOPA) образуется с селективностью 98%. Это объясняется тем, что
гидрирование |
S-энантиомера |
комплекса |
имеет |
меньшую |
энергию |
активации, что |
приводит к значительно более высокому значению TOF и, |
||||
в итоге, высокой энантиоселективности. Упрощенно |
каталитический цикл |
||||
энантиоселективного гидрирования I представлен ниже:

112
После координирования субстрата образуется комплекс (9.19) и (9.20) (или III и II – на предыдущем рисунке) с соотношением S и R диастереомеров 1:9, так как «ненужный» комплекс имеет меньшую энергию, следовательно – он более стабилен. Лимитирующей стадией каталитического цикла является окислительное присоединение водорода (т.е. образование комплексов (9.21) и (9.22)). На этой стадии энергии активации различаются для комплексов (9.19) и (9.20). S- энантиомерный комплекс имеет Еа ниже, чем R-энантиомер, поэтому константы скорости и TOF на стадии окислительного присоединения (и процесса в целом) для S-энантиомера значительно выше (приблизительно в 600 раз). Это приводит к образованию L(S)-DOPA с селективностью 98%.
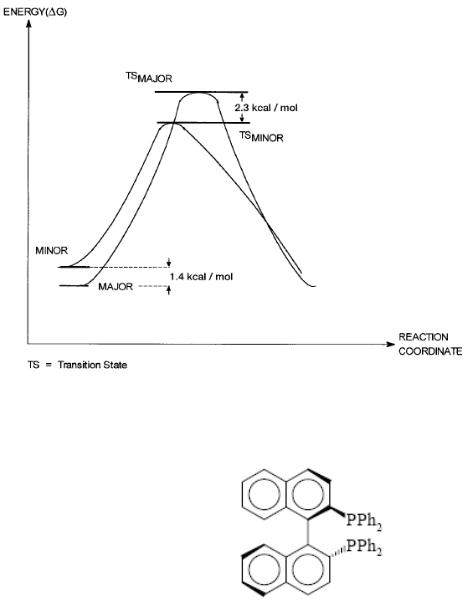
Кинетика и термодинамика стадии окислительного присоединения
водорода была изучена на модельной реакции гидрирования метил- - ацетамидоциннамата с тем же катализатором и была получена нижеследующая энергетическая диаграмма реакции, объясняющая наблюдаемый эффект селективного энантиогидрирования:
Кат., +Н2
113
Еще один хиральный лиганд, используемый в виде комплексов с RuII и RhI для промышленных синтезов лекарственных препаратов, это BINAP:
3.3.2.ИЗОМЕРИЗАЦИЯ ОЛЕФИНОВ
Различают два типа механизмов изомеризации олефинов с миграцией двойной связи:
-металл-алкильный
-металл-аллильный
Изомеризацию по металл-алкильному механизму катализируют гидридные комплексы металлов (например [НCo(CO)4], [HRh(CO)(PPh3)3]), которые образуются по одной из рассмотренных в предыдущем разделе реакций введения водорода в координационную сферу металла. Источником водорода для образования исходного активного гидридного комплекса может служить либо молекула водорода, либо вещество,
содержащее подвижный |
атом водорода, |
например, |
следующие системы: |
|
[Co2(CO)8]/H2, [Ni(P(OEt)3)4]/H2SO4. |
в |
практике |
промышленного |
|
Наибольшее |
значение |
|||
металлокомплексного катализа имеет реакция изомеризации первичных олефинов во вторичные.
