
- •Мономеры для поликонденсации
- •Содержание
- •Глава 1 отличительные признаки поликонденсации 9
- •Глава 2 мономеры и олигомеры для процессов поликонденсации 22
- •Глава 3 пути синтеза поликонденсационных мономеров. 39
- •Глава 4 лабораторные работы по синтезу мономеров 52
- •Введение
- •Отличительные признаки поликонденсации
- •Классификация процессов синтеза полимеров
- •Определение процессов полимеризации и поликонденсации
- •Мономеры и олигомеры для процессов поликонденсации
- •Мономеры Функциональность мономеров.
- •Классификация мономеров.
- •Олигомеры для процессов поликонденсации
- •Реакционная способность мономеров и олигомеров.
- •Пути синтеза поликонденсационных мономеров.
- •Традиционные методы синтеза мономеров. Синтез мономеров типа а–b (мономеров для гомополиконденсации) из соединений типаa–oi.
- •Синтез мономеров типа а–b (мономеров для гомополиконденсации) из соединений типа b–b.
- •Синтез мономеров типа а–а (мономеров для гетерополиконденсации) из соединений типа а–о.
- •Синтез мономеров типа а–а (мономеров для гетерополиконденсации) из соединений типа b–b.
- •Особые реакции синтеза бифункциональных соединений.
- •Особенности реакций синтеза мономеров.
- •Образование реакционных центров в процессах поликонденсации.
- •Лабораторные работы по синтезу мономеров
- •Химизм процесса,
- •Лабораторная работа № 1. Синтез дифенилсиландиола в присутствии эпихлоргидрина, как акцептораHCl.
- •Порядок работы.
- •Проведение эксперимента.
- •Задание
- •Лабораторная работа № 2. Синтез дифенилсиландиола в присутствии бикарбоната натрия,как акцептораHCl.
- •Порядок работы.
- •Проведение эксперимента.
- •Задание
- •Литература
Отличительные признаки поликонденсации
Московская Государственная Академия Тонкой химической технологии им. М.В. Ломоносова
П.В. Иванов, В.И. Маслова, Н.Б. Сокова
Мономеры для поликонденсации
Методическая разработка по дисциплине "Основы физики и химии ВМС"
Москва 2000
ББК 24.7
УДК 541.6
Иванов П.В., Маслова В.И., Сокова Н.Б.
Мономеры для поликонденсации.
Методическая разработка по дисциплине " Основы физики и химии высокомолекулярных соединений ", 1 изд., МИТХТ, 2000 г., 50 с.
Под общей редакцией доцента Иванова П.В.
Рецензенты - д.х.н, профессор Прокопов Н.И.
Пособие предназначено для изучения и практического освоенияраздела дисциплины "Основы физики и химии высокомолекулярных соединений", изучаемой в бакалавриате МИТХТ на четвертом году обучения. Пособие состоит из нескольких глав. В первой главе рассматриваются особенности и отличия поликонденсации от полимеризации. Во второй главе рассматриваются вопросы классификации мономеров, методов их синтеза, свойств и особенностей. Учебнаяразработка посвящена усвоению материала, касающегося проблеме синтеза мономеров для поликонденсации. Особенное внимание уделяется специфике образования кремнийорганических мономеров – органосиланолов в процессе гидролитической поликонденсации органохлорсиланов. Теоретическое изучение вопроса закрепляется практическими лабораторными занятиями по синтезу дифенилсиландиола.
Московская Государственная Академия Тонкой химической технологии им. М.В. Ломоносова, 2000.
Содержание
ВВЕДЕНИЕ 4
Глава 1 отличительные признаки поликонденсации 9
Классификация процессов синтеза полимеров 9
Определение процессов полимеризации и поликонденсации 12
Глава 2 мономеры и олигомеры для процессов поликонденсации 22
МОНОМЕРЫ 27
Функциональность мономеров. 27
Классификация мономеров. 30
Олигомеры для процессов поликонденсации 33
Реакционная способность мономеров и олигомеров. 34
Глава 3 пути синтеза поликонденсационных мономеров. 39
Традиционные методы синтеза мономеров. 39
Синтез мономеров типа а–b (мономеров для гомополиконденсации) из соединений типа a–o. 39
Синтез мономеров типа а–b (мономеров для гомополиконденсации) из соединений типа b–b. 40
Синтез мономеров типа а–а (мономеров для гетерополиконденсации) из соединений типа а–о. 40
Синтез мономеров типа а–а (мономеров для гетерополиконденсации) из соединений типа b–b. 41
Особые реакции синтеза бифункциональных соединений. 42
Особенности реакций синтеза мономеров. 43
Образование реакционных центров в процессах поликонденсации. 47
Глава 4 лабораторные работы по синтезу мономеров 52
Химизм процесса, 52
Лабораторная работа № 1. Синтез дифенилсиландиола в присутствии эпихлоргидрина, как акцептора HCl. 57
Порядок работы. 58
Проведение эксперимента. 59
Задание 59
Лабораторная работа № 2. Синтез дифенилсиландиола в присутствии бикарбоната натрия,как акцептора HCl. 61
Порядок работы. 62
Проведение эксперимента. 63
Задание 63
Введение
Любой полимерный материал состоит из высокомолекулярного соединения - полимера. Синтез полимеров можно осуществить либо из низкомолекулярных соединений – мономеров, либо из высокомолекулярных соединений путем полимераналогичных превращений.В настоящее время известны два основных метода синтеза полимеров изнизкомолекулярных соединений: поликонденсация и полимеризация.Все остальные случаи синтеза полимеров, например полиприсоединение, поликоординация, полирекомбинация, являются частными случаями (или разновидностями) этих двух процессов.
Исходными соединениями для синтеза полимеров являются мономеры или олигомеры. Помимо мономеров при получении полимеров в реальных условиях применяют и другие соединения: инициаторы, катализаторы, растворители и т. п. Совокупность этих соединений называется реакционной системой, а сами участники процесса – компонентами реакционной системы. Компоненты реакционной системы можно разделить на три основные группы. К первой группеследует отнести реакционноспособные компоненты (реагенты)– исходные мономеры,олигомеры, активные полимерные цепи и добавки – катализаторы, инициаторы. Ко второй группе относятся продуктыпроцесса – неактивныемакромолекулы полимера и иногда образующиеся в процессе синтеза низкомолекулярные соединения (например, вода, галогеноводород, аммиак, спирт). Третью группу составляют такие нереакционные компоненты, как растворитель, поверхностно-активные добавки и т. д. Компоненты этой группы служат для регулирования соотношения скоростей реакций, протекающих в реакционной системе.
Изменения, происходящие в реакционной системе, вследствие которых происходит превращение молекул мономеров в молекулы полимера (макромолекулы), называются процессами синтеза полимера. В результате синтеза получается продукт с различной степенью поликонденсации или полимеризации (n). Степень поликонденсации (или полимеризации) непосредственно связана смолекулярной массой полимера:
Мол. масса полимера = nМ,
где n–степень поликонденсации (полимеризации); М – молекулярная масса мономерного звена (или остатка.).
На практике обычно стараются получить продукт с достаточно большой молекулярной массой. Иногда необходимо синтезировать полимер с точно заданными молекулярной массой и молекулярно-массовым распределением, определенной химической (распределениемономерных звеньев по длине цепи) и физической (аморфная, кристаллическая) структурой. Чем разнообразнее требования, предъявляемые к полимеру, тем сложнее процесс его синтеза и, как правило, сложнее реакционная система. Множество реакций, составляющих процесс синтеза макромолекул, можно разделить на три группы, называемыестадиями:
образование (зарождение) реакционных центров;
образование (сборка) макромолекул;
прекращение образования макромолекул.
Каждая стадия может включать в себя одну или несколько химических реакций. Понятие о стадиях является очень важным, так как позволяет правильно ориентироваться во всем многообразии сложных процессов синтеза полимеров.Стадия образования реакционных центров состоит в создании в молекуле реагента (мономера, олигомера) реакционных центров (т. е. активных мест), способных взаимодействовать с молекулами того же или другого реагента.Стадия образования макромолекул состоит в наращивании цепи от мономера до высокомолекулярного полимера. Стадия прекращения образования макромолекулзаключается в дезактивации реакционных центров растущих макромолекул. Это наиболее важная стадия определяет величину молекулярной массы полимера, достигаемую в ходе синтеза.
Все три стадии процесса синтеза полимера протекают, как правило, по одному механизму, то есть являются превращениями реакционных центров одного типа на всех стадиях (например, ионов, радикалов и т. д.). Стадийность процесса синтеза полимеров удобноизобразить графически (рис. 1).

Рис. 1. Схема стадийности процесса синтеза макромолекулы полимера (пояснения см. в тексте)
Так, если на оси абсцисс отложить число последовательно протекающих элементарных реакций i, вследствие которых происходитобразование единичной макромолекулы, а на оси ординат–степеньполиконденсации или полимеризации получающейся макромолекулы,то схематически процесс синтеза полимера, включающего все три стадии, изобразится ломаной кривой ОАВС. На этой кривой точка О отвечает исходному мономеру (n=1), участок ОА –стадии образованияреакционных центров, причем его длина равна числу протекающихна этой стадии реакций (например, трем), участок АВ – стадии образования макромолекулы, участокВС–стадии прекращения образования макромолекул. Стадия образования макромолекулы (линияАВ) изображена на рисунке в виде прямой линии. Это простейший вариант. На самом деле зависимость степени поликонденсации отчисла последовательно протекающих реакций образования макромолекулы не всегда является прямой, а может иметь иную форму функциональной зависимости. Несмотря на ряд упрощений, постадийная схема процессов синтеза позволяет более наглядно представить себе характер того или иного процесса. На рис. 2а показан один из наиболее простых вариантов синтеза полимера: исходное соединение непосредственно начинает образовывать макромолекулу, посколькупервые же реакции приводят к увеличениюn.
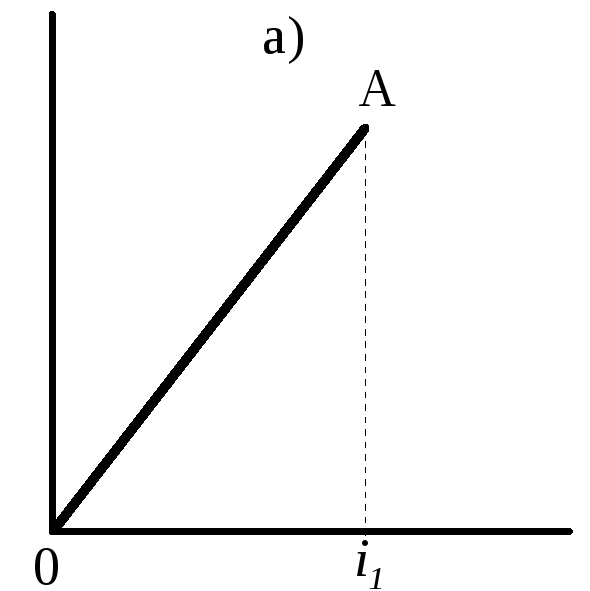

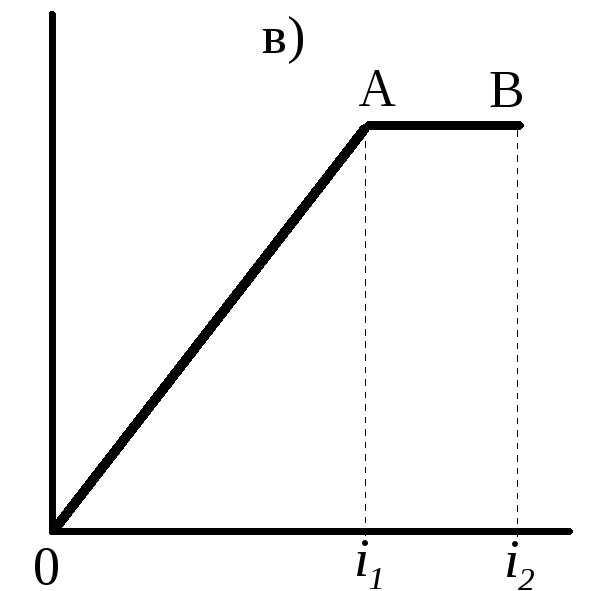
Число реакций, i
Рис. 2. Простевшие варианты процессов синтеза макромолекулы полимера (пояснения см. в тексте).
Нарастание цепи (молекулярной массы) продолжается до точкиА; этот процесс состоит из i1 последовательных реакций. Макромолекулы в точке А активны, они способны к дальнейшему росту. Нарис. 2б показан процесс, в котором исходное соединение, прежде чем образовать макромолекулу, претерпевает ряд (i1) превращений.Это значит, что исходное соединение содержало функциональныегруппы, не способные непосредственно образовывать полимернуюцепь. Поэтому и потребовалось i1 реакций, чтобы создать в нем те реакционные центры, которые способны к образованию полимеров. Далее следует стадия образования макромолекулы, состоящая изi2–i1 элементарных реакций. На рис. 2в показано, что активные концы образовавшихся макромолекул (точка А) продолжают реагировать(участок АВ, но при этом не происходит увеличения n. Рассмотренные стадии процесса имеют место как в поликонденсации, так и в полимеризации.
