
- •Магнитная индукция
- •Направление линий магнитной индукции
- •Сила ампера
- •Действие магнитного поля на рамку с током
- •Формула — 1 Магнитный момент витка
- •Правило Ленца
- •Применение правила Ленца
- •Интерференция света
- •Классическое объяснение явления[
- •Использование.
- •1.1. Законы теплового излучения
- •0,7 Мкм) при таких температурах имеет слишком малую энергию и не может быть обнаружено невооруженным глазом.
- •Строение атома
- •Квантовые постулаты нильса бора
- •Закон радиоактивного распада
Строение атома
Модель
атома Томсона
1897
г.- Дж. Томсоном выдвинута модель строения
атома.
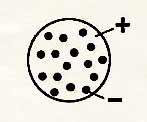 Атом
имеет форму шара. По
всему объему атома
с постоянной плотностью
распределен положительный
заряд.
Внутри (как изюм в кексе) расположены
электроны.
В целом атом электрически
нейтрален.
Когда электроны колеблются
относительно центра сферы, атом излучает
свет.
Опыт
Резерфорда по рассеянию альфа-частиц
1906
г. - Э. Резерфорд проводит опыты для
проверки состоятельности модели атома
Томсона:
Атом
имеет форму шара. По
всему объему атома
с постоянной плотностью
распределен положительный
заряд.
Внутри (как изюм в кексе) расположены
электроны.
В целом атом электрически
нейтрален.
Когда электроны колеблются
относительно центра сферы, атом излучает
свет.
Опыт
Резерфорда по рассеянию альфа-частиц
1906
г. - Э. Резерфорд проводит опыты для
проверки состоятельности модели атома
Томсона:
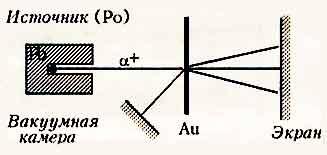 В
вакууме в свинцовом стакане располагался
источник радиоактивного излучения
(альфа-частиц) - полоний(Ро).
Тонкая золотая
фольга бомбардировалась
положительно заряженными альфа-частицами,
скорость которых около 20 ООО км /с.
На
экране регистрировались вспышки от
попадания на него альфа-частиц.
Кроме
основного экрана следы от альфа-частиц
были зафиксированы и на
боковых экранах.
В
вакууме в свинцовом стакане располагался
источник радиоактивного излучения
(альфа-частиц) - полоний(Ро).
Тонкая золотая
фольга бомбардировалась
положительно заряженными альфа-частицами,
скорость которых около 20 ООО км /с.
На
экране регистрировались вспышки от
попадания на него альфа-частиц.
Кроме
основного экрана следы от альфа-частиц
были зафиксированы и на
боковых экранах.
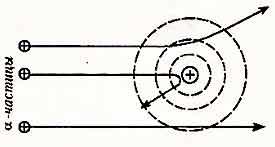
Зная о том, как взаимодействуют одноименно заряженные частицы, а они отталкиваются друг от друга, можно объяснить результаты опыта Резерфорда: - частицы, которые отклонялись, пролетали недалеко от ядра - частицы, которые отражались, попадали точно в ядро - частицы, которые не испытывали отклонений, пролетали далеко от ядра Понимание причин отклонения альфа-частиц позволило Э.Резерфорду выдвинуть собственную планетарную (иначе ядерную) модель строения атома.
73
Квантовые постулаты нильса бора
Опыты
подтвердили правильность ядерной модели
атома Резерфорда, поэтому ученым пришлось
признать ограниченность применения
законов классической физики.
Первым
решился на это признание выдающийся
физик XX в. датский ученый Нильс Бор. В
1913 г. он, основываясь на разрозненных
экспериментальных фактах, с помощью
гениальной интуиции сформулировал в
виде постулатов основные положения
новой теории.
Изучая
противоречия модели атома Резерфорда
законам классисической физики Нильс
Бор в
1913 г. выдвигает "постулаты",
определяющие строение атома и условия
испускания и поглощения им электромагнитного
излучения.
Постулаты Бора показали,
что атомы "живут" по законам
микромира.
I
постулат - постулат
стационарных состояний:
В
атоме существуют стационарные квантовые
состояния, не изменяющиеся с течением
времени без внешнего воздействия на
атом.
В этих состояниях атом не излучает
электромагнитных волн, хотя и движется
с ускорением.
Каждому стационарному
состоянию атома соответствует определенная
энергия атома.
Стационарным состояниям
соответствуют стационарные орбиты, по
которым движутся электроны.
II
постулат - правило
частот:
При
переходе атома из одного стационарного
состояния в другое излучается или
поглощается 1 фотон.
а) Атом излучает
1 фотон(который несет 1 квант энергии),
когда электрон переходит из состояния
с большей энергией (Е k) в состояние с
меньшей энергией (Е n).
Энергия
излученного фотона:
![]() Здесь
(Ek - En) - разность энергий стационарных
состояний.
При Ек
> Eп происходит
излучение фотона.
Частота
излучения:
Здесь
(Ek - En) - разность энергий стационарных
состояний.
При Ек
> Eп происходит
излучение фотона.
Частота
излучения:
 где
k и n - номера стационарных состоянии,
или главные квантовые числа.
б) Атом
поглощает 1 фотон, когда переходит из
стационарного состояния с меньшей
энергией (E n) в стационарное состояние
с большей энергией (E k).
При Ек
< Еn происходит
поглощение фотона.
После
экспериментальных проверок правильности
модели атома Резерфорда и принятия
постулатов Бора ученым пришлось признать
ограниченность применения законов
классической физики для микроскопических
тел.
Модель
атома водорода по Бору
Свои
постулаты Н. Бор применил для построения
теории строения простейшего атома
(атома водорода).
Согласно этой
теории Бор смог
вычислить для
атома водорода:
- возможные радиусы
орбит электрона и размеры атома
-
энергии стационарных состояний атома
-
частоты излучаемых и поглощаемых
электромагнитных волн.
Распределение
энергетических уровней при излучении
(испускании) и поглощении атомом водорода
электромагнитных волн:
где
k и n - номера стационарных состоянии,
или главные квантовые числа.
б) Атом
поглощает 1 фотон, когда переходит из
стационарного состояния с меньшей
энергией (E n) в стационарное состояние
с большей энергией (E k).
При Ек
< Еn происходит
поглощение фотона.
После
экспериментальных проверок правильности
модели атома Резерфорда и принятия
постулатов Бора ученым пришлось признать
ограниченность применения законов
классической физики для микроскопических
тел.
Модель
атома водорода по Бору
Свои
постулаты Н. Бор применил для построения
теории строения простейшего атома
(атома водорода).
Согласно этой
теории Бор смог
вычислить для
атома водорода:
- возможные радиусы
орбит электрона и размеры атома
-
энергии стационарных состояний атома
-
частоты излучаемых и поглощаемых
электромагнитных волн.
Распределение
энергетических уровней при излучении
(испускании) и поглощении атомом водорода
электромагнитных волн:
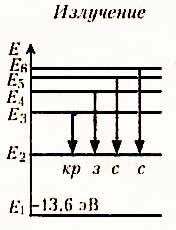 ....
.... При
(n = 1) - основное энергетическое состояние,
ему соответствует радиус орбиты электрона
r = 0,5 • 10 -11 м.
При
(n больше 1) - возбужденные состояния.
При
поглощении атомом кванта энергии
(фотона) атом переходит в возбужденное
состояние, при этом электрон переходит
на более отдаленную орбиту и его связь
с ядром слабеет.
Переходы в первое
возбужденное состояние (Е2) с верхних
уровней соответствует частотам видимой
части (кр з с с) спектра водорода.
Линечатый спектр
атома водорода состоит
из линий, сгруппированных в
серии.
При
(n = 1) - основное энергетическое состояние,
ему соответствует радиус орбиты электрона
r = 0,5 • 10 -11 м.
При
(n больше 1) - возбужденные состояния.
При
поглощении атомом кванта энергии
(фотона) атом переходит в возбужденное
состояние, при этом электрон переходит
на более отдаленную орбиту и его связь
с ядром слабеет.
Переходы в первое
возбужденное состояние (Е2) с верхних
уровней соответствует частотам видимой
части (кр з с с) спектра водорода.
Линечатый спектр
атома водорода состоит
из линий, сгруппированных в
серии.
 Частоты
каждой серии спектра можно подсчитать
по формуле Бальмера-Ритберга:
Частоты
каждой серии спектра можно подсчитать
по формуле Бальмера-Ритберга: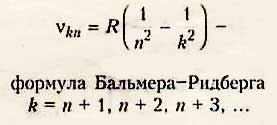 В
спектре водорода обнаружены следующие
серии:
n = I - серия Лаймана -
ультрафиолетовое излучение
n = 2 - серия
Бальмера -
видимое излучение
n = 3 - серия Пашена
- инфракрасное излучение
В
спектре водорода обнаружены следующие
серии:
n = I - серия Лаймана -
ультрафиолетовое излучение
n = 2 - серия
Бальмера -
видимое излучение
n = 3 - серия Пашена
- инфракрасное излучение
75
Формула де
Бройля устанавливает
зависимость длины волны ![]() ,
связанной с движущейся частицей вещества,
от импульса
,
связанной с движущейся частицей вещества,
от импульса ![]() частицы:
частицы:
![]()
где ![]() —
масса частицы,
—
масса частицы, ![]() —
ее скорость,
—
ее скорость, ![]() — постоянная
Планка.
Волны, о которых идет речь, называютсяволнами
де Бройля.
— постоянная
Планка.
Волны, о которых идет речь, называютсяволнами
де Бройля.
Другой вид формулы де Бройля:
![]()
где ![]() —
волновой вектор, модуль которого
—
волновой вектор, модуль которого![]() —
волновое число — есть число длин
волн, укладывающихся на
—
волновое число — есть число длин
волн, укладывающихся на ![]() единицах
длины,
единицах
длины, ![]() —
единичный вектор в направлении
распространения волны,
—
единичный вектор в направлении
распространения волны, ![]() Дж·с.
Дж·с.
Длина волны
де Бройля для
нерелятивистской частицы с массой ![]() ,
имеющей кинетическую энергию
,
имеющей кинетическую энергию ![]()
![]()
В
частности, для электрона, ускоряющегося
в электрическом поле с разностью
потенциалов ![]() вольт
вольт
![]()
Формула де Бройля экспериментально подтверждается опытами по рассеянию электронов и других частиц на кристаллах и по прохождению частиц сквозь вещества. Признаком волнового процесса во всех таких опытах является дифракционная картина распределения электронов (или других частиц) в приемниках частиц.
Волновые свойства не проявляются у макроскопических тел. Длины волн де Бройля для таких тел настолько малы, что обнаружение волновых свойств оказывается невозможным. Впрочем, наблюдать квантовые эффекты можно и в макроскопическом масштабе, особенно ярким примером этому служат сверхпроводимость и сверхтекучесть.
Фазовая скорость волн де Бройля свободной частицы
![]()
где ![]() —
циклическая частота,
—
циклическая частота, ![]() —
кинетическая энергия свободной
частицы,
—
кинетическая энергия свободной
частицы, ![]() —
полная (релятивистская) энергия
частицы,
—
полная (релятивистская) энергия
частицы,  —
импульс частицы,
—
импульс частицы, ![]() ,
, ![]() —
её масса и скорость соответственно,
—
её масса и скорость соответственно, ![]() —
длина дебройлевской волны. Последние
соотношения — нерелятивистское
приближение. Зависимость фазовой
скорости дебройлевских
волн от длины волны указывает на то, что
эти волны испытываютдисперсию. Фазовая
скорость
—
длина дебройлевской волны. Последние
соотношения — нерелятивистское
приближение. Зависимость фазовой
скорости дебройлевских
волн от длины волны указывает на то, что
эти волны испытываютдисперсию. Фазовая
скорость ![]() волны
де Бройля хотя
и больше скорости света, но относится
к числу величин, принципиально неспособных
переносить информацию (является чисто
математическим объектом).
волны
де Бройля хотя
и больше скорости света, но относится
к числу величин, принципиально неспособных
переносить информацию (является чисто
математическим объектом).
Групповая
скорость волны
де Бройля ![]() равна
скорости частицы
равна
скорости частицы ![]() :
:
![]() .
.
Связь
между энергией частицы ![]() и
частотой
и
частотой ![]() волны
де Бройля
волны
де Бройля
![]()
Волны де Бройля имеют специфическую природу, не имеющую аналогии среди волн, изучаемых в классической физике: квадрат модуля амплитуды волны де Бройля в данной точке является мерой вероятности того, что частица обнаруживается в этой точке. Дифракционные картины, которые наблюдаются в опытах, являются проявлением статистической закономерности, согласно которой частицы попадают в определенные места в приёмниках — туда, гдеинтенсивность волны де Бройля оказывается наибольшей. Частицы не обнаруживаются в тех местах, где, согласностатистической интерпретации, квадрат модуля амплитуды «волны вероятности» обращается в нуль.
76
Соотношение неопределенностей
Пример. Пусть ![]() .
Тогда
.
Тогда
![]() ,
,
и мы получаем соотношение неопределенностей Гейзенберга:
![]() .
Кинематика вращательного движения
твердого тела Абсолютно твердым телом
называется тело, деформациями которого
в условиях данной задачи можно пренебречь
.
Кинематика вращательного движения
твердого тела Абсолютно твердым телом
называется тело, деформациями которого
в условиях данной задачи можно пренебречь
Качественно
СН может быть получено из анализа
эволюции волнового пакета (см. п. 2). Было
показано, что эффективные размеры пакета
в координатном и импульсном представлениях,
т.е. неопределенности координаты и
импульса частицы, связаны соотношением ![]() ,
или
,
или![]() ,
так как импульс
,
так как импульс![]() .
Детальный
анализ показывает, что в случае
некоммутирующих наблюдаемых
.
Детальный
анализ показывает, что в случае
некоммутирующих наблюдаемых![]() и
и![]() измерение
одной из них приводит к неконтролируемому
изменению другой наблюдаемой. Возмущение
системы в процессе измерения конечно
и таково, что всегда выполняются СН.
Иными словами, для точного измерения
таких наблюдаемых требуются несовместимые
измерительные приборы.
измерение
одной из них приводит к неконтролируемому
изменению другой наблюдаемой. Возмущение
системы в процессе измерения конечно
и таково, что всегда выполняются СН.
Иными словами, для точного измерения
таких наблюдаемых требуются несовместимые
измерительные приборы.
Найдем
состояния ![]() ,
в которых достигается минимум
неопределенностей,т.е. точное равенство
в СН. Получаем для них систему уравнений
(см. выше вывод СН):
,
в которых достигается минимум
неопределенностей,т.е. точное равенство
в СН. Получаем для них систему уравнений
(см. выше вывод СН):
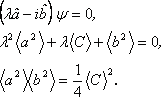
Отсюда находим
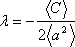 ,
,
и уравнение для определения состояния, минимизирующего произведение неопределенностей, принимает вид:
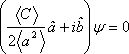 .
.
Основные положения квантовой механики Состояние квантовой системы и волновая функция. Вероятностная интерпретация волновой функции. Принцип суперпозиции. Соответствие между физическими величинами и операторами. Физический смысл собственных функций и собственных значений. Операторы координаты, импульса и энергии. Временн?е уравнение Шредингера. Нестационарные и стационарные состояния. Уравнение Шредингера для стационарных состояний и квантование энергии. Средние значения физических величин. Соотношения неопределенностей Гейзенберга. Законы сохранения в квантовой механике.
82
Естественной радиоактивностью называется самопроизвольное превращение атомных ядер одного химического элемента в ядра атомов другого химического элемента, сопровождаемое радиоактивным излучением. Открытие явления - 1896 г. французский ученый Анри Беккерель при постановке опытов с солями урана. Без каких-либо внешних влияний на уран А. Беккерелем было зарегистрировано неизвестное излучение. В 1898 г. М. Склодовская - Кюри обнаружила излучение тория. а также открыла новые радиоактивные химические элементы полоний и радий. Все химические элементы с порядковым номером более 83 являются радиоактивными. Естественная радиоактивность химических элементов не зависит от внешних условий.
Три вида радиоактивного излучения В 1899 г. Э. Резерфорд обнаружил, что радиоактивное излучение состоит из двух компонентов, которые он назвал "альфа-лучи" и "бета-лучи". В 1900г. французский физик Ф. Вилард установил, что в состав излучения входят еще и гамма-лучи.
Опыт Резерфорда
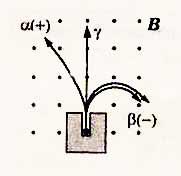 Поведение радиоактивного
излучения было
изучено в
магнитном поле.
Радиоактивный элемент был помещен в
узкий свинцовый стакан, напротив которого
размещалась фотопластинка. Вся установка
размещалась в вакууме.
В отсутствие
магнитного поля на фотопластинке было
обнаружено в центре одно пятно засветки
от излучения.
В
магнитном поле пучок излучения распался
на три.
Составляющие отклонялись в противоположные
стороны: пятно на фотопластинке по
середине оставляла составляющая, не
имеющая заряда, две другие составляющие
радиоактивного излучения отклонялись
в противоположные стороны, что
доказывало присутствие
заряженных частиц в излучении.
В
результате опыта Э.Резерфорд доказал,
что радиоактивное излучение
является неоднородным.
Поведение радиоактивного
излучения было
изучено в
магнитном поле.
Радиоактивный элемент был помещен в
узкий свинцовый стакан, напротив которого
размещалась фотопластинка. Вся установка
размещалась в вакууме.
В отсутствие
магнитного поля на фотопластинке было
обнаружено в центре одно пятно засветки
от излучения.
В
магнитном поле пучок излучения распался
на три.
Составляющие отклонялись в противоположные
стороны: пятно на фотопластинке по
середине оставляла составляющая, не
имеющая заряда, две другие составляющие
радиоактивного излучения отклонялись
в противоположные стороны, что
доказывало присутствие
заряженных частиц в излучении.
В
результате опыта Э.Резерфорд доказал,
что радиоактивное излучение
является неоднородным.
Свойства радиоактивных лучей
Альфа-излучение (альфа
лучи) - это поток полностью ионизированных ядер
атомов гелия.

Бета-излучение (бета-лучи) - это поток электронов.

Гамма-излучение (гамма-лучи) - это электромагнитное излучение.
 Электромагнитные кванты
гамма-излучения не
имеют массы покоя и электрического
заряда, поэтому при прохождении через
вещество они очень слабо взаимодействуют
с ядрами и электронами. Их энергия почти
не меняется, поэтому гамма-излучение
обладает большой
проникающей способностью.
Защитой от гамма-излучения является
толстый слой свинца.
Электромагнитные кванты
гамма-излучения не
имеют массы покоя и электрического
заряда, поэтому при прохождении через
вещество они очень слабо взаимодействуют
с ядрами и электронами. Их энергия почти
не меняется, поэтому гамма-излучение
обладает большой
проникающей способностью.
Защитой от гамма-излучения является
толстый слой свинца.
