
юрин физиология растений
.pdf
|
|
|
Окончание табл. 2.3 |
|
|
|
|
|
|
|
Структурные |
Отличия в спектрах |
|
|
Пигменты |
поглощения; |
|
Окраска |
|
отличия |
|
|||
|
длина волны, нм |
|
|
|
|
|
|
|
|
|
|
|
|
|
Виолаксантин |
Ñ40Í56Î4 |
475 |
|
Желто-оранжевая |
Фикоэритрин |
|
498—598 |
|
Красная |
|
|
|
|
|
Фикоцианин |
|
585—630 |
|
Сине-голубая |
|
|
|
|
|
Аллофикоцианин |
|
585—650 |
|
Синия |
|
|
|
|
|
Желтые пигменты имеют основные полосы поглощения света в синей и фиолетовой частях спектра. Немного они поглощают и зеленые лучи.
2.4. Биосинтез пигментов
Синтез хлорофилла
Это многоступенчатый процесс, который делят на две фазы: темновую и световую. В темноте происходит синтез протохлорофиллида, который отличается от хлорофилла отсутствием остатка фитола и двух атомов водорода. Затем на свету протохлорофиллид присоединяет 2 атома водорода к 7-му и 8-му углеродным атомам и образует хлорофиллид. К последнему присоединяется фитол, и он превращается в хлорофилл (фермент хлорофиллаза); эта реакция тоже идет в темноте.
Биосинтез хлорофилла, все ферменты которого локализованы в хлоропластах, подразделяется на следующие этапы:
-Аминолевулиновая кислота ( -АЛК) порфобилиноген уропорфириноген I и копропорфиноген III протопорфиноген IХпротопорфирин IХ Mg-протопорфирин IХ метиловый эфир Mg-протопорфирина IХ протохлорофиллид протохлорофиллид голохром хлорофиллид à голохром хлорофиллид à хлорофилл.
Первая стадия — исходным веществом в биосинтезе порфиринов является сукцинил СоА (из лимонно-кислого цикла) и глицин, из них образуется -аминолевулиновая кислота. Этот путь характерен для микроорганизмов и животных. Реакция идет с участием фермента — АЛК-синтаза:
92
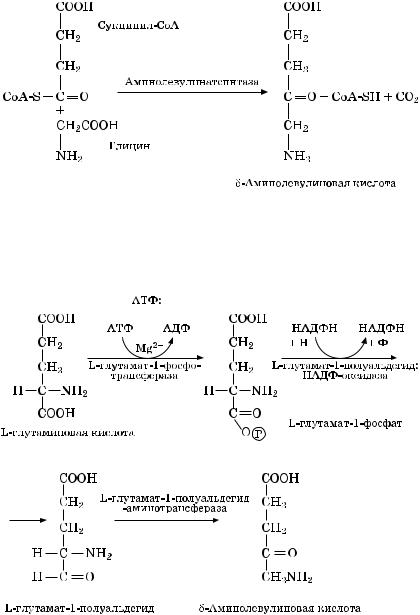
Существует мнение, что АЛК в хлоропластах образуется другим путем, вероятнее всего из интактной молекулы глутамата. Фермент, катализирующий реакцию, удалось выделить из пластид в чистом виде недавно; реакция представляет собой новый внутримолекулярный перенос аминогруппы:
93
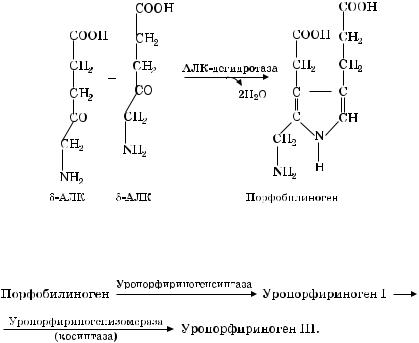
В последнее время уточнили, что -аминолевулиновая кислота образуется из С5-дикарбоновых кислот: глутаминовая кислота через 2-гидрооксиглутаровую преобразуется в 4,5-диоксивалериановую, которая затем амминируется за счет аланина и других кислот.
Это выраженное разветвление путей биосинтеза гема у животных и высших растений происходит, вероятно, на ключевой стадии биосинтетического пути — образовании АЛК.
Интересно было бы выявить, каким из путей синтезируются молекулы АЛК, дающие начало тем небольшим количествам производных гема, которые выявлены у растений, выращенных в темноте: имеет ли место рассмотренный путь синтеза из глутамата или здесь действует путь, который происходит у животных (но его трудно выявить, поскольку в реакциях участвуют очень малые количества субстрата)?
Вторая стадия — образование первичного пиррола: две молекулы -АЛК порфобилиноген превращаются в присутствии фермента АЛК-дегидратазы. Порфобилиноген — это первый предшественник металлопорфиринов, имеющий пиррольную природу.
Третья стадия — образование циклического тетрапиррола. Четыре молекулы порфобилиногена превращаются в уропорфириноген I, а затем III:
94
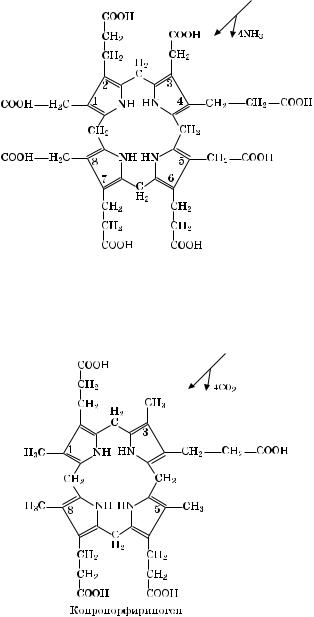
Уропорфириноген III
Четвертая стадия — отщепление 4СО2 от остатков СН2СООНСН3 в положениях 1, 3, 5, 8 молекулы уропорфириногена с уча- стием фермента уропорфириногендекарбоксилазы, так образуется копропорфириноген:
95

Пятая стадия — копропорфиноген превращается в протопорфириноген IХ за счет окислительного декарбоксилирования во 2 и 4 положениях:
1 –ÑÍ2–ÑÍ2–ÑÎÎÍ 2 Î2 ÑÍ2 ÑÍ2 ÑÎ2 Í2Î
Шестая стадия — в результате реакции дегидрирования, при которой отщепляются 6Н из протопорфириногена IХ, образуется протопорфирин.
Седьмая стадия — происходит включение Mg (NН N) и образуется Mg-протопорфирин IХ.
Вероятно, на стадии образования протопорфирина IХ происходит также разветвление путей биосинтеза — один ведет к образованию железопорфиринов (гем), другой — к Mg-порфиринов (хлорофиллам). В растениях обнаружены оба пути, у животных — только первый.
В биосинтезе железосодержащих порфиринов участвует фермент феррохелатаза, который выделен как из пластид, так и митохондрий растений. Этот фермент эффективно преобразует про-
96
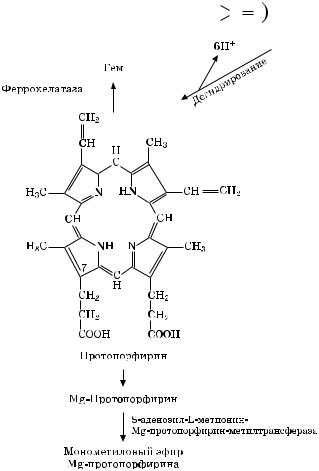
топорфирин в протогем (гем b), который входит в состав цитохромов, каталазы, пероксидазы и гемоглобина. Нужно отметить, что химически встроить Mg2 в протопорфирины намного труднее, чем Fe2 . Какой фермент катализирует включение Mg2 в молекулу протопорфирина, пока неизвестно.
Восьмая стадия — превращение Mg-протопорфирина IХ в монометиловый эфир Mg-протопорфирина. Происходит этерификация метиловым спиртом. Фермент S-аденозил-L-метионин-Mg- протопорфирин-метилтрансфераза осуществляет перенос (СН3-) в шестое положение от S-аденозил-L-метионина. Далее — окисле-
ние пропионата с образованием группы 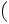 C O .
C O .
97

Девятая стадия — образование протохлорофиллида происходит в результате этерификации (этерификация — образование сложных эфиров из кислот и спиртов) карбоксильной группы метанолом, замыканием пятого (фуранового) кольца окончательным формированием боковых цепей: в четвертом положении винильная группа (–СН СН2) восстанавливается до этильной группы (С2Í5-), получается Mg-винилфеопорфирин à5-протохлорофилл.
Как и хлорофилл, протохлорофиллид находится в связанной с белком форме.
Десятая стадия — в результате неферментативной индуцируемой светом реакции восстановления в кольце IV (появляются два атома Н) протохлорофиллид превращается в хлорофиллид (это хлорофиллы, в молекуле которых нет терпеноидной — обыч- но фитольной — боковой цепи). Спектр действия хлорофиллида подобен спектру поглощения протохлорофиллида, источником водорода в этой реакции служит белок (возможно НАДФН — до-
98
нор водорода). Выделен в чистом виде фермент НАДФН — прото- хлорофиллид-оксиредуктаза. Таким образом, восстановление до хлорофиллида катализируется светом и происходит в пигментбелковом комплексе, который имеет название протохлорофил- лид-голохрома.
Одиннадцатая стадия — последняя стадия синтеза хлорофилла — образование сложного эфира хлорофиллида с фитолом, которая происходит в липидной фазе хлоропластов, поскольку фитол не растворяется в воде, с участием фермента хлорофиллазы. Фитол — полиизопреновое соединение, синтезируется из ацетил-СоА через мевалоновую кислоту.
Хлорофилл b отличается, как мы отмечали, от хлорофилла à только тем, что боковым заместителем при С3 является группа (–СНО) вместо (–СН3). Соотношение хлорофиллов à è b в пределах одного вида — величина довольно постоянная.
Несмотря на большие усилия исследователей, пока никому не удалось детально выяснить, каким путем происходит биосинтез хлорофилла b (его окисление).
Синтез хлорофилла зависит от генетических факторов. В результате генных мутаций появляются растения альбиносы, которые живут, пока имеют запасные вещества из семян. Пятнистость — результат отсутствия синтеза хлорофилла в некоторых частях листа, что также зависит от генов.
Содержание хлорофилла в листе колеблется очень мало. Это связано с тем, что старые молекулы пигмента беспрерывно разрушаются и образуются новые. При этом один процесс уравновешивает другой.
Кроме света синтез хлорофилла зависит и от условий минерального питания. Прежде всего необходимо железо, которое выполняет каталитические функции. При недостатке железа листья желтеют. Большое значение имеет обеспеченность растений азотом и магнием, так как эти элементы входят в состав молекулы пигмента. При нехватке меди хлорофилл легко разрушается.
Этиолированные проростки содержат небольшое количество протохлорофиллид — белкового комплекса (голохром), и при кратковременном освещении в них происходит быстрое стехиометрическое восстановление протохлорофиллида до хлорофиллида, который затем медленно этерифицируется и преобразуется в хлорофилл à. Если проростки затем вновь возвратить в темноту, в них образуется приблизительно такое же количество протохлорофиллида, которое было вначале, и при осветлении он тоже пре-
99
вращается в хлорофиллид. Таким образом, при освещении этиолированных проростков короткими вспышками света (по 10–4 с), которые чередуются с 10—15-минутными темновыми промежутками, можно накопить большие количества хлорофилла.
Хотя у большинства высших растений синтез хлорофилла происходит только на свету, некоторые из них, например сеянцы хвойных растений, могут синтезировать хлорофилл в темноте. Способны к темновому синтезу хлорофилла и многие водоросли, например бурые и цианобактерии. Пока непонятно, почему последняя стадия восстановления пигмента у этих организмов не зависит от освещения (света). Однако показано, что развивающиеся семядоли хвойных синтезируют значительное количество хлорофилла в темноте только до той поры, пока они находятся в контакте с макрогаметофитом, т. е. до того времени, пока макрогаметофит не исчезнет. Семядоли, которые отделяют от макрогаметофита, даже если их поместить в питательный раствор, синтезирует значительно меньше хлорофилла. Следовательно, какое-то вещество из макрогаметофита непосредственно участвует в темновом синтезе хлорофилла.
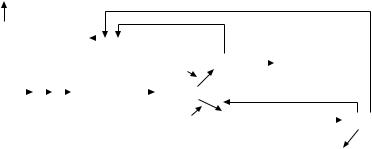
Таким образом, реакцией, на уровне которой происходит на- чальный этап биосинтеза хлорофилла, является синтез АЛК (рис. 2.5).
Неактивные ферменты синтеза АЛК
Активные ферменты |
|
|
Стабильная |
д |
|
|
|
|
|
||||||||||
синтеза АЛК |
|
Синтез |
|
мРНК |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
белков |
2+ |
Протогем |
|
Хлоропластные а |
|||||||
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
Fe |
в |
|
|
цитохромы |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Глу |
|
|
|
|
|
АЛК |
|
|
|
Протопорфирин |
|
г |
|
||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
б |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Mg2+ |
|
Mg-протопорфирин |
|
|
ПХД |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Хлорофилл
Ðèñ. 2.5. Регуляция биосинтеза порфиринов в развивающихся хлоропластах. Стрелки ( ) показывают, чем ингибируется процесс
) показывают, чем ингибируется процесс
АЛК — это субстрат первого основного (решающего) этапа в синтезе тетрапиррола. Это значит, что, вероятно, АЛК лимитирует скорость всего процесса. Об этом свидетельствует и ряд дан-
100

ных, например добавление АЛК к этиолированным проросткам в темноте приводит к увеличению количества протохлорофиллида (ПХД) по меньшей мере в 10 раз.
Считают, что протохлорофиллид или другой контролируемый посредник подавляют синтез фермента (или ферментов), действуя на стабильную мРНК (à).
Поскольку при биосинтезе хлорофилла и биосинтезе гема используется один и тот же накопленный промежуточный продукт, можно думать, что регуляция происходит именно в той точке, где пути биосинтеза расходятся, т. е. на том этапе, на котором атом металла встраивается в молекулу (á, â). Вероятно, протохлорофиллид регулирует включение Mg (ã), а также, как отмечали, синтез белков. Регуляция включения Fe2 осуществляется на стадии протогема (ä) (ðèñ. 2.6).
Синтез каротиноидов начинается с ацетил-CоА через мевалоновую кислоту, геранилгеранилпирофосфат до ликопина. Ликопин (С40Í56) является предшественником всех других каротиноидов. Синтез идет в темноте, но ускоряется при действии света. Ликопин имеет ациклическую структуру (отсутствие кольца с двух концов молекулы) и характерен для плодов томата. Циклизация в концах (одного или двух) молекулы ликопина приводит к образованию разных колец ( - и -иононовых). Так, образование двух -иононовых колец (по обоим концам молекулы) приводит к образованию -каротина. Вообще, последовательность превращения каротиноидов следующая:
-каротин (два -иононовых кольца) -каротин (одно -, другое -иононовое) лютеин ( -иононовые кольца и ОН-группа в кольце при С3);
-каротин зеаксантин (два кольца -иононовые и группа ОН в кольцах) виолаксантин (два -иононовых кольца, кроме ОН-
групп, появляются эпоксигруппы |
C |
C |
в каждом кольце). |
|
O |
||
|
|
|
Фотопротекторная роль каротиноидов, т. е. защита хлорофилла от фотоокисления, еще раз подчеркнем, объясняется их способностью взаимодействовать с возбужденными молекулами кислорода и хлорофилла. В этом случае энергия возбуждения триплетного хлорофилла и синглетного кислорода резонансным путем передается на каротиноиды, а затем рассеивается в виде тепла.
Таким образом, активный ацетил, образующийся из пировиноградной кислоты, служит исходным веществом для биосинтеза в растениях сложных соединений, к каким относятся и каротиноиды.
101
