
№6_2 сем_ПЕРВИЧНЫЕ МЕТАБОЛИТЫ
.pdf
Биологический синтез аминокислот
1. ПРЯМОЕ АМИНИРОВАНИЕ (без затраты АТФ)
Прямое амминирование при биологическом синтезе – это образование глутамата (анион глутаминовой кислоты) из α-кетоглутарата (2-оксоглутарат) и аммиака – катализируется ферментом глутаматдегидрогеназой.
Также по прямому амминированию проходит образование аланина из пирувата при участии
аланиндегидрогеназы: |
|
|
|
CH -CO-COOH+NH + НАД |
CH -CHNH -COOH+2[H] |
||
3 |
4 |
3 |
2 |
Небольшое |
количество |
аминокислот |
образуются в |
результате прямого амминирования. АТФ в этом процессе
не расходуется |
11 |
|

Биологический синтез аминокислот
1. ПРЯМОЕ АМИНИРОВАНИЕ (с затратой АТФ)
Образование |
глутамина |
из |
глутамата |
|
(образование |
которого |
представлено |
на |
|
предыдущем слайде) при участии ионов аммония катализируется глутаминсинтетазой и идет с
затратой АТФ: |
АТФ |
АДФ |
ГЛУТАМАТ |
ГЛУТАМИН |
|
Возможен и обратный процесс: при помощи глутаматсинтетазы аминогруппа глутамина может
быть |
перенесена |
на |
2-оксоглутарат |
с |
образованием глутамата. |
|
12 |
||
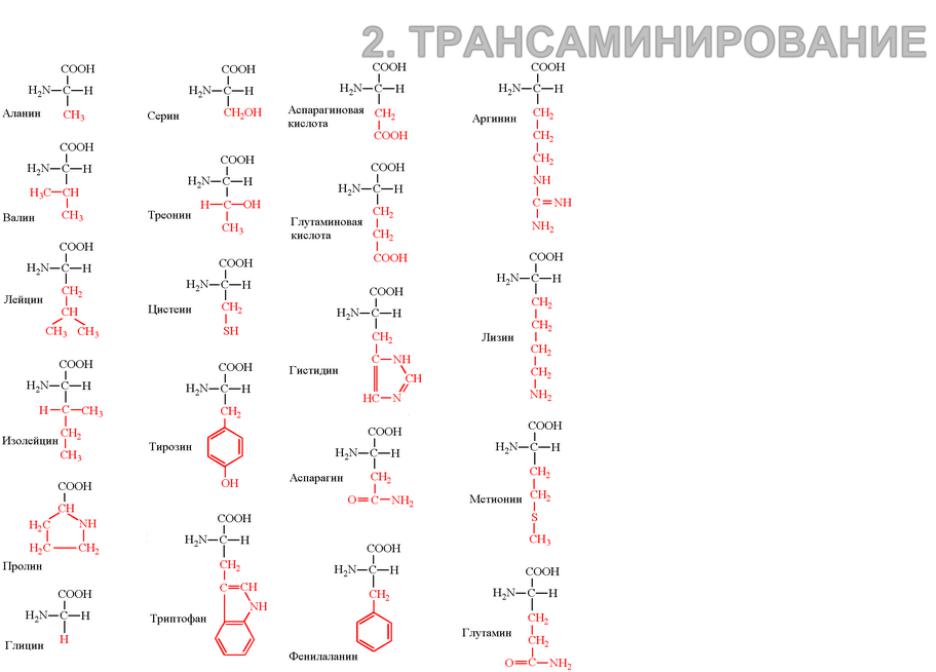
Биологический синтез аминокислот 2. ТРАНСАМИНИРОВАНИЕ
Все остальные аминокислоты получают свою аминогруппу от первичных аминокислот (глутамат, глутамин, аланин) в результате реакций трансаминирования.
Из свободных аминокислот в цитоплазме количественно преобладает глутаминовая кислота
(более половины всего
13
«пула» аминокислот).
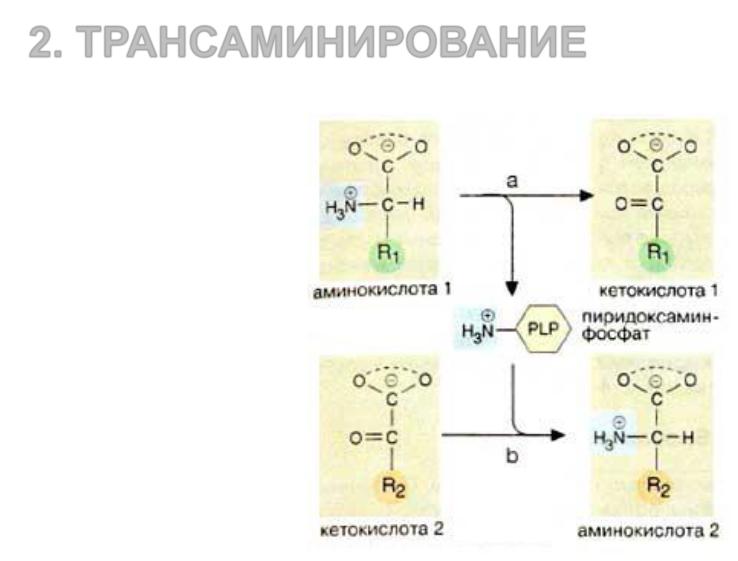
Биологический синтез аминокислот 2. ТРАНСАМИНИРОВАНИЕ
При трансаминировании аминогруппа аминокислоты (аминокислота 1) переносится на 2-кетокислоту (кетокислота 2). Из аминокислоты при этом образуется 2-кетокислота (а), а
из |
первоначальной |
кетокислоты — аминокислота
(b). Переносимая NH2-группа временно присоединяется к связанному с ферментом коферменту
пиридоксальфосфату (PLP),
который вследствие этого
переходит |
в |
пиридоксаминофосфат. |
|
14

ПУТИ БИОСИНТЕЗА АМИНОКИСЛОТ
По
особенностям
биосинтеза
протеиногенные
аминокислоты
подразделяются на пять семейств.
Члены
каждого семейства имеют общих предшественник ов, которые образуются в цитратном цикле или при катаболизме углеводов.
15

БИОСИНТЕЗ НЕЗАМЕНИМЫХ АМИНОКИСЛОТ
16

БИОСИНТЕЗ ЗАМЕНИМЫХ АМИНОКИСЛОТ
Все необходимые для синтеза белков 20 аминокислот образуются из определенных метаболических предшественников:
ПИРУВАТ: АЛАНИН, ВАЛИН, ЛЕЙЦИН
ОКСАЛОАЦЕТАТ: АСПАРТАТ,
АСПАРАГИН, МЕТИОНИН, ЛИЗИН, ТРЕОНИН, ИЗОЛЕЙЦИН
2-ОКСОГЛУТАРАТ: ГЛУТАМАТ,
ГЛУТАМИН, АРГИНИН, ПРОЛИН
3-ФОСФОГЛИЦЕРАТ: СЕРИН, ГЛИЦИН,
ЦИСТЕИН
ФОСФОЕНОЛПИРУВАТ, ЭРИТРОЗО-4-
ФОСФАТ: ФЕНИЛАЛАНИН, ТИРОЗИН, ТРИПТОФАН
5-ФОСФОРИБОЗИЛ-1-ПИРОФОСФАТ:
ГИСТИДИН
17

ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ
АМИНОКИСЛОТ
18

ПРИМЕНЕНИЕ АМИНОКИСЛОТ
В последние годы широкое применение в народном хозяйстве и медицине находят различные аминокислоты.
Особое значение они имеют для сбалансирования белкового питания. Некоторые пищевые и кормовые продукты не содержат в своем составе необходимых количеств незаменимых аминокислот, в частности лизина.
К таким продуктам относятся пшеница, кукуруза, овес, рис и ряд других.
Для ликвидации возможного дисбаланса аминокислоты используют в чистом виде или вводят в состав комбинированных кормов, выпускаемых промышленностью.
19

ПРИМЕНЕНИЕ АМИНОКИСЛОТ
Поэтому основной сферой применения аминокислот
следует считать создание рационов, позволяющих понизить содержание растительных белков в кормах. Показано, что искусственные смеси аминокислот позволяют экономить расход естественных кормов. Кроме добавок к кормам сельскохозяйственных животных аминокислоты используются в пищевой промышленности.
Применяются они и при изготовлении ряда
полимерных материалов, например
синтетической кожи, некоторых специальных
волокон, пленок для упаковки пищевых продуктов. Ряд аминокислот или их производных обладают пестицидным действием. Метионин и
γ-аминомасляная кислота широко
применяются как лекарственные средства.
20
