
- •Химия Методические указания к лабораторным работам
- •Содержание
- •Введение
- •Охрана труда в лаборатории химии Меры безопасности и правила поведения в лабораториях химии
- •Подготовка химических опытов
- •Проведение химического опыта
- •Общие требования к поведению студентов в лаборатории химии
- •Работа с веществами и растворами
- •Обращение с нагревательными приборами, нагревание
- •Работы после окончания химических опытов
- •Первая помощь при повреждениях, вызванных химикатами, и при ожогах
- •Лабораторная работа № 1. Тепловой эффект химических реакций.
- •3.1. Энтропия и свободная энергия системы.
- •4. Объект исследования.
- •5. Контрольные вопросы:
- •6.Описание лабораторной установки и порядок проведения опыта.
- •7. Рекомендации по планированию и проведению эксперимента.
- •9. Список литературы.
- •10. Рекомендации по технике безопасности.
- •3.2. Факторы, влияющие на скорость химической реакции.
- •1. Влияние природы реагирующих веществ.
- •2. Влияние концентрации реагирующих веществ.
- •3. Влияние температуры на скорость реакции.
- •3.1. Примеры решения задач.
- •4. Объект исследования.
- •6. Описание лабораторной установки и порядок проведения опыта
- •7. Рекомендации по планированию и проведению эксперимента.
- •8. Содержание отчета.
- •9. Список литературы.
- •10. Рекомендации по технике безопасности.
- •Лабораторная работа № 3.
- •3.1.2 Молярная концентрация.
- •4. Объект исследования.
- •5. Контрольные вопросы.
- •6. Описание лабораторной установки и порядок выполнения опыта.
- •7. Рекомендации по планированию и проведению эксперимента.
- •Катодные процессы в водных растворах
- •Анодные процессы в водных растворах
- •4. Объект исследования.
- •5. Контрольные вопросы.
- •6. Описание лабораторной установки и порядок выполнения опыта.
- •7. Рекомендации по планированию и проведению эксперимента.
- •3.1. Защита металлов от коррозии.
- •4. Объект исследования.
- •6. Описание лабораторной установки и порядок выполнения опыта.
- •Лабораторная работа №6
- •3.3. Химические свойства оксидов
- •3.4. Химические свойства оснований
- •3.5. Химические свойства кислот
- •4. Объект исследования.
- •5.Контрольные вопросы.
- •6. Описание лабораторной установки и порядок выполнения опыта.
- •I часть. Получение оксидов и гидроксидов
- •II часть. Получение солей
- •Номенклатура кислот и их солей
- •VI. Рекомендации по планированию и проведению эксперимента
- •VII. Содержание отчета
- •Лабораторная работа № 7. Очистка сточных вод.
- •3. Общие сведения:
- •3.1 Методы и оборудование для очистки сточных вод.
- •3.2 Метод ионного обмена.
- •3.3 Мембранные методы очистки сточных вод.
- •3.4 Электродиализ.
- •3.5 Биологическая очистка сточных вод.
- •4. Объект исследования.
- •5.Контрольные вопросы.
- •7.Рекомендации по планированию и проведению эксперимента.
- •8. Содержание отчета.
- •9. Список литературы.
- •10. Рекомендации по технике безопасности.
Лабораторная работа №6
Основные классы неорганических соединений
1.ЦЕЛЬ РАБОТЫ: ознакомиться со свойствами неорганических соединений и способами их получения.
2.РАБОЧЕЕ ЗАДАНИЕ: проделать опыты, ответить на контрольные вопросы и решить предложенный вариант заданий.
3.ОБЩИЕ СВЕДЕНИЯ:
3.1 Классификация неорганических соединений

Оксиды – это сложные вещества, в состав которых атомы кислорода какого-либо другого элемента (ЭхОу). Степень окисления кислорода в оксидах равна-2. Например, Fe2O3- оксид железа (III), CuO-оксид меди (II) или оксид меди (+2).
3.2 Структурные формулы
Структурные формулы - это порядок расположения атомов в молекуле в одной плоскости, (на самом деле атомы в молекулах располагаются в разных плоскостях). Структурные формулы оксидов:
+5 -2
Р2О5

(чёрточка указывает на единицу степени окисления).
У фосфора их 5, у кислорода-2.
Структурные формулы гидрооксидов:
NaOH Al(OH)3
Na –O – H O – H
│
H – O – Al – O – H
Атомы водорода соединяются с атомом серы только через атомы кислорода
|
+1 +6 -2 H2SO4 |
+1 +5 -2 H3AsO4 |
Структурные формулы солей:
Для составления нужно иметь в виду структуру кислотного остатка кислоты, образующей соль и к нему присоединять атомы металла, например:
К3РО4-соль ортофосфорной кислоты, структура соли:
 K
– O
K
– O
K – O – P = O
 K
– O
K
– O
Основная соль (CuOH)2SO3 – сульфит гидроксомеди (II)
Структура кислотного остатка:
 –O
–O
 S
= O
S
= O
– O
а соли:
 H
– O
– Cu
– O
H
– O
– Cu
– O
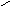 S
= O
S
= O
H – O – Cu – O
Bi(OH)2 NO3 - нитрат дигидроксовисмута (III)
O
H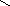 – O
||
– O
||
 Bi
– O
– N
Bi
– O
– N
H – O ||
O

Основными оксидами называются такие, которые при взаимодействии с кислотами образуют соль и воду. Соединение этих оксидов с водой относят к классу оснований (например, оксиду Na2O соответствует основание NaOH).
Кислотными оксидами называются такие, которые при взаимодействии с основаниями образуют соль и воду. Соединение этих оксидов с водой относят к классу кислот (например, оксиду Р2О5 соответствует кислота Н3РО4, а оксиду Сl2О7 – кислота НСlО4).
К амфотерным оксидами называются такие, которые при взаимодействии с кислотами и основаниями с образованием соли и воды. Соединение этих оксидов с водой могут иметь как кислотные, так и основные свойства (например, амфотерному оксиду ZnO соответствует основание Zn(OH)2 и кислота H2ZnO2).
Характерной особенностью оксидов является способность их к образованию солей. Поэтому такие оксиды относятся к солеобразующим. Наряду с солеобразующими существуют и несолеобразующие, или безразличные, оксиды, которые не образуют солей. Примером могут служить CO, N2O, NO.
