
- •Лабораторна робота 1 Глибинне культивування Asp. Niger з метою одержання лимонної кислоти
- •Перше заняття
- •1. Готування посівного й ферментаційного середовищ
- •2. Визначення рН посівного й ферментаційного середовищ і доведення до рН 7,0
- •3. Визначення сухих речовин методом рефрактометрії
- •4. Визначення вмісту цукру за методом Бертрана
- •Друге заняття
- •1.Визначення біомаси
- •2. Визначення рН середовища
- •3. Визначення загальної кислотності
- •4. Визначення вмісту цукру в культуральній рідини по Бертрану
- •5. Визначення лимонної, щавлевої й глюконової кислот й їхній розрахунок
- •Лабораторна робота 2 Культивування цвілевого гриба Asp. Niger поверхневим способом з метою одержання лимонної кислоти
- •Перше заняття
- •1. Підготовка посуду для стерилізації
- •2. Готування живильного й з її стерилізація
- •3. Визначення концентрації сухих речовин у вихідному середовищі
- •4. Визначення рН середовища
- •6. Засівання стерильного середовища спорами продуцента, характеристика умов культивування
- •Друге заняття
- •2. Визначення в збродженому розчині загальної титруємої кислотності й знімання кислоти г/м2 за добу
- •3. Визначення лимонної, щавлевої й глюконової кислот й їхній розрахунок
- •3.2. Визначення щавлевої кислоти
- •4. Визначення сухої ваги міцелію й розрахунок його продукуючої здатності по лимонній кислоті
- •5. Визначення в середовищі залишкового цукру
- •6. Розрахунок кількості спожитого цукру
- •7. Розрахунок виходу лимонної кислоти від спожитого цукру
- •Додатки
- •Застосування органічних кислот
3. Визначення концентрації сухих речовин у вихідному середовищі
У середовищі, яке залишилося після розливу в колби визначається вміст сухих речовин методом рефрактометрії. Для цього 10 – 12 мл середовища профільтровують через складчастий фільтр у пробірку, доводять температуру фільтрату до 20°С і проводять вимірювання показань на рефрактометрі.
4. Визначення рН середовища
рН середовища визначається в нефільтрованій пробі потенціометрично.
5. Визначення вмісту цукру в середовищі
Інверсія цукру (гідроліз до моносахаридів) здійснюється кислотним гідролізом середовища.
Устаткування й посуд: водяна баня, мірна колба на 100 мл.
Реактиви: 25%-ний розчин НС1, насичений розчин Na2СO3.
Хід роботи
У мірну колбу на 100 мл переносять 5 мл середовища, потім додається 45 мл дистильованої води й 2 мл 25% НС1, уміст колби перемішується й колбу поміщають на 5 хв у киплячу водяну баню для того, щоб провести інверсію сахарози до редукуючих цукрів. Після гідролізу вміст колби прохолоджується, нейтралізується содою до припинення виділення вуглекислоти й доводить до мітки дистильованою водою. Потім проводять визначення редукуючих речовин, за методом Бертрана.
У конічну колбу наливають по 20 мл реактивів А і Б. Перемішують. Потім наливають 10 мл гідролізату й 10 мл дистильованої води. Перемішують і ставлять отриману суміш на електроплитку й одночасно потрібно поставити колбу з дистильованою водою. Після появи перших пухирців скипання починають відлік часу кипіння розчину 3 хвилини. Після цього часу колби знімають із плитки. Випадає червоний осад оксиду міді (І). Рідина над осадом повинна мати синій колір; якщо вона безбарвна, потрібно взяти меншу кількість – 5 мл, довівши обсяг до 10 мл додаванням дистильованої води. Розчин фільтрують гарячим, кілька разів промиваючи осад у колбі й на фільтрі гарячою дистильованою водою до повного знебарвлення промивних вод, що стікають із фільтра.
Осад у колбі й на фільтрі розчиняють сірчанокислим залізом у сірчаній кислоті, додаючи його щоразу невеликими порціями. Після розчинення осаду колбу й фільтр промивають холодною дистильованою водою до відсутності кислої реакції в промивних водах. Замірити загальна кількість (b). Уміст колби титрують розчином перманганату калію до слабо-рожевого забарвлення.
Розраховується % вмісту цукру в середовищі й кількість цукру в пробі (400 мл).
Приклад розрахунку.
1. У 10 мл гідролізату знайдено, наприклад, 80,5 мг інвертного цукру.
Складаємо ланцюжок розведення: 5 мл вихідного розчину → 100 мл → 10 мл на визначення цукру по Бертрану. Розраховуємо кількість цукру в 1 мл розчину:

2. Розраховуємо % змісту цукру у вихідному розчині:
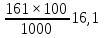
де 1000 – коефіцієнт перерахування мг у г; 100 – приведення показань до %.
3. Розраховуємо кількість цукру в пробі (400 мл):

6. Засівання стерильного середовища спорами продуцента, характеристика умов культивування
Засівання середовища здійснюється в боксі. Стіл і руки протираються ватяним тампоном зі спиртом. На столі розміщається штатив з посівними пробірками, порожні стерильні склянки, колби зі стерильним середовищем і пальник. Колби поміщають із правої сторони, склянки – з лівої. Запалюють пальник, розв'язують склянки, але не відкривають, знімають паперові ковпачки з колб. Склянки розміщають дуже близько до пальника з лівої сторони. Колбу із середовищем беруть у праву руку. Відкривають лівою рукою пробку в колби й обпалюють горлечко колби на полум'ї. Лівою рукою (великим і вказівним пальцями) відкривають серветку на склянці й виливають у нього вміст колби. Закривають склянку серветкою, колбу пробкою й відставляють її вліво. Потім у праву руку беруть посівну пробірку, відкривають її також як колбу, вносять спорову суспензію в склянку, закривають склянку й пробірку, посів закінчений. Потім теж саме роблять із другою пробою. Склянки із засіяним середовищем зав'язують, підписують і ставлять у термостат при температурі 32 – 34°С на 7 – 8 діб на вирощування.
