
ЛЕКЦІЯ №3
Функціональні властивості і перетворення білків
ПЛАН
Функціональні властивості білків і їх модифікація.
Нові білкові продукти.
Перетворення білків у технологічному процесі.
Якісне і кількісне визначення білка.
1. Функціональні властивості білків і їх модифікація.
Під функціональними властивостями білків (термін введений у 1962р. Серклом і Джонсоном) розуміють фізико-хімічні характеристики, які визначають їхні перетворення у процесі технологічної обробки та забезпечують певну структуру, технологічні і споживчі характеристики харчових продуктів.
До найважливіших функціональних властивостей білків відносяться: розчинність, водопоглинаюча і жиропоглинаюча здатність, здатність стабілізувати дисперсні системи (емульсії, піни, суспензії), утворювати гелі і плівки, адгезійні і реологічні властивості (в’язкість, еластичність), здатність до текстурування.
У різних умовах білки мають різні значення цих властивостей, вони виражаються в цифрових показниках і в профілях залежності від технологічних факторів.
Розчинність – характеризується коефіцієнтами КРА і КДБ, які визначають кількість відповідно азоту і білка, яка перейшла в розчин (у% від загальної кількості). Розчинність білків залежить від наявності в молекулі не ковалентних взаємодій: гідрофобних, електростатичних і водневих зв’язків. При меншій взаємодії глобул білка між собою і більшій силі відштовхування розчинність білків, тобто їхня взаємодія з молекулами розчинника буде більшою. Отже, при зміні рН у розчині відбувається взаємодія заряджених іонів (Н+ або ОН-) з протилежно зарядженими білковими частинками. У кислому середовищі білок набуває позитивного заряду внаслідок подавлення дисоціації карбоксильних груп, а в лужному – негативного за рахунок подавлення дисоціації аміногруп. Молекули білка відштовхуються, отже білок набуває більшої розчинності.
Невелика кількість іонів солей теж підвищує розчинність білка, перешкоджаючи електростатичній взаємодії бокових груп білків. Високі концентрації солей знижують гідратацію поліпептидних ланцюгів і відповідно знижується розчинність білків.
Різниця в розчинності є основою для технологічних процесів виділення ізолятів і концентратів білка, впливає на якість тих продуктів, де передбачається гідроліз (автоліз) білків і їх денатурація, сушіння і зберігання продуктів. Це виробництво напоїв, де застосовуються розчинні білки, хлібобулочних і макаронних виробів, де необхідна навпаки низька розчинність цих сполук.
Водопоглинаюча здатність білка зумовлена адсорбцією води з участю гідрофільних залишків амінокислот. Жиропоглинаюча здатність зумовлена адсорбцією жиру за рахунок гідрофобних ділянок. Білки здатні утримувати на поверхні близько 0,2-0,4г води і жиру на 1г білків.
Ця здатність білків залежить також від рН, способу обробки, температури, наявності інших фракцій (вуглеводів, ліпідів). Висока здатність білків утримувати воду збільшує вихід, покращує структуру м’ясних, хлібобулочних виробів, збільшує час зберігання продукту.
Додавання соєвого білка або клейковини підвищує водопоглинаючу здатність борошна. Денатуровані білки знижують водопоглинаючу здатність. Висока жиропоглинаюча здатність забезпечує ніжну однорідну текстуру, виключає відділення жиру, зморщування, знижує втрати при тепловій обробці напівфабрикатів з м’яса, борошна .
Жироемульгуюча і піноутворююча здатність білків широко застосовується у виробництві харчових продуктів завдяки наявності в білках гідрофобних і гідрофільних груп, які розподіляються певним чином на межі розподілу фаз вода-масло або вода-газ.
Широко розповсюджені емульсії, олія у воді і вода в олії у виробництві хлібобулочних, кондитерських виробів, низькокалорійних маргаринів, майонезів, соусів, паст, м'ясних продуктів (застосовуються рослинні і тваринні білки). Використовуючи добавки рослинних і тваринних білків, одержують стійкі емульсії механічно перемішуючи рідини з допомогою мішалок, міксерів, гомогенізаторів.
Піноутворююча здатність білків - утримувати газове середовище є основою виробництва збивних кондитерських виробів (бісквітів, кремів). Білки клейковини формують піну у дріжджовому тісті з участю СО2, утвореного при бродінні. У кондитерських виробах піна утворюється під дією хімічних розрихлювачів при виділенні СО2 з соди та СО2 і NН3 з вуглекислого амонію.
Всі функціональні властивості білків оцінюються певними показниками, як емульгуюча здатність, піноутворююча здатність, стабільність емульсій, піни тощо.
Гельутворююча здатність білків обумовлена утворенням просторової сітки взаємодіючих молекул білків і залежить від мінімальної їх концентрації, від рН, наявності солей, полісахаридів, інших білків.
Утворені білками гелі повинні відповідати певним вимогам, мати необхідні фізико-хімічні властивості, а саме: міцність, еластичність, тіксотропію (здатність переходити в рідкий стан), широкий діапазон рН, здатність до сорбції барвників і ароматизаторів при мінімальній концентрації білка. Наприклад, желатин володіє такими властивостями.
Розрізняють такі гелі як: наповнені (містять інші розчинні або суспензовані білки); змішані (у яких сітка складається з різних видів білків); комплексні (сітка з білків, з’єднаних з іншими сполуками); анізотропні (сітку утворюють орієнтовані молекули білка); ксерогелі (сухі, зберігаються довгий час).
Реологічні властивості. Білки з низьким рівнем полярності утворюють комплекси з властивими їм реологічними властивостями (в’язкістю, еластичністю, пружністю). Такими характерними властивостями володіють білки клейковини, які визначають структуру хліба, створюючи безперервну фазу у виробах з наповнювачами (висівки, родзинки тощо) і крохмальними зернами борошна.
Для підвищення якості і розширення асортименту виробів здійснюють регулювання функціональних властивостей білків, що досягається зміною умов виділення, сушіння, фізико-хімічною дією на ці сполуки, ферментативною і хімічною їх модифікацією. При цьому змінюється склад амінокислот і окремих фракцій, відбувається денатурація, взаємодія між білками, білків з ліпідами, вуглеводами, тощо.
До фізико-хімічних методів модифікації білків відносяться: розчинення білків перед сушінням у розчині кислот, лугів з метою зміни їх заряду або іонного складу, дія високих температур. При цьому підвищується розчинність, гельутворююча, жиропоглинаюча здатність, можливість утворювати певну структуру і т.д. При ферментативній модифікації використовують протеази.
Наприклад, для заміни яєчного альбуміну випускають три види модифікованих піноутворюючих соєвих білків: альбуміни, гідролізати ізоляту і гідролізати борошна.
Реакції ферментативного синтезу білків із пептидів (пластеїновий синтез) застосовують для введення до складу білків незамінних амінокислот або їх похідних - ефірів з метою зміни властивостей, підвищення біологічної цінності.
Гідроліз Концентрування Синтез
Білок → Пептиди (3-20кДа) → Концентрат пептидів → Пластеїн.
З хімічних способів модифікації широко застосовуються дезамінування глутаміну й аспарагіну; ацилювання аміногруп янтарним (суксинілювання), оцтовим (ацетилювання) та іншими ангідридами кислот.
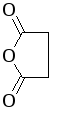
Б ілок
–NH2
+ → Білок –
+ H+
ілок
–NH2
+ → Білок –
+ H+
Функціональні властивості білків також покращуються за рахунок обробки їх речовинами ліпідної природи (лецитин, ацилгліцерини), пектинами, альгінатами, мінеральними речовинами.
Реакційні групи білків взаємодіють з іншими сполуками, які інтенсифікують процеси водопоглинання, гелеутворення, структурування, покращуючи якість харчових виробів.
