
- •Введение
- •Измерение физических величин и вычисление погрешностей
- •Определение погрешностей при прямых измерениях
- •Определение погрешностей при косвенных измерениях
- •Графическое изображение результатов работы
- •Оформление отчета по работе
- •Часть 1
- •Измерения и обработка результатов
- •Лабораторная работа №2 определение момента инерции махового колеса и силы трения в опоре
- •Краткая теория
- •Порядок выполнения работы.
- •Контрольные вопросы
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа № 4 опытная проверка уравнения бернулли
- •Краткая теория
- •Описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Порядок выполнения работы
- •Контрольные вопросы
- •Краткая теория
- •Описание лабораторной установки.
- •Порядок выполнения работы
- •Контрольные вопросы
- •Литература
- •Лабораторная работа №7 определение коэффициента внутреннего трения газа, средней длины свободного пробега и эффективного диаметра его молекул
- •Теоретическое введение. При движении слоев газа параллельно друг другу с различными по величине скоростями между ними возникают силы внутреннего трения (закон Ньютона)
- •Теория метода
- •Порядок выполнения работы.
- •Контрольные вопросы.
- •Литература
- •Лабораторная работа № 8 определение отношения удельных теплоемкостей газа методом адиабатического расширения.
- •Порядок выполнения работы
- •Контрольные вопросы
- •Порядок выполнения работы
- •Контрольные вопросы
Литература
Савельев И.В. “Курс общей физики”, Т.1
Шубин А.С. “Курс общей физики”
Грабовский Р.П. “Курс физики”
Лабораторная работа № 8 определение отношения удельных теплоемкостей газа методом адиабатического расширения.
Приборы и принадлежности: стеклянный баллон, манометр, насос.
Цель работы: определение показателя адиабаты (коэффициента Пуассона) методом Клемана-Дезорма для воздуха.
Теория метода и описание установки.
Удельной теплоемкостью С газа называется скалярная физическая величина, численно равная количеству теплоты Q, которое необходимо сообщить единице массы газа, чтобы увеличить его температуру на 1 К:
![]() (1)
(1)
Величина
теплоемкости газов зависит от условий
нагревания. Выясним эту зависимость,
воспользовавшись первым
законом термодинамики,
который гласит: количество
теплоты Q,
сообщенное системе, затрачивается на
увеличение ее внутренней энергии
![]() и на работу А, совершаемую системой
против внешних сил
и на работу А, совершаемую системой
против внешних сил
![]() (2)
(2)
При
изохорическом (V=const)
нагревании газа
![]() ,
следовательно, и А=0. Тогда все подводимое
к газу тепло идет на увеличении его
внутренней энергии:
,
следовательно, и А=0. Тогда все подводимое
к газу тепло идет на увеличении его
внутренней энергии:
![]()
Из формулы (1) следует, что
![]() (3)
(3)
При изобарном (Р=const) нагревании газа тепло, сообщаемое газу идет и на увеличение внутренней энергии и на совершение газом работы против внешних сил:
![]() ,
,
поэтому
![]() (4)
(4)
Сравнивая
уравнения (3) и (4), получаем
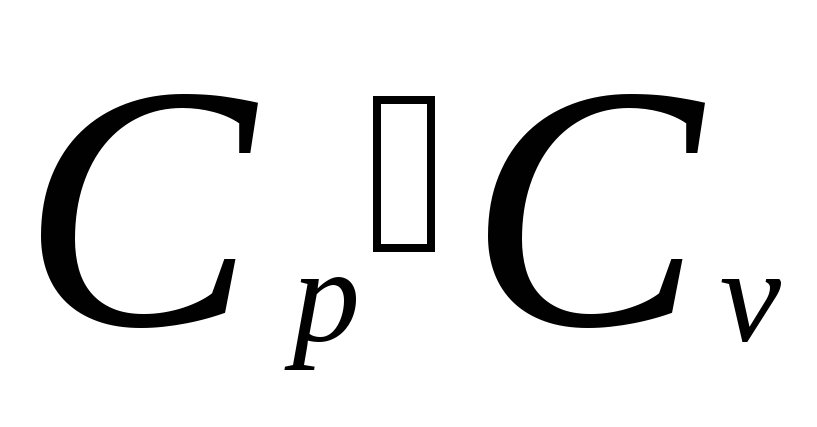 .
.
Отношение
удельных теплоемкостей при постоянном
давлении и при постоянном объеме
![]() играет в термодинамике весьма важную
роль. В частности оно входит в уравнение
Пуассона,
которое описывает адиабатическое
расширение газа
играет в термодинамике весьма важную
роль. В частности оно входит в уравнение
Пуассона,
которое описывает адиабатическое
расширение газа
![]() (5)
(5)
В
данной работе прелагается один из самых
простых методов определения
![]() -
-
метод Клемана и Дезорма. Адиабатическим процессом называется процесс, протекающий без теплообмена с окружающей средой, т.е. считается, что процесс передачи тепла системе от окружающей среды отсутствует.
Экспериментальная установка состоит из стеклянного баллона А (рис. 1), соединенного с манометром В и с насосом.
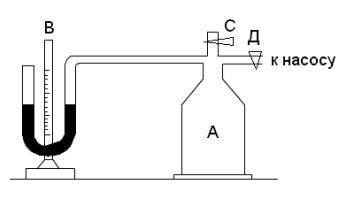
Рис. 1
Если
про помощи насоса накачать в баллон
некоторое количество воздуха, то давление
и температура воздуха внутри баллона
повысятся. Вследствие теплообмена
воздуха с окружающей средой через
некоторое время температура воздуха,
находящегося в баллоне, сравнятся с
температурой внешней среды
![]() .
.
Давление, установившееся в баллоне
![]() ,
,
где Р - атмосферное давление;
Н - разность уровней жидкости в манометре;
В - коэффициент перехода от разности уровней к давлению.
Таким образом, состояние воздуха внутри баллона, которое назовем 1 состоянием, характеризуется параметрами
![]() ;
;
![]() и
и
![]()
Если
на короткое время открыть кран С, то
воздух в баллоне будет расширяться.
Этот процесс расширения можно считать
адиабатическим. Давление в баллоне
установится равным атмосферному Р,
температура газа понизится до
![]() , а объем будет равен
, а объем будет равен
![]() .
.
Следовательно,
в конце адиабатического процесса, что
назовем 2 состоянием, параметры состояния
газа будут Р;
![]() ,
,![]() .
.
Применяя к 1 и 2 состояниям уравнение (5), получим:
![]() или
или ![]() (6).
(6).
Охладившийся
при адиабатическом расширении воздух
в баллоне через некоторое время вследствие
теплообмена нагреется до температуры
внешней среды
![]() ,
давление возрастет до некоторой величины
,
давление возрастет до некоторой величины
![]() ,
,
где h- новая разность уровней в манометре.
Объем
воздуха не изменится и будет равен
![]() .
.
Это состояние воздуха, которое назовем 3 состоянием, характеризуется параметрами
![]() ;
;
![]() ;
;
![]()
Так
как в состояниях 1 и 3 воздух имеет одну
и ту же температуру
![]() (процесс изотерический), то, применяя
закон Бойля-Мариотта (PV=const),
получим:
(процесс изотерический), то, применяя
закон Бойля-Мариотта (PV=const),
получим:
(P+вH)![]() (P+вh)
(P+вh)![]()
![]()
Возведем
обе части уравнения в степень
![]() :
:
![]() (7)
(7)
Решая
совместно уравнения (6) и (7), получим:
![]()
Логарифмируя
это выражение и решая относительно
![]() ,
находим
,
находим
![]()
Так как давления Р, Р+вН и Р+вh мало отличаются друг от друга, то разности логарифмов можно принять пропорциональными разностям самих давлений и приближенно положить
![]()
![]() (8)
(8)
![]()
![]() Таким
образом, экспериментальное определение
Таким
образом, экспериментальное определение
![]() сводится к измерению H
и h,
то есть формула (8) является расчетной
формулой для определения коэффициента
сводится к измерению H
и h,
то есть формула (8) является расчетной
формулой для определения коэффициента
![]() Пуассона
Пуассона
