
Заттарды иіскеп көру Зертханада жұмыс істеу тәсілдері
Зертханалық жұмыс2
Химиялық ыдыстар жӘне олармен жұмыс істеу тӘртібі.
Химиялық тәжірибелердің көпшілігі өте жұқа шыныдан жасалған ыдыстарда жүргізіледі. Бұндай шынылар кәдімгі шыныға қарағанда температураның тез ауытқып кетуіне төзімді келеді. Өте көп қолданылатын ыдыстарға жататындар:
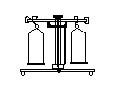
шыныдан жасалған сынауық, стакан, колбалар (Вюрц, конус тәрізді, түбі дөңгелек, түбі жалпақ колбалар) мен реторталар. Сонымен қатар шыны ыдысқа кристаллизаторлар, әр түрлі воронкалар немесе құйғылар, сағат шынысы, аллонж жатады. (3-сурет).

7 3-сурет
1- сынауық, 2- колба,3- құйғы, 4- стакан, 5-тамшуыр, 6- склянка, 7- отбақыраш
Ірі кристалл заттарды еріту алдында оларды ұнтақ күйге дейін үгітеді. Ол үшін фарфордан,шыныдан, металдан жасалған табақшалар мен келішелер қолданылады. (4-сурет)

1 2 3
4-сурет
1-шыны, 2- фарфор,3- металл үгіткіштер
. Күйдіргіш сілтілерді және күшті улы заттарды үгіту үшін бетке маска мен респиратор, ал қолға- резина қолғап киеді. Өте улы заттарды ауа сорғыш шкафта жүргізеді. Еріткіштердің көлемдері өлшеуіш цилиндрлар мен мензуркалар (5-сурет) арқылы өлшеніп алынады және миллилитрмен (мл) өрнектеледі. Еріткіш пен затты стаканға салғаннан кейін шыны таяқшамен араластырады. Бұл процесті тездету үшін ерітіндіні қыздырады(6-сурет). Сулы ерітінділер дайындау үшін міндетті түрде дистильденген су пайдаланылады.

5-сурет 6- сурет
Өлшеуіш ыдыстар Қатты заттардың суда еруі
Осы және басқа да химиялық ыдыстар мен құралдардың атқаратын қызметімен, қолданылатын орнымен жұмыс барысында біртіндеп танысамыз.
Зертханалық жұмыс №2
Тақырыбы: Қондырғыларды жинау.Таразы және таразыда өлшеу.
Тақырыбтың негізгі сұрақтары:
Қондырғы жинаудның негізгі ережелері.
Қондырғы жинау және оған қажетті тетіктерді дайиндау.
Тәжірибе өткізуге зат алу.
Техникахимиялық таразылардың құрылысы.
Техникахимилық таразыда өлшеу ережелері.
Өлшеудің орташа квадрат қателігі.
Мақсат:
қондырғыларды жинауды үйрену
техникахимилық таразыда жұмыс істеу ережелерімен танысу
техникахимилық таразыда өлшеп, оның орташа квадрат қателігін есептеу
Студенттердің алған білімің деңгейі.
Білу қажет:
негізгі қондырғыларды
қондырғыларды жинау ережесі
тапсыпма бойынша қондырғы жинауды
таразыда өлшеудің негізгі ережелерін
техникахимилық таразыда өлшеуді
өлшеудың орташа квадрат қателігін есептеуді.
Студенттердің өз бетімен орындайтын жұмыстары.
Тәжірибе өткізуге арналған заттарды алу.
Практикалық жұмысты орындау кезінде заттар өте аз мөлшерде қолданылады. Олар реактивтер прабиркаларда сақталады. Пробиркадағы қатты заттар микроқасықшамен, ал сұйықты пипеткамен алады. Әрбір қатты заты бар пробирканың тығынында қасықшасы болуы қажет. Бір қасықшаны әр рүрлі заттарға қолдануға болмайды.
Пробиркаға қатты зат саларда қасықшаны пробиркаға салуа болмайды, қасықшаны пробирканың аузында ғана ұстау қажет. Қажетті затты пробирқаға салғаннан кейін, қасықшаны реактиві бар пробирқаға салу қажет.
2-10 тамшы реактивке тамшы немесе капилляр пипеткасын қолданады.Пипеткалардың үсті ашық және резеңке қалпағы бар болады.
Үсті ашық пипеткамен ерітінді алу үшін, оны реактивте бар пробирқаға салып, ерітінді пипеткамен жоғары көтерілгеннен кейін, пипетканың екінші ашық жағын саусақпен басып тұрып, ерітіндіден суырып алады.Содан кейін саусақты сәл көтеріңкіреп 2-3 тамшы ерітіндіні пробирқаға тамызады да, пипетканың, саусақпен тесігін жауып реактивті бар пробирқаға салады.
Ерітінді алатын пипетканы жұмыс жүргізіп жатқан пробирқаға салуға болмайды. Резенке қалпағы бар пипеткамен ерітіндіні алу үшін пипетканың резеңке қалпағын екі саусақпен қысып ерітіндіге батырады да, саусақты жібереді, ерітінді жоғары көтеріледі. Пипетканы ерітіндіден алып, жұмыс жүргізетін пробирканың аузына апрып, екі саусақпен қалпақтан қысып ерітіндіні тамызады.
Қондырғыларды жинау.
Хмиялық эксперимент кезінде қондырғы жинауға көп ауқыт кетеді. Тәжірибенің қондырғының дұрыс жиналуына, таңдап алынуына байланысты болады. Қарапайым қондырғылар 2-6 суреттердегідей түйіндерден;
реакция өтетін бір немесе бірнеше колбадан, пробиркалардан және соңғы өнімді қабылдайтын қабылдағыштан;
қажетсіз қоспаларды жұтатын ыдыстар жиынтығынан;
негізгі реакция өтетін колба немесе қондырғыдан тұрады.
Қондырғы жинаудың негізгі ережелері.
Қажетті қондырғыны жинамастан бұрын ыдыстардың тазалығын, жұмысқа жарамдылығын тексеріп алу қажет.
Диаметрлері сәйкес келетін түтіктерді, тығындарды, қондырғыларды даярлап алу қажет.
Тамшылатқыш құйғышы бар қондырғыларды жинағанда құйғыштың ұшы сұйықтыққа батып тұруы қажет. (Неге?)
Реакцияның нәтежесінде бөленген газ қажетсіз қоспаларды жұтатын ыдысқа бір ұшы сүйыққа батырылған түтік арқылы өту қажет. (Неге?)
Қондырғы артық кедергісіз жинауы қажет.
Тапсырма:
Қажетті заттарды дайындап, қондығы жинау,
әртүрлі бұрышпен түтіктерді ию,
түтіктің диаметірне сәйкес тығындарды тесіп дайындау.
Зертханалық жұмыс 3
Таразы және таразыда өлшеу.
Рычагты таразыда өлшеу дегеніміз, затты массасы белгілі таразы тастарының массасымен салыстыру болып табылады. Таразы тастарының массасы белгілі бірлікте (мг, г, кг, т.б) болады. Таразы лабораториядағы ең қажет қондырғылардың бірі, қандай жұмыс болмасын керек заттың оны салатын ыдыстың массасын анықтау қажет болып табылады.
Затты 0,01 г. Дәлдікпен өлшеу үшін технохимилық таразы қолданылады. Технохимиялық және аналитикалық таразының құрылысы бірдей.
![]()
1- сурет. Технохимиялық таразы және таразы тастары.
(1- баған, 2- арретир, 3-табақшалары, 4-стрелка, 5- шкала, 6-орнықтырма, 7-горизонталь бағытта орнықтыруға арналған бұранда, 8-иін ағаш, 9 табақшаларды тенестіруге арналған бұрандалар).
Екі иығы тең металл рычагың екі басында және ортасында, үш призма орналастырған. Ортадағы призма тіреу нүктесі болатын орталық тағандағы пластинқаға орналастырылады. Бұл пластинка аналитикалық таразыда агаттан жасалған. Ал шеткі екі призма таразының табақшалары ілінеді. Шкалада горизонталь бағыттан аутқыды көрсететін стрелка шкалад нөльді көрсетеді. Таразыны орнықтырып алғаннан кейін орнынан қозғауға болмайды. Таразыдада өлшеместен бұрын оның жұмысқа жарамдылығын тексеріп алады. Көтеріліп, түсірілетін иін ағашты арретирлеп, таразыны жұмысқа дайындайды. Стрелканың шкаладағы нольдік нүктеден ауытқуын бақылайды. Егер стрелка екі жаққа бірдей бөлекке ауытқыса, онда таразыда жұмыс істей беруге болады. Таразыны жұмысқа дайындағаннан кейін арретирді түсіріп қояды.
Таразыда жұмыс істеу ережелері:
таразының табақшасына заттарды, таразы тастарын салып, қайтадан алу үшін, таразыны арретирлеу қажет.
таразының табағына лас және сулы, қыздырылған заттарды салуға болмайды.
сүйықтықты өлшегенде оны таразыға және таразы тастарына тигізбе.
өлшенетін зат таразының сол жақ табағына салынады.
қатты затты әйнекшеге, бюкске, глянс қағазға салып өлшейді.
таразы тастарын пинцетпен алып, сол ұяшыққа қайтадан салу керек
затты өлшеу ушін, ең бірінші сол заттың салмағына шамамен жуықтау деген таразы тасын табақшаға салады, егер тас ауыр болса, одан жеңіл келесісін салады да, екі табақша теңескенше қайталайды, таразы тастарының массамын еспетеп, жұмыс дәптеріне жазу керек
бір жұмысқа қолданылатын заттарды тек бір таразыда өлшейді
затты өлшеп болғаннан кейін табақшаларды босатып, таразыны арретирлейді, табақшада затты қалдыруға болмайды.
Таразыда өлшеудің орташа квадрат қателігі.
Әрбір өлшеген сайын өлшеу қатілігі кетеді. Заттың шын массасына жуықтау үшін сол затты 4-5 өлшеу керек. Бір затты келесі өлшеу кезінде таразының табақшасынан алмайды. Бірінші өлшеу келесі өлшеуден таразыны арретирлеумен ғана ерекшеленеді. өлшеу кезінде кететін қателікті орташа квадрат қателік түрінде береді. Орташа квадрат қатілікті есептеу мынандай түрде жүргізіледі:
Мысалы 1,2,3 .... п өлшеу кезінде келесі мәндер алынды десек а1, а2, а3 ...., ап, Осы алынған мәндердің арифметикалық орта шамасын табамыз:
![]()
![]()
Орташа квадрат қателік келесі түрде анықталады:

Сонымен заттың салмағы А=а±d тең.
Тапсырма:Лаборанттан массасы 1-100 г аралығында зат алып, оны техникахимиялық таразыда 0,01 дәлдікпен бірнеше рет өлшеніз. өлшеудің орташа квадрат қателігін есептеніз.Бақылау сұрактар.
Лабораторияда қолданылған химиялық ыдыстарды атаныздар.
Өлшеуге арналған ыдыстар және олардың қолданылуы.
Фарфор ыдыстар және олардың қолданылуы.
Ыдыстарды жуу және оларды кептіру.
Таразының құрылысы.
Таразыда өлшеудың негізгі ережелері.
Өлшеудың орташа квадрат қателігін анықтау.
Зертханалық жұмыс № 4
Тақырыбы: Сүзу.
Тақырыбтың негізгі сұрақтары:
Қарапайым және қатпырлы сүзугі
Қалыпты қысымда сүзу
Вакууммен сүзу
Ыстықтай сүзу.
Мақсат:
Қалыпты қысымда, вакууммен, ыстықтай сүзуге арналған қондырғыларды жинап үйрету.
Сүзіп үйрету.
Студенттердің алған білімің деңгейі.
Білу қажет:
Қарапайым және қатпарлы сүзгінің қолданылуы,
Сүзуге арналған қондырғыларды жинауды,
Тұнбаны басқа ыдысқа шығынсыз ауыстыруды,
Сумен жұмыс істейтін насосты іске қосып, оның қолданылуын,
Ыстықтай сүзудің методикасы.
Сүзу.
Сұйықты ерімейтын қатты заттан тазарту ушін, сүзу әдісі қолданылады. Сүзу кезінде сұықтықты тесікшелері, бар материал-сүзгіден өткізеді. Сүзгіш материалдар ретінде кварц құмы, асбест, шыны-мақта, фосфор пластинкалар(Гуч ыдысы), нығыздалған шыны (Шот ыдысы), текстильді маталар, мақта, қағаз сүзгілер қолданылады.
Сүзілетін сұйықтықтың қасиетіне байланысты әртүрлі материалдан жасалған сүзгілер қолданылады.
Лабораторияда көбіне қағаз сүлгілер қолданылады. Олар қарапайым және қатпарлы болады. Егер сүзілген тұнба әрі қарай пайдаланылатын болса, қарапайым сүзгі қолданылады. Қарапайым сүзгіні құйғыштың өлшемдеріне сәйкес, шаршы қағазда дәл ортасынан бүгіп, сүзгінің жиегі құйғыштың жиегінен 0,5 см. Төмен түсіп тұратындай етіп бүктелген шаршының жиегін доға етіп қайшымен қию арқылы даярлайды.
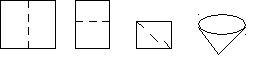
Төрт бөктелген сүзгінің бір бөлігін ашып, құйғышқа салады да, бір саусақпен басып тұрып дистеленген сумен сулайды. Суланған сүзгі құйғыштың қабырғаына жабысып тұруы қажет.
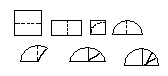
Бүл сүзгіні даярлау қарапайым сүзгі сияқты, бірақ шаршы қағазға бірнеше рет бірдей бөліктерге бүктеу арқылы жасалады.
Оңай сүзілетін сұйықтықтырды-қалыпты қысымда, қиын сүзілетіндерді вакуум арқылы сүзеді.
Тұтқыр және қаныққан ерітінділер ыстықтай сүзіледі.
Студенттердің өз бетімен орындайтын жұмыстары.
Қалыпты қысымда сүзу.
Қалыпты қысымда сүзу ушін, стақан, құйғыш және сүзгі мен таяқшадан түратын қондырғы жинайды:
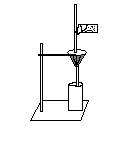
Қалыпты қысымда сүзіге арналған қондырғы.
Құйғышқа сүзгіні салып, сүзілетін сүйықтықты таяқшаның бойымен құяды. Сүзіп жатқан сұйықтық азайғанда оны шайқап, сүзіге тағыда құйып қояды. Сүзгіден өткен сұйықтық фильтрат немесе сүзінді деп аталады. Сүзгіде қалған тұнбаны дистеленген сумен немесе арнайы сүіқтықпен шаяды. Тұнбаға шаятын сүйытқы құяды да, ол ағып кеткенше күтеді, сосын тағы құйып, осылай бір неше рет қайталанады. 4-5 рет шайқағаннан кейін, оның тазалығын тексереді. Ол үшін сүзгіден 1-2 тамшы алып шайылып жатқан ионға сапалы реакция жасайды. Егер тұнба түзілсе жууды әрі қарай жалғастырады. Шаюға қолданған сүітқі негізгі сүйіндіден бөлек жинайды (Неге?). Қиын ерійтін және баяу сүзілетін тұнбаларды бөлініп алу үшін және шаю үшін декантация әдісі қолданылады. Ол үшін тұнбаны сүзбестен бұрын оның стаканнын түбінде тұндырады ал ерітіндісі сүзіледі де тұнбаға шаятын сұйытқыты құйып араластырады, оның тұынын құтып қайталап тағы ерітіндісін сүзеді.
Тапсырма:
қалыпты қысымды сүзіге арналған қондырғыны жинау керек,
металл штативтің құрылысымен және жиналуымен танысу қажет,
50 мл. құм-су, балшық-судан тұратын қоспаны сүзу қажет,
тұнбаны таяқшаның қөмегімен басқа ыдысқа аустырып үйрену қажет,
Вакууммен сүзу.
Қатты затты сүйықтан бөлуді тездету үшін вакууммен сүзі қолданылады. Төменгі қысымда сүзі үшін Бунзен колбасына Бюхнер құйғышынан тұратын қондырғы жинау қажет. Бюхнер құйғышына біреуі диаметірне сәйкес, ал екінші одан 0,5 см. үлкендеуі екі сүзгілерді салады. Кіші сүзгі құйғыштын түбіне салынатын онын үстіне үлкен сүзгіні сулап алады, осы қондырғыны су насосына жалғап сүзгілердін құйғышқа жабысуын байқалады. Таяқшаның қөмегімен тұнбасы бар ерітінді Бюхнер құйғышына құйып оны сақтандырғыш ыдыстар арқылы насосқа жалғап сүзуді жүргізеді. Сүзіп болғаннан кейін Бюхнер колбасын сақтандырғыш ыдыстан ажыратып суды тоқтатады. Тұнбаны құйғыштан алып сүзгі қағазға ауыстырады. Бюхнер құйғышынын орнына Гуч тигілін немесе Шоттын шыны құйшын қолдануға болады.
Тапсырма:
Вакууммен сүзіге арналған қондырғыны жинап, насостын құрлысымен танысу қажет.
Бақылау сұрактар.
Сүзі дегеніміз не?
Жәй және қатпарлы сүзгілердін атқаратын қызметтері.
Сүзгі материалдарды атаныздар.
Қалапта қысымда сүзідін методикасы.
Қысыммен сүзідін методикасы.
Зертханалық жұмыс № 5
Тақырыбы: Заттарды тазарту әдістері.
Тақырыбтың негізгі сұрақтары:
Заттарды тазартдың негізгі әдістері.
Қайтадан кристалдантыру, өнімнің %-тік шығымын есептеу.
Бірден буландыру, өнімнің %-тік шығымын есептеу.
Мақсат:
Қайтадан кристалдандыру және бірден буландыру әдістерінің методикасын меңгеру.
өнімнің шығымы мен қоспанын мөлшерін есептеп үйрену.
Студенттердің алған білімің деңгейі.
Білу қажет:
заттарды тазалатудың негізгі әдістері,
қайтадан кристалдандырудың әдістерінін негізін,
кез-келген затты (аммоний хлориді, йод силицыл, бензой қышқылдары) бірден буландыру методикасын ,
өнімнің %-тік шығымын есептеу.
Қайта кристалдандыру.
Қайта кристалдандыру әдісті қатты заттардың температураға байланысты ерігіштігіне негізделген№
Егіштік қаныққан ерітіндінің концентрациясымен анықталады. Бұл шама берілген жағдай үшін тұрақты.
Ерігіштік 100 г ерітіндіде немесе еріткіште еріген заттып проценттік мөлшерімен сипатталады.
Ерег жоғарғы темпиратурада қаныққан ерітінді дайындап, оны суытса, еріген заттың ккристалдары тұнбаға түседі де, қоспаның мөлшері аз болғандықтан ол ерітіндіде қалады.
Осы әдіспен затты қоспасынан тазартады.
Қайта қристалдану әдісінің мағынасын түсіну үшін келесі мысалдықарастырайық.
Калий бихроматын қайтадан кристалдандыру қажет болсын. 600С темпиратурада 200 мл К2Сr2О7 қаныққан ертіндісін дайындау үшін қанша тұз және су керек екенін есептей қажет. Ерігіштік таблицасынан 600С темпиратурада К2Сr2О7-ныңерігіштігі 32,8 % екенін анықтаймыз. Тұздың мөлшерін есептеймыз
100 г - 32,8 г
200
г - х
![]() г
К2Сr2О7
г
К2Сr2О7
Судың мөлшері 200-65,6=134,4 г немесе мл.Таразыда 65,6 г К2Сr2О7 өлшеп стақанға салып, суды мензуркамен өлшеп құяды. Ерітінді араластыра отырып қыздырып, қатпарлы сүзгімен ыстықтай сүзіге арналған қондырғыда сүзеді.
Егер ерітінді сүзілгеннен кейін қанықпаған болса, фарфор ыдысқа құйып, бетінде жұқа қабықша пайда болғанша суалтады. Егер баяу суытылса ірі кристалдар, ал тез суытылса кіші кристалдар түзіледі. Суыту кезінде орташа кристалдар алуға тірісу қажет (неге ?)
Түзілген кристалдар вакууммен сүзу әдіспен ерітіндіден бөліп алады. Кристалдарды суық еріткішпен жуады. Жуғаннан кейін оны сүзгі қағазына салып, ауда кептіреді. Құрамындағы кристалданған судан арылту үшін кристалды эксикаторда кептіреді. Ауадағы су тамшылармен әрекеттесетін кристалды, бірден эксикаторда кептіреді.
Қайтадан кристалдану кезінде 100С темпиратурада 55 г құрғақ К2Сr2О7 және 105 мл қаныққан ерітінді алынсын. Ерігіштік таблицасынан 100С темпиратурадағы К2Сr2О7 тұзының ерігіштігін қарасаныз, ол 7,8 г. Енді 105 г ерітіндідегі тұздың массасын есептейміз.
100 г - 7,8 г
105
г - х г
![]() г К2Сr2О7
г К2Сr2О7![]()
Алынған заттың құрамында таза 55+8,1=63,1 г К2Сr2О7 бар.
Немесе %-тік мөлшерде
65,5 - 100 %
63,1
- х %![]() %
%
Қоспаның массасы 65,5-63,1=2,5 г немесе % бойынша 100% - 96,1%=3,69 %.
Егер ерітіндіде көп зат қалса оны қайнатып суалтып затты бөліп алады.
Ерігіштігі белгісіз затты қайтадан кристалдандыру үшін не істейді? Ол үшін аз мөлшерде еріткіш алып берілген температураға дейін қыздырып қайтадан кристалдандыратын затты салады. Оны ерітіп, ерітіндіні сүзіп, сүзіндіні бетіне жұқа қабықша тұрғанша султады.
Түзілген кристалдарды бөліп алып тазалығын тексереді де таразыда өлшеп массасын дәптерге жазады. Органикалық еріткіштерді қолданғанда қауіпсіздік ережесін сақтау қажет.
ТапсырмаОқытушынаң тапсырмасы бойынша берілген темпиратурада затты қайта кристалдандырыңыз. Жұмыс жоспарын жасаңыз. Негізгі кристалдың және қоспаның шығымын есептеңіз.
Бірден буландыру.
Оқытушыда (амоний хлориды иод салицил бензой қышқылдары) заттардың бірін алып бірден бұландыру әдісімен тазартып балқу темпиратурасын анықтауға сақтаныз.
Кейбір заттарды қыздырғанда олар балқымай-ақ бірден буланады. Мұндай заттардың буы суынғанда олар газ күйінен қатты күйге көшеді.
Бірден бұландыру әдісінде қолданылатын ыдыстар суретте көрсетілген. Колбаны және фарфор ыдысты су жылытқышында қыздырады. Құм жылытқышта да қыздыруға болады.
Тапсырма Иодты тазарту. Стақанның түбінде йод және 0,2 г калий иодидінің қоспасын салып, суық су құйылған дөнгелек табанды колбамен жауып, стақанды құм жылытқышқа қойып қыздырады. Зат бұланғаннан кейін оны колбаның түбінен шыны қалақшамен қырып түсіріп, бюкске салып таразыда өлшейді. өнімнің %-тік шығымын есептеу қажет.
Бақылау сұрақтары
Қатты заттарды тазарту әдістерінің методикасы.
Қаныққан ерітінді дегеніміз не?
Өнімнің шығымын қалай есептейді?
Қандай заттарды бірден буландыру әдісімен тазартады?
Зертханалық жұмыс № 6
Тақырыбы Таза заттың физика-химиялық сипаттамаларын анықтау.
Тақырыптың негізгі сұрақтары
Қатты заттардың балқу температурасын аңықтау.
Пикнометр және ариометр әдістері бойынша сұйықтықтың тығыздығын анықтау.
Мақсат
қатты заттыңбалқу температурасын аңықтау әдісін меңгеру
сұйықтықтың тығыздығын пикнометр және ариометр әдістері бойынша анықтауды үйрену.
Студенттердің өз бетімен орындайтын жұмыстары.
Қатты заттың балқу темпиратурасын анықтау.
Заттың тазалығын анықтау үшін, сандық та, сапалық та әдістер қолданылады. Сапалық долмен заттың құрамында қандай қоспалар бар екендігін анықталса, сандық әдіспен негізгі заттың мөлшерін анықтауға болады. Химиялық әдітермен қатар физикохимиялық, физикалық тұрақтыларын (балқу тепиратурасы, тығыздығы т.б.) анықтау әдісі де қолданылады.
Химиялық таза зат теқ қана белгілі бір темпиратурада балқиды немесе қатады, сондықтан заттың балқу темпиратурасын бле отырып, оның тазалығы жөнінде айтуға болады.
Заттың балқу темпиратурасын анықтау үшін сүреттегідей колба, термометр, термометрге бегітілген балқу темпиратурасы анықталатын зат бар капилярдан тұратын қондырғы жинайды.
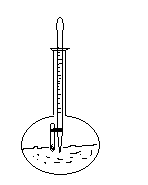
Ол үшін ұнтақталған затты капилярдың жиегімен іліп алып, тығыз толтырылу үшін қатты беткен орналастырылған 50-60 см шыны түтіктің бойымен лақтырады. Капилярдағы заттың биіктігі 2 мм болу қажет. Затпен тығыздалған капилярды дөнгелек резеңкемен термометрге бекітеді. Капилярдағы зат сынып бағанының ортасында тұруы керек. Термометрді заттың балқу темпиратурасын анықтауға арналған ыдысқа орналастырады да электроқыздырғышта қыздырады. Қыздыру жылдамдығы 1-20С болуы қажет. Заттың балқуын бақылып отырып, бірінші тамшы пайда болған кезде температурасының дұрыстығына көз жеткізу үшін, осы тәжірибені екінші дайындалған капиллярмен қайталайды. Бірақ затты қыздыру жылдамдығын 10С-ға кемітіп, қыздыру темпиратурасын 100С-ға төмендетеді. Бірінші тамшының пайда болу темпиратурасын белгіліп, алынған мәндерді анықтамада берілген мәндермен салыстырылады.
Пикнометр әдісі бойынша сұйықтықтың тығыздығын аңықтау.
Салыстырмалы тығыздықты алынған сұйқтықтың массасының дистиленген су массасына қатысымен әрекетеуге болады (бірдей жғдайда). Сұйықтардың тығыздығын анықтау үшін пикнометрия әдісі қолданылады. Ол үшін, ең бірінші көлемі 10-25 мл болатын бос пикнометрді таразыда өлшеп (m), содан кейін зерттелетін сұйықтықпен (m1) өлшейді. Зерттелген сұйықтықтың тығыздығы мына түрде анықталады:
![]()
![]() m2-
су толтырылға пикнотрдің массасы.
m2-
су толтырылға пикнотрдің массасы.
Бұл әдісті тұтқыр емес сұйықтықтарға қолдануға болады. Тұтқыр сұйықтықтрдың тығыздығын ариометр әдісмен немесе гидростатикалық таразы арқылы анықтайды.
Жұмыстың соңында тәжірибеде кеткен абсолют және салыстырмалы қателіктерді есептеу қажет.
Ареометр әдісі бойынша сұйықтықтың тығыздығын анықтау.
Ареометр – жоғарғы бөлігнде тығыздық бірлігінде градуирленген шкаласы бар қалытқы. Жұмыс істеу принципі Архимед заңына негізделен. Тығыздықты анықтау үшін ариометрді ерітіндіге салады да, сұйықтықтың деңгейіне сәйкес келген ариометрдің көрсетуін анақтайды.
Сұйықтықтың тығыздығы анықталғаннан кейін концентрациясын химиктің анықтамасынан қарайды.
Бақылау сұрақтары
Заттардың балқу температурасын аңықтауға арналған қондырғының құрылысы қандай?
Проценттік қателік қалай есептеледі?
сұйықтық тығыздығы дегеніміз не?
газдың ауа бойынша тығыздығы
а) 0,9б)2,45
осы газдың 1 литрінің массасын есептеңіз.
Тақырыбы Сұйықтықтарды тазарту – айдау.
Тақырыптың негізгі сұрақтары
Айдай.
Ағын суды тазарту..
Мақсат
сұйықтарды тазарту метоликасын меңгеру.
Студенттердің өз бетімен орындайтын жұмыстары.
Ағын суды тазарту.
Ол үшін суреттегідей қондырғы жинайды. Ағын суға калий перманганатын қосып Вюрц колбасына (1) құяды. Оның ішіне капилляр түтіктер салады (неге?). колбаны термометр (6) кигізілген тығынмен жабады. Термометрдің сынап деңгейі колбаның бүйіріндегі түтіктің деңгейінде болуы қажет.

Колбаны тоңазытқышпен (2) жалғап, тоңазытқыштың бүйір түтіктерін ағын суға жалғайды. Су төменнен жоғары қарай беріледі (неге?). айдалған су қабылдағышта (3) жиналады. Қабылдағыш ыдыс хлоркальций түтігі (5) мен аллонж (4) кигізілген тығынмен тығындалады да, аллонж тоңазытқышпен жалғанады.
Бақылау сұрақтары
Айдау дегеніміз не?
Қалыпты жағдайда 1 грамм-эквивалент сутегі және оттегі қанша көлем алады?
Әртүрлі газдарды алуға арналған қондырғылардың суреттерін салыныз.
Зертханалық жұмыс-7
Оттегі
1-тәжірибе. Тұздардың ыдырауы нәтижесінде оттегін алу және оның тотығу қасиеттері.(тяга)
Калий
оксохлоратын (V) (бертолет тұзы) катализатор
(![]() қатысында ыдыратып оттегін алыңыз және
оны үш цилндрге толтырыңыз. Оттегі бар
цилиндрдің әрқайсысына жанатын қызыл
фосфор, жанатын күкірт және темір
қабықшасын салыныз. Байқалған құбылыстардың
реакция теңдеулерін жазыңыз.
қатысында ыдыратып оттегін алыңыз және
оны үш цилндрге толтырыңыз. Оттегі бар
цилиндрдің әрқайсысына жанатын қызыл
фосфор, жанатын күкірт және темір
қабықшасын салыныз. Байқалған құбылыстардың
реакция теңдеулерін жазыңыз.
2-тәжірибе. Оксидтердің судағы қатынасы.
Дистилденген суы бар екі пробиркаға кальций оксидін (II) және фосфор оксидін (V) салыңыз. Реакция жүреді ме және ол қандай ортада өтетінін бақылаңыз.
3-тәжірибе
Аквакомплекстердің түзілуі. ![]() Кристаллогидратының алынуы.
Кристаллогидратының алынуы.
Пробиркаға 1 г сусыз мыс сульфатын салып, оған бөлшектеп 5-10 мл дистилденген суды құйыңыз. Байқалған құбылыстарды түсіндіріңіз.Ерітіндіні фарфор ыдысқа ауыстырыңыз және жартылай буландырыңыз. Ерітіндіні суытып, тұнбаға түскен кристаллдарды Бюхнер воронкасы арқылы бөлініз.
4-тәжірибе. Сутегінің асқын тотығын алу.
5 мл 2 М күкірт қышқылын стаканга құйып, оны мұз немесе қармен салқындатыңыз. Кейін оның үстіне 1 г барий пероксидін құйыңыз. Алынған қоспаны шыны таяқшамен 4-5 мин шамасында араластырыңыз. Ерітіндіні тұнбадан бөліп алып, ондағы түзілген сутек пероксидін калий йодиді ерітіндісімен тексеріңіз.
5-тәжірибе . Сутек пероксидСутек пероксиднің сапалық реакциясы.
Калий йодиді ерітіндісін сұйытылған күкірт қышқылы ерітіндісімен қышқылдатып, кейін сары түс түзілгенше тамшылатып сутек пероксидін қосыңыз.Йодтың түзілгенін анығырақ бензолдын тамшыларын қосқаннан кейін байқауға болады. Реакция теңдеулерін жазыңыз.
6-тәжірибе . Натрий пероксидінің гидролизі.
Суы
бар пробиркаға натрий пероксидінің бір
түйіршегін қосыңыз.Қандай газ бөлінгенін
және қандай ерітінді түзілгенін
табыңыз.Реакцияны жылдамдату үшін
![]() катализаторын
қосуға болады.
катализаторын
қосуға болады.
7-тәжірибе Сутек пероксидінің тотығуөтотықсыздану қасиеттері.
а) Күкірт қышқылымен бірдей көлемде қышқылданған калий йодиді ерітіндісіне сутек пероксиді ерітіндісін құйыңыз.Тұнба түзілуін түсіндіріңіз.
б)
Калий тетраоксоманганаттын күкірт
қышқылымен қышқылданған ерітіндісіне
сутек пероксидін құйыңыз. Газдың
бөлінуін түсіндіріңіз.
в) Сутек
пероксидін қыздырғанда қандай газ
бөлінетінін анықтаңыз.Реакцияны
жылдамдату үшін ![]() катализаторын
қолдануға болады.
катализаторын
қолдануға болады.
Күкірт
1-тәжірибе. Ромбалық күкірттің алынуы. (тяга)
Құрғақ
пробиркаға 4-5 мл
![]() құйыңыз
және аз мөлшерде күкірт ұнтағын қаныққан
ерітінді түзілгенше себіңіз. Ерітінді
тамшысын заттық шыныға қойып, бетін
шынымен жауып, микроскоппен кристалдардың
қалай өсетінін бақылаңыз.
құйыңыз
және аз мөлшерде күкірт ұнтағын қаныққан
ерітінді түзілгенше себіңіз. Ерітінді
тамшысын заттық шыныға қойып, бетін
шынымен жауып, микроскоппен кристалдардың
қалай өсетінін бақылаңыз.
2-тәжірибе. Моноклинді күкірттің алынуы. (тяга)
Күкірт
ұнтағын ақырын фарфорлы тигельде
балқытыңыз. Сосын тигельді кристалдық
қабық түзілгенше салқындатыңыз.
Кристалдар орталыққа біріккенде , жылдам
қатпаған күкіртті суымен стаканға
құйыңыз. Лупа көмегімен қараңыз және
түзілген кристалдардың суретін салыңыз.
1-2 тәжірибелердегі түзілген кристалдарды
салыстырып, олардың формасын түсіндіріңіз.
Алынған 2-3 кристаллды
![]() -де
сағаттығ шыныда ерітіңіз және еріткіш
буланғаннан кейін тағыда түзілген
кристалдың формасын бақылаңыз.
-де
сағаттығ шыныда ерітіңіз және еріткіш
буланғаннан кейін тағыда түзілген
кристалдың формасын бақылаңыз.
3-тәжірибе. Күкірттің полиморфты күйге айналуы. (тяга)
Құрғақ пробиркага ақырын күкірт қайнағанша қыздырыңыз. Осы кезде журетін процесті түсіндіріңіз.
4-тәжірибе. Пластикалық күкірттің алынуы. (тяга)
Пробирканы
жартысына дейін күкірттің түйіршіктерімен
толтырыңыз және ақырын плитаның аздаған
жалынымен қыздырыңыз. Балқуын және
түстің өзгеруін және күкірттің
жабысқақтығын бақылаңыз. Күкірт
қайнағанша қыздырылған кезде, оның
кішкене тамшысын салқын сумен
кристализаторға құйыңыз. Алынган массаны
судан ажыратып, фильтр қағаздарының
арасында кептіріңіз. 1-2 сағаттан кейін
пластикалық күкірттің
![]() қасиетінің
өзгеруіне көңіл аударығыз.
қасиетінің
өзгеруіне көңіл аударығыз.
5-тәжірибе. Күкірттің диспропорциолануы.
Тигельдегі күкірт ұнтағына концентрлі сілті ерітіндісін құйыңыз. Қоспаны 10 мин. қайнатыңыз. Қорғасын (II) нитраты қағазының көмегімен ерітіндіде сульфид ионының қатысқанын анықтаңыз.
6-тәжірибе. Күкірттің тотықтырғыш қасиеті.
Бос күкірт металдарды тотықтыруы мүмкін, мүнда ол сульфидтерге дейін тотықсызданып, -2 тотығу дәрежесін көрсетеді. Дайындалған 6г мырыш ұнтағын және 3г біртекті түсті S қоспасын асбестті торға себіп, газдық отқа қыздырамыз. Реакция көп жылу бөлінуімен қатар өатты жарық береді. Түзілген мырыщ сульфиді ақ бұлт тәрізді жоғары көтеріледі.
7-тәжірибе. Күкірттің тотықсыздандырғыш қасиеті.
Пробиркаға
2-3 мл конц.![]() ерітіндісіне
күкірттің аз ғана массасын қайнағанша
қыздырыңыз. Мұнда барий хлориді
ерітіндісін қосу арқылы анықтауға
болатын
ерітіндісіне
күкірттің аз ғана массасын қайнағанша
қыздырыңыз. Мұнда барий хлориді
ерітіндісін қосу арқылы анықтауға
болатын
![]() азот (II) оксидіне дейін тотықсызданады,
ал күкірт
азот (II) оксидіне дейін тотықсызданады,
ал күкірт
![]() ионға дейін тотығады. Сәйкес реакция
теңдеулерін жазыңыз.
ионға дейін тотығады. Сәйкес реакция
теңдеулерін жазыңыз.
Зертханалық жұмыс- 8
Сутек
1-тәжірибе. Сутектің алынуы және оның жануы
а) Газ сіңіретін түтікше орналасқан пробиркаға бірнеше түйір мырыш салып, оған пробирканың 1/3 бөлігіне келгенше 20% күкірт қышқылы құйылады.
Газдың бөлінуін бақылаңыз. Одан бөлінген сутектің тазалығын тексеріңіз. Жарты минуттан соң, от жалынына апарыңыз.Егер пробиркада таза сутек жиналса, онда ол тыныш және көгілдір жалын беріп жанады, егер ауа қоспасы болса, онда әлсіз жарылыс болады. Таза сутек жиналғанына көз жеткізсек, сутекті аяғына дейін жағыңыз. Реакция теңдеуін құрыңыз.
б) Пробиркаға күйдіргіш натр ерітіндісін құйыңыз да, оның үстіне бірнеше алюминий жаңқасын салыңыз. Газдың бөлінуін бақылаңыз. Одан бөлінген газдың тазалығын тексеріңіз.Реакция теңдеуін құрастырыңыз.
2-тәжірибе. Сутектің тотықсыздандырғыш қасиеті
Құрғақ шыны түтікшеден , басынан аяғына дейін газөткізгіш түтіктен тұратын құрылғыны жинаңыз. Түтік қабырғасына аз мөлшерде қара түсті мыс (ІІ) оксидінің ұнтағын салып, оны пробиркаға иілдіріп штативке горизантальды түрде орналастырыңыз. Кипп аппаратынан пробиркаға сутекті жіберіңіз. Пробиркадағы ауаны ығыстырғаннан кейін сутекті аяғына дейін жағыңыз, ал мыс (ІІ) оксидін қыздырыңыз. Мыс (ІІ) оксидімен болатын өзгерісті және ыдыс қабырғасында пайда болған суды бақылаңыз. Мыс тотықсызданғаннан кейін қыздыруды доғарыңыз, бірнеше уақыт сутекті айдаңыз, себебі мыс ауа құрамындағы оттекпен тотығады. Реакция теңдеуін жазыңыз
3-тәжірибе. Молекулалық және атомдық сутектің тотықсыздандырғыш қасиеттерін салыстыру
Екі пробиркаға сұйытылған күкірт қышқылын құйыңыз, оның үстіне бірнеше тамшы калий перманганаты ерітіндісін тамызыңыз. Пробирканың біріне мырыштың түйіршігін салып, екіншісіне Кипп аппаратынан сутек жіберіңіз. Екі пробиркадағы түстің қанық болуын және екі пробирка да түссіздену жылдамдығын бақылаңыз.Бірінші пробиркада тотықсыздандырғыш мырыш емес, сутек екеніне көз жеткізіңіз. Ол үшін күкірт қышқылын қоспай калий перманганат ерітіндісіне мырыш түйіршігін қосыңыз.
Қышқылдаған ерітіндіге мырыш қосқан кезде бірінші атомдық сутек түзіледі. Ол Кипп аппаратынан түсетін молекулалық сутекке қарағанда белсенді:
![]()
Тотығу – тотықсыздану реакциясын құрыңыз.
Бақылау сұрақтары:
Атомдық сутекті қалай алады? Молекулалық сутектен айырмашылығы неде?
Галогендердің тотығу дәрежесі қаншалықты тұрақты және табиғатта қандай қосылыстар құрамында кездеседі?
Егер газ 14,32г мыс (ІІ) оксидінің тотықсыздануына жұмсалатын болса, онда сутек алу үшін сұйытылған күкірт қышқылымен әрекеттесетін мыстың массасын анықтаңыз.Сутектің қолданылу дәрежесі 50%.
Күкірт қышқылы электролизі кезінде катодта 56 (қ.ж) газ бөлінді. Анод өнімінің массасын анықтаңыз.
200 мл судан алынатын сутектің көлемін (қ.ж) анықтаңыз: электролиз; натрий қатысында;
Көміртегі
1-тәжірибе. Көміртектің тотықсыздандырғыштық қасиеттері.
2г
![]() мен
0,3 г ұнтақталған ағаш көмірін араластырып,
қоспаны қиын балқитын пробиркаға
орналастырыңдар. Бүкіл пробирканы
жанғыш жалынымен қыздырып, қоспаны
қатты қыздырыңдар. Түстің өзгеруін
бақылаңдар. Бүкіл ұнтақ қара түсін
қызылға ауыстырғанда қыздыруды
тоқтатыңдар. Реакция теңдеуін жазыңдар.
мен
0,3 г ұнтақталған ағаш көмірін араластырып,
қоспаны қиын балқитын пробиркаға
орналастырыңдар. Бүкіл пробирканы
жанғыш жалынымен қыздырып, қоспаны
қатты қыздырыңдар. Түстің өзгеруін
бақылаңдар. Бүкіл ұнтақ қара түсін
қызылға ауыстырғанда қыздыруды
тоқтатыңдар. Реакция теңдеуін жазыңдар.
2-тәжірибе. Кальций ацетилидінің гидролизі. (тяга)
Кальций карбиді бар сынауыққа бірнеше тамшы су енгізіңдер. Не байқалады?
3-тәжірибе. Көміртегі (IV) оксидінің қасиеттері.
а) екі құрғақ банканы Кипп аппаратынан алынған көмірқышқыл газымен толтырыңдар. Бір банкаға жанып тұрған магний лентасын жылдам енгізіңіз.не байқалады? Реакция теңдеуін жазыңдар. Екінші банкаға абайлап ауада жанған қызыл фосфоры бар қасықты енгізіңіз. Не байқалады? Реакция теңдеулерін жазыңдар. Жанып жатқан магний мен фосфор жалынын сөндіру үшін өрт сөндіргіш құралдарды қолдануға бола ма?
б) сынауықтың 0,25-іне су құйып, лакмустың көк ерітіндісінен аздап қосыңдар да, ерітінді арқылы көмірқышқыл газын өткізіңдер. Көмірқышқыл газы ерітіндісіндегі реакция теңдеулерін жазыңдар. Ерітіндіні қайнатыңдар. Байқалатын түс өзгерісін түсіндіріңдер.
