
Научные стремления 2012-1
.pdf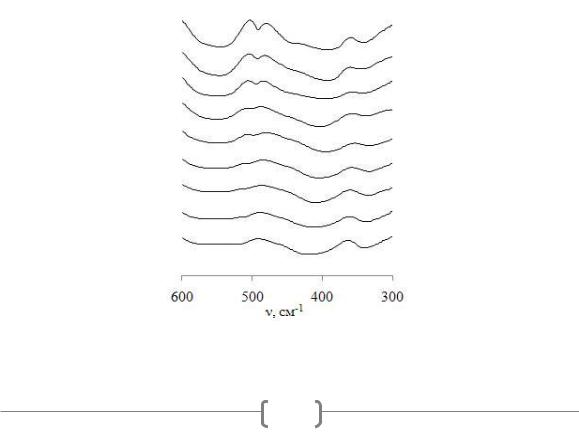
деления 0,001 мм) в динамическом режиме (скорость нагрева и охлаждения 3 – 5 К мин-1).
Анализ рентгеновских дифрактограмм показал, что образцы индатов гадолиния-лантана при х = 0,2 ’ 1,0 были однофазными, что указывает на образование в двойной системе GdInO3 – LaInO3 ряда твердых растворов со структурой орторомбически искаженного перовскита состава Gd1-хLaxInO3 в интервале степеней замещения x от 0,2 до 1,0. При увеличении степени замещения х ионов Gd3+ ионами La3+ наблюдается практически линейный постепенный рост параметров a, b, c и объема элементарной ячейки, при этом степень орторомбического искажения несколько уменьшается (таблица 1). В образцах с x = 0; 0,1 помимо основной фазы присутствовали непрореагировавшие оксид гадолиния Gd2O3 [9] и оксид индия In2O3 [10].
Таблица 1 – Параметры кристаллической решетки a, b, c, объем элементарной ячейки (V) и степень орторомбического искажения (ε) для индатов Gd1–хLaхInO3
|
|
Параметры кристаллической решетки, нм |
|||||
Соединение |
a |
b |
c |
V·103, нм3 |
|
b a |
102 |
|
|
||||||
|
|
|
|
|
|
a |
|
GdInO3 [11] |
0,5556 |
0,5846 |
0,8071 |
262,15 |
0,0522 |
||
Gd0,8La0,2InO3 |
0,5583 |
0,5874 |
0,8106 |
265,83 |
0,0520 |
||
Gd0,7La0,3InO3 |
0,5599 |
0,5876 |
0,8121 |
267,19 |
0,0493 |
||
Gd0,6La0,4InO3 |
0,5625 |
0,5886 |
0,8136 |
269,40 |
0,0465 |
||
Gd0,5La0,5InO3 |
0,5643 |
0,5889 |
0,8149 |
270,58 |
0,0437 |
||
Gd0,4La0,6InO3 |
0,5666 |
0,5903 |
0,8181 |
273,61 |
0,0420 |
||
Gd0,3La0,7InO3 |
0,5661 |
0,5898 |
0,8175 |
272,94 |
0,0418 |
||
Gd0,2La0,8InO3 |
0,5693 |
0,5916 |
0,8186 |
275,69 |
0,0392 |
||
Gd0,1La0,9InO3 |
0,5711 |
0,5927 |
0,8210 |
277,87 |
0,0379 |
||
LaInO3 |
0,5718 |
0,5925 |
0,8212 |
278,21 |
0,0362 |
||
ИК-спектры образцов Gd1-хLaxInO3 при 0,2 ≤ x ≤ 1,0 приведены на рисунке.
5454 |
49 |
44 |
39 |
3434 |
49 |
||||
|
5050 49 |
|
38 |
|
50 |
|
34 |
3434 |
|
|
|
|
39 |
|
|
|
|
34 |
|
51 |
50 |
|
34 |
34 |
51 |
|
|
34 |
|
9
8
7
6
5
4
3
2
1
Рисунок. ИК-спектры образцов Gd1-xLaxInO3 при x = 0,2 (1); 0,3 (2); 0,4 (3); 0,5 (4); 0,6 (5); 0,7 (6); 0,8 (7); 0,9 (8); 1,0 (9)
171

ИК-спектры индивидуальных индатов GdInO3 и LaInO3 отличаются незначительно [12], увеличение степени замещения ионов Gd3+ ионами La3+ приводит к закономерному незначительному уменьшению частот полос поглощения, что связано с увеличением параметров кристаллической решетки соединений. Следует отметить, что в области 600 – 400 см-1 находятся преимущественно валентные колебания связей In – O, в области 400 – 250 см-1 расположены валентные колебания связей Gd – O и валентнодеформационные колебания мостиковой связи In – O – In. Ниже 250 см-1 находятся частоты сложных деформационных колебаний связей In – O и Gd – O.
Установлено, что температурные зависимости относительного удлинения керамических образцов Gd1-xLaxInO3 0,2 ≤ x ≤ 1,0 являются линейными и не содержат каких-либо аномалий, что указывает на отсутствие в исследованном интервале температур каких-либо фазовых переходов. Коэффициент линейного термического расширения для Gd1-xLaxInO3 0,2 ≤ x ≤ 1,0 при увеличении x изменяется незначительно, увеличиваясь от
8,48 · 10-6 К-1 для Gd0,8La0,2InO3 до 9,28 · 10-6 К-1 для LaInO3 (таблица 2), что согласуется с увеличением объема элементарной кристаллической ячейки
этих твердых растворов при увеличении степени замещения.
Таблица 2 – Средние линейные коэффициенты теплового расширения (α) образцов индатов
Gd1-xLaxInO3
Gd1-xLaxInO3, при x |
∙ 106, К–1 |
|
|
0,2 |
8,48 |
0,3 |
8,55 |
0,4 |
8,59 |
0,5 |
8,76 |
0,6 |
8,79 |
0,7 |
8,94 |
0,8 |
9,00 |
0,9 |
9,01 |
1,0 |
9,28 |
Таким образом, для индатов гадолиния-лантана установлены закономерности влияния изовалентного замещения парамагнитных ионов Gd 3+ диамагнитными ионами La3+ в Gd1-хLaxInO3 на кристаллическую структуру, ИК-спектры и коэффициент термического линейного расширения.
|
Литературные источники |
|
|
||
1. |
Соединения редкоземельных элементов. Системы с оксидами |
I – III групп |
/ |
||
П. А. Арсеньев [и др.] // М.: Наука. – 1983. – 280 с. |
|
|
|
||
2. |
Федоров, П.И. Химия галлия, индия, таллия / П. И. Федоров, М. В. Мохосоев, |
||||
Ф. П. Алексеев. – Новосибирск: Наука, 1977. – 222 с. |
|
|
|
||
3. |
Портной, К.И. Кислородные |
соединения |
редкоземельных |
элементов |
/ |
К. И. Портной, Н. И. Тимофеева. – М.: Металлургия, 1986. – 480 с. |
|
|
|||
4. |
Арсеньев, П.А. Кристаллохимия твердых растворов окисных соединений со |
||||
структурой перовскита / П. А. Арсеньев, |
В. В. Фенин, |
А. В. Потемкин // |
Межвузовский |
||
172

сборник / Уральск. политехн. ин-т. – Свердловск, 1979. – Вып.3: Химия твердого тела. – С. 55–59.
5.Писаренко, В.Ф. Скандобораты редких земель – новые лазерные материалы / В. Ф. Писаренко // Соросовский образовательный журнал. – 1996. – № 11. – C. 111–116.
6.Boulon, G. Fifty years of advance in solid-state laser materials / G. Boulon // Optical Materials. – 2012. – Vol. 34. – P. 499–512.
7.New opportunities for lanthanide luminescence / J.-C.G. Bünzli [et al.] // Journal of rare earths. – 2007. – Vol. 25, Issue 5. – P. 257–274.
8.Luminescent properties of a new red-emitting phosphor based on LaInO3 for LED / An Tang [et al.] // Optoelectronics and advanced materials – rapid communications. – 2011. – Vol. 5, №10. – P. 1031-1034.
9.Powder Diffraction File. Swarthmore: Joint Committee on Powder Diffraction Standard: Card № 00-043-1015.
10.Powder Diffraction File. Swarthmore: Joint Committee on Powder Diffraction
Standard: Card № 00-006-0416.
11.Powder Diffraction File. Swarthmore: Joint Committee on Powder Diffraction
Standard: Card № 00-026-0654.
12.Колебательные спектры двойных окислов индия и РЗЭ / Н.П. Поротников [и др.]
//Ж. неорган. химии. – 1980. – т. 25, № 12. – С. 3224–3228.
Kandidatova I.N., Bashkirov L.A., Petrov G.S.
SYNTHESIS AND PHYSICAL AND CHEMICAL PROPERTIES OF GADOLINIUM-
LANTHANUM SOLID SOLUTIONS
Belarusian State Technological University, Minsk
Summary
Indates of gadolinium-lanthanum Gd1-хLaxInO3 were prepared by ceramic method and their crystal structure, IR-spectra and thermal expansion were investigated. It was found that the samples with 0,2 ≤ x ≤ 1,0 subsitution degree had the structure of orthorhombically distorted perovskite. It was observed that IR-spectra of the samples were similar. Temperature dependences of relative elongation had no anomalies due to the phase transitions.
173

УДК 54.057 + 547.917 + 544.77.051
Красковский А.Н.
ПОЛУЧЕНИЕ И СВОЙСТВА НАНОЧАСТИЦ ПЕКТИНАТА КАЛЬЦИЯ
Институт химии новых материалов НАН Беларуси, Минск
Введение. Создание новых форм доставки лекарств является важной и актуальной проблемой современной фармакологии. Причиной этому служит низкая селективность действия многих лекарств, а, следовательно, высокая токсичность препаратов для организма. Для решения этой проблемы лекарственное вещество может быть заключено в полимерную матрицу. Использование полисахаридных микро- и наночастиц для капсулирования биологически-активных веществ позволит получать лекарственные формы с улучшенной растворимостью в биологических жидкостях и контролируемым временем высвобождения действующего вещества в организме [1]. Одним из перспективных материалов для создания новых лекарственных форм является природный биодеградируемый и биосовместимый полисахарид пектин, гели которого используются для включения биологически активных веществ [2–4].
Цель данной работы - синтез пектинатных наночастиц методом ионотропного гелеобразования и изучение их физико-химических свойств.
Экспериментальная часть. В работе были использованы следующие реактивы и материалы: полиэтиленимин (ПЭИ, М ~ 75000, Sigma-Aldrich), пектин цитрусовый (степень этерификации 71%, М ~ 120000-140000, SigmaAldrich), пектин амидированный (степень этерификации 32%, степень амидирования 18%, Herbstreith&Fox), полиоксиэтиленсорбитан моноолеат
(Твин 80).
Пектинатные наночастицы получали методом ионотропного гелеобразования. К 10 мл раствора СаCl2 (10 мг/мл) по каплям через капельную воронку в течение 20-30 мин добавляли 10 мл раствора пектина (1 мг/мл). Полученные наночастицы пектината кальция отделяли от маточного раствора центрифугированием, дважды промывали водой и редиспергировали
внебольшом количестве дистиллированной воды.
Впроцессе синтеза варьировали pH и ионную силу раствора полисахарида, наличие стабилизатора (Твин 80), а также время выдерживания полученных наночастиц пектината кальция в маточном растворе.
Морфологию пектинатных наночастиц исследовали методами атомносиловой (АСМ) и просвечивающей электронной микроскопии (ПЭМ).
Результаты исследований и их обсуждение. Методом ионотропного гелеобразования были синтезированы наночастицы пектината кальция (рисунок 1).
Экспериментально установлено, что при использовании высокоэтерифицированного цитрусового пектина формирование наночастиц пектината кальция не происходит. Известно, что амидированный
низкометоксилированный пектин образует более жесткие гели при
174

взаимодействии с ионами кальция, чем метоксилированный. Поэтому, для формирования наночастиц был взят пектин со степенью этерификации 32% и степенью амидирования 18%. Показано, что методом ионотропного гелеобразования путем взаимодействия амидированного пектина с катионами кальция можно сформировать устойчивые золи полисахаридных наночастиц.
Рисунок 1. Схема синтеза наночастиц пектината кальция
Согласно АСМ-данным, частицы пектината кальция имеют отрицательный заряд (так как адсорбируются только на положительно заряженный подслой ПЭИ) и плоскую округлую форму: перепад по высоте меньше диаметра примерно в 3 раза (рисунок 2).
Рисунок 2. АСМ-изображение наночастиц пектината кальция, адсорбированных на подслое ПЭИ.
Согласно литературным данным [5], размер пектинатных частиц может зависеть от степени ионизации макромолекул полисахарида. В данной работе степень ионизации полианиона регулировали за счет изменения pH и ионной силы раствора пектина.
175
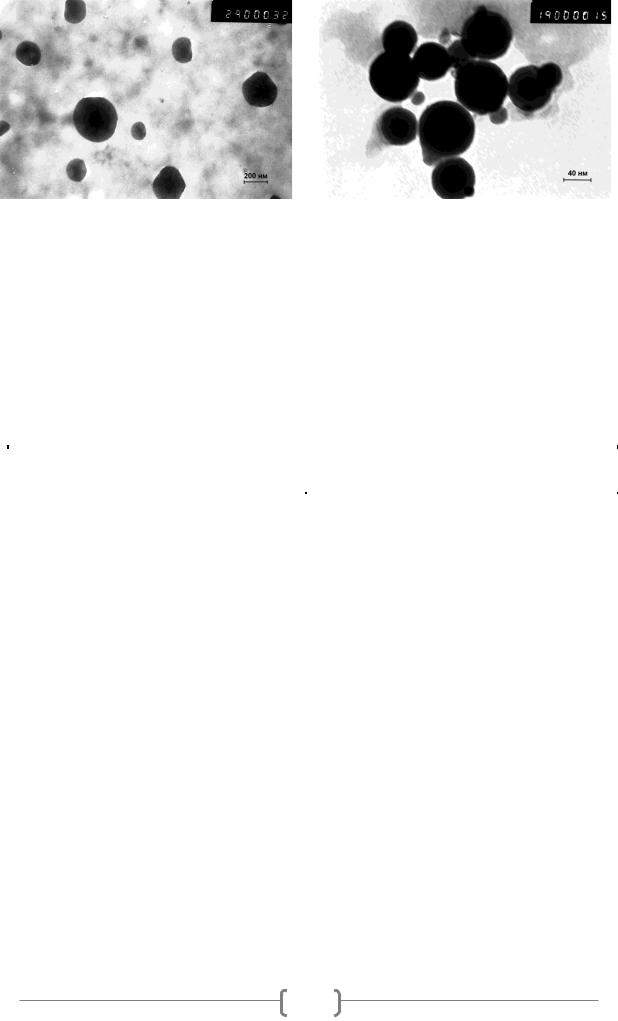
а |
б |
Рисунок 3. ПЭМ изображение наночастиц пектината кальция, синтезированных при рН
5,5 (а) и 3,5 (б).
Показано, что снижение рН (с 5,5 до 3,5), повышение ионной силы раствора пектина (0,2М NaCl), а также введение стабилизатора в процессе синтеза (1% масс. Твин 80) приводит к уменьшению среднего диаметра сформированных наночастиц пектината кальция приблизительно в 1,5–3 раза (рисунок 3, таблица). Следует отметить, что снижение pH и введение стабилизатора также способствуют повышению однородности получаемых наночастиц по размерам (таблица).
Таблица – Размеры наночастиц пектината кальция (по данным ПЭМ-анализа)
Условия синтеза |
Диаметр, нм |
|
|
pH 5,5, H2O |
262±97 |
pH 3,5, H2O |
61±15 |
pH 5,5, 0,2 М NaCl |
182±120 |
pH 5,5, 1 масс.% Твин 80 |
118±25 |
В данной работе также было оценено влияние времени выдерживания синтезированных пектинатных наночастиц в маточном растворе на их размер. Анализ АСМ-данных образцов наночастиц, полученных без и с выдерживанием в маточном растворе (1 сутки), позволяет сделать вывод о незначительном влиянии этого параметра на средний размер и полидисперсность.
Заключение. Таким образом, методом ионотропного гелеобразования были синтезированы наночастицы из амидированного низкоэтерифицированного пектина. Установлено, что их размер можно регулировать за счет изменения pH, ионной силы раствора и введения стабилизатора.
Литературные источники
1.Morris G.A., Kok M.S., Harding S.E., Adams G.G. // Biotechnology and genetic engineering reviews. 2010. Vol. 27. P. 257–284.
2.Young-Bin Song, Ji-Soo Lee, Hyeon Gyu Lee. α-Tocopherol-loaded Ca-pectinate microcapsules: Optimization, in vitro release, and bioavailability/ Colloids and Surfaces B: Biointerfaces, Volume 73, Issue 2, 15 October 2009, Pages 394-398.
176

3.Munjeri O., Collett J.H., Fell J.T. Hydrogel beads based on amidated pectins for colon-specific drug delivery: the role of chitosan in modifying drug release/ Journal of Controlled Release, Volume 46, Issue 3, 2 June 1997, Pages 273-278.
4.Sriamornsak P., Sungthongjeen S., Puttipipatkhachorn S. Use of pectin as a carrier for intragastric floating drug delivery: Carbonate salt contained beads/ Carbohydrate Polymers, Volume 67, Issue 3, 1 February 2007, Pages 436-445.
5.Opanasopit P. Development and Characterization of Pectinate Micro/Nanoparticles for Gene Delivery / P. Opanasopit, A. Apirakaramwong, T. Ngawhirunpat, T. Rojanarata, U. Ruktanonchai / AAPS PharmSciTech, Vol. 9, No. 1, March 2008. – P. 67-74.
Kraskovsky A.N.
SYNTHESIS AND PROPERTIES OF CALCIUM PECTINATE NANOPARTICLES
Institute of Chemistry of New Materials, National Academy of Sciences, Minsk
Summary
Calcium pectinate nanoparticles were prepared by ionotropic gelation. The morphology of nanoparticles was studied by atomic force and transmission electron microscopies. It was established, that size of calcium pectinate nanoparticles can be regulated by the changing pH, ionic force of solution and stabilizer introduction.
177

УДК 536.21:536.413:537.31/.32:54–165:54–31:666.654
Красуцкая Н.С., Клындюк А.И.
СИНТЕЗ И СВОЙСТВА ТВЁРДЫХ РАСТВОРОВ Na0,89Co1–xNixO2
(0,00 ≤ x ≤ 0,20)
Белорусский государственный технологический университет, Минск
Актуальность. Теплота, выделяющаяся в окружающую среду при работе промышленных предприятий и автотранспорта, может быть непосредственно и эффективно преобразована в электроэнергию при помощи термоэлектрогенераторов (ТЭГ) [1]. Для создания ТЭГ необходимы материалы, обладающие высоими значениями электропроводности и термоЭДС, низкой теплопроводностью и устойчивые на воздухе при высоких температурах. Таким комплексом свойств обладает слоистый кобальтит натрия NaxCoO2 и его производные, представляющие собой перспективную основу для разработки новых эффективных высокотемпературных термоэлектриков [2–4].
В настоящей работе изучено влияние частичного замещения кобальта никелем на кристаллическую структуру, микроструктуру, физико-химические и термоэлектрические свойства твердых растворов Na0,89Co1–xNixO2. Установлено, что замещение кобальта никелем приводит к улучшению термоэлектрических характеристик керамики на основе кобальтита натрия; так, фактор мощности твердого раствора Na0,89Co0,9Ni0,1O2 при 1100 К составляет 0,92 мВт/(м К2), что в 2,2 раза выше, чем для базовой фазы
Na0,89CoO2 (0,42 мВт/(м К2)).
Материалы и методы исследования. Твердые растворы состава
Na0,89Co1–xNixO2 ( x = 0,00; 0,05; 0,10; 0,15; 0,20) получали из Na2CO3 (ч.д.а.) и
оксидов Co3O4 (ч.), NiO (ос.ч.) керамическим методом в интервале температур 1133–1203 К на воздухе по методике, описанной в [5]. Идентификацию образцов и определение параметров их кристаллической структуры проводили при помощи рентгенофазового анализа (РФА) (рентгеновский дифрактометр Bruker D8 XRD Advance, излучение CuKα) и ИК-спектроскопии поглощения (Фурье-спектрометр Nexus фирмы ThermoNicolet, интервал частот 300–1500 см–1). Кажущуюся плотность (ρэксп) образцов определяли по их массе и геометрическим размерам. Тепловое расширение, электропроводность ( ) и термо-ЭДС (S) образцов изучали на воздухе в интервале температур 300– 1100 К по методикам [5, 6]. Фактор мощности (P) керамики находили по формуле P = S2 .
Результаты и обсуждение результатов исследования. После завершения синтеза образцы были однофазными, в пределах погрешности РФА, и имели структуру гексагонального кобальтита натрия γ-NaxCoO2 [7]. Как видно приведенных в таблице данных, частичное замещение кобальта никелем приводит к увеличению объема элементарной ячейки твердых растворов Na0,89Co1–xNixO2 и одновременному ее сжатию в направлении оси с
178

(осевое отношение (с/а) твердых растворов Na0,89Co1–xNixO2 (3,583–3,850) меньше, чем у базовой фазы Na0,89CoO2 (3,868)). Кажущаяся плотность
керамики Na0,89(Co,Ni)O2 была ниже, чем фазы Na0,89CoO2 (таблица), из чего следует, что замещение кобальта никелем ухудшает спекаемость керамики на
основе слоистого кобальтита натрия.
Параметры кристаллической структуры(a, c, c/a, V). кажущаяся плотность ( ) и коэффициент линейного термического расширения ( ) твердых растворов Na0,89Co1–xNixO2
(0,00 ≤ x ≤0,20)
x |
a, нм |
с, нм |
c/a |
103·V, нм3 |
, г/см3 |
106· , К–1 |
0,00 |
0,2826 |
1,093 |
3,868 |
75,60 |
3,60 |
13,4 |
0,05 |
0,2911 |
1,072 |
3,683 |
78,70 |
3,39 |
16,7 |
0,10 |
0,2834 |
1,091 |
3,850 |
75,87 |
3,46 |
14,2 |
0,15 |
0,2831 |
1,089 |
3,847 |
75,63 |
3,39 |
16,1 |
0,20 |
0,2993 |
1,072 |
3,583 |
83,19 |
3,29 |
16,8 |
Кристаллиты полученной керамики имели форму пластин, широкой стороной ориентированных, в основном, перпендикулярно оси прессования;
размер пластин составлял до 50 мкм для базового образца Na0,89CoO2 и 10–25 мкм для фазы Na0,89Co0,9Ni0,1O2 (рис. 1).
а) |
|
б) |
|
|
|
Рисунок 1. Электронные микрофотографии сколов керамики Na0,89CoO2 (а), Na0,89Co0,9Ni0,1O2 (б)
Температурные зависимости относительного удлинения образцов в интервале температур 300–1100 К были линейными, из чего следует, что в этом интервале температур оксиды Na0,89(Co,Ni)O2 не претерпевают структурных фазовых переходов. Величина КЛТР керамики изменялась в пределах (14,2– 16,8) 10–6 К–1, возрастая при замещении кобальта никелем.
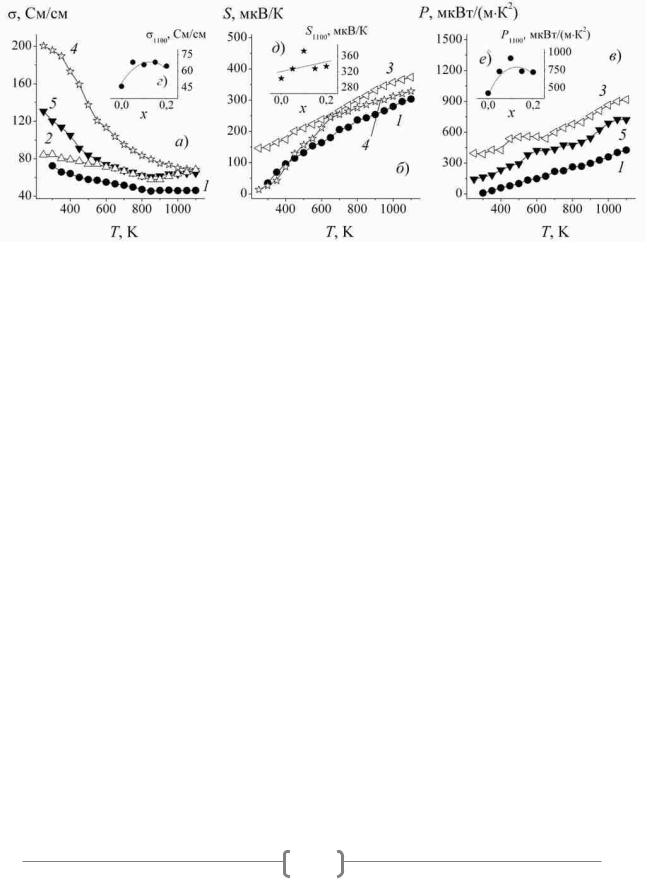
Зависимость σ = f(T) для базовой фазы Na0,89CoO2 и твердых растворов Na0,89Co1–xNixO2 носила металлический характер ( / T < 0), при этом величина электропроводности образцов варьировалась в пределах 84,0–200 См/см при
комнатной температуре и 46,2–68,0 См/см при 1100 К, возрастала при замещении кобальта никелем и слабо изменялась с ростом x (рис. 2 а, г). ТермоЭДС фаз Na0,89(Co,Ni)O2 возрастала с ростом температуры и во всем исследуемом интервале температур была положительна, из чего следует, что основными носителями заряда являются «дырки», т. е. изученные кобальтиты представляют собой проводники p-типа (рис. 2, б). Величина S керамики увеличивалась при увеличении степени замещения кобальта никелем в составе
179
фаз Na0,89Co1–xNixO2 (рис. 2, в).
Величина фактора мощности керамики Na0,89Co1–xNixO2 возрастала с ростом температуры и при замещении кобальта никелем (рис. 2в, e), причем
максимальным значением P |
обладал |
твердый раствор Na0,89Co0,9Ni0,1O2 – |
0,92 мВт/(м К2) при 1100 К, |
что в 2,2 |
раза выше, чем для фазы Na0,89CoO2 |
(P1100 = 0,42 мВт/(м К2)). |
|
|
Рис. 2. Температурные (а–в) и концентрационные (г–е) зависимости электропроводности
(а, г), термо-ЭДС S (б, д) и фактора мощности P (в, е) твердых растворов Na0,89Co1– xNixO2: x = 0,00 (1); 0,05 (2) 0,10 (3); 0,15 (4); 0,20 (5).
Выводы. Установлено, что частичное замещение кобальта никелем в фазах Na0,89Co1–xNixO2 приводит к увеличению объема их элементарной ячейки, ухудшению спекаемости, увеличению электропроводности, термо-ЭДС и коэффииента линейного теплового расширения, и, в целом, улучшает их термоэлектрические свойства. Так, величина фактора мощности образца
Na0,89Co0,9Ni0,1O2 при 1100 К составляет 0,92 мВт/(м К2), что в 2,2 раза выше, чем для базового оксида Na0,89CoO2 (0,42 мВт/(м К2)) и позволяет рассматривать твердые растворы Na0,89Co1–xNixO2 как перспективную основу
для разработки новых высокотемпературных термоэлектриков.
Работа выполнена в рамках ГПНИ «Функциональные и машиностроительные материалы и технологии, наноматериалы и нанотехнологии», подпрограмма «Кристаллические и молекулярные структуры» (задание 1.02).
Литературные источники
1. Rowe D. M., CRC Handbook of Thermoelectrics, CRC Press, Boca Raton, 1995, P.
107.
2.Influence of partial substitution of Cu for Co on the thermoelectric properties of NaCo2O4 / K. Park [et al.] // J. of Alloys and Comp. – 2006. – Vol. 407 – P. 213–219.
3.Park, K. Improvement in high-thermoelectric properties of NaCo2O4 through partial substitution of Ni for Co / K. Park, K. U. Jang // Materials Letters – 2006. – Vol. 60 – P. 1106– 1110.
4.Park, K. Enhanced termoelectric properties of NaCo2O4 by adding ZnO / K. Park,
180
