
- •10. Арени. Бензен та його похідні
- •1. Класифікація. Номенклатура. Ізомерія.
- •2. Методи добування.
- •3. Фізичні властивості.
- •4. Хімічні властивості.
- •5. Екологічні питання.
- •10.1. Технологічна схема синтезу етилбензену.
- •10.2. Технологічна схема виробництва стиролу.
- •10.3. Технологічна схема уловлювання бензену при виробництві малеїнового ангідриду.
3. Фізичні властивості.
Бензен та його гомологи – безбарвні рідини з характерним запахом. Нерозчинні у воді, добре розчинні у більшості органічних розчинників; легко переганяються із водяною парою. Із збільшенням молекулярної маси, температури кипіння закономірно зростають, (табл. 10.1).
4. Хімічні властивості.
Хімічні властивості бензолу та його похідних визначаються наявністю 6-електронної супряженої системи. Арени – хімічні сполуки з яскраво вираженим нуклеофільним характером, тому для них характерні реакції електрофільного заміщення (SE) із збереженням ароматичного циклу. Реакції приєднання (АЕ) для аренів менш характерні, тому як при цьому порушується ароматичність циклу; лише в жорстких умовах арени вступають у реакцію окиснення.
4.1. Реакції електрофільного заміщення (SE) – головний і найважливіший тип реакцій аренів:

Ці реакції відбуваються за механізмом електрофільного заміщення (SE):

На першій стадії спочатку утворюється нестійкий -комплекс, який потім переходить у -комплекс (карбокатіон). Утворення останнього відбувається із порушенням ароматичної системи і переходом одного атома карбону в sp3-гібридний стан. Утворення -комплексу є найбільш енергетичною стадією реакції, тому позитивний заряд карбокатіона делокалізується за допомогою наведених резонансних структур.
|
|
На
другій стадії
відщеплення протону в присутності
сильного нуклеофіла, наприклад
| |
|
Рис. 10.1. Енергетична діаграма реакції електрофільного заміщення. |
Реакція електрофільного заміщення є реакцією другого порядку: V=k[C6H5][E+]. Механізм реакції електрофільного заміщення можна розглянути за допомогою енергетичної діаграми, рис. 10.1. Точка 1 енергетичного профіля відповідає -комплексу (енергія активації Е1); точка 2 – -комплексу (енергія активації Е2); відщепленню протона і утворенню продукта реакції відповідає енергія активації Е3. По даному енергетичному графіку реакція екзотермічна, що відповідає Ер реакції. 4.2. Правила орієнтації при заміщенні у бензольному ядрі. Молекула бензолу симетрична і тому всі атоми карбону абсолютно рівноцінні при утворенні монозаміщених продуктів реакції. Якщо у бензольному ядрі уже є замісник і ми вводимо туди ще один, то при цьому можуть утворюватись наступні ізомери: | |

Положення, яке буде займати наступний замісник визначається природою початкового замісника (М та І-ефектами). Згідно до цього початкові замісники (Х) можна розділити на дві групи: замісники І та замісники ІІ роду.
Замісники І роду (орто- та пара-орієнтанти в реакціях SE) – це атоми або групи атомів, які є донорами електронів. За винятком алкільних радикалів (Alk-) вони мають вільні електронні пари на атомі, що безпосередньо поєднується із ароматичним ядром:

Збагачення ароматичного ядра електронною густиною прискорює реакції SЕ:
|
|
наявність гідроксильної групи (-ОН) дає змогу провести реакцію в „м’яких” умовах та збільшити її швидкість у порівнянні із незаміщеними бензенуми. |
Таким чином, механізм орієнтуючої дії замісників І роду полягає у тому, що вони збільшують ступінь делокалізації позитивного заряду -комплекса у порівнянні із незаміщеним -комплексом бензену. Це означає, що стабільність такого -комплекса збільшується, а енергія активації зменшується, що приводить до прискорення реакції. Порівняння відносної стабільності о-, м- та п--комплексів розглянемо на прикладі реакції SE для фенолу:

Наведена схема показує, що у випадку о- та п--комплексів делокалізація заряду можлива завдяки чотирьом межовим структурам (I-IV), тоді як у випадку м--комплексу така делокалізація можлива лише за рахунок трьох межових структур (І-ІІІ), тому реакція SE йде переважно в орто- та пара-положення.
Замісники ІІ роду (мета-орієнтанти в реакції SE) – це групи атомів, які є акцепторами електронів. Вони мають цілий або частково позитивний заряд на атомі, що безпосередньо поєднується із ароматичним ядром:

Замісники ІІ роду зменшують електронну густину в бензольному ядрі і знижують швидкість реакції SE у порівнянні із незаміщеним бензеном:
|
|
наявність нітрогрупи (–NO2) потребує більш „жорстких” умов нітрування нітробензену, швидкість реакції зменшується у порівнянні з нітруванням незаміщеного бензену. |
Механізм орієнтуючої дії замісників ІІ роду (реакція SE) полягає в тому, що вони зменшують ступінь делокалізації позитивного заряду -комплексу у порівнянні із незаміщеним -комплексом бензену. При цьому стабільність такого -комплексу зменшується, а енергія активації збільшується, що приводить до зменшення швидкості реакції. Порівняння відносної стабільності о-, м- та п--комплексів розглянемо на прикладі реакції нітрування нітробензену:

Наведена схема показує, що у випадку м--комплексу делокалізація заряду відбувається згідно з трьома межовими структурами (І-ІІІ), тоді як у випадку о- та п--комплексів структури (ІІІ) вкрай невигідні, оскільки позитивні заряди знаходяться на двох суміжних атомах і імовірність їх існування дуже мала. Тому делокалізація позитивного заряду у випадку о- та п--комплексів фактично зводиться до двох межових структур – І та ІІ, тому реакція йде переважно в мета-положення.
Узагальнюючи правила орієнтації при заміщені у бензольному ядрі треба відмітити, що:
правила орієнтації не мають обов’язкового характера, а лише вказують на два головних напрямки реакції;
правила орієнтації діють і в небензоїдних ароматичних сполуках.
4.3.Реакції приєднання.
Реакції приєднання (гідрування, хлорування) для аренів малохарактерні і вимагають більш жорстких умов, ніж у випадку алкенів та алкінів.
|
|
реакції відбуваються до повного насичення, тому зупинити їх на стадії часткового гідрування (хлорування) неможливо. |
4.4. Реакції окиснення.
Арени за звичайних умов стійкі до дії сильних окисників (KMnO4, K2Cr2O7, CrO3). Реакція відбувається в “жорстких” умовах із використанням V2O5як каталізатора:

малеїновий ангідрид
Гомологи бензену, що мають бокові вуглеводневі ланцюги, окиснюються значно легше:
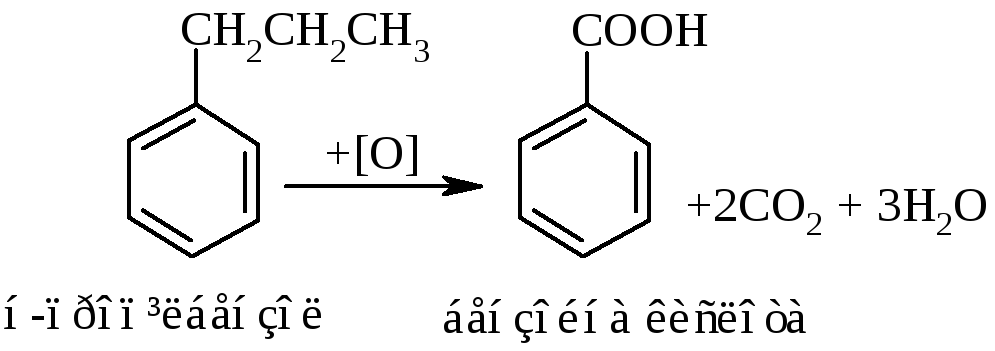
Особливості окиснення гомологів бензену:
незалежно від довжини бічного ланцюга він окиснюється до кінцевої карбоксильної групи;
при наявності кількох бокових ланцюгів, кожний наступний окиснюється у більш “жорстких” умовах, ніж попередній.
4.5. Реакції озонування.
Арени взаємодіють із озоном за схемою:






