- •12. Галогенопохідні вуглеводнів
- •1. Класифікація. Номенклатура.
- •2. Методи отримання.
- •2.1. Пряме галогенування алканів (тема „Алкани”), sr:
- •2.2. Приєднання галогеноводнів до алкенів (тема „Алкени”)
- •2.3. Заміщення функціональних груп (–oh, –Hal) на галоген.
- •2.4. Одержання ароматичних галогенпохідних галогенуванням вуглеводневого радикалу або бензольного ядра.
- •3. Фізичні властивості.
- •4. Характеристика зв’язків вуглець–галоген с–Hal.
- •5. Хімічні властивості.
- •5.2. Реакції нуклеофільного заміщення галогена, пов’язаного з ароматичним ядром.
- •5.3. Реакції відщеплення (-елімінування).
- •6. Екологічні питання.
12. Галогенопохідні вуглеводнів
Галогенопохідні вуглеводнів – це органічні сполуки, до складу яких входить один або декілька атомів галогену, сполучених із вуглеводневим радикалом.
1. Класифікація. Номенклатура.
Загальна формула R–Hal. В залежності від природи та будови радикалу R галогенопохідні вуглеводнів розрізняють: насичені, ненасичені, ароматичні та інші.
В залежності від природи галогену (F, Cl, Br, I) та їх кількості вони бувають: моно- (CH3CH2CH2Br, 1-бромпропан), ди- (ClCH2CH2Cl, дихлоретан) та полі- (CF2=CF2, перфторетилен) похідними. В залежності від того, біля якого атома карбону знаходиться атом галогена галогенопохідні вуглеводнів розрізняють як первинні, вторинні та третинні.Деякі приклади відмічених особливостей будови галогенопохідних вуглеводнів, а також їх номенклатури навдено у табл. 12.1.
Таблиця 12.1.
Назви та фізичні константи деяких галогенопохідних вуглеводнів.
|
Формула |
Номенклатура IUPAC |
Тпл., °С |
Ткип., °С | |
|
замісникова |
раціонально-функціональна | |||
|
|
фторметан |
метилфторид |
-141,8 |
-78,5 |
|
|
хлорметан |
метилхлорид |
-97,7 |
-23,7 |
|
|
бромметан |
метилбромід |
-93,7 |
3,6 |
|
|
йодметан |
метилйодид |
-66,5 |
42,5 |
|
|
хлоретан |
етилхлорид |
-138,7 |
12,3 |
|
|
1-хлорпропан |
пропілхлорид |
-122,8 |
47,2 |
|
|
2-хлорпропан |
ізопропілхлорид |
-117 |
35,4 |
|
|
хлоретилен |
вінілхлорид |
-159,7 |
-13,8 |
|
|
3-хлорпропілен |
алілхлорид |
-136,4 |
44,6 |
|
|
дихлорметан |
метиленхлорид |
-96,8 |
40,2 |
|
|
трихлорметан |
хлороформ |
-63,5 |
61,2 |
|
|
тетрахлорметан |
чотирьоххлористий вуглець |
-22,9 |
76,7 |
|
|
хлорбензол |
фенілхлорид |
-45,2 |
131,7 |
|
|
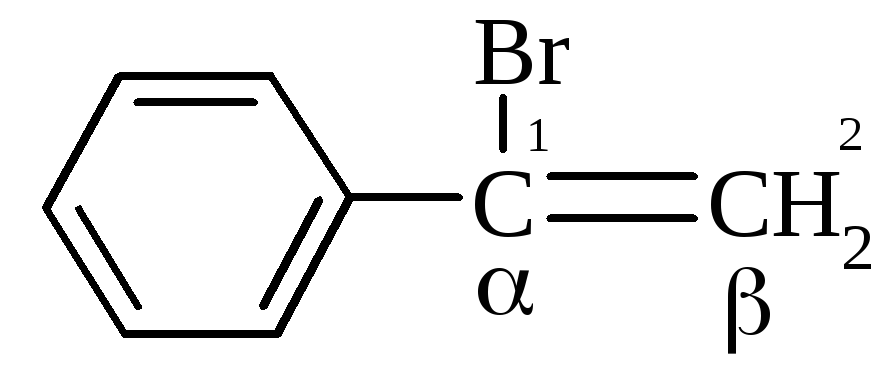
1-бром-1-фенілетилен |
-бромстирол* |
-43,5 |
160** |
Примітки: *за раціональною номенклатурою; ** при 75 мм. рт. ст.
Назва за номенклатурою IUPAC (раціонально-функціональна): алкільний радикал + галоген.
2. Методи отримання.
Як правило, існуючі синтетичні методи отримання хлор-, бром- та йодпохідних вуглеводнів, не придатні для отримання фторпохідних вуглеводнів. Ці методи будуть розглянуті окремо.
2.1. Пряме галогенування алканів (тема „Алкани”), sr:
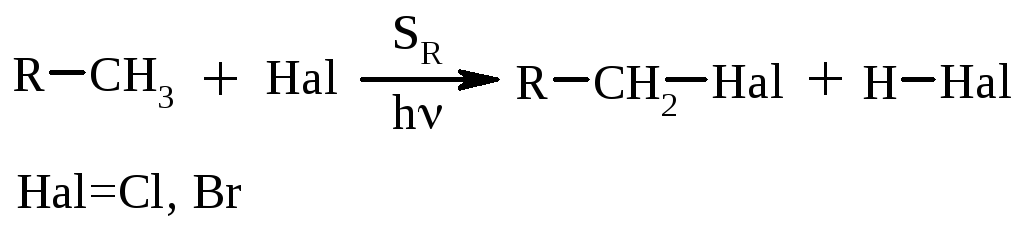
Недоліки: а) отримують суміш моно- та поліпохідних; б) неможливість отримання іодпохідних.
2.2. Приєднання галогеноводнів до алкенів (тема „Алкени”)
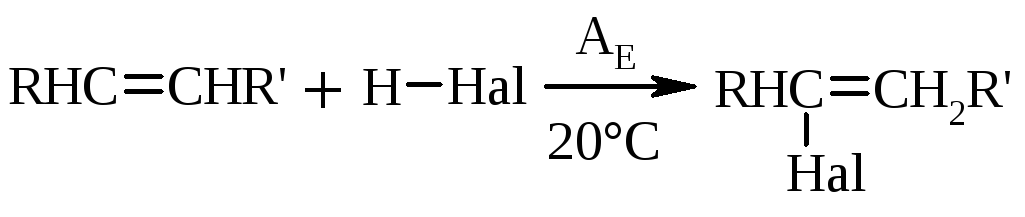
Особливості: а) отримують будь-які монопохідні (Нal=F, Cl, Br, I); б) реакційна здатність змінюється у ряду HI>HBr>HCl>HF; в) у випадку реакцій АЕ приєднання H-Hal проходить за правилом Марковникова.
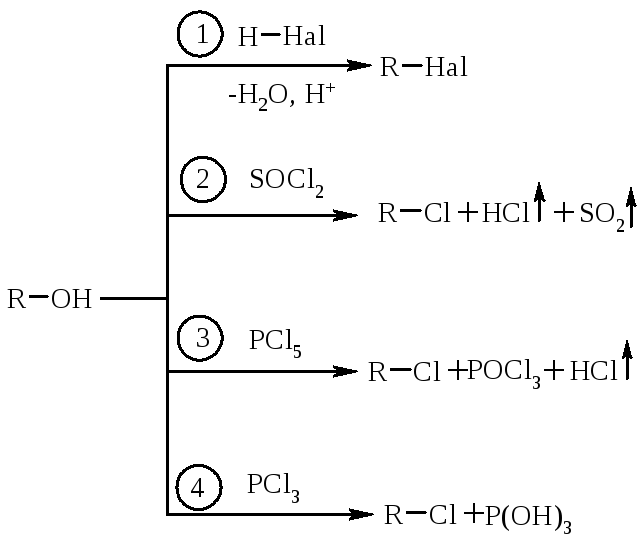
2.3. Заміщення функціональних груп (–oh, –Hal) на галоген.
2.3.1 Одержання із спиртів.
|
|
(Н+ – концентрована H2SO4 для „зв’язування” Н2О). Нal=Cl, Br, I. швидкість реакції для Н-Нal зменшується у ряду: HI>HCl>HBr; для спиртів різної будови: третинний>вторинний>первинний. | |
|
(реакція з хлористим тіонілом зручна, так як всі побічні продукти газоподібні) | ||
|
|
Реакція іде в „м’яких” умовах | |
2.3.2 Заміщення одного галогену іншим (отримання фторпохідних вуглеводнів).
![]()
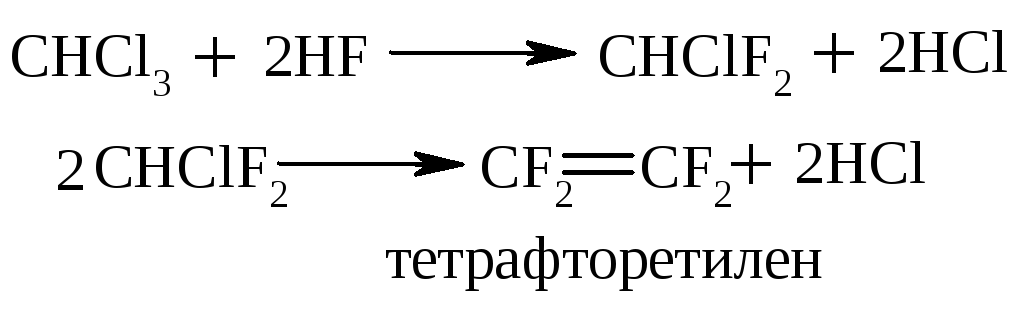
тетрафторетилен – мономер
для отримання промислового
потітетрафторетилену, Ф-4: 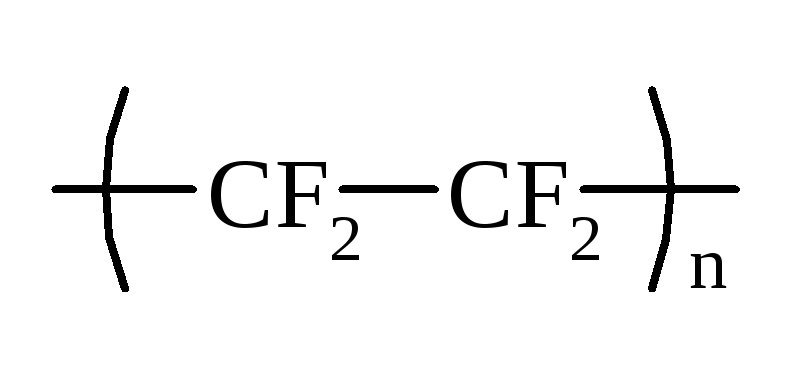 .
.