
- •Андреев в.П. Принципы структурно-функциональной организации и биология эукариотической клетки
- •Свойства мембраны
- •Хромосóмы
- •По g-методу. Примечание: в изображении одной хромосомы объединены две схемы.
- •Нормальный кариотип человека в метафазе митоза
- •Ядрышко
- •Митохондрии
- •Происхождение митохондрий
- •Митохондриальная хромосома
- •Рибосома
- •Эндоплазматическая сеть
- •Комплекс Гольджи
- •Архитектура клетки (цитоскелет)
- •Микротрубочки
- •Функции цитоскелета
- •Межклеточные взаимодействия
- •Щелевидные соединения (нексусы)
- •Межклеточные сигнальные вещества
Свойства мембраны
1.Текучесть. В процессе жизнедеятельности мембраны клетки подвергаются значительным изменениям. Этот процесс возможен благодаря подвижности и динамичности молекул, составляющих мембрану. «Дрейф» компонентов в латеральной плоскости мембраны происходит достаточно легко; это наблюдается при группировке рецепторов, фагоцитозе и др. процессах эндоцитоза и экзоцитоза. Переход белков с внешней стороны мембраны на ее внутреннюю сторону («флип–флоп») невозможен, а переход липидов происходит крайне редко. Для «перескока» липидов и их переноса из одного слоя мембраны в другой необходимы специальные белки транслокаторы. Холестерин может легко переходить с однго слоя мембраны на другой, а незаряженные липиды могут проходить через мембрану.
2. Асимметрия. Все мембраны клетки имеют асимметричную организацию, для поддержания которой существуют специальные механизмы. Так фосфолипид фосфатидилсерин, несущий отрицательный заряд, концентрируется в основном на внутреннем слое мембраны, а гликолипиды (ганглиозиды, цереброзиды) – исключительно в наружном слое мембраны.
3. Полярность. Внутренняя поверхность мембраны (обращенная к цитоплазме) в нормальных условиях жизнедеятельности всегда заряжена отрицательно по отношению к внешней среде. Разность потенциалов между внутренней и внешней поверхностями составляет для разных типов клеток от 4 до 100 милливольт (мВ). Для нервных клеток эта величина, которую называют потенциалом покоя, равна примерно 70-75мВ. Раздражители или факторы, которые гиперполяризуют мембрану, обладают положительным биологическим действием. Существует множество факторов, при воздействии которых на клетку происходит снижение мембранного потенциала ниже уровня потенциала покоя. Следует отметить, что все наркотики и, в частности, алкоголь в первой стадии вызывают развитие гиперполяризационных процессов в нервной системе (возможно, в этом кроется одна из причин наркотической и алкогольной зависимости), а затем наступает длительная деполяризация, истощение и разрушение нервных клеток. Организм должен избегать раздражителей, постоянно деполяризующих мембраны его клеток, поскольку это грозит гибелью.
4. Избирательная проницаемость. Это свойство обеспечивает обмен веществ между клеткой и внешней средой. Процесс прохождения веществ через клеточную мембрану называют трансмембранным транспортом (переносом) веществ; он лежит в основе процессов поддержания клеточного гомеостаза, оптимального содержания в клетке ионов, воды, ферментов и субстратов. Трансмембранный перенос мелких молекул осуществляется путем диффузии и путем активного транспорта. Трансмембранный перенос крупных молекул происходит в форме эндоцитоза, экзоцитоза и трансцитоза.
Перенос веществ через мембраны
Избирательная проницаемость реализуется путем пассивного транспорта (без затрат энергии) и активного (с затратой энергии). Существуют два вида пассивного транспорта: диффузия и облегченная диффузия. Путем диффузии осуществляются движения молекул газов (О2, СО2, N2) и воды в обоих направлениях по градиенту концентрации или электрохимическому градиенту. Облегченная диффузия является специфическим видом транспорта. Она осуществляется с участием компонентов мембраны (белки-переносчики, каналы).
Существуют многочисленные белки-переносчики и ионные каналы. Хорошим примером может служить белок-переносчик, обеспечивающий двунаправленное (из клетки и в клетку) движение анионов (Cl- и HCO-3) через эритроцитарную мембрану. Перенос глюкозы в клетку также осуществляют интегральные гликопротеины. Гормон инсулин мобилизует перемещение этих белков-переносчиков из цитоплазмы в плазматическую мембрану, при этом ускоряется транспорт глюкозы в клетку. Известно не менее шести кодируемых генами ГЛУТ (GLUT) трансмембранных переносчиков глюкозы из внеклеточной среды. Такие переносчики находятся в нервной ткани, в эпителии кишечника, эпителии канальцев почек, сперматозоидах и др. Точечная мутация гена ГЛУТ2 является причиной инсулиннезависимого сахарного диабета.
Транспорт аминокислот также осуществляется с помощью белков-переносчиков. Несколько мутаций гена SLC3А1, кодирующего транспортный белок-переносчик цистеина, сопровождается избыточной секрецией этой плохо растворимой аминокислоты и проводит к образованию камней в почках. Известно не менее десятка переносчиков различных аминокислот.
Обратное всасывание фосфатов происходит в проксимальных канальцах нефрона при помощи двух кодируемых генами NPТ2 переносчиков. Дефекты этих генов являются причиной некоторых болезней, в том числе рахита, который невозможно вылечить витамином Д.
Важными элементами в системе пассивного транспорта являются регулируемые поры, обычно именуемые ионными каналами. Ионные каналы состоят из нескольких связанных белковых субъединиц, формирующих в мембране небольшую пору. Через пору по электрохимическому градиенту проходят ионы Na+,K+,Ca2+,Cl-. Калиевые каналы – интегральные мембранные белки, обнаружены в плазматической мембране всех клеток. Эти каналы участвуют в поддержании мембранного потенциала, регуляции объема клетки и др. Калиевый канал регулирует в β-клетках островков Лангерганса секрецию инсулина в ответ на повышение содержания глюкозы в крови.
Натриевые каналы присутствуют практически в любой клетке. В возбудимых структурах (скелетные мышечные волокна, нейроны, кардиомиоциты) натриевые каналы генерируют потенциал действия. Это плазмалемма нервных клеток, кардиомиоцитов и мышечных волокон, сперматозоидов, чувствительных клеток органов чувств. Натриевые каналы открываются только при возбуждении. (В сетчатке глаза Na+-каналы при возбуждении закрываются, тогда, как в покое открыты). Через открывающиеся Na+ каналы ионы Na+ устремляются внутрь клетки по градиенту концентрации и заряда. При этом происходит снижение трансмембранного потенциала с –75мВ до +30мВ. Возникновение положительной разности потенциалов (деполяризация) индуцирует закрытие Na+-каналов. Таким образом, Na+-каналы являются важнейшими структурами в развитии таких процессов, как возбуждение мембраны (вне синапса) и проведение возбуждения по мембране.
На функцию Na+-каналов влияют ионы Са++: чем выше их внеклеточная концентрация, тем трудней открываются Na+ каналы. В итоге ионы Са++ уменьшают возбудимость мембраны. При гипокальцемии (которая может возникать при удалении паращитовидных желез) в нервных и мышечных тканях значительно повышается возбудимость мембран. Функцию натриевых каналов могут блокировать многие агенты: местные обезболивающие вещества, противосудорожные препараты, токсины, и мн.др.

Антагонистами натриевых каналов (блокирующих их функцию) являются такие яды как тетродотоксин, батрахотоксин. Батрахотоксин (полулетальная доза + 2мг/кг) выделен из кожных желез маленькой (2-3см) колумбийской древесной лягушки. Индейцы ядом из этих лягушек смазывали наконечники стрел. Раньше батрахотоксин считался «самым сильным» небелковым ядом в природе. Сейчас он переместился с первого места на четвертое.
Тетродотоксин – один из самых знаменитых животных ядов. Он содержится в коже и яйцах некоторых жаб, в яйцах калифорнийского тритона, в слюнных железах осьминога. Но наибольшую известность ему принесла рыба фугу, у которой яд содержится в яичниках и печени. Для тетродотоксина полулетальная доза 10мкг/кг (1мкг – миллионная доля грамма). Тетродотоксин относится к нейротропным ядам, которые блокируют проницаемость мембран нейронов вегетативной нервной системы для ионов натрия, что практически мгновенно прерывает нервный импульс.
Каналы водные (аквапорины) – семейство мембранных пор, предназначенные для облегченной диффузии воды. Молекулы воды способны пересекать липидный бислой плазматических мембран. Этому способствуют малые размеры молекулы воды и отсутствие у неё заряда. Однако в некоторых тканях (клетки почечных канальцев, секреторные эпителиальные клетки желез, например, слюнных, слезных и др.), где транспорт воды особенно интенсивен, простой диффузии воды недостаточно для нормального функционирования. В мембранах таких клеток присутствует особый белок – аквапорин, который обеспечивает свободное движение воды через мембрану. Известны 5 типов белков, формирующих водные каналы. Аквапорин 1 экспрессируется в эритроцитах, проксимальных извитых канальцах и петле Генле, тканях глаза; аквапорин 2 – формирует каналы в собирательных трубочках почки. Активность этого канала регулирует антидиуретический гормон (АДГ), увеличивая реабсорбцию воды из просвета трубочек в межклеточное пространство. Нефрогенный несахарный диабет – следствие мутации гена (АQP 2, 107777, 12 q 13) аквапорина 2. Аквапорин 3 – образует водные каналы в печени поджелудочной железе, кишечнике, селезенке, простате; аквапорин 4 – экспрессируется в клетках сосудистого сплетения мозга (этот канал является осморецептором); аквапорин 5 – транспортирует воду в слезных и слюнных железах.
Мембранные каналы для молекулы воды впервые выделил в 1988г. американец Питер Эгр из университета Джона Хопкинса (Балтимор). За исследование белков, служащих каналами для воды и ионов калия, Питер Эгр и Родерик Мак-Киннон удостоены в 2003г. Нобелевской премии.
Управление мембранными ионными каналами
Ионные каналы имеют структурное образование, непосредственно отвечающее за их пропускную способность. Эту структуру называют воротами (аналогия с открытыми и закрытыми воротами). «Ворота» открываются под воздействием разных сигналов. Молекулярный воротный механизм заключается в изменениях общей конформации белка ионного канала под влиянием сигнала.
Регуляция конформационного состояния канала осуществляется различными способами.
Рецептор-зависимые ионные каналы снабжены рецепторами, которые распознают сигнальную молекулу (хим. сигнал). Такие каналы открываются или закрываются при участии нейромедиаторов, биогенных аминов (адреналин, дофамин и др.), АТФ, циклических нуклеотидов. Например, такие нейромедиаторы как гамма-аминомасляная кислота и аминокислота глицин открывают в синапсах определенных нейронов хлорные каналы и пропускают ионы Cl, несущие отрицательный заряд. Проникновение хлора вызывает в нервной клетке состояние гиперполяризации, то есть торможение (передача возбуждения происходит за счет противоположного процесса: деполяризации мембраны нейрона). Глицин (альфа-аминоуксусная кислота) подавляет раздражимость и делает поведение более разумным, повышает скорость реакций, усиливает умственную работоспособность, т.е. обладает ноотронным действием (noos – ум, tropos – действие).
Активность некоторых каналов может изменяться под влиянием метаболических реакций и фосфорилирования.
Потенциалзависимые ионные каналы пропускают катионы при изменении мембранного потенциала. Механочувствительные каналы открываются при деформации мембраны. Например, в коже имеются чувствительные нервные окончания – тельца Пачинни, в которых ионные каналы реагируют на механическое воздействие.
Мембранные каналы чувствительны к температуре, реагируют также на химические вещества, вызывающие чувство прохлады или жжения: ментол, капсаицин (жгучее вещество перца), изотиоцианат горчицы и хрена и мн. др. Активность ионных каналов может изменяться под влиянием токсинов и лекарственных веществ. Некоторые заболевания возникают в результате выработки специфических антител против белков ионных каналов.
Активный транспорт
При активном транспорте перемещение вещества происходит против его концентрационного градиента (от лат. gradus – ступень). В связи с этим этот вид трансмембранного переноса веществ нуждается во внешнем источнике энергии. Таким источником служит гидролиз АТФ.
Примером системы активного транспорта может служить так называемый Na+/K+-насос в клеточных мембранах животных клеток. Этот насос иначе называется Na+/K+ АТФазой, поскольку выкачивание из клетки натрия и закачивание в нее калия сопряжено с гидролизом АТФ до АДФ. Благодаря работе этого насоса в клетках поддерживается высокая концентрация ионов калия (140мМ) и низкая – ионов натрия (12мМ), между тем как в крови и межклеточной жидкости соотношение этих концентраций – обратная. Работа Na+/K+ насоса создает разность потенциалов в 50-70мB (плюс – снаружи плазматической мембраны, минус – внутри).
Трансмембранный Na+-градиент, создаваемый Na+/K+ АТФазой, есть не что иное, как форма запасания энергии. Эта энергия рассеивается в виде тепла, если ионы натрия диффундируют в клетку. Однако в некоторых клетках существуют белки, ответственные за совместный перенос ионов натрия с другими молекулами, например, глюкозой, аминокислотами. При этом глюкоза и аминокислоты двигаются против собственного концентрационного градиента. Такой механизм одновременного переноса функционирует при всасывании аминокислот и глюкозы в кишечнике.

Натрий-калиевый насос – интегральный мембранный белок, состоящий из двух субъединиц. Каталитическая субъединица α гидролизует АТФ, гликопротеин β является структурным элементом. Na+/K+ насос регулирует потоки воды, поддерживая постоянный объем клетки; обеспечивает Na+- связанный транспорт множества органических и неорганических молекул; участвует в генерации потенциала действия нервных и мышечных элементов. На поддержание ионных градиентов животные тратят около трети расходуемой энергии.
Наряду с Na+/K+-насосом существуют и другие АТФазы. Например, протонная и калиевая АТФаза участвует в образовании соляной кислоты в париетальных клетках желудка. Протонная АТФаза перекачивает протоны (Н+) из цитоплазмы в лизосомы, где создается кислая среда. Ca2+-АТФаза мышц откачивает ионы кальция из цитоплазмы в полости гладкой эндоплазматической сети, именуемой в скелетных мышечных волокнах и кардиомиоцитах саркоплазматической сетью (лат. sarcos – мясо). Недостаточность этого насоса проявляется симптомами мышечной усталости при физической нагрузке (Миопатия Броди). Это проявляется в виде частых судорог.
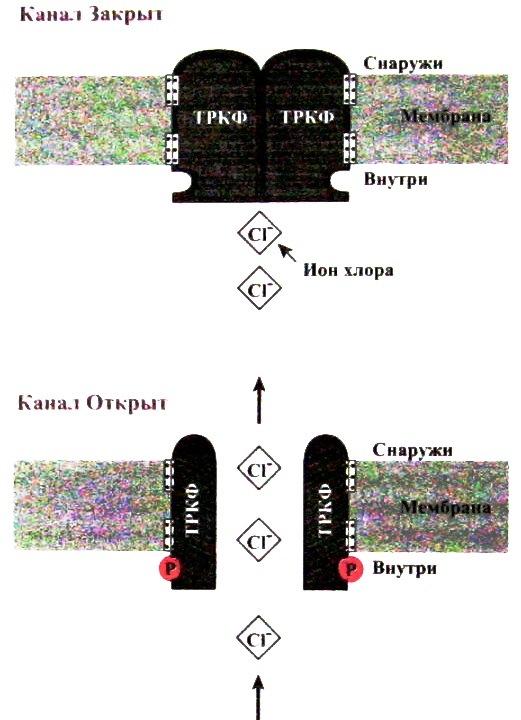
Рис. Схема механизма регуляции транспорта ионов хлора сквозь клеточную мембрану. Если к белку присоединена фосфатная группа, канал – открыт, когда фосфатная группа отщепляется, канал закрывается. (Из кн. Д. Кларк, Л.. Рассел «Молекулярная биология», 2004..)
Белок, который кодируется геном кистозного фиброза, называется транспортер кистозного фиброза (ТрКФ) и находится в клеточной мембране, где его молекулы формируют канал для ионов хлора. У здоровых людей этот канал может быть открыт или закрыт в зависимости от нужд клетки. У некоторых людей наблюдается нарушение контроля проницаемости ионов хлора сквозь клеточные мембраны. Это, в свою очередь, влияет на множество других процессов. Наиболее вредным является то, что слизь, которая выстилает и защищает легкие, становится ненормально густой. (Нехватка ионов хлора приводит к недостатку воды, которая разжижает слизь.) Клетки, которые выстилают воздухоносные пути легких, погибают и заменяются фиброзной рубцовой тканью, отсюда и название болезни – кистозный фиброз. В конце концов, пациент погибает от нарушения дыхания. Эта болезнь – результат гомозиготных рецессивных мутаций. Примерно один из 2000 белых детей страдают кистозным фиброзом.
Эндоцитоз
Эндоцитоз – это везикулярный перенос жидкостей, макромолекул или небольших частиц и микроорганизмов (вирусов, бактерий) в клетку. Существует, по крайней мере, три механизма эндоцитоза:
Пиноцитоз – («клеточное питье»).
Рецепторно-опосредованный эндоцитоз или клатрин-зависимый эндоцитоз.
Фагоцитоз – («клеточная еда»).
Пиноцитоз – это конститутивный (постоянный) процесс поглощения жидкости и растворенных веществ с образованием небольших пузырьков. (Название пиноцитоз происходит от греческих слов «pineo» – пить и «kytos – клетка»). Эти пузырьки переносят небольшие молекулы, воду и растворимые белки, то есть вещества, относящиеся к жидкой фазе внеклеточной среды. Благодаря такому процессу клетки могут поглощать как крупные молекулы, так и ионы, неспособные проникнуть через мембрану.
В цитоплазме клетки многие пиноцитозные пузырьки сливаются друг с другом и формируют ранние эндосомы, которые смещаются в глубь клетки и сливаются с лизосомами; в их полости начинается разрушение веществ. Несмотря на маленькие размеры пиноцитозных пузырьков, их многочисленность позволяет им доставлять в клетку большое количество веществ. Иногда эти пузырьки представляют собой крупные макропиноцитозные образования, создающие складчатость плазматической мембраны. Некоторые микроорганизмы стимулируют образовние подобных складок, что обеспечивает их проникновение в клетку. Пиноцитоз может быть очень интенсивным процессом; в некоторых клетках вся плазматическая мембрана поглощается и восстанавливается за один час. Особенно интенсивно пиноцитоз протекает в эндотелиальных клетках кровеносных капилляров. Путем пиноцитоза вещества попадают из тканевой жидкости в просвет кровеносных капилляров.
Опосредуемый рецепторный эндоцитоз характеризуется поглощением из внеклеточной жидкости конкретных макромолекул. Для этой цели клетка экспрессирует на свою поверхность специфические поверхностные рецепторы, что обеспечивает избирательное связывание молекул во внеклеточном растворе. Рецепторы, способные связывать лиганд (специфическую сигнальную молекулу), накапливаются в специфических участках поверхности клетки, называемых окаймленными ямками. Поверхность этих небольших углублений покрыта с цитозольной стороны плазматической мембраны белком клатрином. При сязывании лиганда с рецептором под плазматической мембраной формируется пузырек – ранняя эндосома, содержащий комплекс лиганд-рецептор, покрытый снаружи клатрином. Белок клатрин предотвращает слияние эндосом с лизосомами и переваривание лиганда ферментом. В пузырьках такого типа лиганд доставляется в различные отделы в пределах одной клетки или переносится в другой слой клеток. Такой тип переноса называют трансцитозом.
Известны четыре типа трансцитоза. При первом типе – рецептор возвращается в плазматическую мембрану, а лиганд разрушается (инсулин, липопротеиды низкой плотности, некоторые вирусы и др.). При втором типе – рецептор возвращается и лиганд возвращается (белок, переносящий железо и др.). Третий тип трансцитоза характеризуется разрушением лиганда и рецептора (эпидермальный фактор роста и др.). Механизм четвертого типа связан с транспортом и лиганда и рецептора. Например, трансцитозом материнские антитела переносятся в клетки молочной железы, а затем у новорожденного из молока они проходят через эпителий кишечника и попадают в лимфатические протоки и кровь.
Нарушения различных типов рецепторно-опосредованного эндоцитоза сопровождаются серьезными заболеваниями человека. Семейная гиперхолестеролемия является примером неполноценного трансцитоза первого типа. Эта болезнь обусловлена различными мутациями гена рецптора липопротеида низкой плотности (ЛНП), который присутствует в большинстве клеток организма и обеспечивает поступление пищевого холестерола в в клетку. Холестерол необходим для синтеза клеточных мембран, биоснтеза стероидных гормонов и др. молекул. Нарушение транспорта ЛНП, в составе которых холестерол попадает в клетку, сопровождается накоплением ЛНП в плазме крови, что приводит к образованию атеросклеротических бляшек в сосудах.
Фагоцитоз (греч. fageo – пожирать) – поглощение крупных частиц (микроорганизмов, остатков разрушающихся клеток и др.). К фагоцитозу способны все клетки, но наиболее активно фагоцитоз осуществляют профессиональные фагоциты (моноциты, макрофаги, нейтрофилы). Эпителиальные клетки и фибробласты также способны к фогоцитозу. В ходе фагоцитоза образуются большие эндоцитозные пузырьки – фагосомы. Фагосомы сливаются с лизосомами и формируют фаголизосомы, в которых происходит переваривание поглощенного материала. Многие паразиты (туберкулезная палочка, токсоплазма и др.) обладают способностью перестраивать мембрану фагосомы, благодаря чему фаголизосома не образуется и фагоцитоз не завершается. Фагоцитоз является очень сложным многоэтапным процессом. Фагоцитоз, в отличие от пиноцитоза, индуцируют сигналы, воздействующие на рецепторы в плазмалемме фагоцитов. Чаще всего такими сигналами являются антитела покрывающие частицу, например, бактерию (рис. 9), подвергающуюся фагоцитозу. Для фагоцитоза обычно требуется полимеризация актина. Этот процесс запускается при взаимодействии молекул частицы с поверхностным рецептором клетки.
Фагоцитоз представляет собой ключевой механизм защиты организма-хозяина от микроорганизмов. Доказательством большого значения фагоцитоза являются случаи, когда при нарушении этого процесса даже маловирулентные микробы вызывают септические состояния (sepsis – гниение). Это, например, бывает когда в фагоцитах не образуется Н2О2 и не выделяется кислородный радикал О2-, необходимый для бактериолиза внутри фагоцитов, а также при недостаточности фермента НАДН-зависимой оксидазы. Этот дефект наследуется рецессивно, он сцеплен с Х-хромосомой. Фагоцитоз поврежденных или постаревших клеток необходим для обновления ткани и заживления ран.

Рис. 9. Электронная микрофотография лейкоцита, поглощающего посредством фагоцитоза бактерию, которая находится в процессе деления (Фото из книги: Молекулярная биология клетки, том II).
Экзоцитоз
Экзоцитоз – перенос частиц и крупных соединений из клетки. Наиболее распространенный способ экзоцитоза – секреция. Это такое выведение из клетки растворимых соединений, которое является одной из функций данной клетки. Специализированные клетки хранят секретируемые молекулы (пищеварительные ферменты, гормоны, нейротромедиаторы) в пузырьках, расположенных вблизи плазматической мембраны. При получении внешнего сигнала происходит слияние пузырьков с плазматической мембраной и освобождение их содержимого. Такой процесс называют стимулированной секрецией. Реже секреция совершается по типу облегченной диффузии или активного транспорта. (Например, секреция ионов Н+ в желудке и канальцах почки).
Удаление из клетки твердых частиц называют экскрецией. При такой форме экзоцитоза удаляемые частицы оказываются в цитоплазматическом пузырьке, который затем сливается с плазмолеммой.
В клетках иммунной системы осуществляется рекреция – перенос твердых веществ через клетку. При этом процессе с одной стороны клетки происходит фагоцитоз, а с другой – экскреция. Так специализированные макрофаги (дендритные клетки, клетки Лангерганса и др.) локализованные в слизистых оболочках и коже захватывают бактериальные клетки, разрушают их до мелких обломков и представляют (презентируют) эти антигены иммуннокомпетентным лимфоцитам.
Ядро
Ядро (лат. nucleus, греч. karyon) – наиболее крупная (диаметром около 10 мкм) видимая в световой микроскоп органелла эукариотической клетки. При микроскопии большинства тканей ядро часто выглядит как крупная округлая или овальная (или другой формы) структура, расположенная чаще всего вблизи центра клетки. Однако в клетках некоторых тканей оно имеет специфическое расположение и строение; в связи с этим некоторые морфологи образно называют ядро «гербом ткани».
Структурные компоненты ядра: ядерная оболочка, ядерный белковый матрикс, ядерный сок, хромосомы, связанные с хромосомами ядрышки.
Ядерная оболочка – двойная мембранная структура, которая окружает нуклеоплазму и изолирует центральные генетические процессы – репликацию ДНК и синтез РНК – от рибосом цитоплазмы, где происходит синтез белка. Область между двумя ядерными мембранами называется перинуклеарным пространством. Внешняя ядерная мембрана несет рибосомы и переходит в шероховатый эндоплазматический ретикулум (лат. reticulum – сеть). Внутренняя поверхность внутренней мембраны имеет тонкую пластинку – ламину, построенную из крупных нитевидных белков (ламина А и ламина В), которая играет ключевую роль в поддержании структурной целостности мембраны. Матрикс ядра включает ламину и внутриядерную фибриллярную сеть. К ламине и внутриядерной фибриллярной сети крепятся хромосомы, а таже разнообразные ферменты и регуляторные белки.
Нуклеоплазма (ядерный сок) – жидкое или гелеобразное вещество, в которое погружены хромосомы и ядрышко.
Обмен макромолекул между ядром и цитоплазмой осуществляется через ядерные поры, образованные белковым комплексом. Этот комплекс – основные ворота для веществ, которые постоянно перемещаются внутрь ядра и из него. Например, матричная РНК (мРНК), субъединицы рибосом, гистоны, рибосомные белки, факторы транскрипции, а также ионы и мелкие молекулы быстро обмениваются между ядром и полостью эндоплазматического ретикулума или цитозолем.

Рис. Комплекс ядерной поры, реконструированный на основе протеомного анализа (изучения структуры белков) порового комплекса.

Ядерный поровый комплекс (ЯПК) формирует цилиндр, приблизительно 120нм в диаметре и 50нм толщиной, состоящий из 16 субъединиц. Каждая субъединица содержит около 30 различных белков. Ядерный поровый комплекс состоит из центральной части – транспортера, через который и проходят молекулы, а также периферических частей. В сторону цитоплазмы от поры отходят филаменты, функция которых состоит в обеспечении связывания и транспортировки макромолекул со стороны цитоплазмы к корзине ядра на ядерной стороне поры. В ядре периферический отдел образует баскет-структуру (структуру, похожую на корзину).
В мембране ядра насчитывается около 5000 поровых комплексов. Во время деления клетки оболочка ядра не «растворяется», а разбирается и превращается в компоненты эндоплазматического ретикулума, а поры становятся отдельными белковыми компонентами, которые уходят в глубь клетки. Новые поровые комплексы формируются из так называемых окончатых мембран. Они представляют собой часть эндоплазматического ретикулума и состоят из гладких цистерн и пороподобных комплексов, морфологически и биохимически сходных с ядерными поровыми комплексами.
