- •Министерство сельского хозяйства республики казахстан
- •Учебно-методический комплекс по физике для группы специальностей «технические науки и технологии»
- •Тема 1. Элементы кинематики
- •Тема 2. Динамика частиц
- •Тема 3. Принцип относительности в механике
- •Тема 4. Работа и энергия
- •Тема 5. Твердое тело в механике
- •Тема 6. Физика колебаний
- •Тема 7. Механические волны
- •Тема 8. Молекулярно - кинетическая теория идеальных газов
- •Тема 9. Статистические распределения
- •Тема 10. Основы термодинамики
- •Тема 11. Реальные газы. Явления переноса
- •Тема 12. Электростатика
- •Тема 13. Проводники и диэлектрики в электростатическом поле
- •Тема 14. Постоянный электрический ток
- •Тема 15. Элементы физической электроники и твердого тела
- •Изучение движения тел по наклонной плоскости
- •Порядок работы
- •Контрольные вопросы
- •Изучение собственных колебаний пружинного маятника
- •Натуральный логарифм этого отношения называется логарифмическим декрементом затухания:
- •Порядок работы
- •Контрольные вопросы
- •Определение момента инерции тракторного шатуна
- •Порядок работы
- •Контрольные вопросы
- •Порядок работы Упражнение 1. Определение момента инерции крестовины без муфт
- •Крестовины вместе с муфтами.
- •Контрольные вопросы
- •1. Напишите и сформулируйте основной закон динамики вращательного движения. Дать определения момента инерции, момента силы.
- •Определение момента инерции маятника максвелла
- •На маятник действуют две силы: сила тяжести ft, направленная вертикально вниз и сила упругости двух нитей 2т (рис.2).
- •Порядок работы
- •Определение момента инерции маятника
- •Контрольные вопросы
- •Определение коэффициента вязкости жидкости методом стокса
- •Порядок работы
- •Определение отношения удельных теплоемкостей газа методом адиабатического расширения
- •Контрольные вопросы
- •Изучение фазовых переходов первого рода
- •Экспериментальная установка
- •Проведение эксперимента
- •Обработка результатов
- •Контрольные вопросы
- •Теория метода
- •Порядок работы
- •Контрольные вопросы
- •1.2. Классификация приборов по принципу действия
- •1.3.Характеристики электроизмерительных приборов
- •1.4.Амперметры, вольтметры, гальванометры
- •1.5.Вспомогательные электрические приборы
- •2. Правила работы с электрическими схемами
- •Для соблюдения техники безопасности при работе с электрическими схемами следует:
- •3.Измерения и обработка результатов измерений
- •Контрольные вопросы
- •Определение удельного сопротивления проводника
- •Контрольные вопросы
- •Определение сопротивления проводников с помощью мостиковой схемы
- •Порядок работы
- •Контрольные вопросы
- •Исследование процесса разряда конденсатора через сопротивление
- •Исследование свойств полупроводникового выпрямителя
- •Порядок работы
- •Контрольные вопросы
- •Градуировка термоэлемента и определение его удельной термоэлектродвижущей силы
- •Теория метода
- •Порядок работы
- •Задачи для аудиторных занятий
- •О т в е т ы к задачам
- •Задания для самостоятельной работы студентов
- •Механика
- •42. При каких условиях сохраняется импульс механической системы….
- •Колебания и волны
- •Молекулярная физика и термодинамика
- •Электростатика
- •Электрический ток
- •2. Некоторые астрономические величны
Тема 11. Реальные газы. Явления переноса
Реальный газ – газ, где учитываются объем (размеры) и силы взаимодействия молекул. Учитывая собственный объем молекул и силы межмолекулярного взаимодействия, голландский физик И.Ван-дер-Ваальс введя поправки в уравнение Менделеева-Клайперона, вывел уравнение состояния реального газа.
Уравнение состояния для 1 моля идеального газа имеет вид pV = RT
Согласно
этой формуле объем газа при сжатии может
стать равным нулю. В случае реальных
газов часть объема занята самими
молекулами. Поэтому объем, занимаемый
газом, должен быть уменьшен на величину
b,
где b-
объем занимаемый самими молекулами,
т.е. (V-b).
Таким
образом, b
–постоянная величина, учитывающая
объемы (размеры) молекул.В![]() реальных газах имеются силы взаимного
притяжения молекул, которые действуют
дополнительно к силам внешнего давления
и как бы сжимают газ. Вследствие этого
возникает добавочное внутреннее давлениеpi,
т.е.
реальных газах имеются силы взаимного
притяжения молекул, которые действуют
дополнительно к силам внешнего давления
и как бы сжимают газ. Вследствие этого
возникает добавочное внутреннее давлениеpi,
т.е.
где (p + pi), а – постоянная величина, учитывающая
силы межмолекулярного притяжения
Т![]() огда,
введя поправки наV
и p,
получим уравнение состояния реального
газа
огда,
введя поправки наV
и p,
получим уравнение состояния реального
газа
- уравнение Ван-дер-Ваальса для 1 моля газа
Величины a и b для различных газов различны и их значение приводятся в справочных таблицах.
Д![]() ля
любой массы газа
ля
любой массы газа
Уравнение Ван-дер-Ваальса не единственное уравнение, описывающее реальные газы. Существуют и другие уравнения, некоторые из них даже точнее описывают реальные газы, но не рассматриваются из-за их сложности.
Для исследования поведения реального газа рассмотрим изотермы Ван-дер-Ваальса – кривые зависимости давления p от объема V при заданных температурах Т, определяемые уравнение Ван-дер-Ваальса для 1 моля газа.
Эти кривые рассматриваются для четырех различных температур и имеют своеобразный характер.
|
|
Задавая различные температуры T1 > T2 > T3 > T4 > T5 получим семейство изотерм Ван-дер-Ваальса. При высоких температурах изотерма реального газа отличается от изотермы идеального газа только некоторым искажением формы. Изобара AD пересекает изотерму в одной точке. Это означает, что каждому значению давления и температуры |
соответствует единственное значение объема, т.е. при высоких температурах вещество находится в однофазном – газообразном состоянии. Невысоким температурам соответствуют изотермы 2-, 3-, 4, на которых имеются изгибы.
Изобара AD пересекает изотерму 4 в трех точках А, В, С. Это означает, что вещество одновременно находится в трех фазовых состояниях. Переход от изотермы 5 к изотермам 4,3,2,1, соответствующий повышению температуры, приводит к тому, что изгибы на изотермах сглаживаются. Расстояние между точками А и С уменьшаются и на изотерме 2 сливаются в одну точку К. Здесь рК = const является касательной к изотерме. Эта изотерма называется критической, соответствующая температура Тк – критической , точка К – критической. Соответствующие этой точке VK и рК – называются критическими.
Состояние с критическими параметрами (VK,,рК,,ТК) называются критическим состоянием.
Температурам, выше критическим соответствует только газообразное состояние вещества. Следовательно, критическая температура ТК – это наивысшая температура, при которой газ может еще может быть превращен в жидкость. При критическом состоянии вещества различия в свойствах пара и жидкости отсутствуют. Критические состояния характеризуется непрерывным переходом пара в жидкость и жидкости в пар.
Мы знаем, что U = U1 + U2 = Eк + Eр.
В![]() случае реального газа, помимо кинетической
энергииЕк
нужно
учитывать потенциальную энергию Ер
взаимодействия молекул.
случае реального газа, помимо кинетической
энергииЕк
нужно
учитывать потенциальную энергию Ер
взаимодействия молекул.
В![]() нутренняя
энергия для1
моля идеального
газа
нутренняя
энергия для1
моля идеального
газа
Т![]() ак
как , то
ак
как , то
Работа сил молекулярного сцепления равна: dA = pi dV,
![]()
Мы знаем, что
Тогда dU которое произошло за счет совершения работы
![]() или
интегрируя, получим:
или
интегрируя, получим:
![]()
- потенциальная энергия
![]()
Тогда - внутренняя энергия 1 моля реального газа.
Следовательно, внутренняя энергия реального газа зависит как от температуры, так и от его объема.
В термодинамически неравновесных системах возникают особые необратимые процессы – явления переноса – в результате которых происходит пространственный перенос энергии, массы, импульса.
К явлениям переноса относятся:
1. Теплопроводность обусловлена переносом энергии (горячий чай – холодная ложка). Если в одной области Ек молекул больше, чем в другой, то в процессе столкновений молекул с течением времени происходит выравнивание кинетической энергии, т.е. температур.
Перенос
энергии в форме теплоты подчиняется
закону Фурье
![]()
jE – плотность теплового потока – энергия, переносимая в форме теплоты через единицу площади в единицу времени, перпендикулярную оси х.
![]() -
коэффициент теплопроводности
-
коэффициент теплопроводности

![]() –градиент
температуры
– изменение температуры на единицу
длины. «-» - при теплопроводности энергия
переносится в направлении убывания
температуры.
–градиент
температуры
– изменение температуры на единицу
длины. «-» - при теплопроводности энергия
переносится в направлении убывания
температуры.
2. Диффузия - самопроизвольное проникновение и перемешивание частиц двух соприкасающихся газов, жидкостей и твердых тел.
Явление диффузии подчиняется закону Фика
![]()
jm – плотность потока массы – масса вещества, диффундирующего в единицу времени через единицу площади, перпендикулярную оси х
D – коэффициент диффузии
![]() -
градиент плотности, «-» показывает,
что перенос массы происходит в направлении
убывания плотности.
-
градиент плотности, «-» показывает,
что перенос массы происходит в направлении
убывания плотности.
Согласно
кинетической теории газов
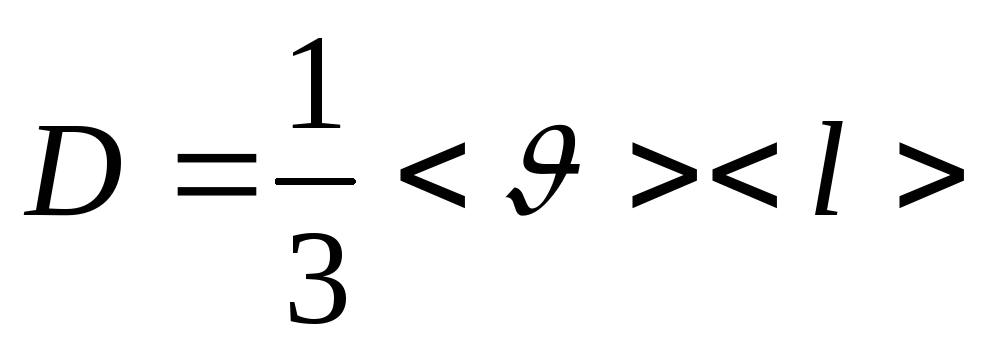
3. Внутреннее трение (вязкость). Механизм возникновения внутреннего трения между параллельными слоями газа (жидкости), движущимися с различными скоростями заключается в том, что из-за хаотического теплового движения происходит обмен молекулами между слоями, в результате чего импульс слоя, движущегося быстрее, уменьшается, а движущегося медленнее – увеличивается, что приводит к торможению слоя, движущегося быстрее, и ускорению слоя, движущегося медленнее. Сила трения между слоями подчиняется закону Ньютона
![]()
Тогда
от одного слоя к другому передается
импульс, по модулю равный действующей
силе
![]()
jp – плотность потока импульса – величина, определяемая полным импульсом, переносимым в единицу времени в положительном направлении оси х через единичную площадку, перпендикулярную оси х.
![]() -
градиент скорости, «-» - указывает, что
импульс переносится в направлении
убывания скорости.
-
градиент скорости, «-» - указывает, что
импульс переносится в направлении
убывания скорости.
Динамическая вязкость определяется по формуле
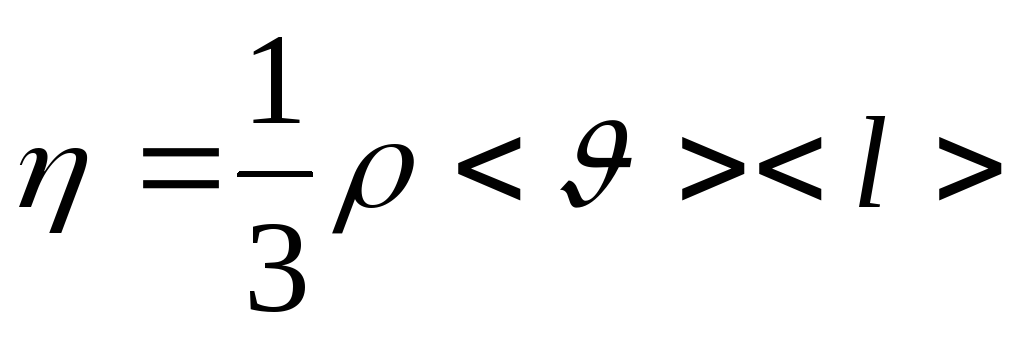
Коэффициенты переноса связаны между собой соотношениями
![]() и
и
![]()