
- •Основы химии нефти и газа
- •Основы химии нефти и газа
- •Основы химии нефти и газа
- •450062, Г. Уфа, ул. Космонавтов, 1 Предисловие
- •Добыча нефти и газа
- •1.2. Происхождение нефти и газа
- •1.3. Основные физико-химические свойства нефтей
- •1.3.1. Физические свойства нефтей и нефтепродуктов
- •1.3.2. Элементный и изотопный состав нефтей и природных газов
- •1.3.3. Групповой химический состав нефтей
- •1.3.4. Фракционный состав нефти
- •1.4. Классификация нефтей
- •1.4.1. Химическая классификация
- •1.4.2. Технологическая классификация
- •2. Химический состав нефти
- •2.1. Углеводороды нефти и нефтепродуктов
- •2.2. Алканы
- •2.2.1. Строение, изомерия, структурные формулы
- •2.2.2. Номенклатура
- •2.2.3. Физические свойства
- •2.2.4. Химические свойства и переработка
- •2.2.5. Алканы нефти
- •2.3. Циклоалканы
- •2.3.1. Номенклатура и изомерия
- •2.3.2. Физические свойства
- •2.3.3. Химические свойства и переработка
- •2.3.4. Циклоалканы нефти, влияние на свойства нефтепродуктов
- •2.4. Арены и углеводороды смешанного строения
- •Строение бензола
- •2.4.1. Номенклатура и изомерия
- •1. Монозамещённые бензолы
- •2. Дизамещённые бензолы
- •3. Полициклические арены
- •2.4.2. Физические свойства
- •Физические свойства аренов
- •2.4.3. Химические свойства и использование
- •2.4.4. Углеводороды смешанного стороения
- •2.4.5. Арены нефти, влияние на свойства нефтепродуктов,
- •2.5. Непредельные углеводороды
- •2.5.1. Алкены и циклоалкены
- •2.5.1.1. Номенклатура
- •2.5.1.2. Физические свойства
- •2.5.1.3. Химические свойства и использование
- •2.5.2. Алкины
- •2.5.2.1. Номенклатура
- •2.5.2.2. Физические свойства
- •2.5.2.3. Химические свойства
- •2.5.3. Непредельные углеводороды нефти и нефтепродуктов,
- •2.6. Гетероатомные соединения и минеральные
- •2.6.1. Кислородные соединения
- •2.6.1.1. Кислоты
- •2.6.1.2 Фенолы
- •2.6.1.3. Кетоны и эфиры
- •2.6.2. Сернистые соединения
- •2.6.2.1. Тиолы
- •2.6.2.2. Сульфиды
- •2.6.2.3. Дисульфиды
- •2.6.2.4. Сернистые соединения нефтей
- •Групповой состав сернистых соединений некоторых нефтей
- •Происхождение сернистых соединений нефти
- •Влияние на свойства нефтепродуктов и применение сернистых соединений
- •2.6.3. Азотистые соединения
- •2.6.3.1. Амины
- •2.6.3.2. Амиды кислот
- •2.6.3.3. Происхождение азотистых соединений нефтей.
- •2.6.4. Смолисто-асфальтовые вещества
- •2.6.5. Минеральные компоненты
- •3.1. Подготовка нефти к переработке
- •3.2. Первичная перегонка нефти
- •3.3. Химические процессы переработки нефти
- •3.3.1. Термический крекинг, пиролиз и коксование
- •3.3.2. Каталитические процессы
- •4. Переработка нефтяных газов
- •5. Очистка и стабилизация нефтепродуктов
- •Стабилизация нефтепродуктов
- •6. Продукты переработки нефти
- •7. Продукты нефтехимического синтеза
2.4.3. Химические свойства и использование
Реакции присоединения. Арены вступают в реакции присоединения с большим трудом. Для этого требуются высокие температуры, ультрафиолетовое облучение и катализаторы. К ним относятся:
Галогенирование:
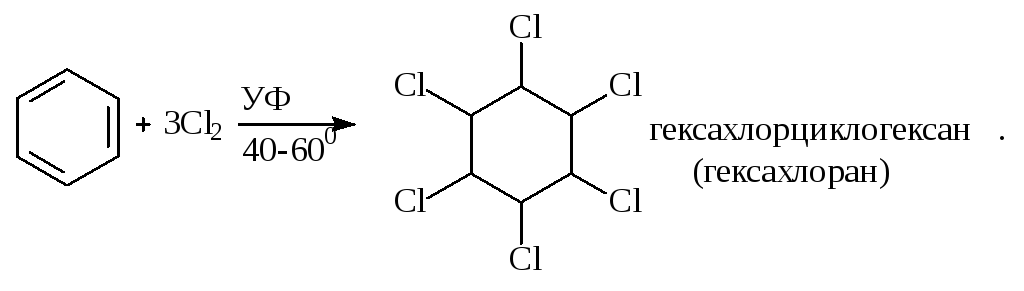
Гексахлоран используется в качестве инсектицида.
Гидрирование:
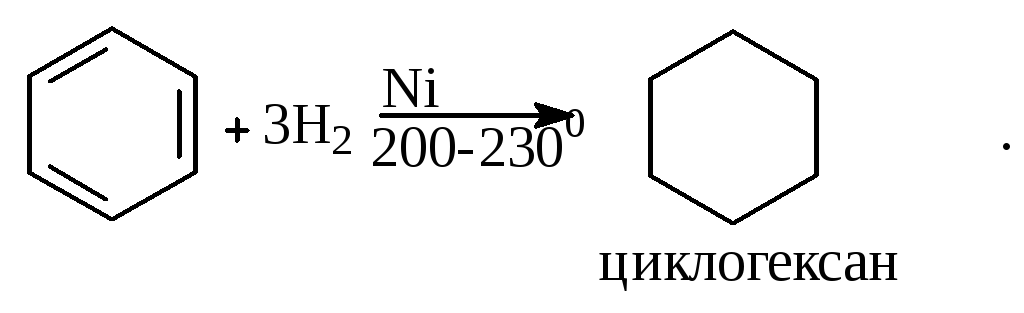
Реакции замещения наиболее характерны для аренов. Они протекают в сравнительно мягких условиях. Особенно легко вступают в реакции замещения гомологи бензола.
Галоидирование. В зависимости от условий галоидирования можно получить продукты различной степени замещения:
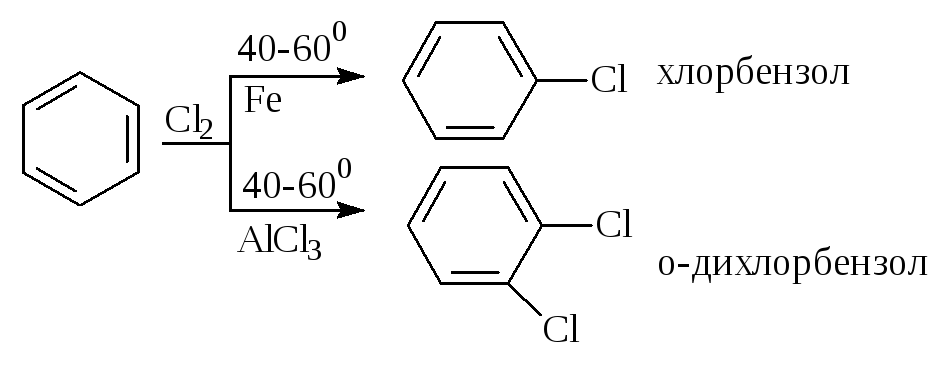
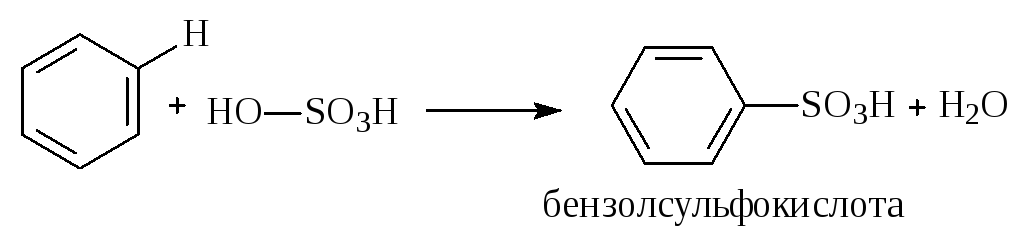
Сульфирование. Концентрированная серная кислота легко замещает водород на остаток серной кислоты с образованием сульфокислоты.
Эта реакция протекает количественно и может служить одним из способов определения содержания аренов в нефтяных фракциях.
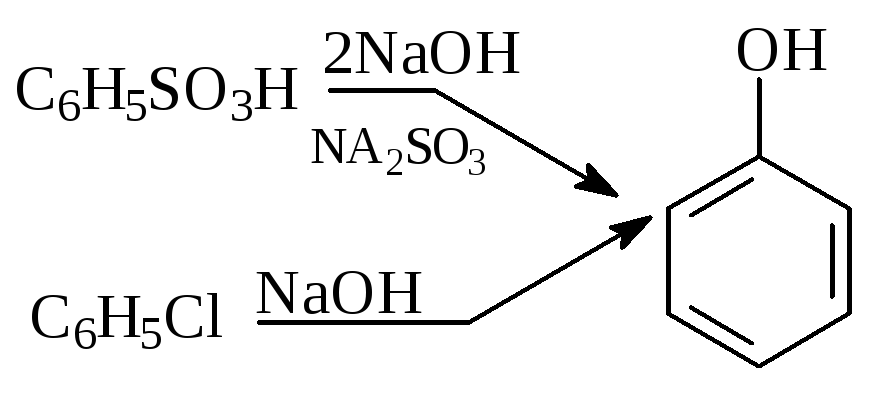
Из бензолсульфокислоты и хлорбензола сплавлением их со щёлочью получают фенол.
Основная область применения фенола - производство фенолформальдегидных смол.
Нитрование. При действии на бензол смесью концентрированных азотной и серной кислот получается нитробензол:

Восстановлением нитробензола получают анилин:

Большая часть анилина используется для производства полиуретановых пенопластов.
При полном нитровании толуола получают взрывчатое вещество тротил (2,4,6-тринитротолуол):
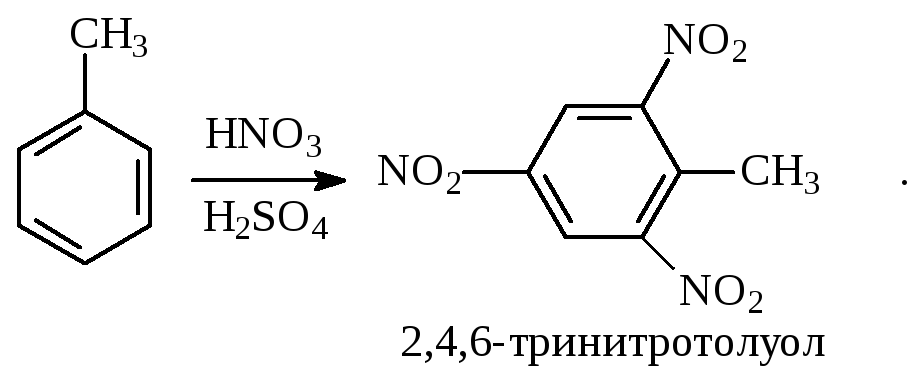
Алкилирование. В присутствии таких катализаторов как АlCl3, HF, H2SO4, HCl, BF3 арены вступают в реакцию алкилирования с алкенами, спиртами, галоидзамещёнными алканами. Таким способом в промышленности получают этилбензол и изопропилбензол:
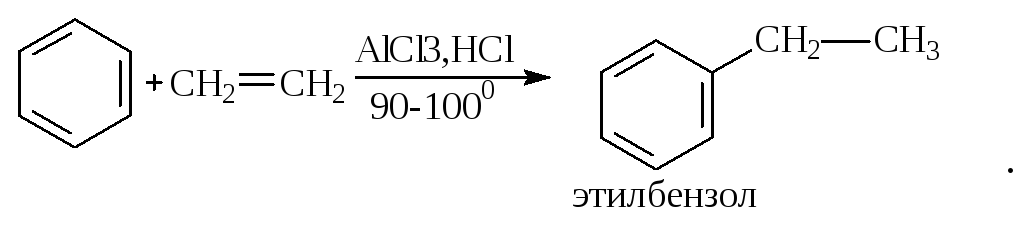
Каталитическим дегидрированием из этилбензола получают стирол, а из изопропилбензола - -метилстирол - ценные мономеры, используемые в производстве каучуков и пластмасс:
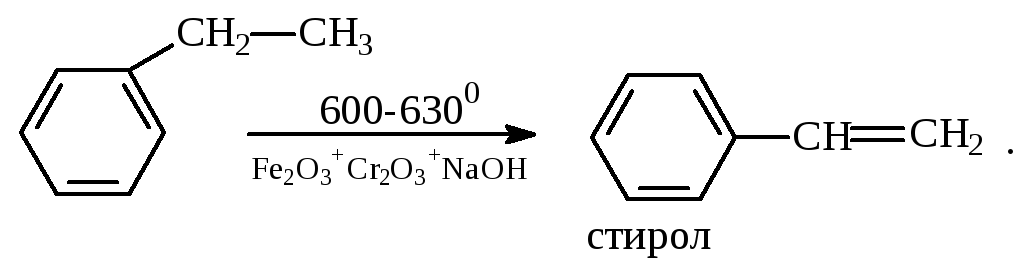
Алкилированием бензола хлоралканами и дальнейшим сульфированием и нейтрализацией образующихся продуктов получают алкиларилсульфонаты - синтетические поверхностно-активные вещества. Эти вещества с некоторыми добавками называют сульфонолами:
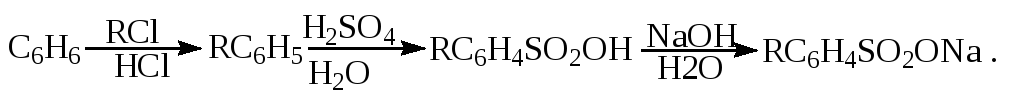
Деалкилирование и гидродеалкилирование. В связи с тем, что наибольшее значение имеет бензол, его в настоящее время получают деалкилированием или гидродеалкилированием толуола:
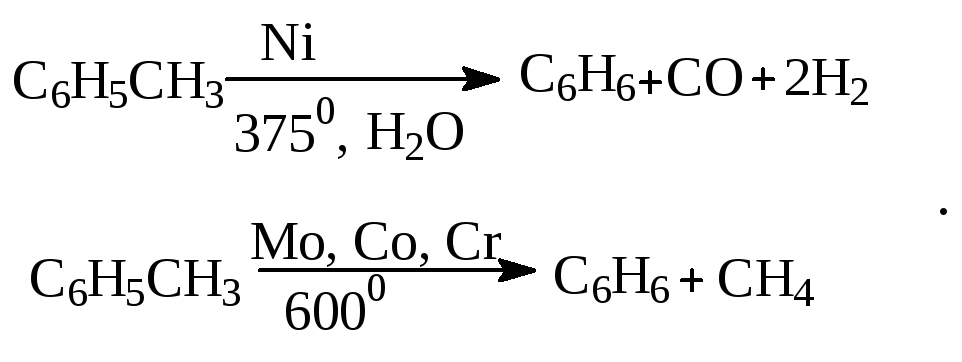
Конденсация с формальдегидом. В присутствии концентрированной серной кислоты арены конденсируются с формальдегидом с образованием нерастворимого осадка бурого цвета:
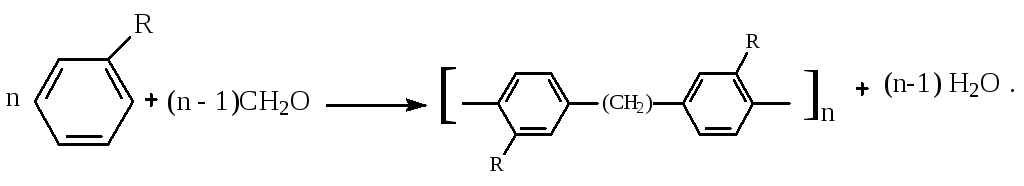
Эту реакцию применяют для аналитического определения аренов в нефтяных фракциях.
Окисление. Арены (кроме бензола, нафталина и других голоядерных гомологов) легко вступают в реакции окисления. В ряду алкилпроизводных аренов устойчивость к окислению падает с увеличением длины и степени разветвления боковой цепи. При этом образуются кислые соединения. Эти свойства аренов широко используются в промышленности для получения кислородсодержащих производных:
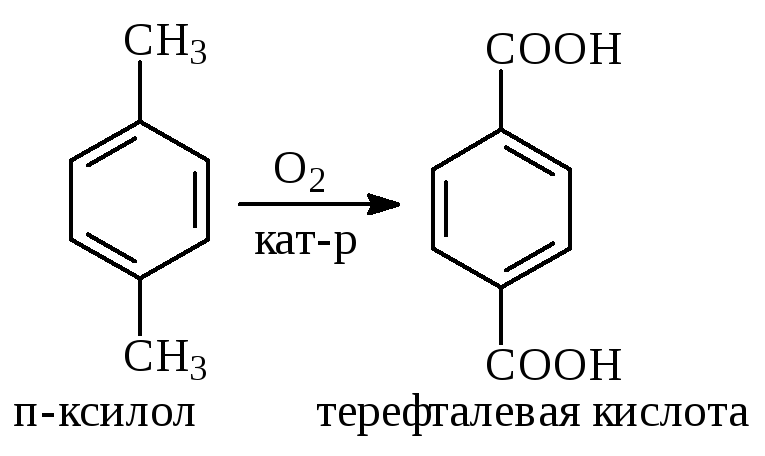

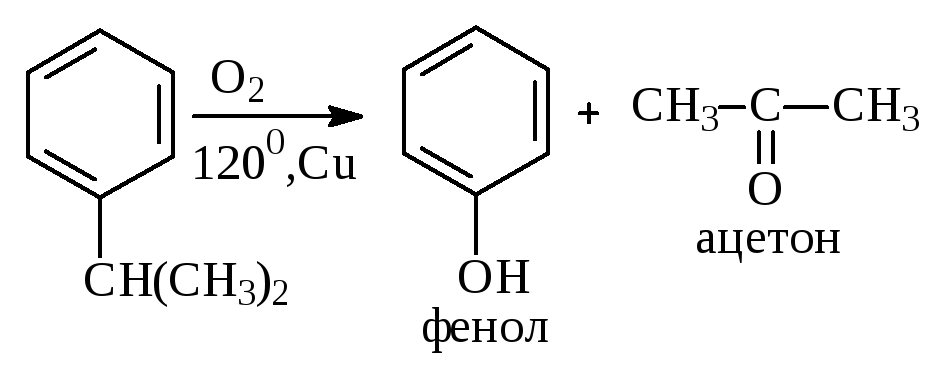
С целью получения терефталевой кислоты разработаны также различные процессы окисления толуола. Наиболее устойчивыми к окислению кислородом воздуха являются бензол и нафталин. Однако и они в очень жёстких условиях (высокая температура, катализатор) окисляются с разрывом бензольного кольца:
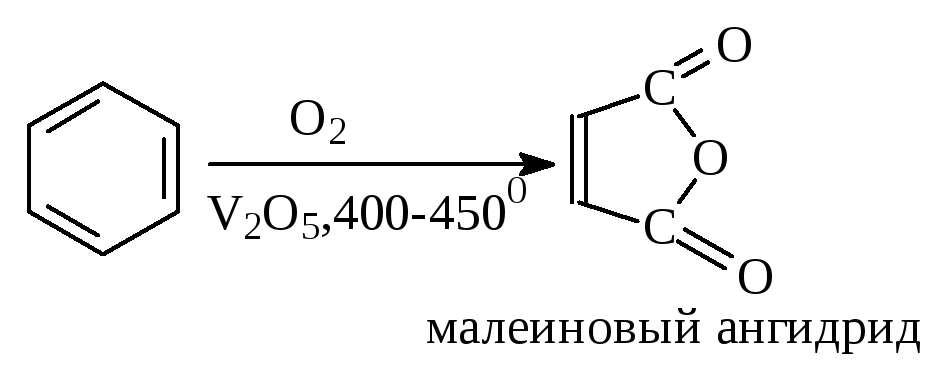
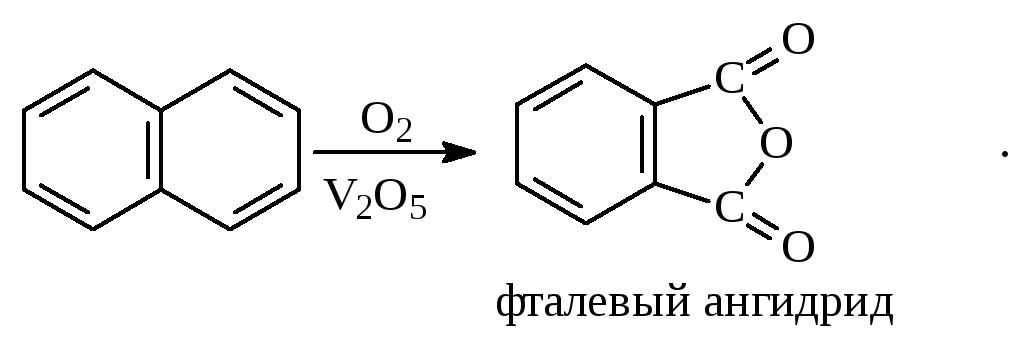
Терефталевая кислота - полупродукт для производства синтетического полиэфирного волокна - лавсана (терилена). Фталевый ангидрид применяется для производства алкидных и полиэфирных смол, пластификаторов, репеллентов. Малеиновый ангидрид используется в производстве полиэфирных смол и присадок к смазочным маслам.
Образование комплексов с пикриновой кислотой. Полициклические арены (нафталин, антрацен и их гомологи) легко образуют комплексные соединения с пикриновой кислотой (2,4,6 - тринитрофенол) – пикраты.
Бензол и его гомологи не образуют стабильных комплексов и могут служить растворителями при комплексообразовании.
Пикраты ароматических углеводородов представляют собой твёрдые кристаллические вещества жёлтого цвета, имеющие чёткие температуры плавления. Каждому полициклическому углеводороду соответствует пикрат с определённой температурой плавления. По температуре плавления пикрата модно идентифицировать полициклический ароматический углеводород.
Комплексообразование с пикриновой кислотой используется как метод выделения полициклических ароматических углеводородов. Пикраты легко разлагаются горячей водой. Пикриновая кислота растворяется в воде, а полициклические ароматические углеводороды выделяются в свободном виде.
