
Метод Клемана-Дезорма
.docЛабораторная работа № 3
Определение отношения молярных
теплоемкостей воздуха
![]()
методом Клемана – Дезорма
Краткая теория
Молярной теплоемкостью
![]() какого-либо вещества называется величина,
численно равная количеству теплоты,
которое нужно сообщить одному молю
вещества, чтобы повысить его температуру
на 1 К:
какого-либо вещества называется величина,
численно равная количеству теплоты,
которое нужно сообщить одному молю
вещества, чтобы повысить его температуру
на 1 К:
![]() ,
,
где dQ – количество, необходимое для нагревания ν молей вещества на температуру dT.
Значение теплоемкости зависит от условий, при которых происходит нагревание вещества. Если нагревать тело при постоянном объеме, то все тепло, сообщаемое телу извне, полностью идет на увеличение внутренней энергии. Если нагревать тело при постоянном давлении, то сообщенное тепло идет не только на увеличение внутренней энергии, но и на работу при расширении. Поэтому теплоемкость при постоянном давлении должна быть больше, чем теплоемкость при постоянном объеме. Особенно эти теплоемкости различаются у газов вследствие относительно большого коэффициента объемного расширения.
Для идеального
газа справедливо следующее соотношение
значений молярных теплоемкостей
![]() и
и
![]() :
:
![]() ,
,
где R - универсальная газовая постоянная.
Отношение молярных теплоемкостей при
постоянном давлении и при постоянном
объеме
![]() играет в термодинамике весьма важную
роль. В частности, оно входит в уравнение
Пуассона, которое описывает адиабатическое
расширение газа постоянной массы в
квазистатическом процессе:
играет в термодинамике весьма важную
роль. В частности, оно входит в уравнение
Пуассона, которое описывает адиабатическое
расширение газа постоянной массы в
квазистатическом процессе:
![]() .
(1)
.
(1)
Одним из самых простых методов определения
![]() является метод Клемана – Дезорма,
который состоит в следующем.
является метод Клемана – Дезорма,
который состоит в следующем.
Рассмотрим процесс (рис. 1), в котором некоторая масса газа проходит последовательно через три состояния. В начальном состоянии «1» газ находился под давлением, превышающем внешнее атмосферное давление и при температуре, равной температуре окружающего воздуха в лаборатории. Из первого во второе состояние газ переходит путем адиабатического расширения; из второго в третье состояние – изохорически, причем конечное давление газа в адиабатическом процессе равно атмосферному, а конечная температура газа в изохорическом процессе равна начальной температуре.
Все последующие выкладки проводятся в переменных P и T, а не P и V, потому что процесс происходит при переменной массе газа, остающегося в баллоне, в то время как газ, находящийся внутри сосуда, имеет вполне конкретные значения давления и температуры. Изменение массы газа никак не сказывается на вычислениях в переменных P, T.
Детально изучим происходящий процесс. Баллон объемом Vб, в котором при комнатной температуре находится сжатый воздух, на короткое время с помощью крана соединяют с атмосферой. Таким образом, воздуху дают достаточно быстро, а, следовательно, адиабатически расшириться до выравнивания давления в баллоне с атмосферным.

Рис.1
Процесс адиабатического расширения
газа изображается на диаграмме в
переменных P и T
участком 1-2 (рис. 1). Точка 1 соответствует
начальному состоянию газа, которое
характеризуется давлением
![]() и комнатной температурой
и комнатной температурой
![]() .
Состояние газа в точке 2 характеризуется
давлением
.
Состояние газа в точке 2 характеризуется
давлением
![]() и температурой
и температурой
![]() .
.
После перекрытия крана оставшийся в
сосуде газ через некоторое время приходит
в тепловое равновесие с окружающей
средой. В результате его температура
становится равной температуре окружающей
среды
![]() .
При этом давление внутри сосуда повышается
до значения
.
При этом давление внутри сосуда повышается
до значения
![]() ,
удовлетворяющего условию
,
удовлетворяющего условию
![]() .
Процесс нагревания газа происходит при
постоянном объеме
.
Процесс нагревания газа происходит при
постоянном объеме
![]() и поэтому изображается на диаграмме
изохорой (участок 2-3 рис. 1), причем точки
3 и 1 будут расположены на одной изотерме
(участок 1-3), соответствующей температуре
окружающей среды
и поэтому изображается на диаграмме
изохорой (участок 2-3 рис. 1), причем точки
3 и 1 будут расположены на одной изотерме
(участок 1-3), соответствующей температуре
окружающей среды
![]() .
Конечное состояние газа характеризуется
давлением
.
Конечное состояние газа характеризуется
давлением
![]() и температурой
и температурой
![]() .
.
Для адиабатического перехода из состояния 1 в состояние 2 справедливо уравнение Пуассона (1), которое в переменных P и T имеет вид
![]() .
.
Тогда, для значений давления и температуры газа в состояниях 1 и 2 справедливо соотношение
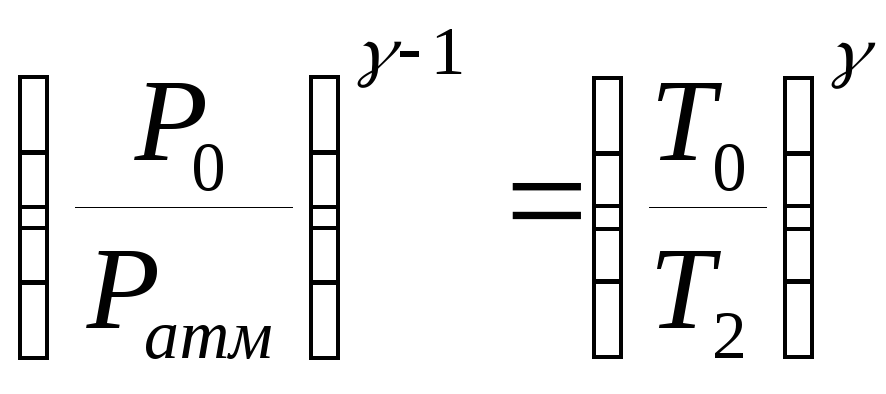 .
(2)
.
(2)
Изохорический процесс выравнивания температуры при закрытом кране подчиняется закону Шарля:
![]()
который в нашем случае принимает вид:
![]() .
(3)
.
(3)
Из уравнений (2) и (3) не трудно получить, что
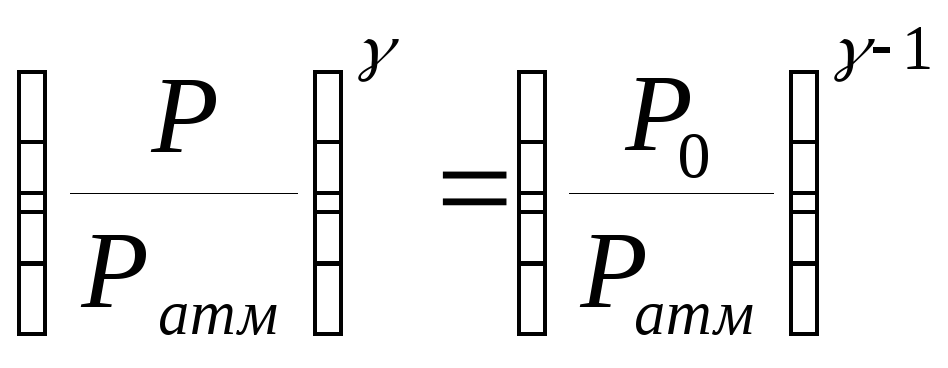 .
(4)
.
(4)
После логарифмировании соотношения (4) находим:
![]() ,
(5)
,
(5)
где
![]() ,
,
![]() .
.
Если значения
![]() и
и
![]() значительно меньше
значительно меньше
![]() ,
то справедливы формулы приближения:
,
то справедливы формулы приближения:
![]()
и
![]() .
.
С учетом рассматриваемого приближения равенство (5) примет вид:
![]() .
(6)
.
(6)
Как следует из соотношения (6), для
определения величины
![]() следует знать избыточное (над атмосферным)
давление внутри сосуда
следует знать избыточное (над атмосферным)
давление внутри сосуда
![]() до адиабатического расширения газа и
его избыточное давление
до адиабатического расширения газа и
его избыточное давление
![]() после изохорного нагревания. В нашем
случае эти величины определяются как:
после изохорного нагревания. В нашем
случае эти величины определяются как:
![]()
и
![]() ,
,
где
![]() и
и
![]() - разность уровней жидкости в коленах
U-образного манометра в
начале и в конце опыта соответственно,
- разность уровней жидкости в коленах
U-образного манометра в
начале и в конце опыта соответственно,
![]() - плотность жидкости манометра.
- плотность жидкости манометра.
С учетом последних формул соотношение (6) примет вид:
![]() .
(7)
.
(7)
Прежде чем проводить расчеты, используя формулу (7), необходимо убедиться, что выполняются все условия, используемые при ее выводе. В частности, следует оценить, как быстро протекает адиабатический процесс, и вообще, можно ли считать процесс выравнивания давлений адиабатическим и квазистатическим. Численная оценка этого времени с учетом параметров установки дает значение t ≈ 0,5 с. Т. к. время установления давления очень мало, то теплообменом в течение этого времени можно пренебречь. С другой стороны, как показывают численные расчеты, это время много больше времени релаксации газа, т. е. времени установления значений давления P и температуры T по всему объему, занимаемому газам в сосуде. Это позволяет считать процесс расширения адиабатическим и квазистатическим, что оправдывает применение к нему уравнения Пуассона.
Однако при выполнении работы невозможно
в точности обеспечить совпадение
моментов перекрытия крана и окончания
выравнивания давлений. В действительности
реализуются два случая. Первый случай
– перекрытие крана произойдет раньше,
чем закончится выравнивание давлений.
Тогда после изохорического нагревания
значение
![]() будет завышенным (на диаграмме рис.1 это
процесс 1-2′-3′).
Второй случай – перекрытие крана
произойдет спустя некоторое время после
окончания выравнивания давлений. В этом
случае сразу после него имеет место
изобарический процесс, в течение которого
газ продолжает выходить из сосуда. Тогда
после изохорического нагревания значение
будет завышенным (на диаграмме рис.1 это
процесс 1-2′-3′).
Второй случай – перекрытие крана
произойдет спустя некоторое время после
окончания выравнивания давлений. В этом
случае сразу после него имеет место
изобарический процесс, в течение которого
газ продолжает выходить из сосуда. Тогда
после изохорического нагревания значение
![]() будет заниженным (процесс 1-2-2′′-3′′
рис. 1).
будет заниженным (процесс 1-2-2′′-3′′
рис. 1).
Приблизив момент перекрытия крана к
расчетному моменту окончания
адиабатического процесса (примерно 0,5
с. после открытия крана), можно определить
с некоторой погрешностью значение
![]() .
.
Экспериментальная установка. Методика эксперимента
Эксперимент проводится на установке, изображенной на рис. 2.
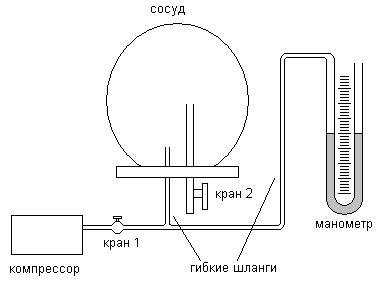
Рис. 2
Сосуд при закрытом кране 2 и открытом
кране 1 накачивают с помощью компрессора
воздухом. При этом давление внутри
сосуда становится несколько больше
атмосферного. После этого кран 1 закрывают
и дают температуре внутри сосуда
сравняться с температурой окружающей
среды (с температурой воздуха в
лаборатории). Установление температуры
происходит за 3-4 минуты. Затем примерно
на t
≈
0,5 с.
открывают кран 2, (что соответствует
спокойному движению крана «туда-обратно»)
после чего его закрывают и ждут
установления равновесного состояния.
Опыт повторяется несколько раз. Результаты
измерений величин
![]() и
и
![]() заносятся в таблицу. По измеренным
значениям показаний манометра
рассчитывается величина
заносятся в таблицу. По измеренным
значениям показаний манометра
рассчитывается величина
![]() согласно формуле (7) и оценивается
погрешность измерений.
согласно формуле (7) и оценивается
погрешность измерений.
Измерения. Обработка результатов измерений
-
Собрать установку (рис. 2), соединив элементы с помощью гибких шлангов. Воздух в баллоне накачивать при открытом кране 1 до тех пор, пока разность уровней в манометре не достигнет 100-200 миллиметров.
-
Закрыв кран 1, выждать 3-4 минуты, чтобы показание манометра перестало меняться. После этого произвести отсчет разности уровней
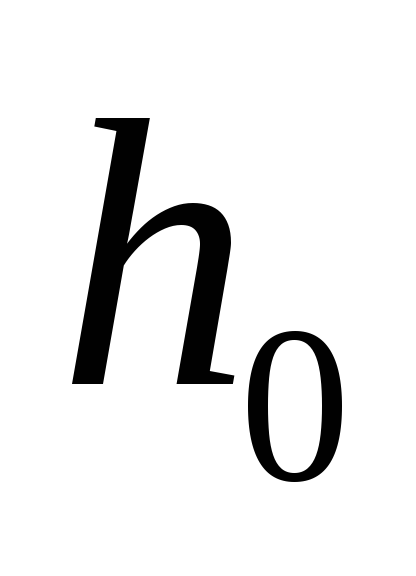 .
. -
Спокойно открыть и закрыть кран 2, уравняв давление в сосуде с атмосферным. После перекрытия крана 2, давление в сосуде начинает расти. Выждав момент, когда давление в сосуде перестанет меняться, сделать отсчет разности уровней
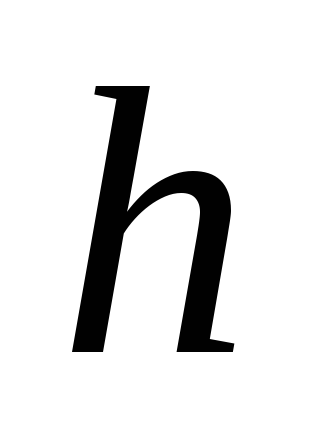 .
. -
Повторить опыт при различных значениях
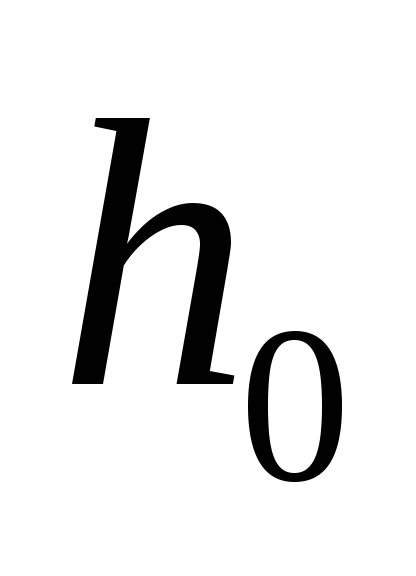 не менее шести раз.
не менее шести раз.
Результаты измерений занести в таблицу:
-
n
1
2
3
4
5
6
h0, мм.
h, мм.
γ
-
Рассчитать величину
 по формуле (7) для каждого опыта. Найти
среднее значение и оценить погрешность.
по формуле (7) для каждого опыта. Найти
среднее значение и оценить погрешность.
