
- •Розділ 19. Функціональна біохімія порожнин рота
- •19.1. Біохімія слини людини
- •19.1.3. Фізико-хімічні властивості слини та їх порушення.
- •19.2. Біохімічні особливості тканин зуба
- •19.2.8. Значення фтору для виникнення карієсу та флюорозу. Фтор – біогенний хімічний елемент, тобто постійна складова частина організму людини.
19.2. Біохімічні особливості тканин зуба
1
Мал.
19.6.
Будова зуба
Зуб побудований з трьох шарів кальцифікованої тканини: емалі, дентину та цементу, його порожнина заповнена пульпою (рис.19.6). Пульпа оточена дентином – основною кальцифікованою тканиною. В області коронки зуба дентин вкритий емаллю, а занурені в щелепу корені – цементом. Складові частини зуба різняться між собою за хімічним складом, особливостями обміну речовин і, відповідно, функціональним призначенням (табл. 19.4)
Таблиця 19.4. Біохімічний склад тканин зуба
|
Складові частини |
емаль |
дентин |
цемент |
пульпа |
|
Вода |
в г на 100 г тканини | |||
|
2,5 |
10 |
15 |
55 | |
|
Органічні сполуки |
1,5 |
20 |
25 |
40 |
|
Неорганічні сполуки |
96 |
70 |
60 |
5 |
|
Ca |
в г на 100 г золи | |||
|
36 |
35 |
35,5 |
30,0 | |
|
Mg |
0,5 |
1,2 |
0,9 |
0,8 |
|
Na |
0,2 |
1,2 |
1,1 |
0,2 |
|
K |
0,3 |
0,1 |
0,1 |
0,1 |
|
P |
17,3 |
17,4 |
17,1 |
17,0 |
|
F |
0,02 |
0,02 |
0,02 |
0,02 |
|
Цитрат |
0,3 |
1,0 |
- |
- |
Емаль – безсудинна, найтвердіша, стійка до зношування мінералізована тканина, яка залишається практично незмінною впродовж усього життя людини і має ектодермальне походження. Вона ззовні вкриває коронку зуба, розміщуючись поверх дентину і тісно з ним зв’язана як структурно так і функціонально. Ці властивості та особливості розташування обумовлюють функцію, яку вона виконує – захищає дентин і пульпу від зовнішніх механічних, хімічних і температурних подразників. Емаль становить 20 – 25 % зубної тканини, своєї максимальної товщини (2,3 – 3,5 мм) вона досягає в ділянці жувальних горбиків.
особливості будови емалі набуті в процесі філогенезу. Основним структурним компонентом емалі є емалеві призми (діаметр 4 – 6 мкм), які концентруються в жмути та утворюють S-подібні вигини (це зумовлює оптичну неоднорідність на шліфтах). Загальна кількість призм в емалі залежить від розміра зуба і коливається в межах 5 - 12 млн. Емалева призма має поперечну посмугованість, яка відображає добове відкладення мінеральних солей. Сама призма на поперечному розрізі має аркадоподібну або лускоподібну форму і складаються із щільно упакованих апатитоподібних кристалів, які щільно прилягають один до одного, але розташовуються під кутом (призмова емаль). Кожен кристал емалі має гідратний шар зв’язаних іонів, завдяки яким здійснюється іонний обмін. Між кристалами знаходяться мікропростори, заповнені емалевою рідиною, яка служить переносником молекул для багатьох речовин. Раніше вважали, що кожну призму оточує оболонка, збагачена органічними речовинами, але з допомогою електронної мікроскопії було встановлено, що міжпризмовий простір емалі містить такі ж кристали, що й сама призма, тільки орієнтовані в іншому напрямку (міжпризмова емаль). Ступінь мінералізації міжпризмової емалі нижчий, ніж призмової. Розрізняють ще безпризмову емаль, яка являє собою внутрішній шар емалі завтовшки 5 – 15 мкм уздовж дентинно-емалевої межі, вона не містить призм.
Неорганічні речовини емалі. Як зазначалося вище, емалеві призми побудовані з кристалів апатитів, розміри яких зростають з віком. Основними є гідроксіапатит (ГАП) та восьмикальцієвий фосфат. Інші види апатитів можуть утворюватися внаслідок ізоморфного заміщення кальцію на близькі до нього за властивостями хімічні елементи (табл.19.5).
Таблиця 19. 5. Вміст апатитів в емалі зуба
|
Апатит (назва) |
Вміст, % |
Структура |
|
Гідроксіапатит |
75,0 |
Ca10(PO4)6(OH)2 |
|
Восьмикальцієвий фосфат |
Ca8H2(PO4)6 · 5H2O | |
|
Карбонатний апатит |
19,0 |
Ca10(PO4)6CO3 або Ca10(PO4)5CO3(OH)2 |
|
Хлорний апатит |
4,4 |
Ca10(PO4)6Cl |
|
Стронцієвий апатит |
1,0 |
SrCa9(PO4)6(OH)2 |
|
Гідроксифторапатит або фторапатит |
0,66 |
Ca10(PO4)6F(ОН) Ca10(PO4)6F2 |
Окремі види апатиту різняться за хімічними та фізичними властивостями – міцністю, здатністю розчинятися (руйнуватися) під дією органічних кислот, а їх співвідношення в тканинах зуба обумовлюється характером харчування, забезпеченістю організму мікроелементами тощо.
р
Рис
. 19.7. Гексагональна форма молекули
гідроксіапатиту
Хімічні та фізичні властивості апатитів суттєво змінюються при включенні до їхнього складу таких елементів як Sr2+ та F2. Зокрема, стронцій активно конкурує з кальцієм за місце зв’язування в кристалічній решітці ГАП. Не зважаючи на їх подібні хімічні властивості, заміна кальцію на стронцій змінює архітектоніку ГАП. Стронцієвий апатит є менш стійким і легше руйнується під дією органічних кислот, що призводить до підвищення ламкості зубів. Підвищений вміст стронцію в харчових продуктах сприяє збільшенню вмісту стронцієвого апатиту та посилює ступінь ризику розвитку карієсу. Особливо небезпечним є надходження в організм радіоактивного стронцію, який, включаючись у структуру апатитів, може викликати локальне променеве ураження тканин.
Стронцій можна витіснити зі складу апатитів великою кількістю кальцію. Встановлено, що п’ятикратне збільшення кальцію в дієті призводить до зменшення включення стронцію на 50 %. Тому у випадках потрапляння радіоактивного стронцію в організм доцільно вживати їжу, збагачену кальцієм.
Карбонатний апатит, як і стронцієвий, має вищу розчинність у кислому середовищі порівняно з ГАП. У тканинах зуба карбонатний апатит розташовується поблизу емалево-дентинної межі, оскільки одонтобласти продукують аніони НСО3-. Посиленому утворенню карбонатного апатиту сприяють вуглеводні харчові продукти, особливо при їх тривалому перебуванні в ротовій порожнині. Крім того, з вуглеводних продуктів утворюється велика кількість органічних кислот, під дією яких карбонатний апатит легко руйнується.
Серед всіх апатитів найвищу стійкість має фторапатит. Він посилює міцність емалі, знижує її проникність, підвищує резистентність до карієсогенних чинників. Фторапатит в 10 разів повільніше розчиняється в кислотах, ніж ГАП. При достатній забезпеченості організму фтором різко (у 4 рази) зменшується кількість випадків захворювання на карієс. Його норма в питній воді коливається в межах 0,5 – 1,2 мг/л, з їжі фтор засвоюється на 20 % гірше порівняно з водою.
В нормі, поступаючи в організм, фтор перетворюється на гідроксифторапатит:
Ca10(PO4)6(OH)2 + 2F- Ca10(PO4)6F(ОН) + 2ОН-
гідроксифторапатит
При надмірній кількості фору в питній воді утворюється не гідроксифторапатит, а кальцію фторид – нерозчинна сполука, яка швидко вилужнюється, в наслідок чого розвивається флюороз:
Ca10(PO4)6(OH)2 + 2 F- 10 Ca F2 + 6 PO43- + 2 ОН-
фторид кальцію
ускладі мінеральних речовин емалі кальцій становить 37 %, а фосфор – 17 %. Властивості емалі значною мірою залежать від співвідношення цих елементів, яке змінюється з віком та залежать від низки чинників. В емалі зубів дорослих осіб молярне співвідношення Са/Р становить 1,67, у дітей є нижчим, а у людей 60-річного віку може досягати 2,0. Як показали дослідження останніх років, можливі суттєві відмінності співвідношення Са/Р у межах одного зуба, що послужило підґрунтям для твердження про неоднорідність структури емалі і, як наслідок, про нерівномірну схильність до карієсу різних ділянок. Зменшення показника нижче 1,3 сприяє розвитку карієсу, оскільки відбувається руйнування кристалів і демінералізація емалі.
Крім кальцію та фосфору до складу емалі входять у невеликій кількості катіони магнію, калію, натрію, а основними аніонами є третинний, вторинний і первинний фосфати, карбонати та бікарбонати і хлор. Численними дослідженнями встановлено, що мікроелементи в емалі розташовуються нерівномірно: у зовнішньому шарі переважають фтор, свинець, цинк, залізо; у глибокому – натрій, магній, карбонати; пошарово рівномірно розподіляються стронцій, мідь, алюміній, калій.
Органічні речовини емалі представлені білками, вуглеводами та ліпідами, а також азотовмісними речовинами (сечовина, пептиди, циклічні АМФ, циклічні амінокислоти).
Білки емалі в основному належать до нерозчинних в кислотах і 0,9 % ЕДТА (етилендиамінотетраоцтовій кислоті) та НСl (хлоридній кислоті). Вони містять велику кількістю серину, оксипроліну, гліцину, лізину. Завдяки надзвичайно високій стійкості, вони виконують роль скелета всієї структури емалі, утворюючи каркас – “корону” на поверхні зуба, ініціюють процеси мінералізації, впорядковують розташування кристалів, захищають від демінералізації. Не випадково у вогнищі демінералізації на стадії білої або пігментованої плями кількість цих білків зростає в 4 рази. Тому каріозна пляма впродовж кількох років не перетворюється на каріозну порожнину, а іноді взагалі не розвивається карієс.
Серед білків емалі важливе місце посідають специфічні білки емалі, які відіграють важливу роль в упорядкованому розташуванні кристалічної фази та ініціації мінералізації. До них належать:
Калькпротеїн (остеокальцин) (молекулярна маса 6 500 Да) – фібрилярний кислоторозчинний кальційзв’язуючий білок, який містить три залишки γ-карбоксиглутамінової кислоти, завдяки чому може зв’язувати 8 – 10 іонів кальцію і тим самим утворює нерозчинну у воді білкову матрицю емалі. Він ініціює ріст кристалів ГАП і міцно зв’язується з ними.
Сіалопротеїд – низькомолекулярний глікофосфопротеїд (молекулярна маса ~70 000 Да), який ковалентно зв’язаний певним числом розгалужених олігосахаридних субодиниць, що містять від 2 до 15 похідних гексоз. Цьому білку належить провідна роль у процесах мінералізації, оскільки він зв’язує залишки фосфорної кислоти складноефірним зв’язком з допомогою гідроксильної групи серину, після чого кристали металів приєднуються іонними зв’язками до фосфату.
Тафтелін (молекулярна маса 43,8 кДа) – кислий фосфоризований глікопротеїни, який складається з 338 амінокислотних залишків. Він містить 1 глікозильований залишок і 5 залишків цистеїну. Білок відіграє роль сигнального, забезпечуючи в ембріональному періоді морфогенез емалевого органа. Тафтелін не відіграє істотної ролі нуклеатора кристалів ГАП, але є важливим білком диференціювання проамелобластів.
Енамелін – білок, який у стадію раннього купола локалізується вздовж емалево-дентинної межі у відростках Томса, а в зрілій емалі – в шийковій частині зуба та вздовж емалево-дентинної межі безпризмової емалі. В емалі, яка формується, він становить 10 %, а в зрілій емалі – 90%, що пов’язано не з посиленням синтезу, а з підвищеною деградацією амелогеніну, який елімінується амелогеніназами.
У залежності від молекулярної маси розрізняють 3 групи енамеліну. Надвеликий (186 кДа) локалізується переважно у зовнішньому шарі емалі, під дією металопротеїнази - енамілізину гідролізується до великого енамеліну (89 кДа), а останній у глибоких шарах емалі руйнується специфічним ензимом – серинопротеїназою – до низькомолекулярного енамеліну (32 кДа).
Молекула енамеліну містить значну кількість серину та глутаміну, які здатні фосфорилюватися, і, подібно до інших неколагенових кислих білків є нуклеатором мінералізації – формує центр кристала і визначає його позицію, орієнтацію в ході подальшого формування супермолекули ГАП.
5. Амелогенін з’являється в емалі на стадії дзвона, у зрілій емалі практично повністю зникає. Його молекула складається з 216 амінокислотних залишків, серед яких переважають пролін, лейцин, глутамін і гістидин. У залежності від молекулярної маси та локалізації розрізняють 3 групи амелогеніну: надвеликий (молекулярна маса 46 і 72 кДа), локалізується в цитоплазмі деяких енамелобластів; великий (молекулярна маса 28, 25, 22, 20 кДа) міститься в емалевих призмах; малий (молекулярна маса 5, 10, 12, 16 кДа) знаходиться в міжпризмовій емалі. У матриці емалі, яка лише формується, наявність різних за молекулярною масою амелогенінів дозволяє регулювати розмір і ріст кристалів шляхом надходження іонів кальцію і фосфору в тканину. Крім того, окремі фрагменти амелогеніну можуть виступати (подібно до енамеліну) у якості нуклеаторів кристалізації.
Крім білків у емалі присутні вільні пептиди та амінокислоти, такі як пролін, гліцин, валін, оксипролін, серин - їх концентрація не перевищує 0,15 %. Вуглеводи представлені глюкозою, галактозою, фруктозою, глікогеном. Дисахариди перебувають у вільній формі, а також утворюють білкові комплекси - фосфоглікопротеїни. Ліпідів дуже мало (0,6 %), здебільшого вони представлені глікофосфоліпідами, які під час утворення матриці відіграють роль сполучних містків між білками й мінералами, зв’язують іони Са2+ та інші катіони, і, таким чином, приймають участь в утворенні ядер кристалізації, стабілізують аморфний фосфат кальцію. Обов’язковим компонентом емалі зуба є цитрат.
Дентин – мінералізована, безклітинна, безсудинна (звапнована) тканина зуба, яка утворює основну його масу і визначає форму. Він міцніший від кістки та цементу, але в 4 – 5 разів м’якший від емалі. Дентин побудований з мінералізованої міжклітинної речовини, пронизаної чисельними дентиновими канальцями (трубочками).
Мінеральну основу дентину складають кристали ГАП, фторапатиту, карбонат кальцію та, незначною мірою, аморфним фосфатом кальцію, які відкладаються у вигляді зерен, брилок та кулястих утворів – калькосферитів. Кристали відкладаються між колагеновими фібрилами, на їх поверхні та всередині самих фібрил. Найважливішими елементами дентину є іони кальцію, калію, магнію, натрію, хлору, концентрація останніх зростає у внутрішніх шарах дентину. Співвідношення Са/Р коливається в межах 1,5 – 1,67. Концентрація фтору знаходиться в прямій залежності від його надходження в організм, оскільки фтор у дентин поступає через кровоносні судини пульпи.
Мінеральний склад дентину відображають наступною формулою: А10(ВО4)6С2, де А – кальцій, барій, кадмій, мідь; В – фосфор, арсен, вісмут, хром, силіцій; С – фтор, хлор, ОН-, СО-3.
Для дентину, як і для емалі, характерний уповільнений обмін мінеральних компонентів, що має велике значення для збереження стабільності тканин в умовах підвищеного ризику де мінералізації та стресу.
Органічний матрикс дентину за своїм складом близький до органічного матриксу кісткової тканини. Білки становлять 20 % від загальної маси дентину і представлені, в основному, колагеном І, ІІІ, ІV, V, VІ типів, протеогліканами та глікопротеїнами. Між колагеновими фібрилами розташовуються ліпідні гранули, вміст ліпідів у дентині досягає 330 – 350 мг/100 г тканини.
Функціональне значення протеогліканів визначається властивостями глікозаміногліканів, які входять до їх складу. Оскільки глікозаміноглікани містять велику кількість гетероатомів, карбоксильних та сульфатних груп, то завдяки своїй високій реакційній здатності вони можуть взаємодіяти з іншими макромолекулами і, тим самим, брати участь в структурній організації дентину та виконувати певні специфічні функції. Так, глікозаміноглікани регулюють процеси агрегації (ріст та орієнтацію) колагенових фібрил і стабілізують структуру колагенових волокон; вони відіграють роль пластифікаторів колагенової сітки, підвищуючи її здатність до розтягування та набухання під час процесу мінералізації; володіють високою здатністю зв’язувати катіони і, тим самим, беруть участь в утворенні ядер (центрів) мінералізації.
Важливу групу розчинних білків складають глікопротеїни, вуглеводний компонент яких може бути представлений глюкозою, галактозою, манозою, фукозою, N-ацетилглюкозаміном. Сіалові кислоти є специфічними компонентами групи глікопротеїнів – сіалопротеїнів, вміст яких є особливо високим в дентині. До цієї групи білків належать кістковий сіалопротеїн, матриксних білок дентину-1, остеопонтин, дентинфосфопротеїн і дентинсіалопротеїн. У процесі синтезу одонтобластами ці білки підлягають численним посттрансляційним модифікаціям – глікозилюванню сіаловою кислотою, сульфуванню та фосфорилуванню і виконують роль антен для неорганічних компонентів, контролюють ділянки та швидкість мінералізації дентину.
Матриксний білок дентину-1 – кислий глікофосфопротеїн, містить 2 молекули N-ацетилнейрамінової кислоти та один протеоглікановий ланцюг, зв’язаний з білком через залишок серину. У його складі міститься 8 залишків фосфорної кислоти та 20 молекул сульфату, які зв’язують іони кальцію. У процесі дентиногенезу цей білок бере участь у формуванні та рості кристалів апатитів дентину, а його недостатність призводить до дефектів формування кристалічної основи дентину.
Дентинсіалопротеїн – глікопротеїни з молекулярною масою 95 000 Да, містить 30 % вуглеводів і 10 5 сіалових кислот. Дентинфосфопротеїн становить 50 % всіх неколагенових білків дентину, має велику молекулярну масу – 151 000 – 167 000 Да. Оскільки цей білок має високу схожість з іонами кальцію, вважають, що він діє як нуклеатор в утворенні первинних кристалів гідроксіапатиту і впливає на формування кристалів у процесі їх росту.
До глікопротеїнів належить також фібронектин. Він має властивості «липкого» білка. Зв’язуючись з вуглеводними групами сіалопротеїнів на поверхні плазматичних мембран, він забезпечує взаємодію клітин між собою та компонентами міжклітинного матриксу. Так, взаємодіючи з колагеновими фібрилами, фібронектин сприяє утворення перицелюлярного матриксу. Для кожної сполуки, з якою він взаємодіє, фібронектин має свій, специфічний центр зв’язування.
Дентин містить білки, які регулюють процес мінералізації. До них належать амелогенін, остеокальцин, остеонектин, остеоадерин. На проліферацію та диференціювання одонтобластів, які беруть участь у формуванні та підтриманні структури і форми мінералізованого матриксу дентину, впливають різні фактори росту – це ФРФ, інсуліноподібний фактор росту-1, ТФР-β, морфогенетичний білок кістки -2 та -4, ІЛ-1- β. Під час пригнічення синтезу ТФр- β знижується синтез фосфосіалопротеїнів і, як наслідок, розвивається гіпомінералізація дентину.
до складу дентину входить також глікоген.він є основним джерелом енергії для процесів формування ядер кристалізації, тому локалізується в місцях утворення центрів кристалізації. Вміст глікогену в тканині є прямо пропорційним до інтенсивності процесів мінералізації, оскільки характерною особливістю тканин зуба є переважання анаеробних процесів енергоутворення – глікогенолізу та гліколізу. Навіть за умови достатньої забезпеченості киснем, 80 % енергетичних потреб тканин зуба покривається за рахунок анаеробного гліколізу, і, відповідно, розщеплення глікогену.глікоген є джерелом фосфорних ефірів глюкози – субстратів лужної фосфатази, ензиму, який відщеплює залишки фосфорної кислоти від глюкозомонофосфатів і переносить їх на білкові матриці, тобто ініціює утворення неорганічної матриці зуба; глікоген також є джерелом глюкози, яка перетворюється в N-ацетилглюкозамін, N-ацетилгалактозамін, глюкуронову кислоту та інші похідні, які беруть участь в синтезі гетеро полісахаридів, про які згадувалося вище.
Вміст цитрату в дентині досягає 1 %. Крім тканин зуба він забезпечує оптимальну концентрацію кальцію в сироватці крові та слині, тим самим регулюючи швидкість процесів мінералізації та демінералізації. Вміст цитрату, як і вміст кальцію, в крові та тканинах регулюють гормони підшлункової та прищитоподібних залоз – інсулін і паратгормон.
Основний процес, у якому утворюється цитрат, це ЦТК. Активність цитратсинтази в кістковій тканині та зубах вища, ніж в інших тканинах.
Цитрат існує в 2 формах: розчинна форма (утворюється в ЦТК) окиснюючись, володіє високою комплексоутворювальною здатністю, бере участь у процесі мінералізації тканин, з'єднуючись із іонами Са, забезпечує їх транспорт; нерозчинна форма входить до складу мінеральних компонентів кістки й зуба, адсорбується на поверхні кристалів ГАП і міцно зв'язується з ними. Білкова частина цього цитрату включається в емаль і дентин і відіграє роль у патогенезі карієсу, тому що цитрат визначає властивості розчинності й проникності емалі.
Структурно-функціональна організація дентину. За часом виникнення розрізняють:
первинний дентин, який утворюється в період формування та прорізування зубів зі швидкістю 4 – 8 мкм/добу, він відкладається одонтобластами і є основою цієї тканини;
вторинний дентин (регулярний або фізіологічний) утворюється в сформованому зубі після прорізування і є продовженням первинного (товщину вторинного дентину використовують для визначення віку індивіда);
т
Рис.
19.8. Розташування дентинних трубочок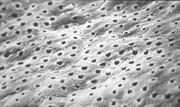
Основна речовина дентину пронизана великою кількістю дентинних трубочок (30 – 75 тис./ мм2) (рис. 19.8).
У просвіті дентинних трубочок розташовані відростки одонтобластів периферійного шару пульпи і циркулює дентинна рідина, з якою поступають органічні та неорганічні речовини, що беруть участь в обмінних процесах дентину. Рідина являє собою транссудат периферійних капілярів пульпи і за білковим складом є схожою до плазми крові.
Отже, поступлення поживних речовин в дентин здійснюється через судини пульпи. Зсередини стінка дентинної трубочки вкрита тонкою плівкою органічної речовини (мембраною Неймана), яка містить високу концентрацію глікозаміногліканів (рис. 19.9).
Завдяки надзвичайно великій кількості дентинних канальців дентин, не зважаючи на високу міцність, має дуже високу проникність. Це визначає швидку реакцію пульпи на ушкодження дентину. При розвитку карієсу дентинні трубочки слугують шляхами розповсюдження мікроорганізмів та запального процесу.
З
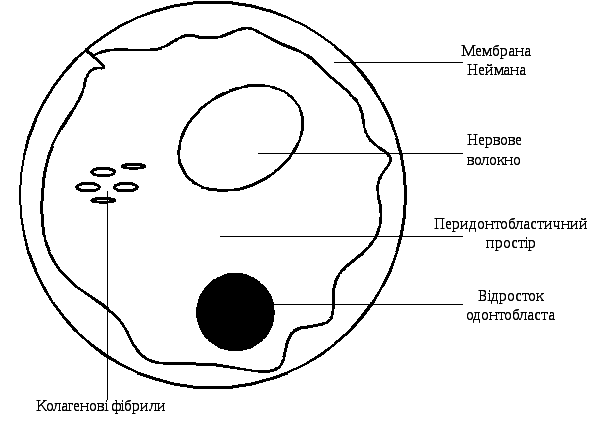 Рис.
19.9. Схематичне зображення дентинної
трубочки
Рис.
19.9. Схематичне зображення дентинної
трубочки
Утворення дентину та підтримання його складу нероздільно зв’язано з клітинами пульпи. У процесі ініціації мінералізації беруть участь іони, які локалізовані в тілах одонтобластів. Активний транспорт цих іонів відбувається за участі Са2+-, К+-, Nа+-АТФаз. Концентрація іонів кальцію в позаклітинній рідині вища ніж у клітинах, тому Са2+-АТФаза переносить іони кальцію за рахунок енергії АТФ проти градієнта концентрації. При цьому активується перенесення іонів К+ та Nа+ в клітини пульпи та з неї. Транспортні К+-, Nа+-АТФази запобігають зростанню осмотичного тиску в клітинах пульпи. Описаний транспорт іонів триває і після прорізування зубів, підтримуючи мінеральний склад зрілого дентину.
Цемент – мінералізована, неваскуляризована тканина зуба, яка вкриває його корінь і за хімічним складом схожа до грубоволокнистої кістки. Товщина цементу мінімальна в ділянці шийки зуба (20 – 50 мкм) і максимальна на поверхні його кореня (100 – 1 500 мкм), він практично не оновлюється.
Цемент поділяють на клітинний, який розташовується в області верхівки кореня та його біфуркації і за структурою нагадує кістку та безклітинний, який вкриває всю поверхню кореня і складається з колагенових волокон і аморфної речовини, яка їх склеює.
Цемент входить до складу підтримуючого апарату зубів і забезпечує його прикріплення до періодонта; захищає дентин кореня від ушкоджувального впливу; забезпечує збереження загальної довжини зуба, компенсуючи стирання емалі внаслідок її зношування, відкладаючись у ділянці верхівки кореня (пасивне прорізування), а також виконує репаративну функцію під час утворення «резорбційних лакун» та у випадку перелому кореня.
Основу цементу становлять солі кальцію (карбонати та фосфати), Вміст фтору в поверхневих шарах цементу вищий, ніж у внутрішніх. Надмірна кількість фтору в цементі та дентині призводить до порушення синтезу глікопротеїнів, що проявляється зниженням твердості зубів і їх руйнуванням.
урізних напрямках тканину цементу пронизують колагенові волокна І, ІІ, ІІІ, V, ХІІ і ХІV типів, клітинні елементи – цементобласти, які синтезують специфічний цементозвязуючий білок, необхідний для адгезії та переміщення мезенхімальних клітин. Основою неколагенового матриксу є два великих глікопротеїни – кістковий салівопротеїн і остеопонтин, які зв’язані з колагеновими білками та клітинами. Вважають, що кістковий салівопротеїн виконує переважно адгезивну функцію для поверхневих клітин зуба і бере участь у процесі мінералізації, а остеопонтин через взаємодію з ανβ3-інтегрином клітинної мембрани регулює міграцію клітин у період цементоутворення. У цементі присутній також фібронектин, який зв’язує клітини з позаклітинним матриксом, а в процесі диференціювання одонтобластів з’являється білок тенасцин, який бере участь у сполученні періодонтальних волокон з цементом. Крім цього, цементобласти синтезують остеонектин, остеокальцин, ламінін і ундулін, особливості структури останнього забезпечують його зв’язування з інтерстиціальними колагенами та колагеном І типу. Ундулін подібний на танесцин і фібронектин і разом з цими білками бере участь у розвитку та диференціюванні клітин.
У процесі утворення цементу проліферацію та диференціювання незрілих цементобластів активують різноманітні фактори росту - ФРФ, ТФР-β, інсуліноподібний фактор росту-1. Поряд з ними виявлена унікальна молекула, властива лише тканині цементу – білок з молекулярною масою14 000 Да, який назвали фактором росту цементу, регуляторну функцію виконує також білок остеопонтин.
19.2.2. Пульпа – особливості біохімічного складу та обміну. Пульпа зуба – це інтенсивно васкуляризована та іннервована спеціалізована пухка волокниста сполучна тканина, яка заповнює коронкову порожнину та кореневий канал.
Вона складається з клітин (одонтобластів, фібробластів, макрофагів, дендритних клітин, лімфоцитів, опасистих клітин) та міжклітинної речовини. Функція одонтобластів і фібробластів полягає в утворенні основної міжклітинної речовини та синтезі колагенових фібрил. Тому клітини мають потужний білок-синтезуючий апарат, який забезпечує утворення великої кількості колагену (І, ІІІ, V, VI типів), протеогліканів, глікопротеїнів та інших водорозчинних білків, зокрема, альбумінів, глобулінів, ензимів. Методом електрофорезу в пульпі виявлено біля 650 неколагенових білків, з яких ідентифіковано понад 96. Частина цих білків характерна лише для пульпи, проте більшість присутні і в інших тканинах (табл.. 19.6).
Таблиця 19.6. Білки пульпи зуба
|
Назва білка |
Біологічна роль |
|
Остеопонтин |
Відіграє ключову роль у побудові мінералізованого матриксу дентину, забезпечуючи взаємодію клітин з матриксом; бере участь у транспорті іонів |
|
Кальцитонін |
Стимулює секрецію остеобластів під час утворення тканини дентину |
|
Остеонектин |
Взаємодіє з факторами росту і активує синтез колагену І типу; необхідний під час розвитку і дозрівання мінералізованої тканини |
|
Інтегрини |
Забезпечують адгезію клітин пульпи до компонентів позаклітинного матриксу |
|
Ламінін |
Склеює епітеліальні клітини з базальною мембраною; бере участь в одонтогенезі |
|
Амелогеніни |
Забезпечують склеювання багатьох типів клітин; слугують джерелом фосфату при побудові тканини дентину |
|
Дентинсіалофосфопротеїн |
Регулює процеси диференціювання одонтобластів, утворення третинного дентину, інгібує мінералізацію пульпи |
|
Лужна фосфатаза |
Бере участь у транспорті біологічно важливих речовин; інгібує мінералізацію пульпи шляхом від’єднання фосфатних груп від протеїнів, які є активаторами процесів мінералізації |
|
Фібронектин |
Бере участь у проліферації фібробластів в одонтобластоподібні клітини |
|
Фактори росту (ФРТ, ФРЕ, ПФР, ФРФ, ЕФР, ТФР-β) |
Стимулюють або інгібують проліферацію клітин |
|
Матриксні металопротеїнази (ММП): ММП-1, -2, -8, -9, -10, -11, -13, -14, -15, -16, -19 та їх інгібітори (ТІМП): ТІМП-1,-2, -3, -4 |
Беруть участь у побудові органічного матриксу дентину |
|
Протеоглікани (декорин, біглікан, версікан) |
Надають пульпі еластичності та стійкості при стисканні |
|
Глікозаміноглікани (хондроїтин-4-сульфат, хондроїтин-6-сульфат, дерматансульфат, кератансульфат, гіалуронова кислота) |
Стабілізують колагенові волокна, утримують воду, беруть участь у мінералізації дентину |
Ліпіди в пульпі представлені фосфатидилхоліном, фосфатидилетаноламіном, фосфатидилсерином, сфінгомієлінами, фосфатидилінозитолом, холестерином і жирними кислотами.
Пульпа характеризується високим рівнем окисно-відновних процесів і тому використанням великої кількості кисню. Регуляція енергетичного балансу пульпи здійснюється шляхом спряження окиснення та фосфорилування. У пульпі зуба виявлена висока активність ензимів вуглеводного обміну, циклу трикарбонових кислот, синтезу РНК. Активність ензимів пентозофосфатного шляху є особливо високою в період активної продукції одонтобластами дентину. Присутні також ензими водно-мінерального обміну – лужна та кисла фосфатази. Лужна фосфатаза каталізує перенесення залишків фосфорної кислоти (фосфат-аніонів) від фосфорних ефірів глюкози на органічний матрикс. Тобто, ензим бере участь в утворенні ядер кристалізації і, тим самим, сприяє мінералізації тканин зуба. Кисла фосфатаза має протилежний, демінералізуючий ефект. Вона належить до лізосомальних кислих гідролаз, які посилюють розчинення як мінеральних, так і органічних структур тканин зуба. У період мінералізації та ремінералізації зуба зростає вміст нуклеїнових кислот, що пов’язано з підвищенням синтезу білків клітинами остеобластами та одонтобластами.
Результатом вищеперерахованих процесів обміну є утворення великої кількості проміжних продуктів, які згодом потрапляють із пульпи в тверді тканини зуба. При карієсі відбуваються деструктивні зміни в одонтобластах, руйнуються колагенові волокна, порушується обмін речовин і активність ензимів. Гемостаз пульпи за умов норми забезпечують вазоактивні речовини – простациклін, ендотелін, NO. При ушкодженні судин їх синтез зменшується, а активується синтез похідних арахідонової кислоти – лейкотрієнів, тромбоксанів, що викликає компенсаторний спазм судин.
Пульпа виступає своєрідним біологічним бар’єром, її функції обумовлені наявністю в ній певних речовин. Так, захисна функція забезпечується завдяки в'язким властивостям гіалуронової кислоти, хондроїтин- і дерматансульфатів, які підтримують певний вміст води в складі пульпи, що сприяє затриманню бактерій, які не володіють гіалуронідазною активністю; макрофаги виконують фагоцитарну функцію та здійснюють синтез цитокінів, гідролаз, лізоциму, компонентів системи комплементу, ФРФ; обмін аскорбінової кислоти забезпечує імунозахисні процеси в пульпі під час запалення; інгібітор колагенази, присутній як у клітинах, так і в міжклітинному матриксі пульпи, перешкоджає дегенерації колагенових волокон, захисну роль відіграють також ензими лужна й кисла фосфатази, неспецифічна естераза. Пластична функція полягає в утворенні вторинного дентину, колагену, протеогліканів, а трофічна забезпечується добре розвинутою кровоносною та лімфатичною системами, які здійснюють трофіку дентину коронки і кореня зуба. за рахунок наявності в пульпі великої кількості нервових закінчень чутливу рецептори отримують і передають інформацію в центральну нервову систему – це визначає її сенсорну функції.
19.2.3. Амелогенез. Процеси мінералізації – демінералізіції – основа мінерального обміну тканин зуба. Утворення емалі зуба (амелогенез) починається після відкладання перших шарів дентину і зв’язане з секрецією енамелобластами специфічних білків. Цей процес складається з трьох стадій:
перша, секреторна, стадія включає ініціацію формування позаклітинного матриксу; поступову деградацію органічного матриксу та ріст кристалів; впорядковане розташування кристалів; контроль за подальшим ростом кристалів по довжині та ширині; формування призматичної структури кристалів емалі;
друга стадія (дозрівання) супроводжується видаленням залишків білових молекул; завершенням росту кристалів; насиченням іонами магнію та фтору;
третя стадія (зрілої емалі) закінчується формуванням емалі та деградацією клітинного шару емалевого органа.
В амелогенезі бере участь велика кількість білків, які різняться за амінокислотним складом, молекулярною масою та рухливістю в електричному полі. Деякі з них ідентифіковані. Це кальційзв’язуючі білки – кальбіндин, кальретикулін, аннексин V, кльмодулін і зв’язані з ним кальцінейтрини А і В, а також білки, які беруть участь в утворенні цитоскелета – тропоміозин, актин, цитокератин, віментин та ензими: F1β-субодиниця АТФ-синтази, креатинкіназа, ендоплазмін, енолаза, малатдегідрогеназа, фосфоглюкомутаза, емалева матриксна серинова протеїназа-1 тощо. В процесі свого синтезу білки підлягають пострансляційній модифікації, яка включає фосфорилування та глікозилування поліпептидних ланцюгів. Гідрофобні молекули білка амелогеніну, який синтезується в процесі амелогенезу в цитоплазмі енамелобластів без участі АТФ, агрегують між собою і утворюють наносфери, які беруть участь в процесі дозрівання емалі (рис. 19.10). Паралельно відбувається спрямоване поступлення іонів октакальцію фосфату для формування кристалів.

Рис. 19.10. Формування наносфер у процесі амелогенезу: А – утворення зв’язку в амелогеніні між амінокислотами С- і N-кінцевої ділянки; Б – з 6 амелогенінів утворюються наносфери
Важливе значення в амелогенезі відіграє тафтелін-інтерактивний білок (ТІР-39) (молекулярна маса 39 000 Да), схожий за будовою на тафтелін. Цей білок бере участь у транспорті синтезованих амелобластами білків у міжклітинний матриксу емалевого органа і внутрішньоклітинному перенесенні амелогеніну. Комплекс тафтелін-ТІР-39 забезпечує зв'язок між дентином і амелобластами в процесі утворення дентинно-емалевої межі.
У людей зустрічається генетично обумовлений незавершений амелогенез, пов'язаний із дефектом гена AMELXу хромосомах енамелобластів. У результаті змінюється амінокислотний склад синтезованих амелогенінів і порушується ріст кристалів на органічному матриксі . Під час тривалого приймання вагітними жінками та дітьми раннього віку антибіотиків тетрациклінового ряду виникає множинна гіпоплазія емалі (тетрациклінові зуби), виникнення якої пов’язують з блокуванням тетрациклінами 30Sсубодиниці рибосоми і блокуванням приєднання аміноацил-тРНК в А-центрі рибосоми, що призводить до порушення елонгації поліпептидного ланцюга, а порушення синтезу білка, своєю чергою, змінює процеси утворення первинних кристалів гідроксіапатитів у твердих тканинах зуба.
Мінералізація тканин зуба – це процес утворення органічної основи, перш за все колагену, та насичення її солями кальцію. Мінералізація є особливо інтенсивною в період прорізування зубів і формування твердих тканин зуба, адже зуб прорізується з немінералізованою емаллю.
Існує кілька теорій мінералізації твердих тканин зуба: згідно першої, фізико-хімічної, в основі мінералізації зуба лежить два процеси – нуклеація (утворення щільного осаду – ядра) та епітаксис (ріст кристалів з утвореного ядра); друга теорія – ензимна: лужна фосфатаза гідролізує фосфорорганічні ефіри, у результаті чого утворюються фосфат-іони, які за наявності іонів кальцію та матриці спричинюють ріст кристалів гідроксіапатитів; третя теорія змішана – згідно неї спочатку синтезується позаклітинний матрикс, а згодом, внаслідок перенасиченого стану розчину фосфату кальцію та за наявності матриці відбувається мінералізація.
Перший етап мінералізації – утворення білків з невеликою молекулярною масою. У складі секреторних гранул містяться високомолекулярні глікофосфопротеїни, які підлягають органічному гідролізу протеолітичними ензимами – енамелізинами, калікреїном і сериновими протеїназами. Кожна протеїназа володіє субстратною специфічністю і гідролізує пептидні зв’язки, утворені певними амінокислотами. Процес протеолізу носить каскадний характер, що супроводжується утворенням білків з різною молекулярною масою та функціями. Утворені в процесі гідролізу низькомолекулярні білки спроможні приєднувати Са2+ і РО43-.
Другий етап – кальцифікація органічного матриксу – відкладання апатитів на матриці. Орієнтований ріст кристалів розпочинається в точках кристалізації (нуклеації) – ділянках із високою концентрацією іонів кальцію та фосфатів. Локально висока концентрація цих іонів забезпечується здатністю всіх компонентів органічної матриці зв’язувати кальцій і фосфати. Зокрема:
гідроксильні групи залишків серину, треоніну, тирозину, гідроксипроліну та гідроксилізину зв’язують фосфат-іони;
вільні карбоксильні групи залишків дикарбонових кислот колагенових фібрил, протеогліканів і глікопротеїнів зв’язують іони Са2+;
залишки γ-карбоксиглутамінової кислоти кальційзв’язуючого білка – остеокальцину зв’язують іони Са2+.
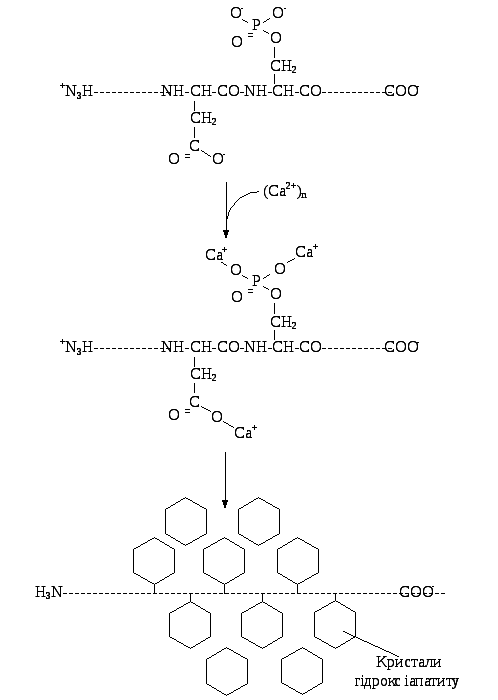
С
Рис. 19.11. Формування
кристалів гідроксіапатиту: до залишків
глутамінової кислоти, аспарагіну та
фосфосерину приєднуються іони кальцію
та фосфату. У процесі подальшої
преципітації формується первинний
кристал гідроксіапатиту
Впорядковане розташування та форма кристалів емалі відрізняється від безформенних пластинчастих призм кістки та дентину. Унікальність емалевих кристалів обумовлена особливістю їх формування та росту. У регуляції росту кристала в довжину, ширину та товщину беруть участь амелогеніни, упаковані в наносфери. Вони рухомі, не зв’язуються з кристалами, а наявність у їх складі глутамінової кислоти дозволяє зв’язувати молекули Н2О та Са2+, сприяючи тим самим росту кристалів.
Специфічним ензимом, який активує процес осадження мінеральних речовин на органічному матриксі, є лужна фосфатаза, адже вона володіє властивістю вивільняти неорганічний фосфат із органічних сполук. Цей фосфат взаємодіє з кальцієм, утворюючи солі, і відкладається там, де діє цей ензим (теорія Робісона). Доведено, що процес мінералізації інгібує пірофосфат, а ензим пірофорилаза, який розщеплює пірофосфат, ліквідує це інгібування. Тому мінералізація відбувається лише в тих тканинах, в яких присутня пірофосфорилаза.
Утворена (первинна) емаль є незрілою. Вона складається з 30 % органічного матриксу та 70 % неорганічних речовин. У вторинній мінералізації беруть участь енамелобласти стадії дозрівання, які містять велику кількість кальцій-зв’язуючих білків. Через енамелобласти в емаль переносяться неорганічні іони і виводяться органічні речовини та вода – відбувається майже 100 – 200-кратне зменшення кількості білків, значно змінюється їх амінокислотний склад. Остаточна мінералізація відбувається вже після прорізування зубів. Частина неорганічних речовин потрапляє з дентину, але основна їх кількість - зі слини. У зв’язку з цим для повноцінної мінералізації дуже важливі мінеральний склад і рН останньої. Такі елементи як Mg2+, Mn2+, Zn2+, Cu2+, Si2+ посилюють процес мінералізації, тоді як Se4+ – навпаки, сповільнює. Цей процес відбувається за участі вітамінів (А, С, D, Е, К), гормонів щитоподібної, підшлункової та прищитоподібних залоз, ензимів (кислої та лужної фосфатаз, АТФази, езимів тканинного дихання, які компенсують витрати енергії).
У процесі обміну речовин в тканинах зуба має місце врівноважений процес кристалізації та декристалізації гідроксіапатиту, утворюються та розриваються зв’язки з молекулами органічної субстанції, тому демінералізація є фізіологічно зворотним до мінералізації процесом, в основі якого лежить розчинення кристалів і руйнування емалі. Розчинність емалі визначається концентрацією та активністю катіонів і аніонів в слині під час контакту з гідроксіапатитом. Демінералізація може посилюватися при порушенні синтезу колагену та неколагенових білків, зниженні вмісту Са2+ в слині та збільшенні концентрації кислих продуктів обміну в ній. Чутливим показником переходу демінералізації з фізіологічного процесу в патологічний процес є зниження в емалі зуба коефіцієнта Са2+/ Р нижче за 1,3.
Однією з загальновизнаних небезпек в ортодонтичній практиці є демінералізація емалі, пов’язана з тривалим використанням брекет-системи. Приклеєні на зуби іноді впродовж 2-3 річного періоду, брекети стають механічною перешкодою для природного самоочищення порожнини рота. Переважна більшість ортодонтичних хворих – це підлітки, емаль у яких ще повністю не сформувалася. Крім того, відсутність стійких навичок по догляду за порожниною рота є основою для збільшення кількості м'якого зубного нальоту навколо основи брекетів, особливо в пришийкових областях і контактних пунктах. Доведено, що змінюється і кількісний склад мікробної флори – вона достовірно збільшується в усіх пацієнтів з брекет-системою. Тривала ретенція мікробної бляшки у таких пацієнтів призводить до вогнищевої демінералізації, оскільки відбувається дифузія кислоти через міжпризмовий простір емалі, дисоціація кальцію та фосфатів у поверхневому шарі. Клінічно це проявляється білими плямами та смужками, що повторюють контури основ брекетів. Список негативних наслідків під час використання брекет-системи доповнюють катаральні гінгівіти, періодонтити, випадки гіперплазії ясен і резорбції верхівок коренів зубів, що є наслідком передозування ортодонтичних сил.
Ремінералізація – це часткова зміна або повне відновлення мінеральних компонентів емалі зуба за рахунок компонентів слини або ремінералізуючих засобів (10 % р-н кальцію глюконату, 3,5 % р-н ремоденту, 2 % р-н фториду натрію). Вона базується на адсорбції мінеральних речовин у пошкоджені (каріозні) ділянки та іонному заміщенні гідроксіапатиту в залежності від характеру харчування та стану обмінних процесів в тканинах зуба. Зокрема, надлишкове поступлення фтору та стронцію призводитиме до заміни гідроксіапатиту на фторапатит та стронцієвий апатит, оскільки гідроксильні групи апатиту заміщуються на фтор, а кальцій заміщується на стронцій.
Критерієм ефективності ремінералізуючих розчинів є такі властивості емалі як проникність і розчинність, а також зникнення або зменшення в розмірі каріозної плями.
Проникність емалі- це процес, який сприяє її мінералізації та здійснюється завдяки наявності в емалі мікропросторів між кристалами гідроксіапатиту та омиванню емалі ззовні ротовою, а з боку пульпи – тканинною рідиною. Проникність – основний фактор дозрівання емалі, тому найінтенсивніше вона відбувається після прорізування зубів, знижується на момент дозрівання тканин зуба та продовжує знижуватися з віком. Раніше вважали, що речовини поступають в емаль шляхом пульпа-дентин-емаль, але тепер достеменно відомо, що основний шлях – це слина-емаль.
Проникнення речовин в емаль відбувається простою та полегшеною дифузією. При цьому вода (емалева рідина) транспортується з області низької молекулярної концентрації в високу, а іони навпаки – з боку високої концентрації в низьку. Іншими словами, іони кальцію переміщаються зі слини, яка ними перенасичена, в емалеву рідину, де їх концентрація незначна. Так, в експериментальних дослідженнях показано, що при нанесенні на поверхню інтактної емалі розчину радіоактивного кальцію, його вже через 20 хв виявляють у її поверхневому шарі, при тривалішому контакті розчину з зубом, радіоактивний кальцій проникає на всю глибину емалі, аж до емалево-дентинного з’єднання. Легко проникають в емаль не лише катіони кальцію, а й магнію, калію, натрію, фтору, срібла, фосфати, бікарбонати, хлориди, фториди, амінокислоти лізин і гліцин, сечовина, глюкоза, фруктоза, галактоза, вітаміни, гормони.
Рівень проникності емалі залежить від розміру мікропросторів у структурі емалі, розмірів іонів чи молекул речовин і здатності цих речовин зв’язуватися в компонентами емалі. Цей показник знижується з віком, при дії лужного середовища ротової рідини і паратгормону і навпаки - підвищують проникність емалі – гормон кальцитонін, кальцитріол, ензим гіалуронідаза, каротин, низькі значення pH (кисле середовище), ультразвук, електрофорез. Іони фтору після аплікації фториду натрію швидко проникають в емаль, після чого різко знижують проникність емалі. Це явище необхідно врахувати в клініці при проведенні ремінералізації зубів. Склад слини теж впливає на проникність емалі. Так, ензим гіалуронідаза посилює проникність іонів кальцію та гліцину, особливо в ділянці каріозної плями; хімотрипсин і лужна фосфатаза знижують проникність фториду кальцію та лізину, кисла фосфатаза посилює проникність всіх іонів і речовин.
19.2.4. Роль вітамінів у регуляції процесів мінералізації тканин зуба. На метаболізм тканин зуба та процеси мінералізації значний вплив чинять вітаміни, зокрема А, С, К, Д, Е.
Вітамін А забезпечує ефективне протікання процесу мінералізації тканин зуба, оскільки активує синтез глікопротеїнів і протеогліканів, впливаючи на активність глікозилтрансфераз – ензимів, які переносять вуглеводні залишки від нуклеозидмоносахаридів (УДФ-глюкоза, УДФ-галактоза, УДФ-N-ацетилгалактозамін) на гідроксильні групи серину та треоніну під час синтезу олігосахаридних ланцюгів глікопротеїнів. Він забезпечує утворення активної форми сульфатів – фосфоаденозинфосфосульфату (ФАФС), який є джерелом сульфату для синтезу сульфатованих глікозаміногліканів – хондроїтин-4-сульфату та хондроїтин-6-сульфату, які беруть участь в процесі формування протеогліканових комплексів. Крім того, глікопротеїни та протеоглікани є основними структурними компонентами муцинів – білків слизових утворень, які вкривають епітеліальні тканини (в тому числі порожнини рота), забезпечуючи їх бар’єрну функцію.
При недостатності вітаміну А пригнічується активність одонтобластів та фібробластів; порушується кальцифікація емалі і дентину; затримується прорізування зубів у дітей, відбувається неправильне їх розміщення та розвиток.
Характерною ознакою гіповітамінозу А є сухість слизової оболонки рота, тріщини та ерозії в куточках губ. Як наслідок втрачаються бар’єрні, захисні функції слизової оболонки рота, зростає інфекційна ураженість.
Вітамін А широко використовують у стоматологічній практиці як засіб, що прискорює епітелізацію ерозій, нормалізує обмінні процеси в епітелії, відновлює слизовий покрив ротової порожнини.
Вітамін Сбере участь в окисно-відновних реакціях, активує окиснення глюкози в пентозофосфатному шляху, який характерний для пульпи зуба; бере участь у гідроксилюванні проліну та лізину під час синтезу колагену, тому гіповітаміноз С викликає гальмування утворення останнього (утворений колаген має меншу стабільність та міцність), порушує формування кристалів гідроксіапатиту, гальмує процеси мінералізації та посилює демінералізацію тканин зуба.
Крім того, зуби в лунках альвеолярного відростка фіксуються періодонтальною зв’язкою, яка утворена колагеновими волокнами. При скорбуті зниження біомеханічних властивостей цих зв’язок та інших навколозубних тканин призводить до розхитування та випадіння зубів.
Паралельно, внаслідок посилення проникності та ламкості капілярів розвиваються клінічні симптоми гіповітамінозу – множинні точкові крововиливи (петехії), розвиваються запальні процеси ясен. Прогресуючі зміни в тканинах порожнини рота при довготривалому гіповітамінозі викликають розвиток виразкового гінгівіту.
Вітамін D. Біологічно активною формою є вітамін D3 – 1,25- дигідроксихолекальциферол (кальцитріол), фізіологічна дія якого полягає в посиленні всмоктування іонів Са2+ в кишках шляхом стимуляції синтезу високоспецифічного Са2+-зв’язуючого та Са2+-транспортуючого білка. Отже, кальцитріол регулює процеси кальцифікації тканин зуба за механізмом, подібним до дії стероїдних гормонів.
Гіповітаміноз D у дітей в період формування тканин зуба зумовлює неповноцінну мінералізацію, гіпопластичні дефекти та карієс молочних зубів. На стан постійних зубів у дорослих вітамін D має незначний вплив, однак наслідки гіповітамінозу в дитячому віці проявляються у дорослих гіпоплазією емалі, порушенням процесів мінералізації тканин зуба, що сприяє розвитку карієсу.
Вітамін К бере безпосередню участь у процесах мінералізації тканин зуба. Первинними центрами зв’язування іонів Са2+ з білками (колагеном, протеогліканами, кальцій-зв’язуючим білком – кальпротеїном) є дві карбоксильні групи залишків γ-карбоксиглутамінової кислоти, яка утворюється шляхом карбоксилування глутамінової кислоти в γ-положенні під дією ензиму γ-глутамілкарбоксилази, коензимом якої виступає вітамін К.
Недостатність вітаміну К гальмує утворення γ-карбоксиглутамінової кислоти в молекулах калькпротеїну, а, отже, знижує його здатність зв’язувати іони Са2+ в точках нуклеації, що в цілому гальмує мінералізацію тканин зуба.
Вітамін Е. Біологічна дія вітаміну Е пов’язана з його антиоксидантними властивостями. Він інгібує вільнорадикальні реакції, пероксидне окиснення вищих ненасичених жирних кислот – структурних компонентів біологічних мембран і, тим самим, стабілізує структуру та забезпечує нормальне функціонування біологічних мембран клітин тканин зуба.
Недостатність вітаміну Е викликає депігментацію емалі, зменшує стійкість тканин зуба, підвищує проникність капілярів ясен.
Вітамін Е вводять внутрішньом’язево та в пародонтальні кишені під час лікування пародонтозу, а також у вигляді аплікацій при лікуванні ерозій і виразок слизової оболонки ротової порожнини.
19.2.5. Гормональна регуляція процесів мінералізації тканин зуба. Іони Са2+є інтегральними компонентами багатьох біоструктур та еволюційно прадавніми внутрішньоклітинними месенджерами, що беруть участь у багатьох метаболічних процесах та фізіологічних функціях, у тому числі мінералізації тканин зуба.
Гомеостаз кальцію визначається функціонуванням кількох анатомо-фізіологічних систем: кісткової, яка слугує резервуаром кальцію; нирок, уздовж канальців яких відбувається реабсорбція іонів кальцію та фосфатів і тонкої кишки, у верхніх відділах якої здійснюється всмоктування (абсорбція та реабсорбція) іонів кальцію і фосфатів, які споживаються у складі продуктів харчування або надходять у порожнину кишок шляхом вивільнення цих іонів у процесі метаболізму.
Своєю чергу, ефекторна функція кісток, кишок і нирок відносно гомеостазу кальцію є об’єктом гуморального контролю трьох фізіологічно активних сполук: паратгормону, кальцитріолу та кальцитоніну.
Паратгормон синтезується в головних і ацидофільних клітинах прищитоподібних залоз і має гіперкальціємічний ефект, водночас зменшуючи концентрацію фосфатів у крові. У тканині зуба паратгормон стимулює функціональну активність остеокластів, що призводить до резорбції як органічного матриксу, так і неорганічних структур із вивільненням кальцію в екстрацелюлярний простір і кров.
Кальцитріол (1,25-дигідроксихолекальциферол) – сполука гормонального типу дії, що утворюється з біологічного попередника, яким в організмі людини та вищих тварин є жиророзчинний вітамін D3 (холекальциферол). Біологічна функція кальцитріолу полягає в стимуляції всмоктування іонів Са2+ і фосфатів в кишці. Кальцитріол є єдиною природною фізіологічно активною сполукою, ефект якої полягає в транспортуванні Са2+ проти концентраційного градієнта, що існує на мембрані ентероцитів; тим самим кальцитріол підтримує фізіологічну концентрацію кальцію та фосфатів у плазмі крові, що забезпечує умови для нормальної побудови тканин зуба.
Кальцитонін синтезується в парафолікулярних С-клітинах щитоподібної залози. На відміну від паратгормону та кальцитріолу, кальцитонін є гормоном гіпокальціємійної дії, тобто зменшує концентрацію в плазмі крові іонів Са2+ та неорганічних фосфатів. Механізм дії кальцитоніну полягає в пригніченні функцій остеокластів та сповільненні їх утворення з клітин попередників. У результаті цих клітинних ефектів резорбція як органічної, так і неорганічної складової матриксу гальмується, що призводить до зменшення надходження в кров кальцію та фосфатів. Фізіологічним стимулятором секреції кальцитоніну є зростання концентрації Са2+ в плазмі крові.
Паротин – глікопротеїн, який виділяють привушні та піднижньощелепні слинні залози. Цей білок складається з α-, β-, γ-субодиниць, остання є активною по відношенню до мезенхімальних тканин – хрящів, трубчастих кісток і дентину зуба. Паротин посилює проліферацію хондрогенних клітин, стимулює синтез нуклеїнових кислот і, у тому числі, ДНК в одонтобластах, мінералізацію дентину та кісток; це супроводжується зниженням вмісту кальцію та глюкози в плазмі крові.
19.2.6. Поверхневі утвори на зубах. За фізіологічних умов на поверхні емалі утворюються кутикула та пелікула, тоді як зубний наліт і зубний камінь відіграють певну роль у розвитку стоматологічної патології.
Кутикула у вигляді тонкої оболонки вкриває поверхню емалі зубів після їх прорізування і стирається в процесі жування. Вона складається з двох шарів – первинного та вторинного. Первинний розташовується внутрішньо і являє собою тонкий (0,5 – 1,5 мкм) шар глікопротеїнів, а вторинний, зовнішній, - не що інше як редукований епітелій емалевого органа.
На відміну від кутикули впродовж усього життя на поверхні емалі знаходиться пелікула. Вона являє собою тонку органічну плівку завтовшки 1 – 4 мкм, щільно фіксовану на поверхні зуба. її утворення розпочинається з адсорбції специфічних білків слини на гідроксіапатитах емалі (з виникненням іонних зв’язків і гідрофобних взаємодій) через 20 – 30 хв після приймання їжі. В утворенні пелікули беруть участь білки, збагачені проліном, лактоферин, гістатини 1 і 5, цистатин SA ІІІ, лактопероксидаза, лізоцим, вуглеводи (аміноцукри та моносахариди).
Пелікула володіє вибірковою проникністю та забезпечує процеси дифузії іонів у поверхневий шар емалі, а також захищає емаль від впливу хімічних чинників, вона регулює процеси мінералізації та демінералізації емалі, здійснює контроль за складом мікробної флори, яка бере участь в утворенні зубного нальоту. Після механічного очищення пелікула відновлюється на поверхні емалі впродовж кількох годин.
Зубний наліт – структура, яка утворена скупченням різних видів мікроорганізмів, занурених у матрикс, утворений продуктами їх життєдіяльності, компонентами слини та неорганічними речовинами. Склад зубного нальоту непостійний і залежить від мікрофлори та метаболічних реакцій, які перебігають за участі цих мікроорганізмів. Так, в міру старіння нальоту починає переважати анаеробна флора, для якої характерна висока ензим на активність і утворення органічних кислот.
Зубний наліт на 78 – 80 % складається з води. У сухому залишку переважають мінеральні речовини, білки та вуглеводи. Вміст макро- та мікроелементів у зубному нальоті варіює. Кальцій (3,4 мкг/мг) і фосфор (8,4 мкг/мг) в основному поступають зі слини, присутні також натрій (1,3 мкг/мг) і калій (4,2 мкг/мг); висока концентрація фтору (6 – 180 мкг/г) та незначна – заліза, магнію, марганцю.
У ранньому нальоті виявляють триацилгліцероли, холестерин, гліцерофосфоліпіди, згодом ліпіди утворюють комплекси з вуглеводами. Білки становлять біля 8 % від сухої маси. Мікроорганізми здатні гідролізувати білки кислими та слаболужними протеїназами з вивільненням пептидів і амінокислот, котрі, своєю чергою, дезамінуються та декарбоксилуються. Тому у зрілому нальоті зростає концентрація глутамінової кислоти, яка утворюється шляхом трансамінування. З вільних амінокислот утворюються продукти гниття – сірководень, аміак, крезол, фенол, метилмеркаптан, індол, скатол тощо, які обумовлюють виникнення несвіжого дихання (галітоз). Вуглеводи (7 – 14 % сухого залишку) представлені фруктозою, глюкозою, гексозамінами, сіаловими кислотами, глікозаміногліканами та гомополісахаридами; висока активність глікозидаз, з допомогою яких глікопротеїни слини деглікозилюються з утворенням вільних вуглеводів, які використовуються мікроорганізмами для забезпечення енергетичних затрат. Сахароза, яка потрапляє в порожнину рота з їжею, перетворюється сахаразою мікроорганізмів зубного нальоту на фруктозу та глюкозу, з останньої утворюється піровиноградна кислота, яка в аеробних бактерій перетворюється на СО2 і Н2О, а в анаеробних – відновлюється до молочної кислоти. З пірувату також може утворюватися оцтова та мурашина кислоти. Лактатдегідрогеназа бактерій активується високими концентраціями фруктозо-1,6-дифосфату, тоді як утворення оцтової та мурашиної кислот інгібується великою кількістю гліцеральдегід-3-фосфату. при надмірному поступленні вуглеводів деякі бактерії зубного нальоту (особливо стрептококи) здатні синтезувати глікоген, механізм утворення та розпаду якого відбувається шляхом, аналогічним до такого у ссавців. Різниця полягає в тому, що мікроорганізми використовують не УДФ-глюкозу, а АДФ-глюкозу.
За участі бактеріальних глікозилтрансфераз утворюються липкі полісахариди (глікани), які адсорбуються на поверхні зуба і через гліканзв’язуючий білок об’єднують мікроорганізми. Глікани в зубному нальоті представлені леванами та декстранами (рис. 19.12).
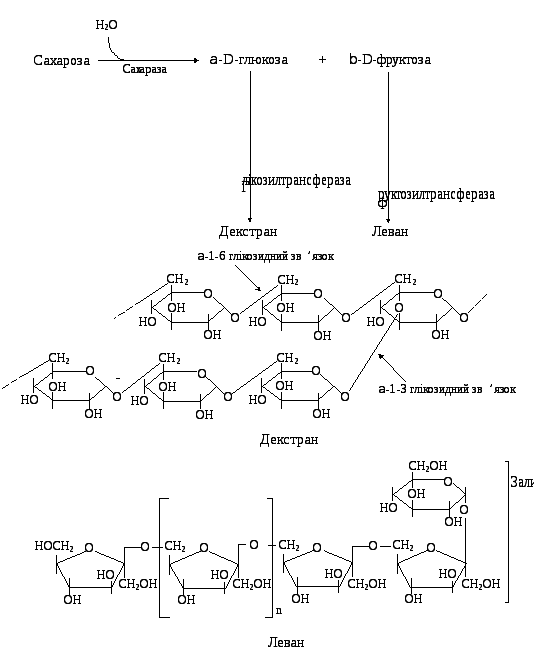
Рис. 19.12. Утворення липких полісахаридів у зубному нальоті
Леван – полісахарид, який складається з залишків фруктози, зв’язаних β (2→6)-глікозидними зв’язками та з’єднаних з молекулою сахарози. Декстран – розгалужений полісахарид, утворений залишками α-D-глюкози, зв’язаних α (1→6) і (1→3)-глікозидними зв’язками.
Липкі полісахариди адгезують бактерії на емалі. Контакт між ними та гідроксіапатитами забезпечується водневими зв’язками, іонами кальцію та білками адгезинами, до яких належить глікопротеїн з молекулярною масою 200 кДа, що синтезується стрептококами.
Зубний наліт характеризується високою метаболічною активністю, у ньому знаходиться понад 50 ензимів, серед яких фосфатази, нуклеази, ензими гліколізу, ЦТК, пероксидази тощо (рис. 19.13).
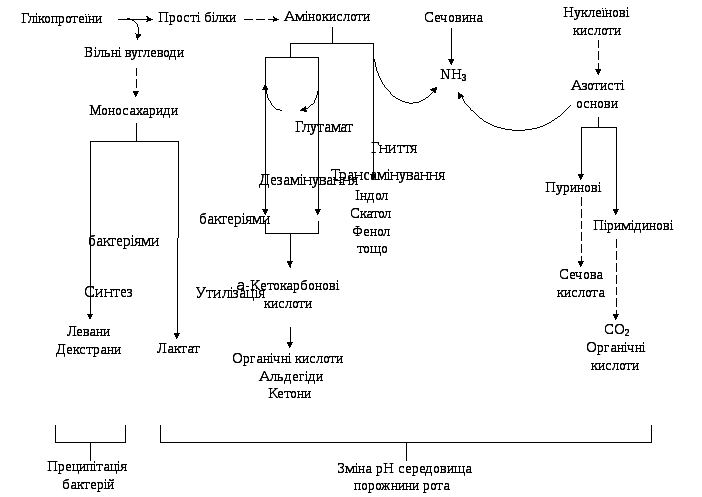
Рис. 19.13. Метаболічні процеси в зубному нальоті
Згодом кристали фосфату кальцію відкладаються всередині зубного нальоту і щільно зв’язуються з поверхнею емалі. Цей процес займає приблизно 12 діб і після мінералізації зубний наліт перетворюється на зубний камінь. Бактерії продовжують накопичуватися на поверхні, що сприяє росту зубного каменю. У залежності від розташування на поверхні зуба розрізняють над- і під’ясенний зубний камінь. Джерела надходження у них фосфорно-кальцієвих солей різні: у над’ясенний вони поступають зі слини, а в під’ясенний – з ясенної рідини.
70 – 90 % зубного каменя припадає на неорганічні речовини – кальцій, неорганічний фосфат, магній, у невеликій концентрації там знаходяться також свинець, молібден, кремній, алюміній, стронцій, кадмій, фтор тощо. Кальцій і фосфор осідають на органічному матриксі у вигляді солей: на початковій стадії здебільшого утворюється слабомінералізований брушит (СаНРО42Н2О), який легко видаляється механічно. Крім брушиту утворюються й інші види кристалів:
вітлокіт, у структурі якого присутні безводний фосфат кальцію (Са3РО4)2 та іони магнію, марганцю та заліза;
монетит – вторинна сіль фосфорної кислоти (СаНРО4), розчинність якого швидко зростає при при кислих значеннях рН;
октакальцій фосфат Са8(НРО4)2(РО4)45Н2О. який слугує проміжною зв’язуючою ланкою між монетитом і брушитом та гідроксіапатитом, а також відіграє важливу роль у нуклеації солей. Подібно до брушиту та монетиту при лужних значеннях рН він перетворюється на гідроксіапатит.
До складу зубного каменя фтор входить у вигляді фторапатиту та фториду кальцію, а також комплексу з органічними сполуками в складі бактерій. Застосування фтормісних зубних паст в перші 10 діб утворення каменя призводить до накопичення фтору в складі цього утвору.
Неорганічні речовини зубного каменя зв’язуються з білками, кількість останніх коливається в межах 0,1 – 2,5 % і залежить від виду каменя. Вільні амінокислоти представлені здебільшого аланіном, лейцином, гліцином, глутаміновою та аспарагіновою кислотами, а також проліном, лізином, серином і треоніном. Глутамат і аспартат можуть зв’язувати іони кальцію, а залишки серину, треоніну та лізину – НРО43-, що є дуже важливим для ініціації мінералізації зубного нальоту та подальшого утворення зубного каменя.
Вуглеводи (10 %) представлені в зубному камені здебільшого глікозаміногліканами, глюкозою, фруктозою, занозою та аміноцукрами. Вміст ліпідів незначний – наявні в зубному камені гліцерофосфоліпіди, які вивільняються з клітинних мембран мікроорганізмів під час їх розпаду, зв’язують іони кальцію та ініціюють утворення фосфорно-кальцієвих солей. А в подальшому – гідроксіапатитів. В утворенні зубного каменя беруть участь також молекули АТФ, які необхідні для фосфорилування органічних сполук, вони також вивільняють ортофосфорну кислоту, яка є компонентом різних мінеральних кристалів.
Для формування зубного каменя необхідні:
утворення органічного матриксу, яким слугує зубний наліт;
відкладання мінеральних сполук на органічному матриксі з утворенням центрів кристалізації;
ріст кристалів у центрах мінералізації.
Первинний шар бактерій , які фіксуються на поверхні зуба, здебільшого представлений Str.sanguis, а на поверхні слизової оболонки ясен - Str.salivarium. Згодом на них нашаровуються інші бактерії з утворенням мікробних асоціацій. У міру збільшення анаеробної флори вивільняється велика кількість молочної кислоти, котра поглинається та метаболізується вайлонеллами. На цих ділянках відбувається підвищення рН. Цьому також сприяє зменшення кількості молекул СО2 та накопичення в зубному нальоті аміаку. Останній утворюється з сечовини за участі уреолітичних бактерій та з гідролізованого мікоплазмами аргініну. У реакціях трансамінування α-кетокислоти перетворюються на аспартат і глутамат і разом з аміаком активно приєднують іони РО43-, Mg2+, Ca2+, що сприяє формуванню центрів кристалізації. Відкладанню фосфатів також сприяє зміна міцелярної структури слини, коли фосфат кальцію випадає в осад. Це стає можливим при зміні кількості специфічних білків слини та пірофосфату; останній разом із статзеринами інгібує утворення зубного каменя. Утворений таким чином первинний преципітат, який складається переважно з брушситу, трансформується в пластинчастий гідроксіапатит, а згодом у гексагональний гідроксіапатит. Накопичення фосфорно-кальцієвих солей відбувається за участі лужної фосфатази та молекул АТФ.
19.2.7. Біохімічні зміни в тканинах зуба при карієсі. Одним з самих поширених захворювань зубів є карієс (сaries dentis). В основі цієї патології лежить прогресуюча демінералізація твердих тканин зубів під впливом органічних кислот, які утворюються внаслідок ензимної діяльності мікроорганізмів, з подальшим виникненням дефекту в вигляді порожнини. Карієс належить до незворотних процесів, зруйновані емаль і дентин не відновлюються. В економічно розвинених країнах ураженість населення карієсом становить 95 – 98 %.
Всі етіологічні чинники, які призводять до виникнення карієсу, поділяють на загальні та місцеві. До загальних належать неповноцінна дієта та питна вода; соматичні захворювання, зсув у функціональному стані органів і систем у період формування та дозрівання тканин зуба; екстремальні впливи на організм; спадковість. Місцеві чинники включають наявність зубної бляшки та зубного нальоту, порушення складу та властивостей ротової рідини, вуглеводні харчові залишки в порожнині рота, резистентність тканин зуба та відхилення в їх біохімічному складі, а також стан пульпи та зубо-щелепної системи в цілому в період закладки, розвитку та прорізування зубів.
Проте, навіть у регіонах із високою розповсюдженістю карієсу зустрічаються люди, у яких це захворювання відсутнє – їх називають карієсрезистентними і навпаки, людей, у котрих інтенсивність ураження зубів карієсом перевищує середньогруповий рівень, називають сприйнятливими до карієсу.
Карієсрезистентності сприяє заміщення гідроксіапатиту на фторапатити – міцніші, кислотостійкіші та слаборозчинні сполуки; підвищений вміст у поверхневому шарі емалі цинку, заліза, вольфраму; молібдену та ванадію, вітаміни D, С, А тощо, концентрація цитрату; тоді як селен, навпаки, знижує її.
Провідним чинником у розвитку карієсу, згідно сучасних поглядів, є посилене утворення органічних кислот та зниження рН в ротовій рідині, що призводить до прогресуючої демінералізації тканин зуба. Органічні кислоти утворюються внаслідок ензимного розщеплення вуглеводів під дією мікрофлори порожнини рота. Продуктами анаеробного бродіння є органічні кислоти: молочна, піровиноградна, мурашина, масляна, пропіонова тощо (рис. 19.14). Результати експериментальних досліджень показали, що протеолітичні ензими також спроможні руйнувати органічну фракцію емалі з подальшим вивільненням фосфатів. Разом із тим вважають, що роль протеїназ зубного нальоту важливіша у патогенезі виникнення гінгівіту та пародонтиту, коли активність кислих і слаболужних протеїназ зростає в 4 – 5 разів, що супроводжується деградацією глікопротеїнів і інших білків тканин пародонта.

Рис. 19.14. Участь органічних кислот у демінералізації емалі зуба
Механізм декальцифікації апатитів під дією органічних кислот полягає в витісненні Са2+ протонами водню, концентрація яких різко зростає при закисленні середовища, з гідроксіапатиту. Реакція має наступний вигляд:
Са10 (РО4)6(ОН)2 + 2 Н+ → Са9Н2 (РО4)6(ОН)2 + Са2+
Процес демінералізації емалі супроводжується зміною форми, розміру та просторової організації кристалів гідроксіапатиту. до певного моменту втрата іонів Са2+ не супроводжується руйнуванням його кристалічної решітки, але з часом разом з іонами Са2+ втрачаються фосфати і тоді кристалогідрати руйнуються.
Вивільнений Са2+ використовується для нейтралізації кислих продуктів ротової рідини. Але при цьому співвідношення Са/Р знижується, а процеси демінералізації переважають над процесами мінералізації.
Одним із профілактичних заходів виникнення карієсу є виключення сахарози з харчового раціону. З цією метою виготовляють велику кількість різноманітних замінників цукру (сорбітол, ксилітол, сахарин тощо).
Сорбітол – шестиатомний цукроспирт, який у невеликій кількості міститься у фруктах і синтезується в печінці. У слині відсутня сорбітолдегідрогеназа, тому сорбітом не метаболізується в порожнині рота, а його використання не викликає значного зниження рН у зубному нальоті. У кишках сорбітом всмоктується частково шляхом пасивної дифузії.
Ксилітол – п’ятитомний цукроспирт. Міститься в овочах, фруктах, його отримують також із кори дерев. За солодкістю близький до сахарози. Ксилітол підлягає незначному перетворенню бактеріями зубного нальоту. Потрапляючи в мікробну клітину, ксилітол фосфорилується і інгібує транспорт глюкози та фруктози, а нерегульоване накопичення ксилітол-5-фосфату в бактеріальній клітині супроводжується осмотичним надходженням води з подальшим лізисом мікроорганізму. Але, як і сорбітол, ксилітол викликає осмотичну діарею.
З плодів дикорослих африканських рослин виділені надзвичайно солодкі на смак білки – міракулін, монелін, тауматин, їх використовують для виготовлення жувальних гумок і зубних паст. Достатньо часто в якості підсолоджувала використовують сахарин – амід ортосульфобензойної кислоти, але в дослідах на щурах було доведено, що він є слабим канцерогеном і викликає рак сечового міхура.
у лікуванні карієсу широко використовують гліцерофосфат та глюконат кальцію як засоби ремінералізуючої терапії, а також фторування як спосіб посилення стійкості (резистентності) емалі.
