
- •Розділ 19. Функціональна біохімія порожнин рота
- •19.1. Біохімія слини людини
- •19.1.3. Фізико-хімічні властивості слини та їх порушення.
- •19.2. Біохімічні особливості тканин зуба
- •19.2.8. Значення фтору для виникнення карієсу та флюорозу. Фтор – біогенний хімічний елемент, тобто постійна складова частина організму людини.
19.1.3. Фізико-хімічні властивості слини та їх порушення.
19.1.3.1. Кількісні показники секреції слини. За добу у здорової дорослої людини виділяється 1,5 – 2,0 л слини. Швидкість її секреції нерівномірна. Так, під час сну вона становить 0,05 мл/хв, у період бадьорості поза прийомом їжі 0,03 - 0,5 мл/хв, після стимулювання - 2,0 – 2,5 мл/хв і більше.
Об’єм і швидкість секреції слини залежать від багатьох чинників, у тому числі, від віку: у новонароджених дітей виділяється мало слини, що обумовлює деяку сухість слизової оболонки ротової порожнини в перші місяці життя; із прорізуванням молочних зубів (5 – 6 міс) секреція слини значно зростає аж до фізіологічної слинотечі. У період статевого дозрівання (після 12 – 14 років) секреторні процеси в слинних залозах перебігають особливо інтенсивно, що зумовлено гормональною перебудовою організму. Вікова перебудова розпочинається після 60 років і секреція слини поступово зменшується Так, молоді люди впродовж 15 – 20 хвилин спльовують 20 – 30 мл слини, а люди похилого віку 2 – 10 мл. Це пояснюється тим, що нестимульована слина («слина спокою») на 66 % складається з секрету підщелепних і під'язикових залоз, а з віком об’єм паренхіматозних елементів саме цих залоз зменшується (частина залозистих клітин перестає виділяти білковий секрет і починає виділяти секрет, збагачений кислими та нейтральними глікозаміногліканами.). Крім того, у людей похилого віку значно знижується секреторна активність малих слинних залоз. Секреторна ж активність привушних залоз не залежить від віку, тому при стимуляції, наприклад, під час жування, виділяється достатня кількість слини.
Розрізняють два типи порушення слиновиділення, які супроводжують низку гострих і хронічних захворювань – гіпер- та гіпосалівацію. Гіперсалівація – збільшення секреції слини слинними залозами – не впливає на стан слизової оболонки рота. Її спостерігають в період адаптації до знімних пластмасових протезів, при гострих запальних процесах слизової оболонки рота, подразненні клітин слинних залоз ртуттю та йодом, при деяких органічних ураженнях вегетативних центрів, епілепсії та паркінсонізмі, енцефаліті та менінгіті. При ящурі, наприклад, виділення слини збільшується до 7 – 8 л на добу, що слугує одним із найважливіших діагностичних критеріїв. Наслідки гіперсалівації залежать від її ступеня її вираженості та тривалості і проявляються утрудненням ковтання та мови, розвитком ангулярного хейліту. Надмірне слиновиділення створює значні труднощі стоматологам при роботі з такими пацієнтами.
Гіпосалівація – зменшення секреції слини слинними залозами – один із симптомів розладів нервової системи (істерія, неврастенія), медикаментозного впливу (атропін), гіповітамінозів А і В, лихоманки (малярія, тиф, пневмонія), ендокринних порушень (діабет, клімакс, тиреотоксикоз), у хворих на рак після великих доз опромінення, у хворих із синдромом Сьєгрена (автоімунне захворювання, для якого характерні ксеростомія та ксерофтальмія). Тривала гіпосалівація, своєю чергою, призводить до порушення процесу травлення, а також сприяє розвитку карієсу зубів.
Об’єм і швидкість слиновиділення залежать від вигляду та якості їжі і змінюються в залежності від характеру подразника. При потраплянні в порожнину рота твердої, густої їжі виділяється рідка слина, вологої та рідкої – слина, збагачена муцином. У табл. 19.1 приведені дані слиновиділення з привушних залоз при введенні в порожнину рота різних речовин.
Таблиця 19.1. Слиновиділення з привушних залоз (впродовж 5 хв) у дорослої людини
під час їжі або введенні в порожнину рота різних речовин (Бірюков А.Д.)
|
Найменування речовин
|
Кількість слини, мл (мол)
|
|
Хліб
|
5,0
|
|
Сухарі
|
4,0
|
|
Молоко
|
2,6
|
|
5% розчин лимонної кислоти
|
6,4
|
|
0,2% розчин хлоридної кислоти
|
6,0
|
|
35% розчин спирту
|
4,0
|
|
2% розчин кухонної солі
|
2,8
|
|
Хінін
|
3,8
|
|
Перець у порошку
|
8,4
|
Часте вживання солодощів призводить до пригнічення функціональної активності слинних залоз, тоді як раціональна дієта, інтенсивне пережовування їжі, споживання кислої, пряної їжі підсилюють виділення слини.
Секреторну функцію слинних залоз оцінюють методом сіалометрії. спочатку впродовж 6 хв збирають нестимульовану слину, а потім вимірюють кількість слини після парасимпатичної стимуляції. У якості стимулятора часто використовують 1% розчин пілокарпіну. Для кількісної оцінки секреції малих слинних залоз використовують смужки фільтрувального паперу, що прикладають до досліджуваної ділянки і визначають їх масу до і після дослідження.
Оптимальний час збору слини - з 10 години ранку до 12 годин дня, тому що в цей часовий інтервал відзначається максимальна секреція і найбільша стабільність хімічного складу слини.
19.1.3.2. Густина, в’язкість та рН слини. Густина змішаної слини коливається в межах 1,001 – 1,017 г/мл, а в’язкість становить 1,2 – 1,4 і залежить від кількості муцину.
Буферні властивості слини визначаються бікарбонатною та фосфатною системами, а також білками. Разом вони формують першу лінію захисту проти кислих або лужних впливів на тканини порожнини рота. Всі буферні системи мають різні межі ємності: фосфатна найактивніша при рН 6,8 – 7,0, гідрокарбонатна – при рН 6,1 – 6,3, а білкова забезпечує буферну ємність при різних значеннях рН. Буферна ємність слини, тобто здатність нейтралізовувати кислоти та луги, розглядається як захисний механізм при дії, насамперед, кислих продуктів на зуби. Буферна ємність нестимульованої слини становить 4,45 – 4,65 ммоль/л НСl, а стимульованої - 5,09 – 5,29 ммоль/л НСl.
Роль концентрації протонів водню (рН) у ротовій порожнині вивчена достатньо добре, з нею пов’язана теорія Міллера про виникнення карієсу. Чисельними дослідженнями встановлено, що рН слини в порожнині рота за умов норми знаходиться в межах 6,4 – 7,3 (за іншими даними 6,4 – 7,8). Концентрація водневих іонів у порожнині рота впливає на активність ензимів слини, процеси мінералізації та ремінералізації емалі, мікроциркуляцію, активність мікрофлори, специфічну і неспецифічну резистентність тканин порожнини рота.
Їжа впливає на рн у порожнині рота прямо й опосередковано. Прямий вплив зв'язаний з наявністю в харчових продуктах органічних і неорганічних кислот, лужних компонентів, а непрямий – із стимулюванням слиновиділення й активуванням ензимної активності мікрофлори порожнини рота.
Приймання кислотовмісних, здебільшого вуглеводних харчових продуктів (цукор, хліб, фрукти, соки тощо) викликає швидке зрушення рн у порожнині рота (до 5,0 і нижче). Ацидоз у нормі короткочасний, тому що відбувається проковтування їжі, самоочищення порожнини рота слиною, адсорбція вуглеводів зубним нальотом. Постійне вживання великої кількості вуглеводів, затримка їжі в порожнині рота, головним чином у міжзубних проміжках, можуть призвести до значних зрушень рн у кислий бік, а згодом і до карієсу. Цукрозамінники (ксиліт, сорбітол, пластилін) мають низьку ацидогенність.
Білкова їжа містить у своєму складі речовини (сечовина, нітрати, нітрити, глутамін тощо), які при дисоціації в ротовій рідині утворять іони, головним чином NН4+, здатні зв'язувати Н+. При цьому відбувається незначне зрушення рН у лужний бік, що не перевищує 8,0. наслідком алкалозу в ротовій рідині є мінералізація зубного нальоту й утворення зубного каменя. Процес каменеутворення перешкоджає розвитку карієсу і рідко супроводжується збільшенням числа каріозних порожнин і плям.
У змішаній слині, ясенній рідині та, найбільшою мірою, зубному нальоті існує велика кількість мікроорганізмів, деякі з них у процесі своєї життєдіяльності утворюють уреазу, яка гідролізує сечовину з утворенням аміаку. Інші, що містять гліколітичні ензими (стрептококи, лактобактерії, дріжджоподібні гриби роду Candida тощо), розщеплюють вуглеводи до органічних кислот. Це супроводжується зсувом рн у кислий бік. Буферні системи зубного нальоту, найсильнішою з яких є фосфатна, не здатні цілком нейтралізувати кислоти внаслідок низьких дифузійних властивостей зубного нальоту. Проте в присутності фтору сповільнюється утворення кислот бактеріями.
Функціональна активність слинних залоз теж значною мірою впливає на кислотно-основний стан ротової порожнини. після стимуляції слиновиділення концентрація іонів Н+ у слині дещо зменшується, оскільки відбувається вимивання іонів Н+ із зон, де вони посилено утворюються. Вирівнюванню рн сприяють також буферні системи крові.
21.1.4. Біохімічний склад слини та його зміни при різних патологічних станах. Секрет всіх слинних залоз людини на 97 – 99 % складається з води, решту (1 – 3 %) становить сухий залишок, який містить органічні та неорганічні речовини, вміст яких у слині в нормі залежить від віку, характеру їжі, швидкості секреції й істотно змінюється при патології.
Органічні речовинистановлять ⅔ усього сухого залишку слини і представлені, в основному, молекулами великих розмірів – простими та складними білками, ліпідами, вуглеводами, а також азотовмісними речовинами небілкової природи, вітамінами, гормонами (табл.19.2).
Таблиця 19.2. Вміст органічних речовин у слині
|
Компоненти |
Концентрація |
Компоненти |
Концентрація |
|
Загальний білок |
2,0 – 5, 0 г/л |
Креатинін |
2,0 – 10,0 ммоль/л |
|
Фракції білків, % |
|
Сечовина |
200,0 мг/л |
|
Альбуміни |
7,0 – 8,0 |
Сечова кислота |
0,005- 0,03 г/л |
|
-Глобуліни |
11,0 – 12,0 |
Залишковий азот |
100,0 - 200,0 мг/л |
|
β-Глобуліни |
45,0 |
Глюкоза |
0,06 –0,17 ммоль/л |
|
γ-Глобуліни |
18,0 |
Гексозаміни |
100,0 мг/л |
|
Муцин |
2,0 – 3, 0 г/л |
Фукоза |
90,0 мг/л |
|
Лізоцим |
0,15 – 0,25 г/л |
Нейрамінова кислота |
12,0 мг/л |
|
Амілаза |
380,0 мг/л |
Загальні гексози |
195,0 мг/л |
|
Імуноглобулін А |
190,0 мг/л |
Піровиноградна кислота |
9,0 мг/л |
|
Імуноглобулін G |
14,0 мг/л |
Молочна кислота |
33,0 мг/л |
|
Імуноглобулін М |
2,0 мг/л |
Холестерол |
80,0 мг/л |
Основними органічними компонентами слини є білки.Вони синтезуються як у секреторних клітинах (муцин, фактор росту епітелію, лактоферин), так і в протоках слинних залозах (лізоцим), а також мають сироваткове походження (альбуміни, β-ліпопротеїни, імуноглобуліни класу G і М). Білки виконують травну, захисну, буферну та регулівну роль і існують у слині в вигляді класів, кожен з яких володіє генетичним поліморфізмом.
У кількісному відношенні переважають глікопротеїни, серед яких більша частина припадає на муцин. Муцин – це сума глікопротеїнів слизової природи, більшість яких секретується піднижньощелепними, підязиковими та малими слинними залозами. Цей білок виконує в слині низку функцій, а саме: «огортає» слизову оболонку порожнини рота і зуби, захищаючи їх від ушкодження; інгібує дифузію іонів у тверді тканини зубів; зв'язує іони кальцію, забезпечує в'язкість слини, підтримує буферні властивості ротової рідини.
Ізоелектрична точкак муцину знаходиться у сильно кислому середовищі, він осаджується при рн 3,0 – 3,5. Виявлено дві ізоформи цього білка, які різняться за молекулярною масою: муцин-1 ((М-1) – 250 000 Да, муцин-2 (М-2) – 1 000 000 Да, відсотковий вміст білкового та вуглеводного компонентів коливається в різних межах. У складі білкової частини вивчених глікопротеїнів слини переважають амінокислоти серин, треонін, гліцин, пролін. Вуглеводний компонент включає N-ацетилнейрамінову, сіалові кислоти, N-ацетилгалактозамін, галактозу, фукозу, маннозу. Олігосахариди, зв’язані з муцином, володіють антигенною специфічністю, яка відповідає групоспецифічним антигенам, які присутні також у вигляді сфінголіпідів і глікопротеїнів на поверхні еритроцитів і у вигляді олігосахаридів у молоці та сечі. Концентрація групоспецифічних речовин у слині дорівнює 10 – 130 мг/л і достовірно відповідає групі крові; дослідження слинних групоспецифічних речовин використовують у судовій медицині для встановлення групи крові в тих випадках, коли зробити це в інший спосіб неможливо.
У слині людини знаходиться низка білків, які беруть участь у формуванні пелікули зуба, стабілізації гідроксіапатиту і відіграють суттєву роль у протикарієсному захисті слини. До таких білків належать: кислі білки, збагачені проліном, що становлять 25 – 30 % від усіх білків слини; статзерин - білок з 43 амінокислотних залишків, що має великий негативний заряд; цистатини - клас фосфопротеїнів, збагачених цистеїном; гістатини – клас білків, збагачених гістидином тощо.
Збагачені проліном білки (молекулярна маса 6 000 – 12 000 Да) поділяють на три групи – кислі, лужні та глікозильовані. Вони адсорбуються на поверхні емалі і є компонентами набутої пелікули зуба. Кислі білки зв’язуються з статзерином і запобігають його взаємодії з гідроксіапатитом при кислих значеннях рН, а, отже, у такий спосіб перешкоджають демінералізації емалі та інгібують надлишкове осідання мінералів на ній; вони зв’язують певні види мікроорганізмів і беруть участь в утворенні мікробних колоній у зубному нальоті. Глікозильовані білки беруть участь у змочуванні харчової грудки, а лужні – зв’язують таніни їжі захищаючи слизову оболонку рота від їх ушкоджувальної дії, а також надають слині в’язко-еластичних властивостей.
Цистатини – клас кислих білків з молекулярною масою 9 500 – 14 000 Да, які синтезуються в привушних і піднижньощелепних слинних залозах. Всього виявлено 8 слинних цистатинів, з них 6 охарактеризовано (цистатин-S, HSP-12, SA, SN, SAI, SAIII), їх роль полягає в інгібуванні активності трипсиноподібних протеїназ - катепсинів B, H, L, G, в активному центрі яких знаходиться цистеїн, що обумовлює антимікробну та антивірусну функції, також вони захищають білки слини від ензимного розщеплення. Цистатини SА та SAIII беруть участь в утворенні пелікули зуба, їх адгезивні властивості пов’язані з подібністю амінокислотної послідовності цих білків до фібронектину та ламінілу.
Сімейство гістатинів представлено в слині 12 пептидами з різною молекулярною масою. Основними представниками гістатинів є гістатин-1 (38 амінокислотних залишків); гістатин-3 (32 амінокислотних залишки) і гістатин-5, що є N-кінцевим фрагментом гістатину-3 (24 амінокислотних залишки). Вони виступають потужними інгібіторами росту Candida albicans та Str.mutans,), гістатин-1 бере участь в утворенні пелікули зуба та слугує потужним інгібітором росту кристалів гідроксіапатитів у слині.
Статзерини – фосфопротеїни з молекулярною масою 5 380 Да. Разом із іншими білками вони інгібують спонтанну преципітацію фосфорно-кальцієвих солей на поверхні зуба, у ротовій порожнині та слинних залозах, пригнічують ріст аеробних і анаеробних бактерій.
Лактоферин — залізозв’язуючий білок з молекулярною масою 80 кда. Він утворюється в ацинарних клітинах слинних залоз, а також із нейтрофільних лейкоцитів. Цей білок володіє бактеріостатичною дією за рахунок здатності конкурентно з мікроорганізмами зв'язувати іони заліза. Однак, у літературних джерелах зазначається, що N-кінцевий фрагмент лактоферину, який містить 11 амінокислотних залишків, має виражену бактерицидну активність за рахунок здатності формувати пори в мембрані мікроорганізмів, після чого розвивається їх осмотичне ушкодження.
лептин – білок з молекулярною масою 16 000 Да, який бере участь у процесах регенерації слизової оболонки. Взаємодіючи з рецепторами кератиноцитів, викликає експресію факторів росту кератиноцитів і епітелію. Які шляхом фосфорилування сигнальних білків сприяють диференціюванню кератиноцитів.
Глікопротеїн 340 – білок, збагачений цистеїном, з молекулярною масою 340 000 Да; належить до антивірусних білків. Будучи аглютиніном він, за присутності іонів кальцію, зв’язується з аденовірусами та вірусами, які викликають гепатит, ВІЛ-інфекцію; захищає білки слини від протеолізу шляхом інгібування активності еластаза лейкоцитів.
α- і β-дефензини – низькомолекулярні пептиди з молекулярною масою 3 000 – 5 000 Да, які мають β-структуру та велику кількість цистеїну. Джерелом α-дефензинів є лейкоцити, а β-дефензинів – кератиноцити та слинні залози. Дефензини чинять вплив на грампозитивні- та грамнегативні бактерії та гриби, вони формують іонні канали в залежності від типу клітин. А також агрегують з пептидами мембран і в такий спосіб забезпечують транспорт іонів через мембрани. У бактеріальних клітинах вони пригнічують синтез білка.
На противагу дефензинам, інші пептиди – кателідини мають структуру α-спіралі і не містять цистеїну. Зв’язуючись з ліпополісахаридами та двовалентними катіонами бактеріальних клітин, вони вмонтовуються в їх мембрану, формуючи іонні канали та пори, що згодом викликає загибель мікроорганізмів. Потужною антимікробною дією володіє калькпротеїн – пептид, який потрапляє в слину з епітеліоцитів і нейтрофільних гранулоцитів.
у слині виявлена низка специфічних білків. До них належать салівопротеїн, який регулює фосфорно-кальцієвий обмін, індукує відкладання фосфорно-кальцієвих сполук на зубах та кальційзв’язуючий білок – фосфопротеїн, який має високу спорідненість до гідроксіапатиту, бере участь в утворенні зубного нальоту та зубного каменя. Тканинний активатор плазміногену завдяки своїй участі в процесі фібринолізу, забезпечує місцевий гомеостаз, поліпшує процеси регенерації ушкодженої слизової оболонки рота.
Зростання вмісту білка в змішаній слині спостерігають при запальних процесах слинних залоз і органів порожнини рота і зв'язано це, головним чином, з посиленням проникності судин. При цьому в слині зростає вміст альбумінів, β- і γ-глобулінів, а також інших білків, наприклад, лактоферину, продуктів розпаду фібриногену, ензимів тощо. Так, при сіалозах збільшення білка в слині відбувається, здебільшого, за рахунок альбумінів, при хворобі Шегрена в слині виявляють підвищений вміст сіркомукоїдних білків, β2-макроглобуліну. Збільшення концентрації ТАП у змішаній слині характерно, зокрема, для паротиту, червоного плоского лишаю слизової оболонки порожнини рота. Патогенетичне значення збільшення ТАП у слині може виявлятися в тому, що з плазміногену утворюється значно більше плазміну, який розщеплює не тільки фібрин, але й секреторний компонент sIgА і, тим самим, знижує місцеву резистентність.
Ротова рідина володіє вираженими бактерицидними властивостями за рахунок наявності в ній речовин білкової природи – імуноглобулінів, ензимів, лейкоцитарних факторів. Основним класом імуноглобулінів, що надходять у ротову порожнину, є igА. Впродовж доби у слинних залозах секретується 50 - 250 мг igА, що становить 5 – 10 % від загальної кількості імуноглобуліну цього класу всього організму. У слині знаходиться як секреторний igА (sIgА, складається з 2-х молекул igА, з'єднаних із секреторним компонентом (SС)), так і вільні SС фрагменти та вільні субодиниці IgА – вони синтезуються місцево, або проникають у слину з крові. Значно менший вміст у слині Ig G і ще менше Ig М. Співвідношення IgА: Ig G : IgМ у слині становить приблизно 20:3:1. Імуноглобулін М нерідко зовсім не виявляється в ротовій рідині. Найбільша концентрація IgА відзначається в секреті привушних слинних залоз, у слині під’язикових і підщелепних залоз його концентрація в 2 рази менша.
Вміст імуноглобулінів у слині залежить від віку та статі. Плазмоцити, що містять IgА з'являються в травному каналі через місяць після народження, а sIgА виявляють у слині через 2 місяці, причому трохи раніше в слині з'являється секреторний компонент, а пізніше повна молекула sIgА. Прорізування зубів (6 місяців) супроводжується різким підвищенням sIgА у слині, що обумовлено значним збільшенням мікрофлори порожнини рота. У віковий період від 1 - 2 до 11 - 12 років вміст IgG і IgА у слині дітей збільшується в кілька разів і продовжує повільно зростати. У жінок секреція IgА вища, ніж у чоловіків.
Основним джерелом IgА у ротовій порожнині є плазматичні клітини великих слинних залоз. Ці клітини утворюються з В-лімфоцитів, що фіксуються в тканині слинних залоз на ранній стадії клонального диференціювання. Вони синтезують димери IgА, які проникають через базальну мембрану і латеральні міжклітинні канали епітелію в просвіт протоків слинних залоз. Секреторний компонент IgА, який утворюється в ацинарних клітинах слинних залоз теж потрапляє в просвіт протоків. У латеральних міжклітинних канальцях протокового епітелію та на поверхні самих епітеліальних клітин IgА з'єднується із секреторним компонентом нековалентними і дисульфідними зв'язками. Кількість IgА у слині є чинником, що визначає можливість виникнення і характер перебігу патологічних процесів.
Крім імуноглобулінів у слині знаходяться в невеликій кількості компоненти системи комплементу: фактор В, СЗ, С4; вони проникають з кровотоку через зубоепітеліальне прикріплення.
Частина білків слини представлена ензимами. У ротовій порожнині їх налічують понад 60, а за походженням поділяють на три основні групи: секретовані паренхімою слинних залоз, утворені в процесі життєдіяльності бактерій і утворені в процесі розпаду лейкоцитів у порожнині рота.
Серед ензимів слини, першою чергою, слід виділити глікозидази, до яких належить альфа-амілаза. Майже 70 % цього ензиму продукують привушні слинні залози, впродовж доби утворюється близько 0,6 г амілази. У немовлят вміст -амілази в слині незначний, до кінця першого року життя досягає рівня дорослих. рН оптимум дії цього ензиму коливається в межах 6,7 – 7,4, температурний оптимум становить 37 – 40° С, повна денатурація настає при 60° С. Амілаза чутлива до кислого середовища - при зниженні рН інгібується, хоча може зберігати високу активність у лужному середовищі (до рН =9,0) Ізоферменти-амілази представлені 11 білками, котрі об’єднують у сімейства А і Б. Молекулярна маса досягає 58 000 Да. Особливостями просторової структури є те, що її молекула складається з двох поліпептидних ланцюгів (субодиниць), кожен з цих ланцюгів містить іон кальцію, який стабілізує структуру активного центра, при м’якому видаленні кальцію методом діалізу ензим повністю втрачає свою активність. Крім того, молекула амілази містить один іон цинку. Амілаза гідролізує1 – 4 глікозидні зв’язки у молекулах полісахаридів і глікогену, але оскільки їжа в ротовій порожнині довго не затримується, то з крохмалю та глікогену тут утворюються переважно декстрини.
збільшення вмісту -амілази в змішаній слині спостерігають при пародонтозі, гальванізмі, дріжджовому стоматиті, цукровому діабеті, виразковій хворобі шлунка та дванадцятипалої кишки, хронічному панкреатиті. Зменшення амілолітичної активності слини відбувається при карієсі, в осіб зі значним дефіцитом зубного ряду, у хворих на пелагру, при аліментарній дистрофії, у післяопераційний період. Окрім -амілази в змішаній слині відзначають активність ще кількох глікозидаз – α-L-фукозидази, α- і β-глюкозидаз, α- і β-галактозидаз, α-D-манозидази, β-глюкуронідази, β-N-ацетилгексозамінідази, нейрамінідази. α-L-фукозидаза синтезується привушними слинними залозами і гідролізує α-(1→2) глікозидні зв’язки в коротких олігосахаридних ланцюгах. α- і β-глюкозидази, α- і β-галактозидази, нейрамідиназа мають бактеріальне походження, вони найактивніші в кислому середовищі, де можуть гідролізу вати глікозидні ланцюги слинних муцинів з вивільненням сіалових кислот і аміноцукрів.
л
Рис. 19.3. Фрагмент
муреїну, який знаходиться в мембрані
грампозитивних бактерій: стрілкою
вказане місце дії лізоциму
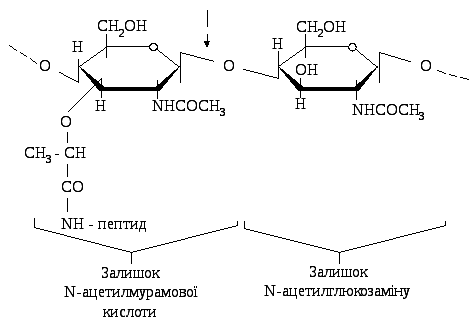
Ензим дістав свою назву через здатність гідролізувати глікозидні зв'язки між N-ацетилглікозаміном і N- ацетилмурамовою кислотою в глікопептидах клітинної оболонки мікроорганізмів (рис. 19.3).
Ц
Рис.
19.4. Структура молекули
лізоциму
Збільшення концентрації лізоциму спостерігають при пародонтозі, сіалопатіях, у хворих на щелепний остеомієліт максимальний вміст лізоциму в слині відзначають у період закритого процесу, а після розкриття й у період видужання кількість його знижується. Значне зменшення концентрації лізоциму в слині відбувається при гострому перебігу карієсу (особливо при переході процесу на пульпу і пародонт), хронічному паротиті, гінгівітах, виразковому стоматиті, афтозному та герпетичному стоматитах, інтоксикаціях сполуками фтору, цинку, свинцю, тривалому введенні тетрацикліну та пеніциліну, тривалому користуванні протезами з акрилових полімерів.
Фосфатази (кисла та лужна) беруть участь у фосфорно-кальцієвому обміні, відщеплюють неорганічний фосфат від сполук фосфорної кислоти і цим зумовлюють мінералізацію кісток і зубів.
Лужна фосфатаза – Zn-місний металопротеїд. Її максимальну активність виявляють при рн 8,4 - 9,4. Лужна фосфатаза утворюється в під'язикових слинних залозах мікроорганізмами порожнини рота, лейкоцитами, злущеними клітинами епітелію.
При запальних процесах у порожнині рота активність лужної фосфатази змішаної слини корелює з тяжкістю захворювання, а зниження активності цього ензиму спостерігають при закисленні слини та декомпенсованому каріозному процесі.
Кисла фосфатаза найбільшу активність виявляє при рн 4,7 – 6,0. Вона утворюється в привушних і під'язикових слинних залозах, її джерелами є також бактерії, дріжджі, лейкоцити порожнини рота, у слині визначають до 4-х її ізоензимів.
підвищується активність кислої фосфатази при запальних процесах (гінгівіт, пародонтит) В осіб з високою активністю цього ензиму відзначена стійкість до карієсу. Разом із тим варто пам’ятати, що зміна фосфатазної активності слини може і не бути пов'язана з патологією слинних залоз чи пародонта, оскільки її концентрація зростає при низці патологічних процесів внутрішніх органів.
Пероксидази належать до класу оксидоредуктаз і представлені групою ензимів з дуже подібною біологічною активністю. Їх поділяють на 2 групи: пероксидази слини, які утворюються в слинних залозах і мієлопероксидази (синтезуються лейкоцитами ротової порожнини). Пероксидази слинних залоз володіють спорідненістю до тіоцианату, а мієлопероксидаза лейкоцитів - до хлоридів. Крім синтезу власних ензимів, слинні залози здатні транспортувати пероксидази крові.
У привушних залозах активність пероксидаз у три рази вища, ніж у підщелепних. Пероксидази в ротовій порожнині виявляють свою бактерицидну і бактеріостатичну дію лише в присутності гідрогену пероксиду (утворюється мікроорганізмами, проявляє деяку дезинфікуючу дію в порожнині рота) та аніонів CNS-, Cl-, з яких утворюються гіпотіоціанат (OCNS)- і гіпохлорит (HOCl-). Ці сполуки сприяють перетворенню амінокислот мікроорганізмів на токсичні альдегіди, внаслідок чого бактеріальні клітини гинуть. Оскільки велика частина аеробних бактерій ротової порожнини, у тому числі лактобацили, стрептококи, пневмококи генерують пероксид водню, вони є чутливими до дії пероксидаз.
Велике патогенетичне значення у слині мають протеїнази (колагеназа, еластаза, катепсин Д). За умов норми ці ензими локалізуються в лізосомах секреторних клітин, макрофагів, поліморфноядерних лейкоцитів тощо. При ушкодженні тканин, наприклад, при запаленні, вони виходять із клітин, що супроводжується підвищенням локальної протеолитичної активності і сприяє альтерації. Колагеназа (металопротеїназа) каталізує деградацію колагену. основним джерелом цього ензиму, ймовірно, є мікрофлора порожнини рота, а при запаленні – лейкоцити й ушкоджені тканини. У нормі колагенолітична активність слини досить незначна і, отже, наявність її в слині є маркером запального процесу. Еластаза (серинова протеїназа) розщеплює еластин, колаген, протеоглікани, основними її джерелами є поліморфноядерні лейкоцити, що мігрують у порожнину рота, крім того еластаза надходить у слину з ясенною рідиною. Катепсин Д (карбоксильна протеїназа) міститься у всіх тканинах, каталізує внутрішньоклітинний розпад білка. Зростання активності цих ензимів корелює з тяжкістю запального процесу.
Інгібітори протеїназ захищають білки слини від протеолітичного розщеплення. Частина з них секретується слинними залозами (головним чином, привушними та піднижньощелепними) у порожнину рота, а частина надходить із крові; їх джерелом є також лейкоцити, макрофаги, мікрофлора клітин злущеного епітелію. До специфічних інгібіторів протеїназ належать 1-протеїназний інгібітор, 2-макроглобулін, а до секреторних - кислотостабільні інгібітори протеїназ, зокрема, інгібітори цистеїноних протеїназ – цистатини. При запальних процесах (особливо при пародонтиті) антипротеїназна активність слини зменшується, що сприяє розвитку деструктивних процесів у тканинах.
Вміст нуклеаз (ДНКази та РНКази) у слині нижча, ніж у сироватці крові, однак за відносною активності в кілька разів перевищує останню. Основним джерелом цих ензимів є слинні залози та лейкоцити. Вони активні стосовно вірусів, у яких гідролізують нуклеїнові кислоти до низькомолекулярних продуктів.
Карбоангідраза (КА) – ензим, який належить до класу ліаз. З одинадцяти відомих на теперішній момент ізоензимів карбоангідрази лише КА-II і КА-VI беруть участь у підтриманні кислотно-лужного гомеостазу в ротовій порожнині. Вони утворюються в цитозолі ацинарних клітин привушних і піднижньощелепних слинних залоз, але карбоангідраза-ІІ і бере участь у процесі утворення бікарбонатів слини, а КА-VІ виділяється в ротову порожнину і захищає зуби від ураження карієсом, оскільки виявляє свою активність у пелікулі зуба, беручи участь у перетворенні гідрокарбонату та продуктів метаболізму бактерій на СО2 і Н2О
Гіалуронідаза змінює рівень проникності тканин, у тому числі емалі зуба, калікреїн володіє вазодилятаторним впливом - впливає на синтез колагену, стимулює секрецією слини, лімфокінів, посилює проліферацію фібробластів, пришвидшує міграцію лейкоцитів у вогнище запалення. З літературних джерел відомо, що він володіє остеотропним впливом
Крім перерахованих, до складу слини входять ензими обміну вуглеводів, аденілатциклаза, уреаза, ензими переамінування та декарбоксилування амінокислот, ензими тканинного дихання, АТФази (Na+, K-, Ca2+-залежні), ліпаза, арилсульфатаза, ß-глюкуронідаза, ензими обміну нейромедіаторів.
Дослідження активності ензимів слини має суттєве значення для діагностики захворювань порожнини рота й оцінки активності патологічного процесу. Слина є джерелом генетичних маркерів – поліморфізм білків, наявність водорозчинних глікопротеїнів,. які володіють антигенною специфічністю, відображає число локусів і алелей, а також частоту алелей у людей різних рас, що має велике значення в антропології, популяційній генетиці, судовій медицині.
Небілкові азотисті компоненти слини - амінокислоти, сечова кислота, сечовина, креатинін (2,0 – 10,0 мкмоль/л) здебільшого надходять у слину з крові, тому їх концентрація в слині змінюється паралельно до зміни їх рівня в плазмі, проте велика частка сечовини, що міститься в слині, секретується привушними, піднижньощелепними та малими слинними залозами. Відомо, що рівень сечовини в слині зростає при захворюваннях нирок. У порожнині рота сечовина розщеплюється за участі уреолітичних бактерій осаду слини:
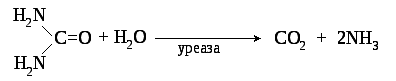
Нітрати (NO3-) та нітрити (NO2-) потрапляють у ротову порожнину з їжею, тютюновим димом і водою. За участі нітратредуктаза бактерій нітрати перетворюються на нітрити, останні, своєю чергою, можуть взаємодіяти з вторинними амінами (амінокислоти, ліки) з утворенням канцерогенних нітрозосполук.
Вміст вуглеводів у змішаній слині становить 37 – 38 % сухого залишку, здебільшого вони знаходяться в комплексі з білками. Вільні вуглеводи, швидко утилізують ся мікрофлорою ротової порожнини і перетворюються на органічні кислоти Концентрація глюкози значною мірою залежить від кількості вуглеводів у їжі, її визначення в слині слід проводити глюкозоксидазним методом, оскільки присутність інших редукуючи речовин значно спотворює істинні значення. .
У слині в невеликій кількості (60 – 70 мг/л) присутні ліпіди, вони потрапляють у ротову порожнину з секретом привушних і піднижньощелепних слинних залоз і лише 2 % - з плазми крові. Частина слинних ліпідів представлена вільними довголанцюговими насиченими та поліненасиченими жирними кислотами – пальмітиновою, стеариновою, ейкозопентаєновою, олеїновою тощо. Крім жирних кислот у слині наявний вільний холестерин і його ефіри, триацилгліцероли, гліцерофосфоліпіди.
Присутні також вітаміни (В1, В2, В3, В6, РР, С, Н) та гормони (становлять 10 – 15 % від їх концентрації в крові), які потрапляють у слину з плазми через слинні залози та ясенну рідину, а також при прийманні гормонів per os. У слині виявлені кортизол, альдостерон, тестостерон, естрогени та прогестерон, їх метаболіти. Вони знаходяться переважно в вільному стані. Кількість андрогенів і естрогенів залежить від ступеня статевого розвитку і може змінюватися при патології репродуктивної системи; рівень прогестерону та естрогенів у слині, так само як і в плазмі, змінюється в різні фази менструального циклу. У нормі в слині також присутні інсулін, вільний тироксин, тиреотропін, кальцитріол. Слинні залози синтезують специфічний гормон – паротин. Він знижує рівень Са2+ крові та посилює його надходження в тканини, тим самим сприяє мінералізації зубів та кісткової тканини. Крім паротину слинні залози виділяють фактор росту нервів (ФРН), фактор росту ендотелію (ФРЕ), епідермальний фактор росту (ЕФР), фактор росту тромбоцитів (ФРТ), інсуліноподібний фактор росту (ІФР), еритропоетин, ренін, тимоциттрансформуючий фактор.
ФРН – поліпептид схожий з проінсуліном, його молекулярна маса – 13 000 Да. Він впливає на розвиток симпатичної нервової системи і метаболізм її нейронів, посилює поглинання глюкози нервовими клітинами. Виділення ФРН у порожнину рота зі слиною стимулює загоєння ушкоджених ділянок слизової оболонки.
ФРЕ - глікопротеїн із молекулярною масою 6 500 Да.Він стимулює регенерацію та загоєння ушкодженого епітелію порожнини рота, активує лужну фосфатазу. Йому властиві також гіпотензивна дія, він стимулює секрецію АКТГ, пригнічує секрецію шлункового соку, чинить антиульцерогенний вплив.
ЕФР– глікопротеїн із молекулярною масою 70 000 Да. Розрізняють α- і β-форми ФРЕ. Цей фактор стимулює диференціювання одонтобластів і посилює в них синтез ДНК у момент дозрівання тканин зуба. З віком ФРЕ пригнічує поділ одонтобластів, гальмує синтез колагену І типу та знижує активність лужної фосфатази.
ФРТ індукує синтез лужної фосфатази та протеогліканів в одонтобластах пульпи та кісткової тканини.
ІФРчинить аутокринну та паракринну дію, пришвидшує ріст клітин, їх диференціювання та мінералізацію твердих тканин зуба.
L-аргінін чинить захисний вплив на слинні залози за умов стресу, попереджаючи активацію розпаду тканинних глікопротеїнів. Під впливом NO-синтази з нього синтезується оксид азоту (NO).
Зміна концентрації гормонів у слині дозволяє оцінити стан надниркових залоз, гонадотропну функцію, ритми утворення та виділення гормонів. Так, при полікістозі яєчка, що супроводжується непліддям, у слині підвищується концентрація вільного тестостерону, а при ураженні надниркових залоз і використанні кортизолу з замісною метою в слині зростає вміст 17α-гідрокситестостерону. У пацієнтів із гіпофункцією гіпофіза та бронзовою хворобою визначення кортизолу в слині значно інформативніше ніж у крові та сечі. На ранніх термінах вагітності та при раку печінки в слині з’являється хор іонічний гонадотропін; при пухлинах щитоподібної залози зростає концентрація тиреоглобуліну, а у хворих з гіпофункцією щитоподібної залози концентрація тироксину та трийодтироніну в слині знижується майже вдвічі, тоді як концентрація тиреотропіну зростає порівняно зі здоровими людьми в 2,8 рази.
Неорганічні компоненти становлять ⅓ усього сухого залишку слини і представлені аніонами хлоридів, бромідів, фосфатів, бікарбонатів, роданідів тощо, а також катіонами Na+, К+, Са2+, Мg2+ тощо (табл. 19.3).
Таблиця 19.3. Вміст неорганічних компонентів у змішаній слині людини
|
Компоненти |
Концентрація, ммоль/л |
Компоненти |
Концентрація, ммоль/л |
|
Кальцій |
1,45-2,42 |
Фтор |
0-0,005 |
|
Калій |
20,6-37,9 |
Йод |
0,1 |
|
Натрій |
3,47-24,3 |
Фосфор неорганічний |
2,39-6,81 |
|
Магній |
0,08-0,53 |
Фосфор ліпідів |
0,0016 – 0,064 |
|
Хлор |
8,4-17,7 |
Бікарбонати |
3,48-10,7 |
|
Мідь |
0,3 |
Тіоционат |
0,52-4,66 |
Вони потрапляють у слину здебільшого із крові і підтримують оптимальні умови середовища, в якому здійснюється гідроліз харчових речовин ензимами слини (осмотичний тиск, необхідний рівень рН).
Концентрація кальцію в слині нижча, ніж у сироватці крові і варіює в залежності від швидкості секреції та віку (значно зростає з посиленням слиновиділення та в людей похилого віку, що має значення в утворенні зубного каменя). Його виявляють у слині як у зв'язаній з білками, так і в іонізованій формах. На відміну від тварин, у людей кальцій не може накопичуватися в слинних залозах. концентрація фосфору в слині людей майже вдвічі вища, ніж у плазмі крові та мало залежить від швидкості секреції (підвищується лише при значному уповільненні слиновиділення). Фосфати слини приблизно на 80 % складаються з неорганічних сполук фосфору, вони входять до складу фосфатного буфера і, отже, мають значення для підтримання рн. Іонна активність як кальцію так і фосфору в ротовій порожнині є показником розчинності гідрокси- та фторапатитів. В експериментальних роботах досліджено, що свіжозібрана слина здорової людини, яка не має каріозних дефектів у зубах, сприяє активному включенню міченого фосфату (32Р) в емаль і дентин зуба. Слина, отримана в людей з множинними каріозними ураженнями зубів, фактично перешкоджає надходженню 32Р в тканини зуба. Аналогічні результати були отримані з радіоактивним кальцієм (45Са).
Концентрація Na+, Сl-, бікарбонатів у слині зростає зі швидкістю її секреції. Вміст К+ не залежить від швидкості слиновиділення і є в 2 - 5 разів вищим, ніж у плазмі крові. Хлорид-аніон виступає активатором альфа-амілази, він є головним протиіоном катіонів калію та натрію, разом вони зумовлюють певне значення іонної сили ротової порожнини.
У людей, які палять, концентрація роданідів значно перевищує нормативні величини, тому що в тютюновому димі крім нікотину, фенолів, чадного газу, канцерогенів типу бензпіренів тощо міститься синильна кислота, яка метаболізується під впливом ензиму роданідази до роданідів, під впливом яких утворюються речовини канцерогенної дії – нітрозаміни. Останні, поряд з бензпіреном, нікотином можуть бути причиною розвитку передракового стану органів ротової порожнини – лейкоплакії або злоякісних новоутворень. При хронічній інтоксикації цими речовинами збільшується в’язкість слини, знижується рН, посилюється відкладання зубного каменю, що сприяє розвитку гінгівіту та пародонтиту.
Слина, як і інші біологічні рідини, містить велику кількість мікроелементів. Вони виступають активаторами окремих ензимів білкового, вуглеводного, ліпідного обмінів, що перебігають у ротовій порожнині. Фізіологічна роль багатьох з них ще не цілком з’ясована. Разом з тим відомо, що вміст фтору та цинку впливає на стійкість до карієсу. Так, при зменшенні кількості цинку знижується концентрація sіgа й активність лізоциму в змішаній слині і збільшується ураження зубів карієсом.
Основний ефект фтору зв'язаний з його впливом на структуру емалі, яку він зміцнює. Концентрація фтору в слині визначається його надходженням в організм, лише при концентрації 1 мг/л і більше він починає поступати з ротової рідини в емаль. Але у випадку перенасичення слини фторапатитом відбувається процес підповерхневої демінералізації, що є характерною ознакою карієсу. Однак багато даних свідчать і на користь його позитивного впливу на імунну систему, у тому числі і на місцевий імунітет у ротовій порожнині. За даними експериментальних досліджень, а також у клінічних дослідженнях показано, що споживання невеликих доз фтору призводить до збільшення вмісту лізоциму в слині та крові, підвищення активності фагоцитів. у хворих на флюороз завжди відзначають високу концентрацію лізоциму.
Підвищення концентрації деяких мікроелементів спостерігають у слині осіб з металевими зубними протезами внаслідок корозії металів, яка може виникати при зміщенні рн слини в кислий бік. Так, при корозії протезів з нержавіючої сталі в слині збільшується вміст заліза, міді, марганцю, алюмінію, титану; при корозії протезів з хромокобальтових сплавів - хрому, нікелю, кобальту, заліза; протези з нержавіючої сталі та золота підвищують вміст золота, міді, срібла.
При отруєнні солями важких металів, прийманні деяких препаратів (наприклад, вісмуту) у слині зростає рівень ртуті та свинцю, а при червоному плоскому лишаї - титану та алюмінію.
Значне збільшення концентрації мікроелементів може стати причиною токсичного та алергійного стоматиту, глоссалгії, спричинити зміну (аж до повної втрати) смакових відчуттів, порушення слиновиділення.
Чому кальцій і фосфор, які знаходяться в слині, не випадають в осад? Це обумовлено тим, що слина є колоїдною системою, яка містить агрегати досить малих нерозчинних у воді часточок (0,1 – 100 нм), що знаходяться в дисперсному стані.
Речовина, яка знаходиться в дисперсному стані, утворює нерозчинне «ядро», останнє адсорбційно взаємодіє з іонами електроліту (стабілізатора), що знаходиться в водній фазі. Молекули стабілізатора дисоціюють у воді, внаслідок чого навколо ядра утворюється подвійний електричний шар – адсорбційний і дифузний. Увесь комплекс, який складається з нерозчинного в воді ядра, дисперсної фази та двох шарів стабілізатора, отримав назву міцели. Вважають, що нерозчинне ядро міцели формує фосфат кальцію [(Са3(РО4)2] (рис. 19.5).
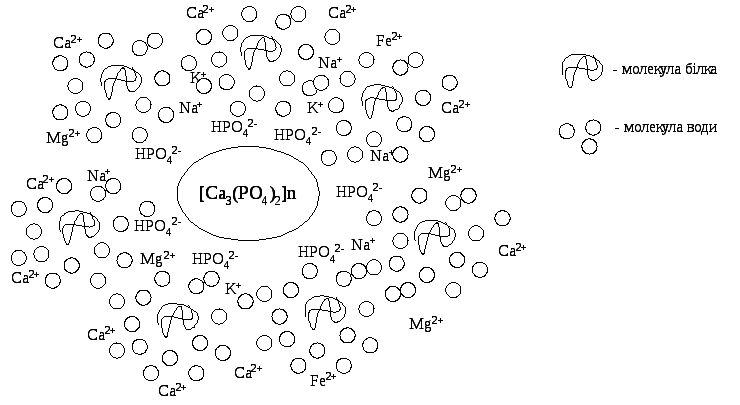
Рис. 19.5. Модель будови міцели слини
На поверхні ядра накопичуються молекули моногідрофосфату (НРО42-), які в надлишковій кількості містяться в слині. Білки (зокрема, муцин), які зв’язують велику кількість води, сприяють розподілу всього об’єму слини між міцелами, внаслідок чого вона структурується, набуває високої в’язкості, стає малорухомою.
У кислому середовищі заряд міцели може зменшуватися вдвічі, оскільки іони моногідрофосфату зв’язують протони. Замість них з’являються іони дигідрофосфату – Н2РО4-, які не беруть участі в процесі ремінералізації емалі та зменшують стійкість міцели. Залуження призводить до зростання кількості фосфат-іонів, які взаємодіють з іонами кальцію. Це призводить до утворення погано розчинної сполуки Са3(РО4)2. яка осаджується у вигляді зубного каменя. Зміни структури міцел у слині спричинюють також утворення каменів у протоках слинних залоз і розвиток слинокам’яної хвороби. З усіх 14 рідин нашого організму лише 3 в умовах патології схильні до утворення каменю – слина, міхурові жовч і сеча. Це обумовлено низкою особливостей, а саме: вони перенасичені гідроксіапатитом; у них спостерігається значне коливання рН (у слині в межах 5 – 8, у міхуровій жовчі - 5,6 - 8, у сечі 5 - 7,5); у цих рідинах концентрація фосфату значно перевищує концентрацію кальцію.
21.1.4. Захисні механізми слини при палінні. Важливим фактором порушення захисних механізмів у ротовій порожнині є паління. У курців описані численні ураження ротової порожнини, прямо зв'язані зі стажем і інтенсивністю паління. Так, тривале паління призводить до нікотинового стоматиту, що є своєрідною реакцією слизової оболонки на подразнення. У таких людей спостерігають лейкоплакію, ромбоподібний глоссит, кандидоз порожнини рота тощо. Паління сприяє відкладенню бактеріальних бляшок і формуванню м'якого нальоту на зубах, що є істотним чинником у формуванні гінгівіту та пародонтиту.
Паління впливає на склад слини та характер слиновиділення. Так, у слині курців відзначається зниження активності протеїназ і лізоциму, інгібування утворення інтерлейкіну-1, що супроводжується пригніченням місцевого імунітету; нікотин гальмує процес утворення супероксидного аніон-радикалу і пероксиду водню у фагоцитах ротової порожнини, що призводить до пригнічення механізму кисень-залежного кіллінгу. Під впливом паління змінюється і швидкість секреції слини: відразу після паління внаслідок подразнювальної дії тютюнового диму відбувається посилення секреції слини, але у «хронічних» курців швидкість салівації знижена і слина має підвищену в'язкість. Характерним також є зниження проліферативної активності В і Т-лімфоцитів. У зв'язку з цими порушеннями клітини імунної системи меншою мірою реагують на патологічні процеси в ротовій порожнині, проте дослідження слини курців на вміст sIgА демонструють його підвищення, що є механізмом компенсації в умовах посиленого ушкодження слизової оболонки ротової порожнини.
