
- •Розділ 4. Обмін вуглеводів та його порушення
- •4.1. Функції вуглеводів та їх класифікація
- •4.2. Анаеробне перетворення вуглеводів (дихотомічний розпад)
- •4.3. Аеробне окиснення вуглеводів
- •4.4. Метаболізм глікогену
- •4.5. Глюконеогенез
- •4.6. Альтернативні шляхи обміну моносахаридів
- •4.7. Регуляція вмісту глюкози в крові
- •При різних метаболічних станах
- •4.8. Цукровий діабет
4.6. Альтернативні шляхи обміну моносахаридів
4.6.1. Пентозофосфатний шлях окиснення глюкози (ПФШ). Можливість існування прямого окиснення глюкози без попереднього розщеплення на фосфотріози була встановлена дослідженнями О. Варбурга та В.О. Енгельгардта.
О
Рис.
4.19.
Метаболічна
карта ПФШ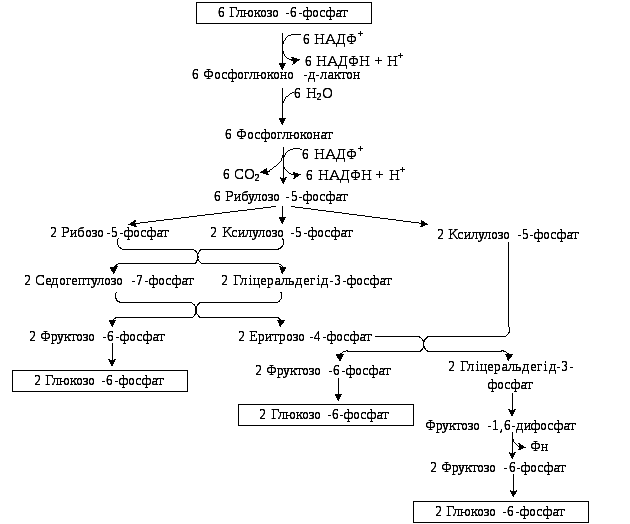
У ПФШ умовно виділяють дві стадії – окисну та неокисну (рис. 4.19). Окисна стадія розпочинається окисненням глюкозо-6-фосфату з утворенням НАДФН і 6-фосфоглюконолактону, який гідролізується до 6-фосфоглюконової кислоти (тому ПФШ називають також фосфоглюконатним) з подальшим її дегідруванням і декарбоксилуванням з утворенням пентози (рибулозо-5-фосфату). Ці реакції окисної стадії незворотні.
Неокисна стадія ПФШ включає зворотні реакції ізомеризації пентоз через проміжні сполуки — гептозу (седогептулозо-7-фосфат), тетрозу (еритрозо-4-фосфат), тріозу (гліцеральдегід-3-фосфат) і перетворення їх на фруктозо-6-фосфат. Утворений фруктозо-6-фосфат перетворюється на глюкозо-6-фосфат або розпадається шляхом гліколізу. Таким чином ПФШ може переходити в гліколітичний.
Так здійснюється утилізація пентоз, утворених в окисній стадії ПФШ, і рибозо-5-фосфату, утвореного при розпаді нуклеїнових кислот.
Реакції неокисної стадії ПФШ перебігають і у зворотному напрямку. За рахунок цього пентози можуть синтезуватись із глюкози не через окисну стадію ПФШ, а із проміжних продуктів гліколізу – фруктозо-6-фосфату і гліцеральдегід-3-фосфату. Сумарний перехід п'яти молекул фруктозо-6-фосфату дасть шість молекул рибозо-5-фосфату. Такий напрямок реакцій неокисної стадії ПФШ має місце в тканинах, в яких потреба в пентозах більша, ніж потреба в НАДФН.
Ферментативні реакції пентозофосфатного шляху
І Стадія:
1. Спочатку глюкозо-6-фосфат окиснюється НАДФ-залежною глюкозо-6-фосфатдегідрогеназою з утворенням 6-фосфоглюконолактону та НАДФН (для перебігу реакції необхідні іони магнію або кальцію).
2. За допомогою специфічного ферменту глюконолактонази та іонів магнію, марганцю або кальцію 6-фосфоглюконолактон перетворюється на 6-фосфоглюконову кислоту:
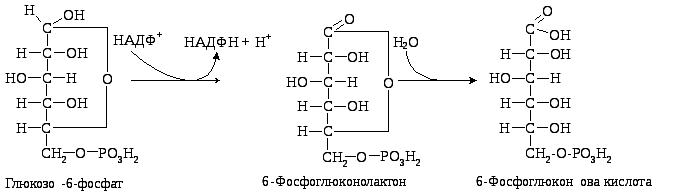
3. Наступним етапом є реакція окиснення 6-фосфоглюконової кислоти під дією фосфоглюконатдегідрогенази (декарбоксилюючої), коферментом якої є також НАДФ. Утворена при цьому 3-кето-6-фосфоглюконова кислота декарбоксилується під дією цього ж ферменту, утворюючи рибулозо-5-фосфат.
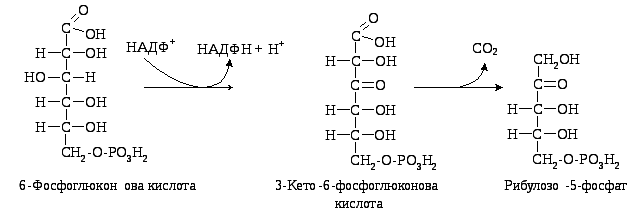
4. Рибулозо-5-фосфат під дією ферменту пентозофосфатізомерази перетворюється на рибозо-5-фосфат, а з нього під дією ферменту епімерази утворюється ксилулозо-5-фосфат.

Утворенням рибулозо-5-фосфату (який може легко перетворюватися на свій ізомер рибозо-5-фосфат), тобто окиснювальною стадією, може завершуватися функціонування ПФШ. Така метаболічна ситуація відбувається в печінці, надниркових і статевих залозах, молочній залозі при лактації, тобто в тканинах з переважанням анаболічних процесів із збалансованою потребою в НАДФН (необхідному для синтезу жирних кислот, стероїдів) та рибозо-5-фосфаті (необхідному для синтезу нуклеотидів, нуклеїнових кислот).
ІІ стадія. Реакції цього типу не пов’язані з використання кисню та перебігають в анаеробних умовах. Ключовими реакціями цієї стадії є транскетолазна та трансальдолазна.
1. Коферментом у транскетолазній реакції виступає ТПФ, який є проміжним переносником глікольальдегідної групи з ксилулозо5-фосфату на рибозо-5-фосфат:

2. Трансальдолазна реакція — взаємодія двох молекул седогептулозо-7-фосфату з двома молекулами гліцеральдегід-3-фосфату з утворенням еритрозо-4-фосфату та фруктозо-6-фосфату (по дві молекули, відповідно):
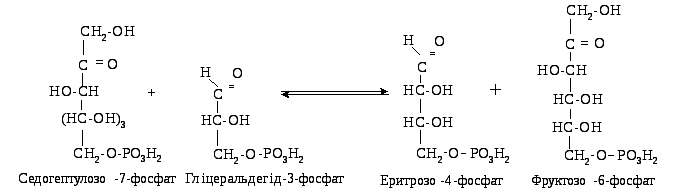
3. Друга транскетолазна реакція полягає у взаємодії двох молекул ксилулозо-5-фосфату (утворених у першій реакції) із двома молекулами еритрозо-4-фосфату з утворенням гліцеральдегід-3-фосфату та фруктозо-6-фосфату (по дві молекули):
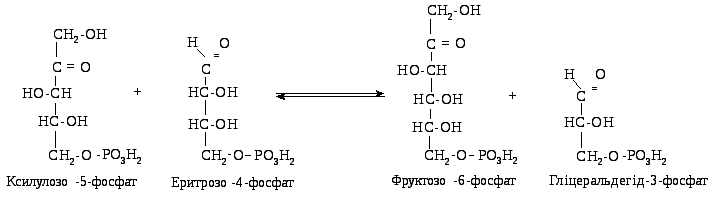
Ці етапи є перетином ПФШ із гліколізом: утворений гліцеральдегід-3-фосфат може надходити до фонду метаболітів гліколізу.
Можлива також конденсація двох молекул гліцеральдегід-З-фосфату (через стадію ізомеризації в діоксіацетонфосфат) з утворенням фруктозо-6-фосфату.
4. Ізомеризація п'яти молекул фруктозо-6-фосфату в п'ять молекул глюкозо-6-фосфату (фермент - фосфогексоізомераза) завершує пентозофосфатний шлях.
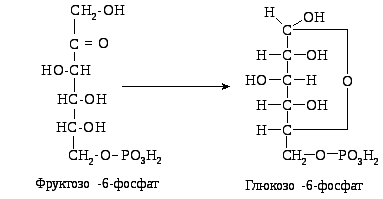
Вибір напрямку і варіанту ПФШ визначається наявністю субстратів і потребою клітини в продуктах. Так, при потребі в НАДФН і рибозо-5-фосфаті ПФШ може закінчуватись утворенням пентоз і сумарне рівняння буде таким:
![]()
Коли потреба в НАДФН перевищує потребу в пентозах, окисна стадія доповнюється переходом пентоз у глюкозо-6-фосфат, який знову окиснюється до пентоз. Сумарний процес можна представити, розглядаючи 6 молекул глюкозо-6-фосфату:
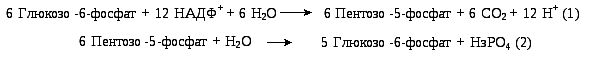
Сумуючи рівняння (1) і (2), отримаємо:
![]()
Слід зауважити, що всі молекули СО2 утворюються із різних молекул глюкозо-6-фосфату.
Значною потребою в НАДФН відрізняються жирова тканина, молочна залоза в період лактації, печінка (для синтезу жирних кислот), кора надниркових залоз і сім'яники (для синтезу стероїдних гормонів), еритроцити (для відновлення окисненого глутатіону). Тому в цих тканинах велика частина глюкози окиснюється пентозофосфатним шляхом.
Коли потреба в рибозо-5-фосфаті для синтезу нуклеотидів значно більша, ніж потреба в НАДФН, то відбувається його утворення з фруктозо-6-фосфату реакціями неокисної стадії ПФШ.
Рибозо-5-фосфат, що утворюється при розпаді нуклеотидів і нуклеїнових кислот, через реакції неокисної стадії ПФШ включається в гліколіз та аеробний розпад і, таким чином, може служити джерелом енергії.
Регуляторний фермент ПФШ - глюкозо-6-фосфатдегідрогеназа. Активність його гальмується продуктом реакції – НАДФН, таким чином інтенсивність ПФШ залежить від швидкості використання НАДФН у реакціях анаболізму та контролюється співвідношенням у клітині НАДФ+/НАДФН.
4.6.1.1. Біологічне значення ПФШ. Роль ПФШ пов'язана з утворенням двох речовин – НАДФН, необхідного для синтезу різних речовин, і метаболіту – рибозо-5-фосфату. До основних функцій пентозофосфатного обміну можна віднести:
1. за рахунок цього процесу в організмі утворюється приблизно ½ пулу НАДФН (решта - в результаті дії НАДФ-залежних ізоцитратдегідрогенази та малатдегідрогенази), який використовується у відновному синтезі жирних кислот і стероїдів, у знешкодженні аміаку при відновному амінуванні.
2. ПФШ є джерелом рибозо-5-фосфату, який використовується для утворення нуклеотидів нуклеїнових кислот ДНК та РНК, коферментних біомолекул НАД (НАДФ), ФАД, АТФ, КоА, циклічних нуклеотидів 3',5'-АМФ та 3',5'-ГМФ, у синтезі гістидину; ПФШ в еритроцитах генерує НАДФН, необхідний для протидії пероксидному окисненню ненасичених жирних кислот фосфоліпідів еритроцитарних мембран, тобто для попередження гемолізу еритроцитів.
У зв'язку із зазначеними біохімічними функціями, реакції ПФШ найактивніше перебігають у тканинах із вираженим анаболізмом, а у клітинах, де найінтенсивніше відбувається синтез ліпідів, вільних нуклеотидів і нуклеїнових кислот (жирова тканина, печінка, молочна залоза в період лактації, кора надниркових залоз, сім'яники). У тканинах з переважанням окиснювального метаболізму, зокрема, у скелетних м'язах, реакції ПФШ протікають дуже повільно.
4.6.1.2. Порушення ПФШ. Відомо приблизно 80 варіантів глюкозо-6-фосфатдегідрогенази еритроцитів, які відрізняються за каталітичною активністю, спорідненістю до субстратів, чутливістю до температури, рН, інгібіторів, електрофоретичною рухливістю. Активність ферменту може бути зниженою різною мірою, аж до нульової. Наявність у людини варіанту глюкозо-6-фосфатдегідрогенази з активністю, близькою до нуля, клінічно проявляється гемолітичною анемією. Механізм розвитку гемолітичної анемії полягає в наступному: в еритроцитах НАДФ+ переводить окиснений глутатіон у відновлений. Останній попереджує пероксидне окиснення ліпідів мембран, захищає від окиснення SН-групи білків, підтримує відновлений стан заліза в гемоглобіні. Знижена продукція НАДФН внаслідок вираженої недостатності глюкозо-6-фосфатдегідрогенази зумовлює зниження рівня в еритроцитах відновленого глутатіону, накопичення Н2О2 і, як наслідок, гемоліз еритроцитів.
При вираженій недостатності ферменту (активність нижча 10 %) анемія розвивається під впливом деяких лікарських засобів, які володіють властивостями оксидантів (протималярійних, сульфаніламідних тощо). Або після споживання в їжу бобів Vicia Faba (кінські боби). У людей із менш вираженою недостатністю ферменту клінічні прояви, як правило, відсутні.
4.6.2. Метаболізм фруктози. Важливими субстратами енергетичного обміну є моносахариди – фруктоза та галактоза, які надходять в організм людини переважно з харчовими дисахаридами рослинного і тваринного походження: фруктоза – у складі сахарози, що гідролізується в кишечнику ферментом сахаразою до глюкози і фруктози, галактоза – в складі “молочного цукру” лактози, що розщеплюється кишковою лактазою до галактози та глюкози.
Після проникнення через плазматичні мембрани всередину клітин фруктоза та галактоза включаються в обмінні процеси шляхом їх перетворення на фосфорильовані ефіри глюкози або її метаболітів – інтермедіатів гліколізу.
Основним джерелом фруктози в організмі людини є її надходження з продуктами харчування, певна кількість синтезується в спеціалізованих тканинах ( у сім'яних везикулах). Її концентрація в сім'яній рідині досягає 10 ммоль. За рахунок здатності мітохондрій сперматозоїдів окиснювати фруктозу в процесі фруктолізу, вона є енергетичним джерелом для руху сперматозоїдів.
У певній концентрації фруктоза міститься в кришталику ока, де вона також утворюється з глюкози через сорбітол. Активність цього метаболічного шляху збільшується при цукровому діабеті; оскільки проникнення сорбітолу через клітинні мембрани є утрудненим, він разом із фруктозою нагромаджується в кришталику, що становить біохімічну основу розвитку діабетичної катаракти.
Включення фруктози в обмін глюкози здійснюється двома шляхами:
1. Під впливом неспецифічної гексокінази, що каталізує фосфорилування різних гексоз:
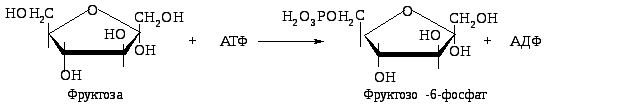
Утворений D-фруктозо-6-фосфат є метаболітом гліколітичного окиснення глюкози. Цей шлях метаболізму фруктози реалізується в клітинах багатьох органів, особливо в м'язах і нирках.
2. Під впливом специфічної фруктокінази, яка каталізує фосфорилування фруктози не за 6-м, а за 1-м вуглецевим атомом (рис. 4.20):
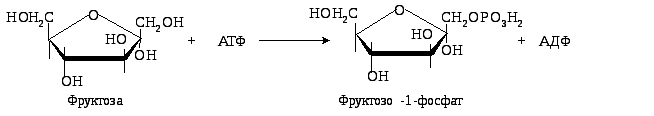
Рис.
4.20. Метаболізм фруктози: А – перетворення
фруктози на діоксіацетон і
гліцеральдегід-3-фосфат; Б – шлях
залучення фруктози в гліколіз і
гліконеогенез; В – шлях залучення
фруктози в синтез глікогену
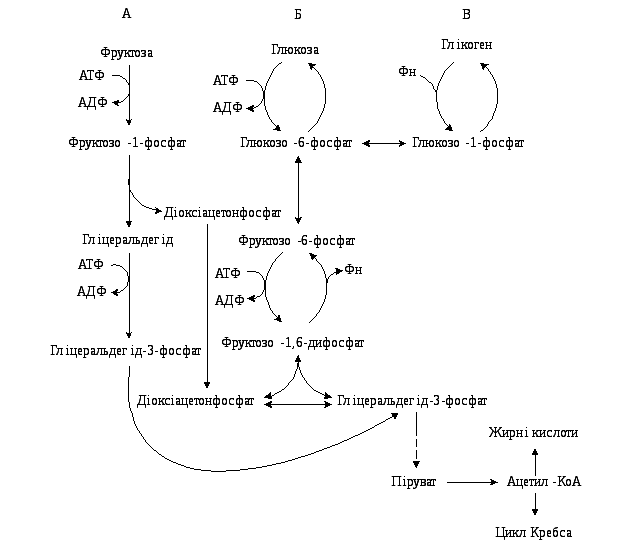
Цей шлях перетворення фруктози функціонує в печінці.
Утворений D-фруктозо-1-фосфат розщеплюється під дією альдолази (фруктозо-1-фосфатальдолази) на дві тріози:
![]()
Діоксіацетонфосфат, що утворився, є інтермедіатом гліколізу і перетворюється на гліцеральдегід-3-фосфат при дії тріозофосфатізомерази
Інший продукт альдолазної реакції, гліцеральдегід, фосфорилується також з утворенням гліцеральдегід-3-фосфату (фермент — тріозокіназа):
![]()
Таким чином, фруктокіназний шлях обміну фруктози перетинається з гліколізом на етапі утворення двох молекул фосфотріози — гліцеральдегід-3-фосфату.
Оскільки перетворення фруктози на тріози здійснюється без участі двох регуляторних реакцій гліколізу (гексокіназної та фосфофруктокіназної), які обмежують швидкість процесу, катаболізм фруктози відбувається значно швидше порівняно з глюкозою.
Синтез ендогенної фруктози відбувається через утворення шестиатомного спирту сорбітолу з глюкози за схемою:
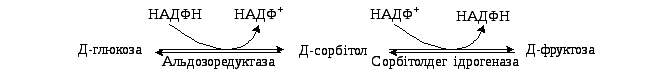
4.6.2.1. спадкові ензимопатії метаболізму фруктози. Ці патології пов'язані з генетичними дефектами синтезу ферментів метаболізму фруктози. До них належать:
а) непереносимість фруктози — захворювання, молекулярною основою якого є уроджена недостатність фруктозо-1 -фосфатальдолази, що спричиняє накопичення в тканинах фруктозо-1-фосфату, який є інгібітором деяких ферментів вуглеводного обміну, зокрема фосфорилази глікогену. Патологія зазвичай виявляється під час переходу від грудного годування дітей до їжі, що містить цукор і проявляється фруктоземією, фруктозурією та тяжкою гіпоглікемією, яка розвиваються після споживання продуктів, що містить фруктозу;
б) фруктоземія — патологія обміну фруктози, спричинена недостатністю фруктокінази. Ензимопатія характеризується порушенням клітинної утилізації фруктози без суттєвих клінічних проявів.
4.6.3. Метаболізм галактози. Галактоза включається в процес гліколізу складнішим порівняно з фруктозою шляхом (рис. 4.21).
Рис. 4.21. Шлях
перетворення галактози на глюкозу в
печінці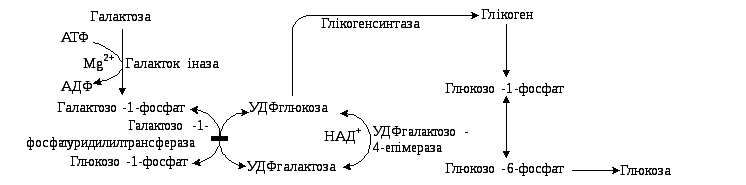
Специфічна галактокіназа каталізує фосфорилування галактози на галактозо-1-фосфат. У наступній реакції бере участь УДФ-глюкоза, яка використовується також для синтезу глікогену. Фермент печінки галактозо-1-фосфат-уридилтрансфераза каталізує обмінну реакцію між галактозо-1-фосфатом і УДФ-глюкозою. Далі залишок галактози в УДФ-галактозі під дією УДФгалактозо-4-епімерази переходить на залишок глюкози (реакція епімеризації біля 4-го атому вуглецю). УДФ-глюкоза може знову взаємодіяти з галактозо-1-фосфатом або перетворюватися на глюкозо-1-фосфат, чи використовуватися на синтез глікогену.
У
Рис.
4.22. Шлях перетворення глюкози на лактозу
в молочній залозі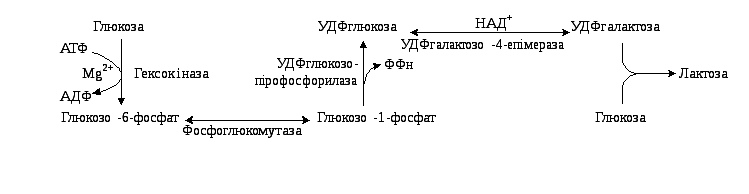
4.6.3.1. Спадкові ферментопатії метаболізму галактози. Спадковий дефект синтезу галактозо-1-фосфатуридилтрансферази проявляється природженою ензимопатією — галактоземією. Внаслідок неспроможності біохімічних систем організму перетворювати галактозу на глюкозу, у крові та внутрішніх органах хворих нагромаджується галактоза та галактозо-1-фосфат, спостерігається тенденція до гіпоглікемії, спостерігається компенсаторна мобілізація жирів, все це клінічно проявляється гепатомегалією, цирозом печінки, порушенням функцій нирок, помутнінням кришталика, затримкою розумового розвитку.
Патологію виявляють у ранньому дитячому віці при споживанні молока, її розвиток може бути сповільнений дотриманням певної дієти (виключення з харчового раціону продуктів, що містять галактозу).
Дуже рідко, але все ж зустрічаються дефекти галактокінази та уридилфосфат-4-епімерази. Вони проявляються галактоземією, галактозурією, проте тяжкі клінічні прояви при цьому відсутні.
