
БХ - 4 семестр / Разное / Ф
.pdf
Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
Отличия Е и неферметативных катализаторов
Каталитическая эффективность - скорость Е реакций выше (в 108 – 1014 раз), чем в некатализируемой реакции.
Высокая специфичность.
Реакции протекают в «мягких» условиях при t = 37° C, рН~7,0, постоянном атм. давлении.
Скорость реакции регулируется.
11/16/2012 |
61 |
Доказательства белковой природы Е
Идентичные свойства ВМС
Чувствительность к рН, t°, факторам денатурации и др.
При парентеральном введении образуют АТ
Гидролиз Е дает свободные протеиногенные АК
Искусственный синтез Е
11/16/2012 |
62 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
31 |

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
Свойства ферментов
Белковая природа определяет многие свойства ферментов
Высокая чувствительность к pH, у каждого
фермента существует свой pH-оптимум
Термолабильность - высокая чувствительность к действию температуры
Специфичность
Многоуровневая разнообразная регуляция
11/16/2012 |
63 |
Оптимум рН разных ферментов
11/16/2012 |
64 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
32 |

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
Механизмы рН зависимости
ионизация и изменение заряда
–поверхностных групп молекулы Е, в т.ч. и его активного центра,
–субстратов, т.к. большинство S являются кислотами.
11/16/2012 |
65 |
рНзависимое изменение заряда белка
66
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
33 |

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
Термолабильность
11/16/2012 |
67 |
Специфичность Е
Виды специфичности:
1. Субстратная специфичность
Абсолютная - аргиназа
Относительная (групповая) - ферм ЖКТ
Стереоспецифичность D- и L-изомеры
2. Каталитическая 4 пути катализа Г6Ф
(фосфоглюкомутаза, Г6Ф-аза, фосфоглюкоизомераза, Г6Ф ДГ)
11/16/2012 |
68 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
34 |

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
Специфичность химотрипсина
11/16/2012 |
69 |
Этапы взаимодействия Е и S
1.Сближение и ориентация S по отношению к каталитической группе Е.
2.Напряжение и деформация чувствительной к действию Е связи, из-за индуцированного соответствия S и Е (образование ЕS комплекса).
3.Общий кислотно-основной катализ.
4.Ковалентный катализ.
11/16/2012 |
70 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
35 |

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
Механизм взаимодействия Е и S
Теория Э Фишера (1894) жесткого стерического соответствия (ключ-замок)
Теория Д.Кошланда (1957) индуцированного взаимодействия Е и S (рука-перчатка)
Современные представления – синтез обеих теорий
11/16/2012 |
71 |
Динамика белковой молекулы
11/16/2012 |
72 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
36 |

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
Схема Е-S взаимодействия
11/16/2012 |
73 |
Теория промежуточных соединений
В 1913 г Л. Михаэлис и М. Ментен создали общую теорию действия Е
1.E+S ↔ ES
2.ES ↔ ES*
3.ES* ↔ ES**
4.ES** ↔ EP
5.EP ↔ E+ P
Реакции протекают внутри ES комплекса
11/16/2012 |
74 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
37 |

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
Кинетика ферментативной реакции
11/16/2012 |
75 |
Зависимость активности Е от [S]
11/16/2012 |
76 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
38 |

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
Активность фермента зависит от
[S]
11/16/2012 |
77 |
График зависимости скорости реакции от [S]
Метод «двойных обратных величин» (график Лайнуивера-Берка)
11/16/2012 |
78 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
39 |
Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
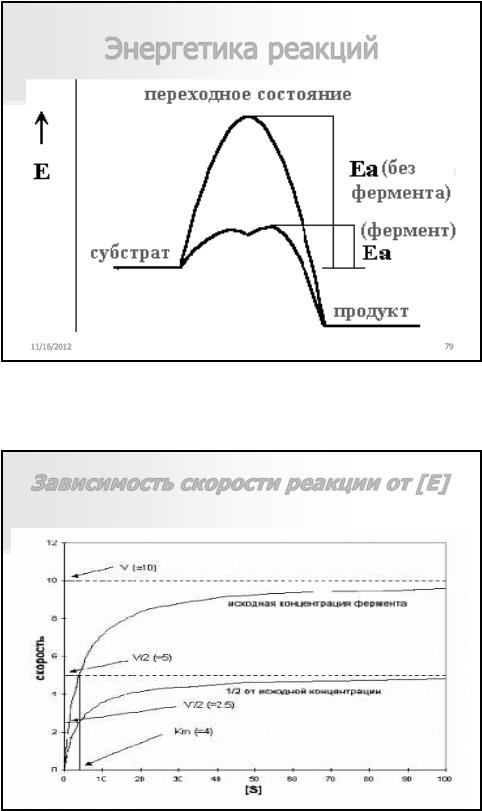
Энергетика реакций
11/16/2012 |
79 |
Зависимость скорости реакции от [E]
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
40 |
