
- •Биологическое окисление 1
- •Содержание
- •Биоэнергетика
- •История учения о БО
- •Antoine Lavoisier
- •Теория активации кислорода
- •Критическая оценка теории Баха-Энглера
- •Хромогены и гистогематины
- •Редокс-реакции, редокс потенциал
- •Maкроэргичность ATФ
- •ATФ-AДФ цикл
- •Образование субстратов БО
- •Stages 1 and 2
- •Stage 3
- •Ферменты и коферменты БО
- •Структура FAD и FMN
- •Мх: локализация
- •Общий план строения Мх
- •Internal structure of a mitochondrion
- •The Comparative Characteristics
- •Membrane Composition:
- •Tricarboxylic Acid Cycle
- •Krebs’
- •Role of TCA
- •Plastic Role of
- •Regulation of
- •Regulation of the TCA Cycle (cont’d)
- •Inhibitors of Krebs Cycle
- •Content
- •Introduction
- •The Ways of Oxygen Consumption
- •Biologic Oxidation (BO)
- •Biomedical Importance of BO
- •Energy Conversion: Mitochondria
- •Chemiosmotic Coupling
- •Electron Transporting Chain, ETC
- •Electron Transporting Chain (ETC)
- •ETC functions
- •ETC Complexes: Overview
- •Complex I (NADH-CoQ reductase)
- •Coenzyme Q (CoQ) or Ubiquinone
- •Complex II (Succinate-CoQ reductase)
- •Complex II and III
- •Complex IV: Cytochrome c Oxidase
- •ATP/ADP translocase
- •Respiratory Chain Functioning
- •Functional scheme of ETC
- •Inhibitors of Oxidative Phosphorylation
- •The Structures of Several Inhibitors of
- •The Sites of Action of Several Inhibitors of ETC and/or OP
- •Several Uncouplers of OP
- •Uncoupler Action
- •Endogenous Uncouplers Enable
- •P/O Ratio
- •Disorders of Mitochondrial
- •Clinical Manifestation and
- •Some Mitochondrial Diseases
- •LHON
- •MERRF, MELAS et al.
- •Can Mitochondrial Diseases be Treated?
- •Cytochromes P450 are monooxygenases important for the detoxification of many drugs
- •Cytochrome b5
- •Monooxygenase System (Microsomal
- •Functioning of Microsomal
- •Microsomal Oxidation and Cytochrome P450

Maкроэргичность ATФ
1.Отрицательно заряженный «хвост» создает сильное отталкивание
2.ATФ4- ADФ3- + Фн2- + H+
[ATФ4-] = [ADФ3-] = [] = [H+] = 10-3 M
Если [H+] будет 10-3 M, pH=3. Но pH=7, значит [H+] =10-7, и хим равновесие сильно сдвинуто влево
ADФ3- и Фн2- резонансные гибриды, для которых характерна высокая устойчивость
В результате
G(ATФ4-) >> G(ADФ3-) + G(Фн2-) + G(H+)
07/06/19
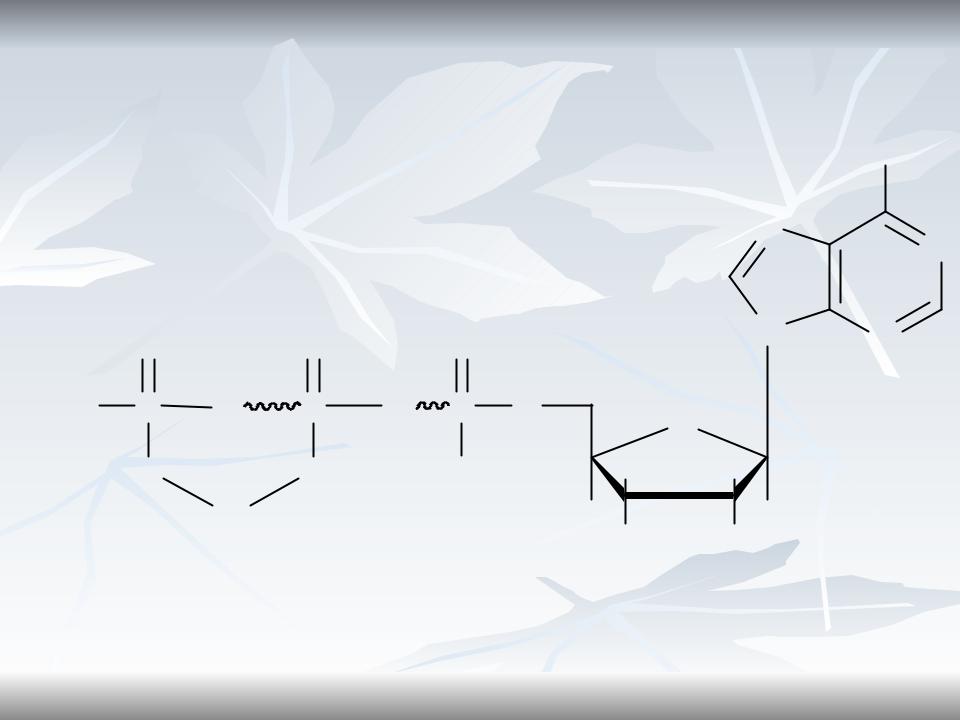
Mg2+ стабилизирует структуру АТФ NH2
|
|
|
|
|
N |
N |
|
|
|
|
|
|
|
O |
O |
O |
|
|
N |
N |
|
|
|
||||
-O P |
O P |
O P |
O |
|
O |
|
|
|
|
|
|
|
|
O |
O |
O- |
|
H |
H |
|
|
Mg |
|
H |
OH |
H |
|
|
|
|
|
OH |
|
…
07/06/19

ATФ-AДФ цикл
|
|
Тепло |
ATP |
||||
CO2 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Продукция энергии |
|
Потребление энергии |
|||||
|
|
Углеводы, |
|
|
Мышечной сокращение |
||
|
|
Липиды, |
|
|
|
Активныйтранспорт |
|
|
|
Белки |
|
|
|
Б/с |
|
|
|
|
|
|
|
Детоксикация |
|
|
|
|
|
|
|
Термогенез |
|
O2  AДФ + Фн
AДФ + Фн 
07/06/19
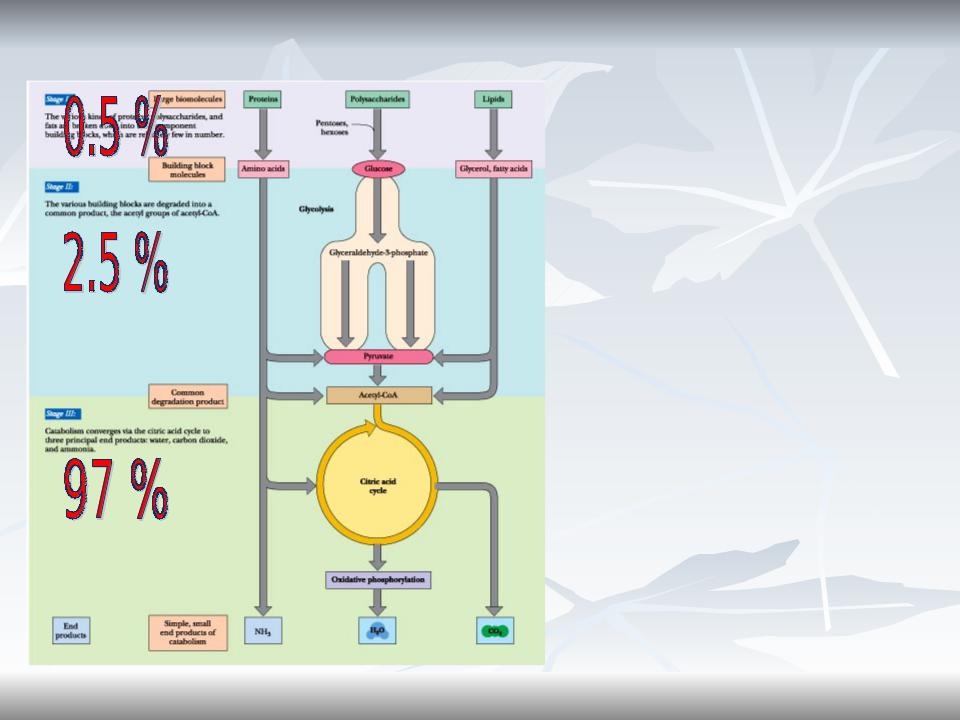
Образование субстратов БО
Стадия I:
Б, Ж, У расщепляются на относительно небольшое кол-во мономеров
Стадия II:
Полученные строительные блоки превращаются в унифицированные метаболиты (ПВК, ацетил КоА и др.).
Стадия III:
Катаболиз унифицированныех метаболитов до СО2 и Н2О с
выделением полезной конвертируемой энергии
07/06/19
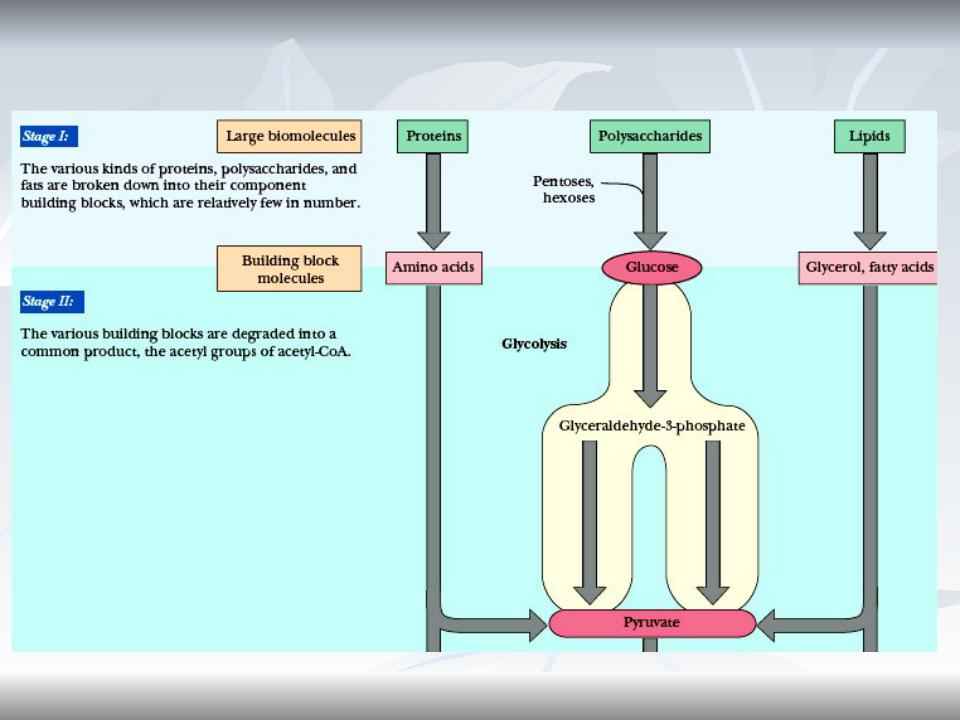
Stages 1 and 2
07/06/19
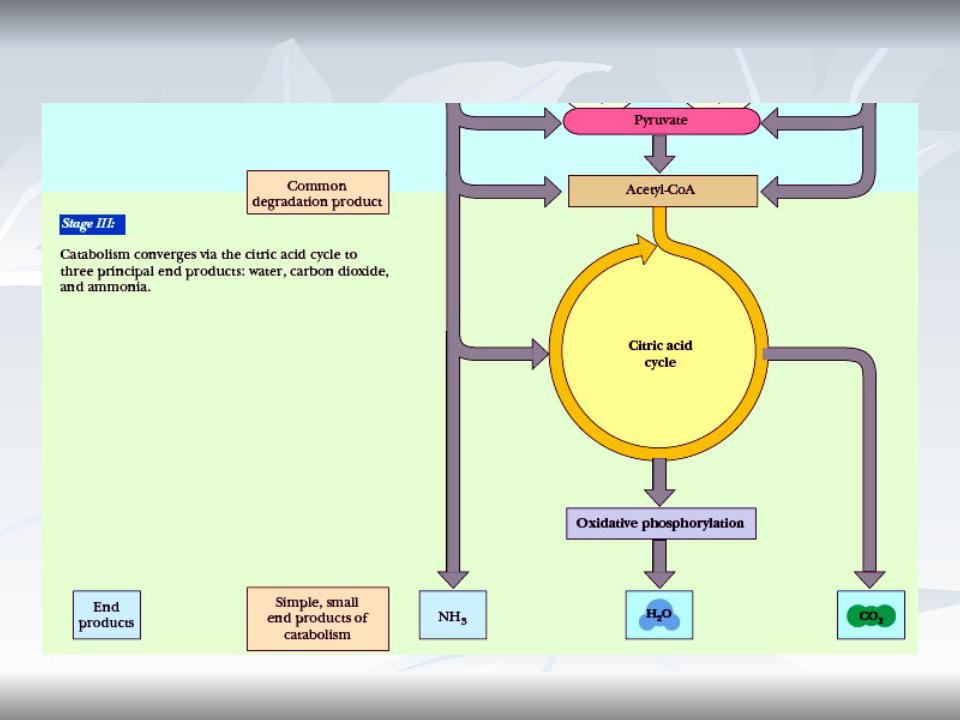
Stage 3
07/06/19

Ферменты и коферменты БО
Оксидоредуктазы
оксидазы
ДГ
Пиризин-зависимые (NAD+, NADH+)
Флавин-зависимые (FMN, FAD)
Гидропероксидазы
Окигеназы
07/06/19

NAD(P)+
07/06/19
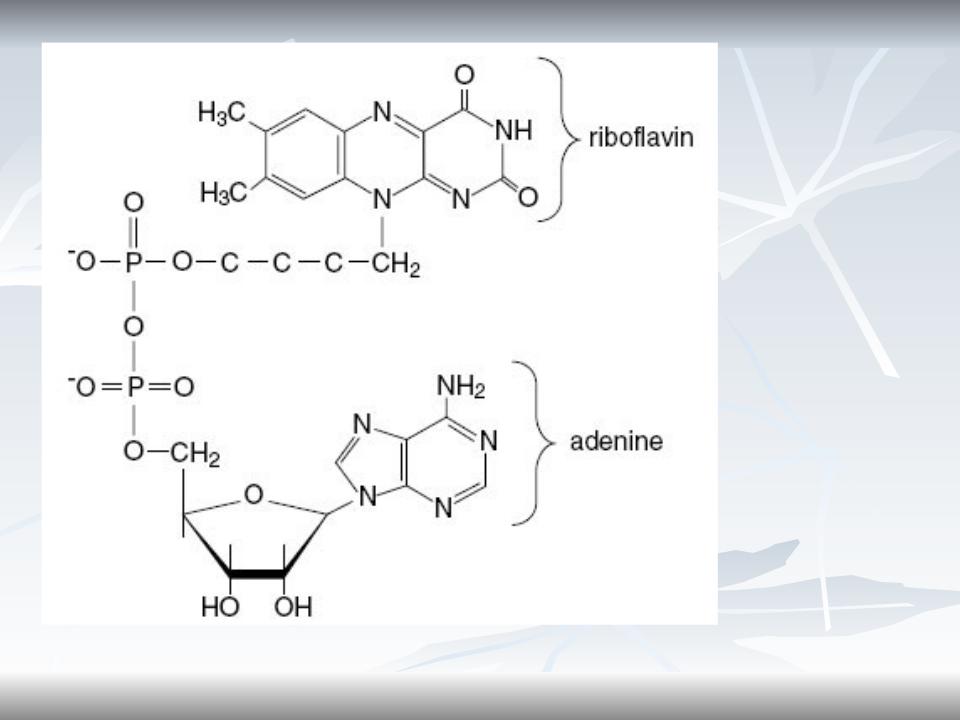
FAD, FMN
07/06/19
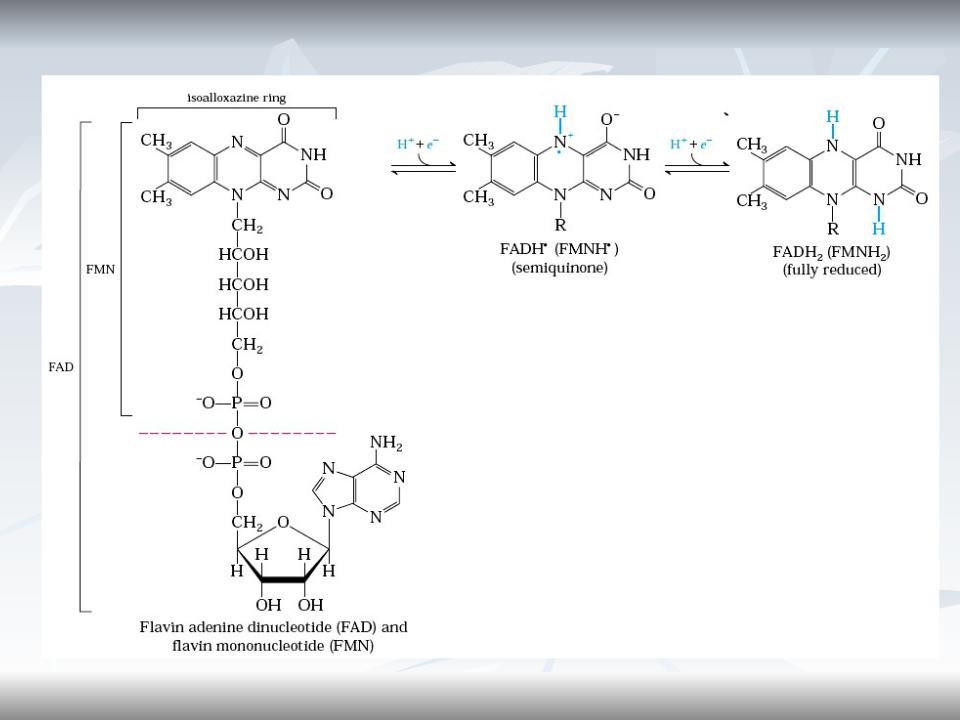
Структура FAD и FMN
FMN consists of the structure above the dashed line on the FAD (oxidized form).
The flavin nucleotides accept two hydrogen atoms (two electrons and two protons), both of which appear in the flavin ring system.
When FAD or FMN accepts only one hydrogen atom, the semiquinone, a stable free radical, forms.
07/06/19
