
1_-_enzimologia_i_BO / 01-08-ФиБО-2012 small
.pdf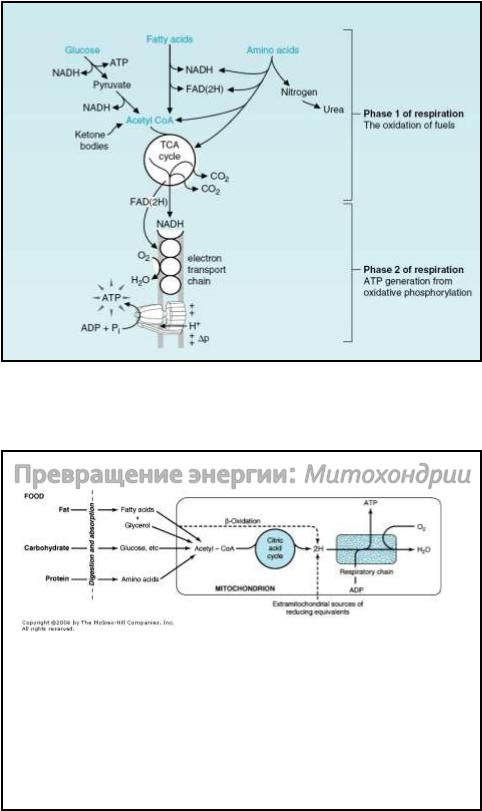
Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
243
Превращение энергии: Митохондрии
•После цитозольной стадии БО, энергия производится из частично окисленных молекул углеводов и используется для производства АТФ
•Производства энергии более эффективно на сопрягающих мембранах
•При аэробном окислении продукция АТФ из «пищевых» молекул max эффективно
16.11.2012 |
244 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
121 |
Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
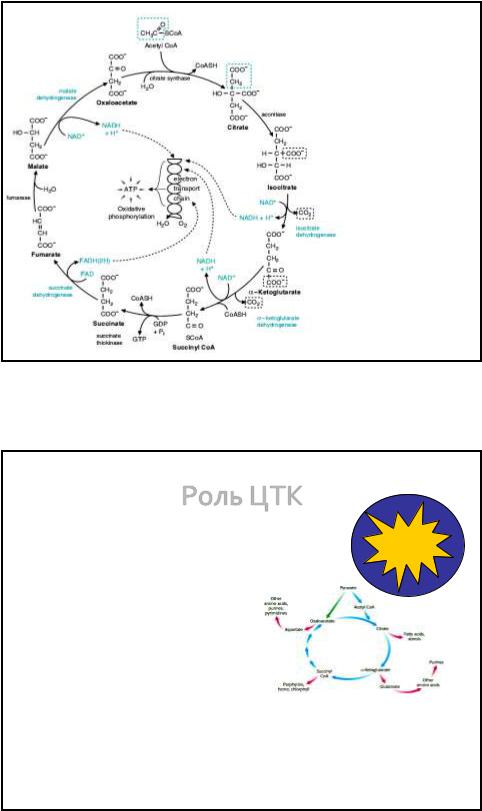
Цикл Кребса
Ганс Адольф Кребс, 1937.
ЦТК:
общий финальный путь окисления всех субстратов БО
Находится в матриксе Мх
245
Роль ЦТК
• Энергетическая |
12 ATP |
–1 оборот ЦТК = 12 ATP.
•Пластическая
α-KG glu.
–OA asp.
–Succinyl-CoA heme.
•Регуляторная
–ЦСМ (образование мочевины в печени) связан с ЦТК.
246
16.11.2012
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
122 |
Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
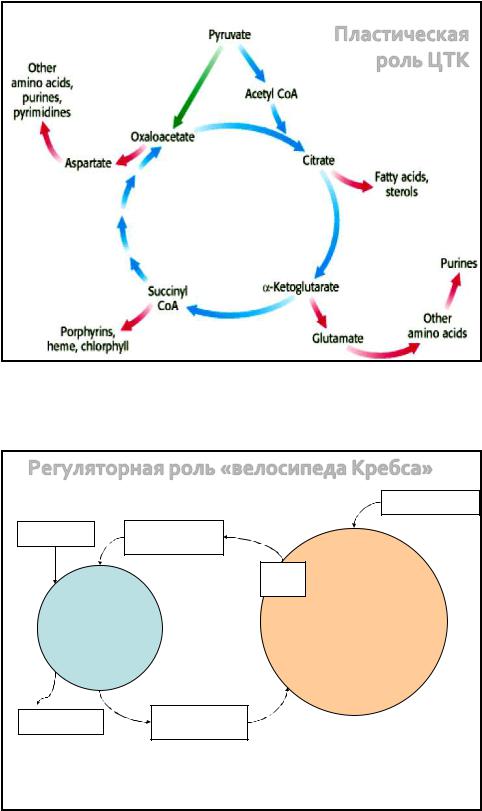
Пластическая роль ЦТК
|
247 |
Регуляторная роль «велосипеда Кребса» |
|
|
Ацетил-KoA |
NH3, CO2 |
аспартат |
|
|
|
OA |
ЦСМ |
ЦТК |
Мочевина |
фумарат |
|
248 |
|
16.11.2012 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
123 |
Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
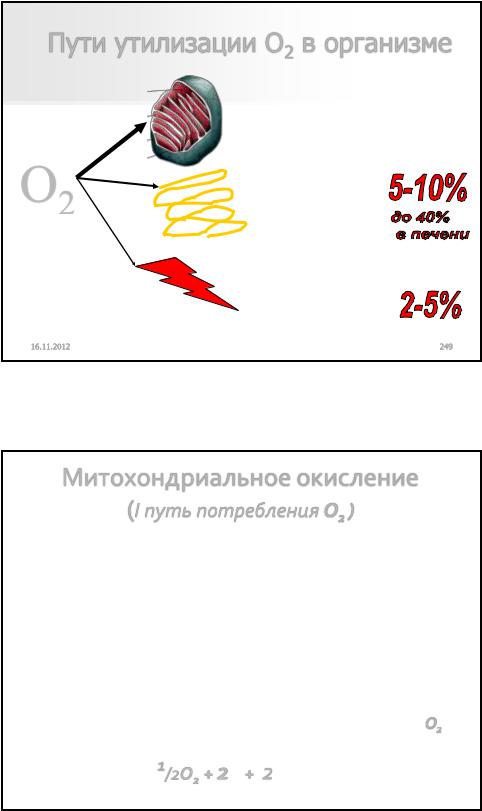
Пути утилизации О2 в организме
Митохондриальное дыхание 
O2 |
Микросомальное |
|
|
|
окисление |
|
Перекисное |
|
окисление |
16.11.2012 |
249 |
Митохондриальное окисление
(I путь потребления О2 )
•Локализуется во внутренней мембране Мх на
митохондриальной ДЦ (ЭТЦ), основная функция
которой:
– Генерация протонного потенциала μН+ - трансформация энергии химической связи в энергию потенциала (электрическую) и далее в энергию химической связи АТФ
В основе реакций митохондриального окисления реакций лежит двухэлектронное восстановление О2
|
1/2О |
2 |
+ 2е- + 2Н+ → Н О |
|
16.11.2012 |
|
2 |
250 |
|
|
|
|
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
124 |

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
Митохондрии: локализация в клетке
•Митохондрии: вытянутые цилиндры, 0.5 - 1.0
μm.
•В живых клетках Мх мобильные и пластичные органеллы, постоянно изменяющие форму, способные к делению и слиянию в соответствии с
физиологическим состоянием ткани
16.11.2012 251
Общая структура Мх
•В печени около 67% общего белка Мх находится в матриксе, 21% - во внутренней мембране, по 6% - в межмембранном пространстве и в наружной мембране.
•Каждые из этих компартментов содержит специфические белки, выполняющие определенные функции
16.11.2012 |
252 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
125 |
Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
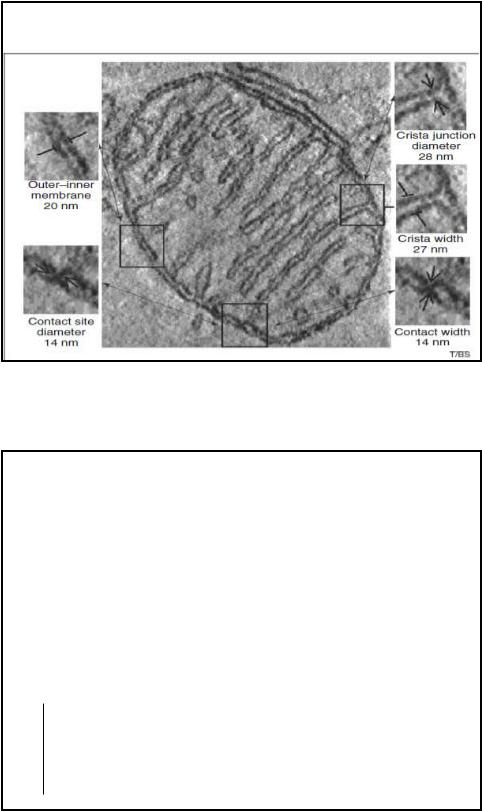
Структура Мх
16.11.2012 |
253 |
Сравнительная характеристика мембран Мх
|
|
Признак |
Внутренняя |
Наружная |
|
|
|
|
|
1 |
|
Форма |
Складчатая |
Гладкая |
|
|
|
|
|
2 |
|
Плотность |
1,2 |
1,1 |
|
|
|
|
|
3 |
|
ФЛ/Б |
0.27/0,73 |
0,82/18 |
|
|
|
|
|
4 |
|
Проницае- |
Высоко- |
Низко- |
|
|
мость |
селективная |
селективная |
|
|
|
Содержание |
|
|
|
|
|
|
5 |
|
Кардиолипин |
Высокое |
Низкое |
|
|
|
|
|
6 |
|
Холестерин |
Низкое |
Выше |
|
|
|
|
|
7 |
|
Ферменты |
СДГ, комп. ДЦ |
МАО,ф.с.ЖК. |
|
16.11.2012 |
|
254 |
|
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
126 |
Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
Сравнительная характеристика ферментов мембран Мх
Наружная мембрана
–МАО (моноаминооксидаза)
–Элонгаза ЖК
–Холинфосфотрансфераза
–Фосфолипаза А
Maтрикс
–Ферменты ЦТК
–Ферменты ˘β-окисл ЖК
–ПВК-карбоксилаза
–ГДГ
Внутренняя мембрана
•NADH ДГ
•СДГ
•Цитохромы b, c1, c, a, a3
•транслоказы (трансфераза)
–Ацил-карнитин
–АДФ-ATФ
–Фосфат
–Глу-асп
–Глу-OH-
–ПВК
–Малат-цитрат
–Малат-α-КГ
16.11.2012 |
255 |
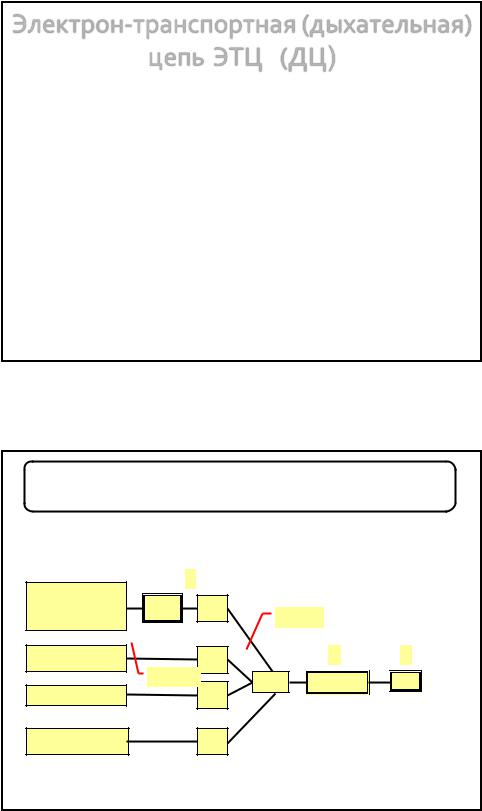
Липидный состав мембран Мх
Внутренняя мембрана:
• 70% белка и 30% липидов
• Специф. ФЛ - кардиолипин
• Мало хол и сфинголипидов
• Много ФХ и ФЭ
Внешняя мембрана:
• 70% липидов и 30% белка
• Мало кардиолипина
• Много ФХ и ФЭ
• Больше хол и сфинголипидов
16.11.2012 |
256 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
127 |
Кафедра биохимии ГомГМУ, 2012 |
|
|
|
|
|
16.11.2012 |
|
Электрон-транспортная (дыхательная) |
|||||||
|
|
цепь ЭТЦ (ДЦ) |
|
|
|||
• |
В Мх содержатся ферментные ансамбли - ЭТЦ ДЦ (до 70 |
||||||
|
белков) транспортирующие восстановленные эквиваленты и |
||||||
|
направляющие их на финальную реакцию с О2 с |
|
|
||||
|
образованием воды |
|
|
|
|
|
|
• |
Компоненты ДЦ иммобилизованы во внутренней мембране |
||||||
|
Мх |
|
|
|
|
|
|
• Движущей силой транспорта электронов по ДЦ является |
|||||||
|
разница ОВП (редокс-потенциала) ее компонентов |
|
|
||||
|
|
NAD/NADH – 0.32V |
|
|
|||
|
|
KoQ/KoQH2 |
+ 0.04 v |
|
|
||
|
|
O2/H2O |
+ 0.82 |
|
|
|
|
|
16.11.2012 |
|
|
|
|
|
257 |
|
Схема ДЦ и действие ингибиторов |
|
|||||
|
-ОН ацил-КоА, |
* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ПВК, изоцитрат, |
NAD+ |
FP1 |
|
|
|
|
|
α-КГ, малат, глу |
|
|
амитал |
|
|
|
|
сукцинат |
|
FP2 |
|
* |
* |
O2 |
|
|
|
|
|
|||
|
|
малонат |
|
|
|
|
|
|
|
|
CoQ |
b – c1– c |
aa3 |
|
|
|
|
|
FP3 |
||||
|
α-глицерофосфат |
|
|
|
|
H2O |
|
|
|
|
|
|
|
||
|
ацил КоА |
|
FP4 |
|
|
|
|
|
16.11.2012 |
|
|
|
|
|
258 |
Введение в биохимию. Энзимология. |
|
|
|
|
|
||
Биоэнергетика |
|
|
|
|
|
|
128 |
Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
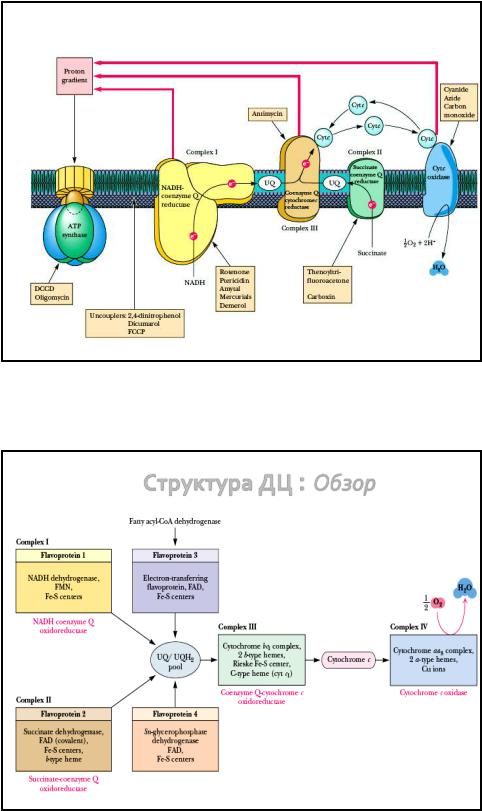
Участки связывания ингибиторов ДЦ и ОФ
16.11.2012 |
259 |
Структура ДЦ : Обзор
16.11.2012 |
260 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
129 |

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
Механизм образования АТФ в Мх
(гипотезы сопряжения ТД и ОФ)
• Химического сопряжения (Э. Слейтер) при
транспорте е- в ДЦ образуется интермедиант с (~) макроэрг связью, идущей на синтез АТФ
• Конформационного сопряжения (П. Бойер)
изменения конформации белков при транспорте е- в ДЦ депонируют энергию (модель мыш сокращение)
•Хемиосмотического сопряжения (П. Митчел, 1961) Нобелевская премия 1978 г
16.11.2012 |
261 |
Хемиосмотического сопряжения
(П. Митчел, 1961)
16.11.2012 |
262 |
Введение в биохимию. Энзимология. |
|
Биоэнергетика |
130 |
