зачет1
.doc
|
Атеросклероз: характеристика понятия, этиология, этапы и основные звенья патогенеза, принципы терапии.
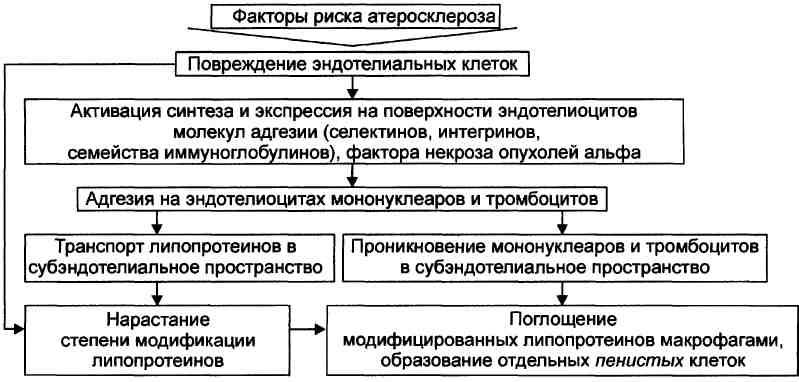
Атеросклероз — прогрессирующие изменения преимущественно во внутренней оболочке артерий эластического и мышечно-эластического типа, заключающиеся в избыточном накоплении ЛП и других компонентов крови, в реактивном образовании фиброзной ткани и происходящих в ней комплексных изменений. Этиология. Первые признаки начинающегося атерогенеза обнаруживаются уже у детей 9—10 лет. К 25 годам они выявляются (в виде липидных полосок) на поверхности аорты. В 10—15-летнем возрасте липидные полоски формируются в коронарных артериях, а у большинства 30-40-летних людей они выявляются в сосудах мозга. В процессе прогрессирования атеросклероза развиваются фиброзные бляшки, происходят их кальцификация, изъязвление и другие изменения. Атеросклероз является разновидностью артериосклероза, а именно атероматозной его формой. СТАДИИ АТЕРОГЕНЕЗА. Атеросклеротические изменения происходят преимущественно во внутренней оболочке артерий. Этот процесс протекает в три стадии: жировой полоски, фиброзной бляшки и комплексных нарушений. Жировая полоска — раннее морфологическое проявление атеросклероза. С момента рождения человека в сосудах можно обнаружить пятна желтоватой окраски размером 1-2 мм. Эти пятна, являющиеся отложениями липидов, с течением времени увеличиваются и сливаются друг с другом. ГМК и макрофаги появляются во внутренней оболочке артерий, макрофаги накапливают ли-пиды и превращаются в пенистые клетки. Так возникает жировая полоска, состоящая из ГМК и содержащих липиды макрофагов. Но отложение липидов в виде жировых полосок в стенке артерий не означает обязательного перехода процесса в следующую стадию (формирование фиброзной бляшки). Фиброзная бляшка располагается во внутренней оболочке артерий и растёт эксцентрично, со временем уменьшая просвет сосуда. Фиброзная бляшка имеет плотную капсулу, состоящую из клеток эндотелия, ГМК, Т-лимфоцитов, пенистых клеток (макрофагов), фиброзной ткани, и мягкое ядро, содержащее эфиры и кристаллы холестерина. Холестерин образуется не за счёт локального синтеза, а поступает из крови. Комплексные нарушения заключаются в уменьшении толщины капсулы фиброзной бляшки менее 65 мкм и нарушении её целостности — появлении трещин, изъязвлений, разрывов. ПАТОГЕНЕЗ. Выделяют следующие этапы атерогенеза: инициация его, прогрессирование атерогенеза, формирование атеромы, образование фиброатеромы, развитие осложнений атеросклероза. Инициация атерогенеза
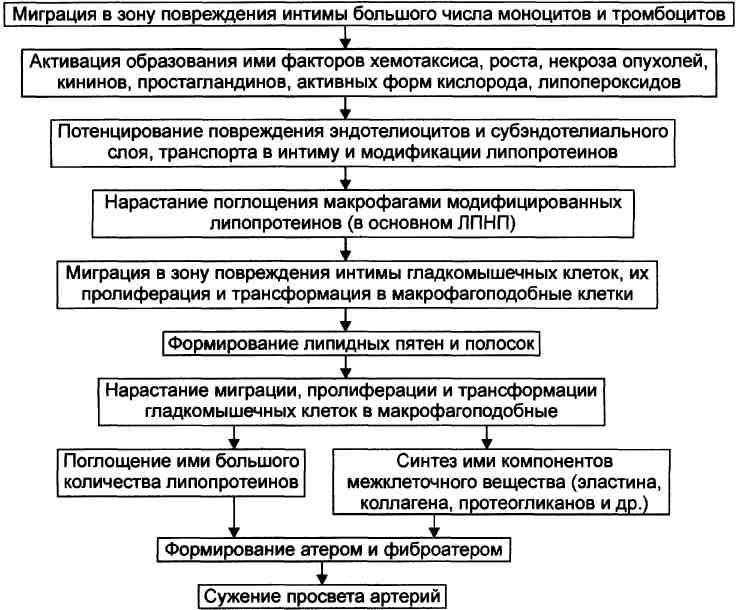
Прогрессирование атерогенеза
Переходный этап. Этот этап атерогенеза — липосклеротический — характеризуется нарастанием процессов поступления ЛП в интиму, их модификации, образования и распада пенистых клеток. Это приводит к значительному увеличению содержания в интерстициальном пространстве модифицированных ЛП и компонентов соединительной ткани. Формирование атеромы и фиброатеромы. Формирование атеромы и фиброатеромы обусловлено: Массированным проникновением моноцитов крови в интиму артерии; Увеличением масштаба миграции из средней оболочки сосуда ГМК, их пролиферации и приобретение ими синтетического фенотипа (трансформация); Прогрессирующей активацией синтеза компонентов межклеточного вещества соединительной ткани. ПРИНЦИПЫ ПРОФИЛАКТИКИ И ТЕРАПИИ Этиотропный принцип имеет целью исключение или уменьшение степени атерогенного действия факторов риска, особенно у лиц с высокой возможностью развития атеросклероза (на основе анализа возможных факторов риска у конкретного пациента). Патогенетический принцип направлен на разрыв «цепочки атерогенеза». Симптоматический принцип преследует цель устранения и/или уменьшения выраженности симптомов атеросклероза, особенно имеющих тягостный, неприятный характер или чреватых ишемией и некрозом тканей. |
Недостаточность кровообращения: характеристика понятия, причины, виды.
Недостаточность кровообращения - наличие дисбаланса (несоответствие) между потребностью органов и тканей в кислороде, питательных веществах и доставкой этих агентов с кровью. Причины: расстройства сердечной деятельности, нарушения тонуса стенок кровеносных сосудов и изменения ОЦК и/или реологических свойств крови. Виды: классифицируют по критериям компенсированности расстройств, остроте развития и течения, выраженности признаков. Компенсированность расстройств: - компенсированные (признаки расстройств кровообращения выявляются при нагрузке) - некомпенсированные (признаки нарушения кровообращения обнаруживаются в покое) Острота развития и течения: - острая (развивается в течение нескольких часов и суток). Частые причины: инфаркт миокарда, острая сердечная недостаточность, некоторые аритмии (тахикардия, выраженная брадикардия, мерцательная аритмия и др.), шок, острая кровопотеря. - хроническую (развивается на протяжении нескольких месяцев или лет) Причины: перикардиты, длительно текущие миокардиты, миокардиодистрофии, кардиосклероз, пороки сердца, гипер- и гипотензивные состояния, анемии, гиперволемии различноro генеза. Выраженность признаков: Стадия I - начальная - первой степени. Признаки: уменьшение скорости сокращения миокарда и снижение фракции выброса, одышка, сердцебиение, утомляемость. Выявляются при физической нагрузке и отсутствуют в покое. Стадия II - второй степени (умеренно или значительно выраженная недостаточность кровообращения). Указанные для I стадии признаки обнаруживаются не только при физической нагрузке, но и в покое. Стадия III - конечная - третьей степени. Характеризуется значительными нарушениями сердечной деятельности и гемодинамики в покое, а также развитием существенных дистрофических и структурных изменений в органах и тканях.
Механизмы повреждения миокарда и изменение основных показателей функции сердца при коронарной недостаточности. Реперфузионная альтерация миокарда: причины патогенез.
Механизмы повреждения сердца. 1)Расстройство энергообеспечения кардиомиоцитов (Дефицит кислорода, преобладание холинергических влияний на сердце, повреждение и разрушение митохондрий и мембран клеток) 2)Повреждение мембран и ферментов кардиомиоцитов (Активация гидролаз, нарушение конформации молекул белка, липопротеидов, фофсолипидов, механические повреждения) 3)Дисбаланс ионов и жидкости (увеличение концентрации К вне клеток, накопление жидкости в клетках, повышение концентрации Na и Ca в клетках) 4) Расстройства механизмов регуляции сердечной деятельности. (Эти расстройства развиваются на одном или нескольких уровнях регуляции: взаимодействия БАВ (гормонов, нейромедиаторов) с рецепторами, образования клеточных посредников регуляторных влияний, метаболических клеточных реакций, регулируемых внутриклеточными посредниками). Изменение основных показателей функций сердца: 1) Изменения ЭКГ (снижение сегмента ST, инверсия зубца T) 2) Снижаются ударный и сердечный выброс. 3) Конечное диастолическое давление в полостях сердца возрастает. 4) Снижается скорость систолического сокращения и диастолического расслабления. |
Коронарная недостаточность: характеристика понятия, виды, причины возникновения, последствия, механизмы.
Коронарная недостаточность – несоответствие коронарного кровотока потребностям миокарда. Клинически коронарная недостаточность проявляется как ишемическая болезнь сердца (ИБС). ИБС – заболевание, которое возникает вследствие абсолютной или относительной коронарной недостаточности. Причины Коронарогенные: атеросклероз(95%); образование тромбов; эмболия(тромбоэмболия); спазм коронарных сосудов (под влиянием катехоламинов, простагландинов F2ά, тромбоксана А2, вазопрессина); сдавление коронарных сосудов. Некоронарогенные: -↑АД; недостаточность аортального клапана; анемия; гипоксия; функциональное перенапряжение миокарда. Факторы риска I порядка: -артериальная гипертензия; -гиперлипидемия; -курение; -мужской пол; -гиподинамия. II порядка: -стресс; -пожилой возраст; -гипергликемия; -ожирение. Механизм: Этиологические факторы → нарушения энергообеспечения кардиомиоцитов, повреждения мембран и ферментов к/м, расстройства механизмов регуляции сердца → дисбаланс ионов и жидкости → повреждение и/или гибель к/м. Клинические формы -стенокардия; -инфаркт миокарда; -кардиосклероз (↑ соединительной ткани на месте разрушенных к/м.) Стенокардия – типовая форма коронарной недостаточности, характеризующееся появлением боли вследствие ишемии миокарда. Боль –сжимающая за грудиной, отдает в левую руку, часть лица, миокард; -кратковременная; проходит после приема нитроглицерина. Стенокардия напряжения – боль при физической нагрузке, быстрой ходьбе. Стенокардия покоя – боль появляется без физической нагрузки. Инфаркт миокарда - форма ИБС, края характеризуется появлением очага некроза, возникающего вследствие несоответствия между притоком и потребностью в кислороде и питательных веществах. Виды По локализации: -передний(повреждается передняя стенка); - задний. По распространенности: -мелкоочаговый; -крупноочаговый; -обширный. Боль –продолжительная (неск часов); -интенсивная; -нитроглицерин не помогает. Проявления -↓АД; -ЧСС↑; гиперферментация (разрушаются к/м и из них выходят в кровь ферменты креатинфосфокиназа, лактатдегидрогеназа, аспартатаминотрансфераза); -↑ т-ра; ↑ СОЭ. Осложнения Ранние: -отек легких; -кардиогенный шок; -аритмии; -тромбоэмболия; -разрыв сердца; -острая аневризма сердца; -острая сердечная недостаточность. Поздние: хроническая аневризма; -аутоиммунный процесс(постинфарктный синдром). |
|
Аритмии сердца: основные виды, причины возникновения, механизмы развития, последствия для организма.
Аритмия – типовая форма патологии сердца – характеризуется нарушением частоты и периодичности генерации возбуждения и/или последовательности возбуждения предсердий и желудочков. Виды Аритмии сердца в результате нарушения автоматизма Автоматизм – способность ткани сердца спонтанно генерировать электрические импульсы. Номотропные – импульсы генерируются синусо-предсердным узлом. 1.Синусовая тахикардия -↑ ЧСС выше нормы при генерации с/п узлом импульсов с одинаковыми интервалами между ними. 2.Синусовая брадикардия - ↓ ЧСС ниже нормы при генерации с/п узлом импульсов с одинаковыми интервалами между ними. 3.Синусовая аритмия – неравномерные чередования электрических импульсов, исходящими из с/п узла. Гетеротропные 1.Предсердный медленный ритм – редкие сокращения сердца. 2.Атриовентикулярный ритм – импульсы в с/п узле генерируются с меньшей частотой, чем в клетках атриовентрикулярного узла. 3.Желудочковый ритм. 4.Диссоциация с интерференцией. 5.Выскакивающие сокращения. 6.Миграция водителя ритма Аритмии в результате нарушения проводимости Замедление и блокада проведения Причины: - повышения парасимпатической влияний на сердце; -повреждения клеток проводящей системы сердца факторами физической., химической., биологической. природы. Нарушение синоаурикулярного проведения – торможение или блокада передачи импульса возбуждения от синусо-предсердного узла к предсердиям. Нарушение внутрипредсердного проведения – в связи с несимметричным расположением синусо-предсердного узла по отношению к предсердиям возбуждение их в норме происходит неодномоментно. Нарушение атриовентрикулярного проведения – замедление или блокада проведения импульсов возбуждения от предсердий в желудочки. Внутрижелудочковые нарушения проведения импульса возбуждения – торможение или блокада распространения электрического импульса по ножкам пучка Гиса, его разветвлениям и волокнам Пуркинье. Ускорение проведения возбуждения – синдром Вольфа-Паркинсона-Уайта(тахикардия, мерцание или трепетание предсердий и желудочков). Аритмии в результате нарушения возбудимости Возбудимость – способность ткани воспринимать и генерировать раздражения. Экстрасистола – внеочередное, преждевременный импульс, вызывающий сокращение всего сердца или его отделов Пароксизмальная тахикардия Трепетание предсердий – высокая частота сокращений предсердий правильного ритма Фибрилляция (мерцание) – нерегулярная, хаотичная электрическая активность предсердий или желудочков
|
Сердечная недостаточность: характеристика понятия, виды, причины, общие механизмы развития, проявления.
Сердечная недостаточность – состояние, при котором сердце не может обеспечить органы и ткани достаточным количеством артериальной крови. Виды По происхождению 1.Миокардиальная – вследствие действия повреждающих факторов на миокард. Причины Физические – механическая травма, действие электрического тока Химические – высокие концентрации БАВ, этиловый спирт Биологические – стрептококки, стафилококки и их токсины 2.Перегрузочная – вследствие перегрузки сердца. Причины Перегрузка объемом – чрезмерное ↑ объема притекающей к сердцу крови (при ↑ОЦК, деформации клапанов сердца) Перегрузка давлением – сопротивление, крое оказывается при выбросе крови (при сужении аорты, перегрузки легочной артерии). 3.Смешанная По первичности нарушения сократительной функции миокарда 1.первичная(кардиогенная) - ↓ сократит. способности миокарда при его повреждении 2.вторичная(некардиогенная) - ↓ ОЦК По локализации 1.Левожелудочковая; 2.Правожелудочковая; 3.Тотальная По скорости развития 1.Острая; 2.Хроническая. Механизм Этиологические факторы → нарушения энергообеспечения к/м, повреждение мембран и ферментов к/м, дисбаланс ионов и жидкости к/м. расстройства регуляции миокарда → силы и скорости сокращения и расслабления миокарда → СН. Механизмы компенсации 1.↑сократимости миокарда при ↑ его растяжимости; 2. сократимости миокарда при возрастании нагрузки на него; 3. сократимости сердца при ↑ЧСС; 4. сократимости сердца при ↑ симпатоадреналовых влияний на него. Механизмы декомпенсации 1.Рост к/м происходит быстрее, чем образование капилляров; 2.Рост к/м быстрее, чем нервные волокна; 3.Несоответствие между ростом к/м и образованием митохондрии. Проявления Застой крови в тех отделах, из которых кровь притекает к сердцу. Проявления л/ж СН – застой крови в МКК -одышка; -кашель(с мокротой и примесью крови); -признаки сердечной астмы, приступ удушья; -отек легкого Проявления п/ж СН – застой крови в БКК -↑ печени в размере (боль в правом подреберье); -↑ селезенки в размере (боль в левом подреберье); -↑ яремных вен (в шее); -асцит (накопление крови в брюшной полости); -гидроторакс (накопление жидкости в плевральной полости); -гидроперикард (жидкость накапливается в области перикарда); -цианоз (синюшность кожных покровов); -↑ т-ра; В тяжелых случаях – сердечная кахексия |
Механизмы компенсации снижения сократительной функции миокарда при сердечной недостаточности: компенсаторная гиперфункция и гипертрофия миокарда. Патогенез декомпенсации гипертрофированного сердца.
- Повышение сократимости миокарда при его растяжении притекающей кровью (механизм Франка-Старлuнга). Обеспечивает увеличение развиваемого миокардом напряжения и скорости сокращения и расслабления. - Увеличение силы сокращений миокарда в ответ на повышенную нагрузку. Происходит при неизменной длине миоцитов. Такой механизм называют гомеометрическим, поскольку он реализуется без значительного изменения длины мышечных волокон. - Возрастание сократимости сердца при увеличении ЧСС. - Повышение сократимости сердца в результате возрастания симпатико-адреналовых влияний. Характеризуется увеличением частоты и силы сокращений. Всё это ведет к повышению: силы сокращений сердца, скорости сокращений, скорости расслабления миокарда. Компенсаторная гиперфункция сердца Функционирование названных выше механизмов обеспечивает экстренную компенсацию сократительной функции перегруженного или повреждённого миокарда. Это сопровождается значительным и более или менее длительным увеличением интенсивности функционирования сердца - его компенсаторной гиперфункцией. Компенсаторная гипертрофия сердца Гиперфункция миокарда обусловливает экспрессию отдельных генов кардиомиоцитов. Она проявляется увеличением интенсивности синтеза нуклеиновых кислот и белков. Ускорение синтеза нуклеиновых кислот и белков миокарда приводит к нарастанию его массы - гипертрофии. Биологическое значение компенсаторной гипертрофии сердца заключается в том, что увеличенная функция органа выполняется его возросшей массой. Патогенез декомпенсации гипертрофированного сердца. 1. Отставание роста микрососудов от нарастания массы миокарда –> относительная коронарная недостаточность. 2. Отставание биогенеза митохондрий от нарастания массы миофибрилл –> нарушение энергетического обеспечения кардиомиоцитов. 3. Отставание активности АТФазы миозинов от потребной –> снижение сократимости миокарда. 4. Отставание скорости синтеза структур кардиомиоцитов от должной –> нарушение пластических процессов; дистрофия миокарда. |
|
Гипертоническая болезнь: характеристика понятия, этиология, стадии, механизмы развития, принципы лечения.
Гипертоническая болезнь (эссенциальная гипертензия) – симптоматическая болезнь, характеризующееся ↑ АД, не связанным с поражением какого-либо органа. Этиология: Повторный, затяжной психоэмоциональный стресс. Главные факторы риска: избыток Na – обусловливает усиление транспорта жидкости в клетки и их набухание, далее утолщение, сужение просвета; повышение чувствительности миоцитов стенок сосудов и сердца к вазоконстрикторным факторам; нарушение экспрессии генов, контролирующих синтез клетками эндотелия сосудорасширяющих агентов (оксид азота, простациклин). Причины -наследственная предрасположенность; -психоэмоциональное перенапряжение; -пожилой возраст; -атеросклероз; -сахарный диабет; -ожирение; -гиподинамия; -курение; -изб. потребление поваренной соли; -алкоголь. Классификация гипертонической болезни: 1. АД выше 160/95, нет морфологических и функц. нарушений 2. + есть морфологические нарушения: -гипертрофия левого желудочка; -ангиопатия сетчатки глаза; -нефросклероз; -атеросклероз. 3. + функциональные нарушения: -ухудшение зрения; -сердечная недостаточность; - почечная недостаточность; -инсульт головного мозга. Стадии: Стадия I гипертонической болезни: Инициальный фактор патогенеза гипертонической болезни — развитие невротического состояния. Характеризуется активацией центрогенного нейрогенного звена патогенеза гипертонической болезни. Центрогенный нейрогенный механизм включает: - Формирование корково-подкоркового комплекса устойчивого возбуждения. Он включает симпатические ядра заднего отдела гипоталамуса. - Усиление прессорных (гипертензивных) влияний на ССС. Реализуется по двум взаимозависимым — нервному и гуморальному — каналам. - Реализацию действия указанных выше гуморальных агентов. Это параллельно с активацией симпатической нервной системы обеспечивает повышение веноконстрикцию, увеличение возврата венозной крови к сердцу, увеличение ОЦК. Стадия II гипертонической болезни: Стабилизация АД на повышенном уровне. Стабилизацию АД на повышенном уровне обеспечивают рефлексогенный эндокринный, гемический механизмы. На этой стадии регистрируются стабильно повышенное (гипертензивное) АД, а также признаки поражения тканей и внутренних органов (гипертрофия сердца, выраженный атеро- и артериосклероз, нефросклероз). Стадия III гипертонической болезни: Проявляется органическими изменениями и характеризуется повреждением структурных элементов, грубыми расстройствами функций тканей и органов с развитием полиорганной недостаточности. Наиболее часто наблюдаются: - Выраженный атеро- и артериосклероз, приводящие к инфарктам в различных органах (наиболее часто — миокарда) и инсультам. - Кардиомиопатии. Одной из причин является нарушение сбалансированности роста структур миокарда — комплекс изнашивания гипертрофированного сердца. - Склеротическое поражение почек (первично-сморщенная почка). Это название указывает на первично-гипертензивный генез патологии почек при гипертонической болезни. - Дистрофические и склеротические изменения в других органах (мозге, эндокринных железах, сетчатке, сердце). Лечение: контроль АД, факторов риска, изменение образа жизни, лекарственная терапия. Немедикаментозное лечение: диета, физическая активность, психологические методы, водные процедуры. Лекарственная терапия: блокаторы медленных кальциевых каналов, диуретики, в-адреноблокаторы., ингибиторы АПФ, антагонисты ангиотензина II, а-адреноблокаторы. |
Артериальные гипотензии: характеристика понятия, виды, этиология и патогенез.
Артериальные гипотензии - снижение АД ниже 100/60 мм рт. ст. у мужчин и 95/60 мм рт. ст. у женщин. Виды: Физиологическая: 1) Индивидуальный вариант нормы. 2) Артериальная гипотензия высокой тренированности. 3) Адаптивная (компенсаторная) артериальная гипотензия. Патологическая: 1) Острая (коллапс (вследствие острого снижения функции сердца), продолжительное снижение АД, сопровождающееся анурией, нарушением периферического кровообращения и сознания, например при шоке). 2) Хроническая (Первичная – нейроциркуляторная и идиопатическая, Вторичная). Этиология и патогенез. По инициальному звену механизма развития выделяют нейрогенные, эндокринные и метаболические АГ. Нейрогенные. 1)Центрогенные (повторный стресс –> невроз –> активация нейронов –> усиление п/с влияний на с-с систему –> уменьшение общего периферического сосудистого сопротивления и сердечного выброса крови –> АГ) 2) Рефлекторные (уменьшение или прекращение тонических влияний симпатической нс на стенки сосудов и сердца –> снижение общего периферического сосудистого сопротивления и АД –> АГ. Эндокринные. 1) Надпочечниковые (Дефицит катехоламинов, минерало- и глюкокортикоидов –> снижение тонуса стенок артериол и общего периферического сосудистого сопротивления –> АГ). 2) Гипофизарные (Недостаточный эффект вазопрессина, адренокортикотропного, тиреотропного и соматотропного гормонов –> снижение тонуса артериол и общего периферического сосудистого сопротивления, сердечного выброса –> снижение АД –> АГ). 3)Тиреоидные (Брадикардия развивается вследствие снижения или отсутствия положительного хронотропного эффекта тиреоидных гормонов в связи с их дефицитом, снижения активности симпатико-адреналовой системы. Снижение величины сердечного выброса, тонуса стенок сосудов, общего периферического сосудистого сопротивления). Метаболические. Причины: дистрофические изменения в органах и тканях, гипогидратация организма. Патогенез: снижение тонуса стенок сосудов –> падение общего периферического сосудистого сопротивления, сократиткльной функции сердца –> уменьшение сердечного выброса крови, воды в организме –> снижение АД –> АГ. |
Ишемия: характеристика понятия, причины, механизмы возникновения, проявления и последствия. Понятие об эмболии. Компенсаторные реакции при ишемии.
Ишемия — несоответствие между притоком к тканям и органам артериальной крови и потребностью в ней. При этом потребность в кровоснабжении всегда выше реального притока крови по артериям. Причины Причины ишемии могут иметь различное происхождение и природу. По природе причины ишемии делят на физические, химические и биологические. Физические факторы: сдавление артериальных сосудов (например, опухолью, рубцовой тканью, инородным телом, жгутом), сужение или закрытие просвета изнутри (например, тромбом, эмболом, атеросклеротической бляшкой), действие чрезмерно низкой температуры. Химические факторы. Многие химические соединения обладают способностью вызывать сокращение ГМК артериальных сосудов и сужение их просвета. Примеры: никотин, ряд ЛС (мезатон, эфедрин, препараты адреналина, АДГ, ангиотензины). Биологические факторы: БАБ с сосудосуживающими эффектами (например, катехоламины, ангиотензин II, АДГ, эндотелии), БАВ микробного происхождения: их экзо- и эндотоксины, метаболиты с вазоконстрикторным действием. По происхождению выделяют ишемии, причина которых имеет эндогенное или экзогенное происхождение (инфекционное и неинфекционное). Механизмы возникновения ишемии Механизмы, обусловливающие преимущественное снижение притока артериальной крови к тканям и органам: нейрогенный, гуморальный и механический. Нейрогенный механизм (нейротонический и нейропаралитический). Характеризуется преобладанием эффектов симпатической нервной системы на стенки артериол в сравнении с парасимпатической. Это сопровождается повышенным выбросом норадреналина из адренергических терминалей. Нейропаралитический. Характеризуется устранением или снижением («параличом») парасимпатических влияний на стенки артериол. Гуморальный механизм. Заключается в увеличении содержания в тканях веществ с вазоконстрикторным действием (например, ангиотензина II, АДГ) и чувствительности рецепторов стенок артериол к агентам с сосудосуживающим действием (например, при увеличении в тканях [Са2+] или [Na+]). Этиологический фактор механического характера. Характеризуется наличием механического препятствия движению крови по артериальным сосудам. Эмбол — образование, циркулирующее в полостях сердца, кровеносных или лимфатических сосудах и в норме в них не встречающееся. По происхождению различают эндогенные и экзогенные эмболы, а по локализации в сосудах — артериальные и венозные. Экзогенные. Чаще всего - пузырьки воздуха и инородные тела (например, осколки пули, ЛС на масляной основе при их введении в холодном состоянии). Эндогенные: фрагменты тромбов (тромбоэмболы), кусочки жировой ткани, пузырьки газов. Эмболия — циркуляция в кровеносном или лимфатическом русле образования, в норме в нём не встречающегося, и закрытие либо сужение им кровеносного или лимфатического сосуда. Механизмы возникновения ишемии, обусловливающие преимущественно значительное увеличение потребления тканями кислорода и/или субстратов обмена веществ. Значительное повышение функции органа и ткани и возрастание интенсивности метаболизма. Проявление ишемии: Снижение пульсации артериальных сосудов Понижение температуры участка органа и ткани Побледнение участка ткани и органа Изменения в сосудах микроциркуляторного русла. Снижение лимфообразования и лимфооттока Уменьшение диаметра артериол и капилляров Уменьшение количества и диаметра артериальных сосудов. Основные последствия ишемии: Гипоксия Накопление в тканях избытка метаболитов, ионов, БАВ. Снижение специфической функции или ткани Развитие дистрофий, гипотрофии, атрофии, гипоплазии участка ткани или органа. Понижение «неспецифических» функции ткани и органа. Инфаркт участка ткани и органа. |